enfermedad de Lyme
enfermedad de Lyme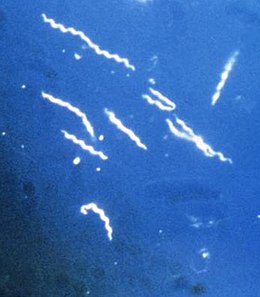 Borrelia burgdorferi , una de las tres variantes conocidas de la bacteria parásita que causa la enfermedad de Lyme. Las borrelia tienen una forma característica de serpentina y espiral, de ahí su nombre espiroquetas .
Borrelia burgdorferi , una de las tres variantes conocidas de la bacteria parásita que causa la enfermedad de Lyme. Las borrelia tienen una forma característica de serpentina y espiral, de ahí su nombre espiroquetas .
| Especialidad | Enfermedades Infecciosas , Dermatología , Neurología y Cardiología |
|---|
| ICD - 10 | A69.2 |
|---|---|
| CIM - 9 | 088.81 |
| Enfermedades DB | 1531 |
| MedlinePlus | 001319 |
| eMedicina | 330178, 965922 y 786767 |
| eMedicina | med / 1346 ped / 1331 neuro / 521 emerg / 588 |
| Malla | D008193 |
| Incubación min | 1 día |
| Incubación máxima | 44 días |
| Síntomas | Eritema migrans crónico , fatiga , dolor de cabeza , artralgia , mialgia , fasciculación , parestesia , vértigo , arritmia cardíaca , dolor neuropático crónico ( d ) , fiebre , neuritis , meningitis , meningoencefalitis ( en ) , miocarditis , artritis , encefalomielitis ( en ) y cardiomiopatía hipertrófica |
| Enfermedad transmitida | Transmisión por garrapatas ( d ) , Ixodes pacificus e Ixodes scapularis |
| Causas | Borrelia burgdorferi |
| Medicamento | Ceftriaxona , cefuroxima , amoxicilina , doxiciclina y azitromicina |
| Paciente del Reino Unido | Enfermedad-de-lyme-pro |
La enfermedad de Lyme es una enfermedad transmitida por vectores y una zoonosis (enfermedad infecciosa que afecta a los seres humanos y a muchos animales). La enfermedad de Lyme lleva el nombre de las ciudades de Lyme y Old Lyme , dos ciudades de los Estados Unidos , en el estado de Connecticut, donde se informó por primera vez en 1975 y se identificó en 1977. Transmitida por pinchazos de aguja, garrapatas duras Ixodes es una enfermedad bacteriana causada por borrelia ( Borrelia burgdorferi , estrechamente definida, predominante en América del Norte).
La expresión borreliosis de Lyme a menudo designa “enfermedad de Lyme europea”, debido a una mayor diversidad de borrelia (principalmente Borrelia garinii , B. afzelii … o B. burgdorferi en sentido amplio). La enfermedad de Lyme y la borreliosis de Lyme son a menudo sinónimos, debido a Borrelia burgdorferi en el sentido amplio. Las otras borreliosis se denominan fiebres recurrentes (cosmopolitas transmitidas por piojos y regionales por garrapatas blandas ).
La enfermedad se caracteriza por una gran diversidad (genética, epidemiológica, clínica y diagnóstica) por ser multiorgánica (que puede afectar a varios órganos) y multisistémica , pudiendo afectar a varios sistemas con por tanto manifestaciones clínicas polimórficas (cutáneas, reumatológicas y neurológicas). ). Se está expandiendo y se está convirtiendo en la enfermedad transmitida por vectores más común que se transmite a los humanos en el hemisferio norte.
En casi el 90% de los casos, se trata eficazmente con terapia con antibióticos durante 2 a 4 semanas. Sin tratamiento, puede evolucionar a lo largo de varios años, pasando clásicamente por tres etapas más o menos diferenciadas, a veces intercaladas con períodos de latencia y que pueden superponerse para ciertos síntomas. Tras una posible fase latente, la enfermedad puede, de forma aguda o crónica, adquirir formas más cutáneas, articulares o neurológicas.
La existencia e importancia de formas no curadas por el tratamiento estándar, o la atribución de patologías crónicas a la enfermedad de Lyme, plantean el problema de la "enfermedad de Lyme crónica", la complejidad del diagnóstico clínico, la interpretación problemática de las pruebas serológicas, las pautas contradictorias para el diagnóstico, el tratamiento y el tratamiento con antibióticos de la enfermedad de Lyme crónica alimentan una controversia social conocida como Guerra de Lyme en los Estados Unidos o Escándalo de Lyme en Francia.
Historia de la enfermedad
La borreliosis existe desde hace mucho tiempo:
- según los restos de ADN bacteriano encontrados en su cadáver, el primer ser humano que se sabe que se ha infectado con Borrelia burgdorferi es Ötzi , hace unos 5.300 años;
- se ha reconstruido la historia evolutiva de B. burgdorferi en América del Norte, lo que sugiere su presencia durante al menos 60.000 años, mucho antes de que los humanos llegaran a América;
- varias líneas muy antiguas y ampliamente distribuidas (incluso en América del Norte) han encontrado recientemente las condiciones para el desarrollo de una epidemia (Walter et al. , 2017); su diversidad y amplia distribución refuta la hipótesis de un surgimiento ligado a modificaciones genéticas recientes (incluso a la manipulación genética (en 2019, se están discutiendo en Estados Unidos para saber si la enfermedad de Lyme se ha utilizado como arma biológica).); el surgimiento de la enfermedad de Lyme es sin duda el resultado de alteraciones antropogénicas de los ecosistemas y el clima que han favorecido brotes de garrapatas y / o bacterias y un número creciente de infecciones humanas;
- la enfermedad toma su nombre de la ciudad de Lyme ( Connecticut ) donde se reportó en 1975 ser identificada como resultado de una picadura de garrapata en 1977. Pero la mayoría de sus manifestaciones ya habían sido descritas en Europa, a fines del siglo XIX. º siglo, pero escasamente.
Primeras descripciones en Europa
- En 1883 , un médico alemán, Alfred Buchwald, describió (en Breslau ) una anomalía de la piel que parece ser lo que hoy se llama acrodermatitis atrófica crónica , pero Buchwald no la relacionó con una picadura de garrapata, y este síntoma no estará presente en Lyme (donde la borrelia dominante es diferente de las que se encuentran en Eurasia);
- En 1909 , Arvid Afzelius (dermatólogo sueco) notó la aparición de otra lesión cutánea en forma de anillo, a veces después de una picadura de garrapata Ixodes , y que llamó eritema migratorio . En 1913, Bruce Lipschutz (dermatólogo austríaco) lo llamó eritema migratorio crónico.
- En 1922 , los médicos franceses Garin y Bujadoux asociaron esta lesión dermatológica con un ataque más general de parálisis "más o menos grave, a veces fatal, tras la picadura de garrapatas" ( Ixodes hexagonus ). Los dos franceses atribuyen esta meningorradiculitis linfocítica (a veces asociando meningitis y polineuritis ) a un "virus" que debe buscarse no en la sangre sino en el tejido nervioso.
- En 1934 , en Alemania, se describió el eritema migratorio asociado con daño articular.
- En 1941 , el alemán Alfred Bannwarth (de) asoció el daño articular con la meningoradiculitis de tipo linfocítico ( síndrome de Bannwarth que a veces se llamaba síndrome de Garin-Boujadoux-Bannwarth ).
- En 1951 , los efectos beneficiosos de la penicilina sobre estas condiciones sugieren un origen bacteriano.
Redescubierto en los Estados Unidos
En 1969 , se publicó en Estados Unidos el primer caso documentado de eritema migratorio crónico, ocurrido en un cazador en el bosque.
En 1975 , dos madres en la ciudad de Lyme con niños diagnosticados con artritis reumatoide juvenil observaron que muchos otros niños en la ciudad tenían problemas similares. Alerted, un equipo de epidemiólogos de la Universidad de Yale , dirigido por Allen Steere, rápidamente destacó una situación atípica:
- la prevalencia de oligoartritis en esta comuna era cien veces mayor que la de artritis reumatoide juvenil en los Estados Unidos;
- los casos nuevos fueron más numerosos en verano y claramente divididos en focos geográficos;
- El 25% de los pacientes tuvo una asociación con eritema crónico.
Allen Steere (en) luego llamó a la enfermedad "enfermedad o artritis de Lyme" el nombre de la ciudad, atribuyéndola a una transmisión por garrapata en un artículo publicado en 1977.
De garrapatas a bacterias
En 1977 , se informó de la picadura de la garrapata Ixodes dammini (ahora Ixodes scapularis ) en un caso humano de eritema migratorio crónico.
En 1982 , Willy Burgdorfer aisló la bacteria espiroqueta responsable de la enfermedad en el tracto digestivo de I. scapularis , conocida como la "garrapata del venado" en América del Norte. Después de la inoculación en el conejo, se muestra que esta espiroqueta puede causar eritema migratorio. También observó una fuerte reacción entre el suero de los pacientes y las bacterias. Es en su honor que esta bacteria se llamará Borrelia burgdorferi en 1984 . Al mismo tiempo, se detectaron espiroquetas idénticas o similares en Europa (Suiza), en garrapatas Ixodes ricinus .
La responsabilidad de esta espiroqueta se confirmará aislándola de la sangre, la piel y el líquido cefalorraquídeo de pacientes con enfermedad de Lyme.
En 1984, el dermatólogo alemán Klaus Weber mostró un aumento de anticuerpos tipo IgG en la sangre de pacientes con acrodermatitis atrófica crónica , estableciendo así una primera relación entre las manifestaciones precoces y tardías de la enfermedad.
Etiología
Agentes
Siguen siendo bacterias del género Borrelia , clasificadas entre las espiroquetas por su carácter serpentiforme y espiral.
Borrelia burgdorferi sl ( sensu lato) designa un "complejo" de alrededor de 30 especies, varias de las cuales son patógenas para los seres humanos. Los tres principales son: Borrelia burgdorferi ss ( sensu stricto ), B. garinii , B. afzelii . Al principio del XXI th métodos de siglo genética molecular se utilizaron (tipificación molecular de bacterias) para detectar nuevas especies patógenas para los seres humanos: como B. spielmanii o B. bavariensis Eurasia, o B. bissettii Eurasia, América, Australia .
También se demostró (en 2016) que ciertas cepas de la misma especie de Borrelia son más patógenas para los humanos que otras.
Cualquiera que sea la especie de Borrelia involucrada, el ataque inicial puede manifestarse (a veces) por eritema migratorio; de lo contrario, las evoluciones difieren. Las asociaciones no son absolutas, sino preferenciales, lo que explica en parte el predominio geográfico de ciertas formas complicadas de la enfermedad.
- En América del Norte , B. burgdorferi ss ( sensu stricto ) predomina casi exclusivamente, causando principalmente la artritis de Lyme y dolores reumáticos (pero siempre sin acrodermatitis ).
- En Eurasia , B. burgdorferi ss es más raro, mientras que B. burgdorferi sl ( sensus lato ) predomina y se dirige también a otros órganos. En Europa, los dos agentes más comunes son Borrelia garinii que causa principalmente daño neurológico o "neuroborreliosis" y Borrelia afzelii , que causa principalmente daño cutáneo, en particular acrodermatitis atrófica crónica . El tipo de bacteria puede variar en el espacio y el tiempo pero, por ejemplo, se realizó un análisis de genospecia en 710 garrapatas extraídas de enero a diciembre de 2009 de la piel de soldados alemanes en entrenamiento en la zona de Seedorf (noroeste de Alemania): 84% de borrelia eran de la especie B. afzelii , el 11% eran B. burgdorferi , el 3% eran B. garinii y el 3% eran B. spielmanii (nota: el 99,2% de las garrapatas eran I. ricinus , el 0,7% eran I. hexagonus y el 0,1% H .concinna ).
Vectores
GarrapatasLos vectores son principalmente garrapatas del género Ixodes . Estos principales vectores tienen en común que tienen un ciclo de transmisión con tres huéspedes sucesivos, en bosques o prados húmedos, de 2 a 7 años según la especie y el clima. En América del Norte, el vector principal es Ixodes scapularis [ = I. dammini ], en el noreste y el medio oeste. Todas las etapas, especialmente las ninfas y las hembras adultas, pueden picar a los humanos. Ixodes pacificus , la fuente de aproximadamente el 5% de los casos notificados en los Estados Unidos, se encuentra en el oeste. Su eficacia patógena en humanos es menor (solo la etapa adulta pica a los humanos).
En Eurasia y especialmente en Europa, el vector principal es Ixodes ricinus . Predomina en las regiones boscosas, picando a los humanos en todos los estadios (larvas y ninfas en primavera, adultos al final del verano).
En Eurasia templada y fría, especialmente Asia y la mayor parte de la antigua URSS , el vector principal es Ixodes persulcatus .
Ciertos artrópodos chupadores de sangre como tábanos , mosquitos, etc. podrían ser vectores potenciales de Lyme. Este posible papel del vector accesorio está en discusión.
Relaciones entre garrapatas y borrelia.La proporción de garrapatas infectadas varía mucho según la etapa de desarrollo, las especies, las estaciones y las regiones: menos del 2% de I. pacificus en California, hasta el 30% de las garrapatas infectadas en Francia, el 60% en Austria y el 100% en Long Island .
En Francia, un estudio realizado en 2021 por el INRAE muestra que el 15% de las garrapatas que pican a los humanos son portadoras de la bacteria Borrelia bugdorferi sensu lato .
La bacteria se desarrolla en dos etapas: se multiplica primero en el intestino medio de la larva , en esta etapa, la bacteria es " inmóvil ", es decir, incapaz de moverse por sí misma. Luego, en una segunda fase, bajo el efecto de la ingesta de sangre (de un primer pequeño roedor hospedador), la bacteria se vuelve móvil y capaz de penetrar en el hemocele de la garrapata y llegar a las "glándulas salivales" de la garrapata. Ninfa o garrapata adulta.
De allí pasa a la saliva y se inyecta en los siguientes hospedadores (mamífero, ave, reptil…). Esto explica por qué generalmente es a través de la picadura de una ninfa de garrapata, y no por la picadura de una larva, que la bacteria se transmite a los grandes mamíferos.
Excepcionalmente, la bacteria también puede extenderse a los ovarios de la garrapata, lo que da lugar a la llamada transmisión transovárica “vertical”, la garrapata transmite la bacteria directamente a su descendencia. Esto explica por qué, en estos casos, una larva de garrapata puede ser infecciosa, incluso antes de haberse alimentado de sangre.
En 2017, el INRA lanzó un proyecto de ciencia ciudadana para un mejor conocimiento de los vectores de la enfermedad de Lyme, en relación con el plan nacional de control de la enfermedad de Lyme. Una aplicación para teléfonos inteligentes permite a todos los ciudadanos informar sobre picaduras de garrapatas, y se les invita a enviar garrapatas a los laboratorios para analizar y conocer mejor la distribución de las especies de vectores y Borrelia.
Embalses
El reservorio de borrelia está formado por pequeños roedores, garrapatas hospedadoras principales en la etapa de larvas o pupas. En esta etapa inicial, las larvas y pupas se alimentan primero de la misma especie de roedor pequeño. Al comienzo del verano, las ninfas infectadas infectan a su hospedador y, al final del verano, el hospedador infectado infecta a las larvas. Las larvas infectadas mudan , pupan y el ciclo comienza de nuevo al año siguiente. Este ciclo inicial es fundamental para el mantenimiento de la borrelia en la naturaleza.
A medida que continúan desarrollándose (de ninfa a adulto), las garrapatas contaminadas transmiten la bacteria a otros huéspedes (roedores, grandes mamíferos, aves, a veces reptiles). En este punto, las garrapatas se reproducen y el ciclo comienza de nuevo. Esta parte del ciclo es fundamental para el mantenimiento de las garrapatas, pero no para la borrelia .
Las especies que desempeñan un papel real de reservorio pueden variar entre países y regiones. En Europa se han identificado más de 300 especies de esta forma: principalmente pequeños roedores, pero también mamíferos de tamaño mediano (zorro, liebre, etc.) o mamíferos de gran tamaño como ciervos , o incluso aves. Estas especies de embalse son las de los animales salvajes que habitan en zonas boscosas, sotobosque, prados, húmedos y templados… en contacto regular y permanente con el hábitat habitual de las garrapatas. Los ciclos europeos parecen más complejos y variados que en América.
En América del Norte, a diferencia de Europa, las especies de reservorio predominantes se destacan con mayor claridad. Por ejemplo, en el noreste y el medio oeste: el ratón de patas blancas y el venado de cola blanca . Las aves migratorias podrían desempeñar un papel en la propagación de garrapatas en Canadá.
Los animales domésticos también pueden estar infectados, en particular perros, ovejas, vacas y caballos, que pueden presentar daño articular (caballos) o riñón (perros) a diferencia de las especies silvestres con infecciones invisibles.
El ser humano que entra en este ciclo, al exponerse a las garrapatas, es de hecho una hueste terminal accidental de garrapatas.
Co-infecciones
Una sola garrapata puede inyectar hasta cinco patógenos diferentes en su hospedador, juntos o de manera tardía, la coinfección con varias especies de Borrelia en garrapatas incluso parece ser la regla en lugar de la excepción.
Así, las posibles coinfecciones transmitidas por garrapatas a los humanos son:
- En los Estados Unidos , la garrapata Ixodes scapularis a menudo también transmite Anaplasma phagocytophilum (agente de la ehrlichiosis humana ) y, con menor frecuencia, Babesia microti (agente de babesiosis ), Borrelia miyamotoi , Borrelia mayonii (agentes de la fiebre recurrente transmitida por garrapatas).
- en Europa , la garrapata Ixodes Ricinus también puede transmitir Anaplasma phagocytophilum y Babesia microti, agente de babesiosis, y también encefalitis por garrapata (causada por un virus);
- en Asia , también se describen coinfecciones.
Agentes conocidos distintos de Borrelia causan síntomas generalmente inespecíficos (dolor de cabeza, dolor articular y muscular, fatiga, etc.) y una fiebre más alta que en la enfermedad de Lyme.
El impacto real en la salud de otros patógenos potenciales que constituirían un “patobioma” de garrapatas aún no se comprende bien. Según Johnson et al. (2014), las coinfecciones podrían explicar, al menos parcialmente, la variabilidad en la gravedad y las manifestaciones clínicas, en ocasiones crónicas, observadas en la expresión de la enfermedad de Lyme;
Métodos de contaminación
Picaduras de garrapatas
Los seres humanos se contaminan cuando encuentran garrapatas vector (contaminadas), que se encuentran en particular en áreas boscosas húmedas con maleza tupida; desde la primavera hasta principios del otoño. Se ubican en la alfombra vegetal a menos de un metro de altura.
Cazan "al acecho" detectando la presencia de un huésped cercano utilizando sensores sensibles al CO 2 , el calor y las sustancias bioquímicas ( órgano de Haller ).
Una vez en el cuerpo del huésped, una garrapata busca zonas calientes y húmedas como los pliegues del cuerpo: en el ser humano, la curva del codo o rodilla, axila, ingle… Puede pasar por debajo de la ropa y llegar a la piel donde se fija por su tribuna para hacer su comida de sangre.
Esta comida de sangre dura de 3 a 5 días. La transmisión ocurre durante la comida, por el paso de bacterias desde el tracto digestivo de la garrapata a sus glándulas salivales. La saliva y las bacterias se inoculan en la epidermis , no directamente en un vaso sanguíneo. Esta progresión no comienza hasta después de la picadura de la garrapata, pasan varias horas antes de que se vuelva contaminante. Además, una garrapata que se elimina con bastante rapidez no transmite la enfermedad.
El riesgo de desarrollar la enfermedad de Lyme después de una picadura de garrapata es del orden del 1 al 5%. Solo un tercio de los pacientes con enfermedad de Lyme han conocido o recordado una picadura de garrapata.
Otros
La transmisión directa de madre a hijo en el útero es posible cuando la madre se infecta durante el embarazo. La enfermedad no tiene ningún efecto sobre el feto si la madre recibe tratamiento con antibióticos adecuados.
Los otros modos de transmisión no han sido demostrados: de persona a persona (tocando, besando o teniendo relaciones sexuales), por aire, agua, comida, lactancia, transfusión de sangre, etc.
No hay riesgo de contaminación directa de una mascota infectada.
Los CDC de EE. UU. Recomiendan que los pacientes de Lyme con una infección activa durante la terapia con antibióticos no donen sangre, ya que aquellos que han completado su tratamiento pueden ser donantes. En Francia, la actitud es similar (aplazamiento temporal).
Epidemiología
Datos actuales
PredominioLa enfermedad de Lyme existe en todos los continentes, pero predomina en la zona templada del hemisferio norte, donde es el principal vector de la enfermedad (incluso en Europa). La enfermedad afecta a más niños pequeños y mayores de 45 años, con un pico de frecuencia que corresponde a la actividad de las garrapatas (desde principios de la primavera hasta finales del otoño). Las zonas del norte y de gran altitud se ven cada vez más afectadas, sin duda porque se están calentando .
En los Estados Unidos , cada año se notifican a los CDC casi 30.000 casos , el 95% de los cuales se encuentran en 14 estados del noreste y del medio oeste , pero los estudios estiman que el número de casos diagnosticados es del orden de 300.000, con la misma distribución geográfica. . La prevalencia de la enfermedad también está aumentando en Canadá , lo que se demuestra notablemente por el seguimiento serológico en perros; En 2019, se estimó que alrededor de un tercio de los casos se notificaron en áreas de emergencia de la enfermedad en Canadá.
En Europa , su incidencia aumenta con un gradiente sur-norte y oeste-este, generalmente entre una latitud de 35 ° norte y 60 ° norte, y por debajo de una altitud de 1300 m . Se estima en 65.000 casos al año, distribuidos de forma heterogénea, con un máximo en Eslovenia y Austria con más de 100 casos por 100.000 habitantes.
En Bélgica , de 2000 a 2016, una media de 200 a 300 personas fueron hospitalizadas por año por esta enfermedad; casi 10.000 consultan a un médico de cabecera por eritema migratorio .
En Suiza , habría de 200 a 600 consultas por año para nuevos casos de enfermedad de Lyme (estimación para 2008-2018).
En Francia , en 2005 se estimaron 43 casos por cada 100.000 habitantes. Esta tasa se elevó a 84 [70-98] casos por 100.000 habitantes en 2016 , pero con una incidencia que varía mucho según la región: la enfermedad parece excepcional en el borde mediterráneo (clima demasiado seco para el vector) pero alcanza más de 100 casos por 100.000 habitantes en el Este y Lemosín y puede superar los 200 casos por 100.000 habitantes en determinadas regiones según la red Sentinelles en 2018.
Actividades de riesgoPaseos por el bosque, campamentos, jardinería, actividades naturalizadas, caza, trabajos agrícolas y especialmente forestales exponen a las personas a la enfermedad:
- de 2.975 trabajadores agrícolas y forestales evaluados en el este de Francia a principios de la década de 2000, el 14,1% ya había tenido al menos un contacto con la borreliosis de Lyme y el 3,4% con el virus de la encefalitis . La edad, la ocupación y el lugar de residencia influyeron significativamente en su estado serológico: el 17,5% de los madereros eran seropositivos. La seroprevalencia en Alsacia (26,9%) y Lorena (16,5%) fue significativamente mayor que en las otras regiones; De manera similar, la seroprevalencia del virus de la encefalitis transmitida por garrapatas fue mayor en Alsacia (5,5%), pero las tasas de seroprevalencia para estas dos infecciones variaron según las áreas de bosque.
- De 310 forestales belgas (estudio de 2018), el 21,6% eran seropositivos para la enfermedad de Lyme. Los que se encontraban con mayor frecuencia en los bosques o que habían informado de más de 100 picaduras fueron los más afectados. La intensidad de las picaduras y el uso de medidas de protección redujeron la tasa de seroprevalencia mientras que la cantidad de sombra que arrojan los árboles en el suelo la incrementó.
- Entre los 181 guardabosques italianos en la región de Friuli-Venezia Giulia (extremo noreste de Italia), a principios de la década de 2000, la prevalencia serológica de la borreliosis de Lyme era del 23,2% (en comparación con el 0,6% del virus de la encefalopatía transmitida por garrapatas y el 0,6%). para la ehrlichiosis ). El trabajo en las colinas y la jardinería en el noreste de la región y un historial múltiple de picaduras de garrapatas aumentaron el riesgo de enfermedad de Lyme. Estos datos sostienen para un eco paisaje factor de ( eco-epidemiológica ).
Nota: Los factores de riesgo fueron similares para la borreliosis de Lyme diagnosticada mediante la prueba de Western blot o según el historial clínico.
Síntesis epidemiológica
La epidemiología de la enfermedad de Lyme es la de una zoonosis "con focos naturales", es decir, cuya distribución es irregular con zonas endémicas localizadas, separadas por zonas más o menos francas (a escala nacional - diferencias regionales - como en escala regional - diferencias locales -, etc. ).
Esta zonificación fluctúa en el tiempo y el espacio, dependiendo de las condiciones climáticas y ecológicas, la temporada, el número y el movimiento de los hospedadores (aves y grandes mamíferos en particular…) portadores de garrapatas y / o borrelia.
La progresión de la enfermedad desde la década de 1970 se debe principalmente a un aumento en la incidencia y una extensión de las áreas afectadas, y menos a una mejora en la detección y vigilancia.
Factores de emergencia
El aumento de la prevalencia de esta enfermedad puede deberse a la evolución genética de agentes, vectores y huéspedes, en relación con cambios en los ecosistemas.
El calentamiento global da como resultado temperaturas mínimas más altas (noche e invierno) y primaveras más tempranas, lo que probablemente suena en la distribución local de garrapatas, su densidad de población y tasa de supervivencia.
A este fenómeno global se suma el desarrollo forestal y agrícola: drenaje , fragmentación forestal y paisajística , tala , reforestación , etc. Estas actividades humanas pueden alterar la dinámica de las poblaciones faunísticas y los equilibrios sylvocynégétique .
Estos procesos reducen la biodiversidad , considerada un elemento estabilizador. Se manifiestan por un aumento en la densidad de vertebrados domésticos y salvajes (huéspedes reservorios competentes) con una disminución en sus grandes depredadores.
América del nortePor ejemplo, en Estados Unidos, de patas blancas ciervos y ratones de patas blancas (hosts primarios para Lyme vector garrapatas) han experimentado un rápido incremento en la densidad.
En el noreste, el XVII ° siglo hasta el comienzo del XIX ° siglo, los colonos se aclaró grandes extensiones de bosques para actividades agrícolas con una virtual desaparición de los ciervos y sus depredadores. Al final de la XIX XX siglo, la región fue industrializada y la agricultura declina; Se reforestan tierras abandonadas, hábitat propicio para la multiplicación del venado cola blanca. Durante el XX ° siglo, esta reforestación se acompaña de un desarrollo residencial suburbano en zona boscosa. Las condiciones están entonces maduras para una mayor proximidad permanente ratones-ciervos-garrapatas-humanos.
EuropaEn Europa, como en América del Norte, una mayor presencia humana en el bosque o en el borde del bosque (hábitat periurbano, actividades de caza o de ocio, etc.) aumenta la posibilidad de contacto entre garrapatas, humanos y sus animales domésticos. (perro, caballo…).
El contexto de guerra y guerra civil también podría favorecer este tipo de zoonosis; así, en Serbia , poco después del comienzo de las guerras conocidas como Guerras de Yugoslavia , se observó un fuerte aumento de los casos de borreliosis de Lyme.
La globalización , el comercio internacional y el turismo también juegan un papel en la distribución geográfica de hospedadores y parásitos. Por ejemplo, en Francia, se sospechaba que una nueva mascota , la ardilla coreana o la ardilla siberiana , liberada en la naturaleza por sus dueños, era un nuevo huésped reservorio porque se adaptó rápidamente: una de las poblaciones más grandes de ardillas listadas (entre diez y veinte miles de individuos) se encuentra así en el bosque de Sénart .
Fisiopatología
Reacciones inmunes
Después de la inoculación, excepto en el caso de alergia a la saliva de las garrapatas, hay poca reacción inflamatoria inmediata, ya que la borrelia puede modificar sus antígenos de superficie, las proteínas de la superficie exterior u Osp (AF), y escapar de las primeras defensas inmunitarias. Si no se tratan, se difunden localmente en la piel desde el sitio de inoculación ( eritema migratorio ).
Luego se difunden a través de la sangre a los tejidos articulares, neurológicos y cardíacos. En el sujeto inmunocompetente , después de varias semanas o meses, las respuestas de anticuerpos suelen controlar la infección diseminada, incluso sin tratamiento, y los síntomas remiten.
En especies reservorios de borrelia, como los ratones, las infecciones no parecen ser patógenas a pesar de la persistencia de la bacteria durante toda la vida, lo que sugiere que el sistema inmunológico de algunos huéspedes silvestres ha evolucionado conjuntamente con la bacteria para "tolerarla".
Los seres humanos no son un reservorio natural; su sistema inmunológico permanece activado hasta que se eliminan las bacterias (las bacterias pueden persistir durante mucho tiempo en sitios ubicados en varios tejidos). Se discute esta persistencia y su importancia médica en varios tejidos. Sin tratamiento, la bacteria se demostró años después de la inoculación, especialmente en lesiones cutáneas tardías ( acrodermatitis atrófica crónica o ACA).
Fue recientemente (2019) confirmó que, en algunos casos, incluso después del tratamiento antibiótico intenso y a largo plazo, las bacterias pueden persistir durante un largo tiempo en el cuerpo, en varios órganos (por ejemplo, cerebro , corazón , riñones y el hígado ), en el forma de agregados (del tipo biofilm ) protegidos del sistema inmunológico por el alginato .
Esta persistencia también se observa en el modelo animal ( in vivo , en ratones inmunocompetentes , perros y primates no humanos en los que se encontró una forma de B. burgdorferi que sobrevivió al tratamiento con antibióticos.
En macacos y rhesus y en ratones infectados voluntariamente, recientemente hemos demostrado claramente esta persistencia de Borrelia viva y metabólicamente activa, después de un tratamiento antibiótico que supuestamente los había erradicado.
Los estudios en humanos también han proporcionado evidencia clínica de la existencia de una forma crónica de la enfermedad de Lyme que puede explicarse por una infección por espiroquetas persistente, por ejemplo, 3 meses después del tratamiento de la parálisis facial , en los tendones, en un caso de artritis de Lyme crónica o en pacientes. cuyos síntomas persistieron después del tratamiento con antibióticos.
En los seres humanos, la infección no crea inmunidad protectora, incluso si los anticuerpos todavía están presentes.
Historia natural de la enfermedad.
Clásicamente, la enfermedad evoluciona en tres fases, no obligatorias. Cada fase puede ser reveladora o enredarse con otra, con brotes o remisiones en cada fase. Además de las variaciones según áreas geográficas (América y Eurasia), la enfermedad también es variable según los pacientes (algunos solo presentan la fase primaria, otros la fase terciaria).
La fase primaria, o fase temprana localizada, que ocurre de 3 a 30 días después de la inoculación, es una fase cutánea, representada por eritema migratorio. En el 20 al 30% de los casos está ausente o pasa desapercibido.
La fase secundaria, o diseminada temprana, se manifiesta en las semanas o meses posteriores a la inoculación. Puede ser revelador (aparecer primero). Según el caso (germen causal relacionado con el área geográfica), los trastornos pueden ser neurológicos, articulares, cardíacos o cutáneos.
Estas dos primeras fases a veces se agrupan en una sola fase llamada temprana, especialmente en Europa, porque los trastornos son diversos (mayor variedad de borrelia). La enfermedad de Lyme se presenta como un todo polimórfico (enfermedades aparentemente diferentes). Mientras que en América del Norte, la enfermedad de Lyme se presenta más en forma conjunta, única o predominante.
La fase terciaria ocurre meses o años después de la inoculación. Es un signo de una infección persistente o resurgente, también puede ser revelador. Estas formas tardías se reconocen cuando forman conjuntos típicos y coherentes desde un punto de vista clínico y biológico. Son discutidos o controvertidos cuando la clínica no es característica y la biología no está validada.
Formas clínicas
Se está discutiendo la existencia e importancia de las formas asintomáticas. Su frecuencia sería del orden del 5% de seropositivos en áreas endémicas, y hasta el 20% en poblaciones en riesgo (trabajadores forestales). Estos casos asintomáticos indicarían un antiguo contacto con la bacteria o una vieja infección que se ha curado.
Fase primaria
Es una fase temprana y local, que produce el característico eritema migratorio , pero no sistemático. Corresponde a una infección cutánea inicial, localizada alrededor del punto de la picadura.
Esta lesión aparece de 3 a 30 días después. Se encuentra con mayor frecuencia en las extremidades inferiores o en la parte inferior del tronco; más raramente en la cabeza (niños pequeños).
Es un eritema anular con un borde activo que se extiende centrífugamente, mientras que el centro se aclara con una pequeña mancha roja central (secuela de la picadura de la garrapata). El diámetro inicial del anillo es de unos pocos cm, luego hasta 15 cm de media, que puede superar los 20 cm (se ha publicado un caso de 70 cm).
Este eritema migratorio puede tener algunas diferencias entre su forma americana y europea.
Forma europeaLa lesión es única, ligeramente cálida, pero indolora y sin prurito. En Europa, donde la enfermedad es causada con mayor frecuencia por B. afzelii o B. garinii , la inflamación es generalmente menos intensa en esta etapa que en América del Norte, y el crecimiento (migración) del eritema suele ser más lento.
Este eritema migratorio suele ser aislado, sin fiebre, sin síndrome inflamatorio. Más raramente, puede haber signos de diseminación temprana con fiebre, dolor, trastornos neurológicos.
Forma americanaA menudo está formado por múltiples lesiones. La parte central permanece roja u oscura y se vuelve más endurecida . Su borde exterior también permanece rojo, pero más raramente, la porción de piel entre el centro y el borde vuelve a su color normal. A veces aparece una necrosis central o una vesícula en el sitio de la picadura, posiblemente con un prurito intenso y persistente, si la enfermedad no se ha tratado a tiempo.
Más a menudo que en Europa, puede haber signos de diseminación temprana con fiebre, dolor, trastornos neurológicos.
Cuando se presentan los aspectos característicos de estas dos formas, el eritema migratorio es prácticamente patognomónico , y es suficiente por sí solo para el diagnóstico.
Este eritema migratorio se resuelve espontáneamente en 4 a 6 semanas. Con un tratamiento temprano, la progresión es más rápida: la lesión desaparece en menos de una semana y la enfermedad no progresa a formas más complicadas.
Fase secundaria
Ocurre con mayor frecuencia desde unas pocas semanas hasta unos meses después de la inoculación, cuando la lesión inicial ha permanecido ausente o ha pasado desapercibida, o sin una terapia antibiótica adecuada.
Esta etapa corresponde a la diseminación bacteriana, seguida de un enfoque en tejidos particulares.
Las manifestaciones están dominadas en Europa por trastornos neurológicos ("neuroborreliosis") y en América por trastornos reumatológicos ("artritis de Lyme"). Más raramente, se encuentran trastornos cardíacos, cutáneos y oculares.
Si la fase primaria está ausente (fase secundaria reveladora), el diagnóstico puede confirmarse mediante la combinación de argumentos clínicos, epidemiológicos y biológicos (en esta etapa, la infección activa suele detectarse en el líquido cefalorraquídeo y en las pruebas serológicas. Relevante, mejor que en fase tres).
NeuroborreliosisLa incidencia de estas neuroborreliosis (formas neurológicas de la enfermedad de Lyme) varía según el país y la región. En Europa, más del 15% de la neuroborreliosis se encuentra entre las enfermedades de Lyme, mientras que en Estados Unidos esta proporción no supera el 8%.
En Europa, también varía según la región, por cada 100.000 habitantes: Dinamarca 0,5 casos, Suecia 1 caso, Alemania 3 casos, Alsacia 10 casos.
Las formas más frecuentes (70 a 80% de neuroborreliosis) son la meningorradiculitis ( polineuritis con infección del líquido cefalorraquídeo ). Aparecen después de 3 semanas a más de 3 meses después de la picadura de la garrapata.
En primer lugar, se trata de trastornos sensoriales, más a menudo que motores, en el área del eritema migratorio. Los dolores son intensos (ardor, desgarro), a menudo en la reaparición nocturna y provocan insomnio. Estos dolores no siempre tienen una ruta raíz estricta. Puede haber daño asociado a los pares craneales , que se manifiesta principalmente por parálisis facial periférica, bilateral en un tercio de los casos.
La neuroborreliosis es la causa más común de parálisis facial periférica en los niños.
Más raramente, en el 0,5 al 8% de los casos, podemos encontrar meningitis aguda , mielitis aguda , encefalitis aguda .
En estas manifestaciones neurológicas agudas o subagudas, el diagnóstico se realiza mediante el estudio del líquido cefalorraquídeo ( LCR ). La punción lumbar para confirmar la meningitis linfocítica . La serología LCS se asocia con la búsqueda de síntesis intratecal de anticuerpos específicos.
En niños, con parálisis facial periférica, una serología sanguínea positiva se considera suficiente para confirmar el diagnóstico y prescribir antibioticoterapia.
La radiculitis hiperalgésica es resistente a los analgésicos habituales. Pueden desaparecer espontáneamente en unas pocas semanas o meses. Ceden más rápidamente en unos días con la terapia antibiótica adecuada.
Artritis de LymeLas manifestaciones articulares estuvieron en el origen del redescubrimiento de la enfermedad en Estados Unidos, donde son más frecuentes (60% de los pacientes) que en Europa (10 a 15%). Puede verse a cualquier edad, pero con mayor frecuencia en niños.
En Europa, son tempranos (unos pocos días a unas pocas semanas después de la inoculación) y la mayoría de las veces se curan espontáneamente. En Estados Unidos, son más tarde (6 meses en promedio hasta 2 años), para volverse crónicos con mayor frecuencia, llevando la imagen de la artritis de Lyme. En Europa, los trastornos articulares se clasifican como fase secundaria, mientras que en América pertenecen a la fase terciaria.
En su forma más típica, la artritis de Lyme afecta a una sola articulación grande (monoartritis u oligoartritis), con dolor y derrame de líquido sinovial , especialmente en la rodilla (con menos frecuencia hombro, codo, etc.). Este deterioro es asimétrico, recurrente (con recaídas y remisiones), a veces permanente, y es probable que dure varios años en ausencia de tratamiento.
La mayoría de los pacientes se recuperan con la terapia antibiótica adecuada, pero algunos conservan sinovitis posinfecciosa , refractaria a los antibióticos.
Otros eventosCon la excepción de la astenia marcada, los trastornos generales son raros. En particular, no suele haber fiebre en la enfermedad de Lyme.
En menos del 5% de los casos, puede haber trastornos cardíacos por bloqueo auriculoventricular , que se manifiestan por palpitaciones o molestias intermitentes. Estos últimos trastornos son espontáneamente regresivos y muy raramente requieren la colocación de un marcapasos permanente. Es posible la pericarditis prolongada. La enfermedad de Lyme debe evaluarse sistemáticamente en cualquier paciente joven con bloqueo auriculoventricular paroxístico inexplicable.
En la misma proporción, podemos encontrar una manifestación denominada linfocitoma de borrelio. Es un nódulo rojo violáceo, de 1 a 2 cm , que se localiza con mayor frecuencia en la cara, el lóbulo de la oreja, la areola mamaria o el escroto .
En el 1% de los casos existen diversos trastornos oftalmológicos: conjuntivitis , uveítis , queratitis, etc.
Fase terciaria
La línea divisoria entre las formas secundaria y terciaria es difícil de establecer. Una forma secundaria continúa convirtiéndose en terciaria, o aparecen manifestaciones terciarias, aparentemente primitivas, años después de la infección.
Los fenómenos autoinmunes podrían explicar estos síntomas, pero la responsabilidad directa de la bacteria durante estas manifestaciones tardías sigue siendo debatida.
Se trata de formas crónicas: cutáneas, articulares o neurológicas. Desde el punto de vista clínico, son poco específicas (también se pueden encontrar aparte de la enfermedad de Lyme), a excepción de la acrodermatitis atrófica crónica.
Formas de pielLa acrodermatitis atrófica crónica , o ACA, anteriormente también llamada "enfermedad de Pick-Herxheimer", está relacionada de alguna manera con la enfermedad de Lyme: el germen se aisló en la biopsia de la lesión. Este es el síntoma más evidente de esta tercera fase, pero se ve principalmente solo en Europa y no en todos los pacientes.
La ACA comienza con un cambio en el color y la textura de la superficie de la piel, generalmente en un área expuesta al sol de las extremidades superiores o inferiores. La atrofia da como resultado superficies de la piel que se vuelven muy delgadas y transparentes, adquiriendo una apariencia que recuerda al papel de fumar arrugado y un color rojo a violáceo, a veces con la apariencia de ciertos líquenes planos . La ACA inicialmente localizada puede luego extenderse gradualmente y, a veces, volverse bilateral.
Formas reumatológicasEs una artritis de Lyme (ver sección fase secundaria) que persiste y se prolonga al ser refractaria a la terapia con antibióticos.
Formas neurológicasLa "neuroborreliosis tardía" incluye varias entidades, que incluyen encefalitis (daño cerebral) y polineuropatías (daño a los nervios). Aparecen más de 6 meses después de la picadura de la garrapata.
La encefalitis o encefalomielitis, crónica o tardía, se manifiesta por diversas alteraciones: alteraciones cognitivas, dificultad de concentración asociada en ocasiones a un estado de fatiga, dolor, debilidad muscular, alteraciones motoras…. El vínculo con la enfermedad de Lyme se reconoce cuando la síntesis de anticuerpos específicos se encuentra en el líquido cefalorraquídeo.
La polineuropatía aparece primero con picos de dolor, a veces acompañados de entumecimiento y hormigueo en las manos o los pies. Se asocia clásicamente con acrodermatitis atrófica. También se puede aislar un dolor radicular crónico que se manifiesta como ciática.
Formas discutidas o controvertidasSon poco conocidos y difíciles de relacionar formalmente con la borreliosis.
Se han descrito manifestaciones dermatológicas (distintas del linfocitoma y la acrodermatitis ): morfea , esclerodermia , dermatomiositis … pero el vínculo con la enfermedad de Lyme sigue siendo hipotético y debatido.
Algunos pacientes, después de un tratamiento antibiótico bien realizado, presentan trastornos subjetivos crónicos (cefalea, fatiga y dolor articular) mientras que el objetivo clínico y biológico está a favor de la curación. Luego hablamos de "síndrome de borreliosis post-Lyme" o síndrome de enfermedad post-Lyme PLDS . A partir de ahí, y siguiendo una confusa continuidad, surgió el término “enfermedad de Lyme crónica”. Indefinido o mal definido, reúne todo un conjunto de diversas patologías crónicas, relacionadas con la enfermedad de Lyme. Estos son reclamos, que aparecieron en los Estados Unidos en la década de 1990, y son hechos tanto por pacientes tratados y tratados, pero no curados, como por pacientes no diagnosticados o tratados previamente por la enfermedad de Lyme. Este movimiento asociativo pretende defender este diagnóstico y beneficiarse de terapias alternativas.
Diagnóstico
Diagnóstico positivo
La exploración clínica sigue siendo el elemento básico del proceso diagnóstico de una enfermedad de Lyme. Investigamos la noción de picadura de garrapata y eritema migratorio, el origen geográfico y las actividades del paciente mediante la evaluación de las lesiones más o menos características. Los diversos exámenes se organizan e interpretan de acuerdo con estos datos clínicos. En 2019, el diagnóstico de la confirmación más consensual basado en la serología en dos niveles para cada etapa de la infección, excepto en la presencia de eritema migrans ( 1 st etapa) que consideran la infección como cierta.
SerologíaExisten dificultades de diagnóstico serológico en Europa debido a la diversidad de las especies patógenas involucradas, como la de los reactivos; de ahí la falta de estandarización. Mientras que en Estados Unidos, la serología es más fácil de interpretar (criterios estándar de los CDC ), debido a la presencia de una especie patógena muy predominante ( B. Burdorgferi en sentido estricto). No obstante, en la década de 2010 , incluso en los Estados Unidos, "la variabilidad entre laboratorios era considerable y sigue siendo un problema en las pruebas de detección de la enfermedad de Lyme" .
Durante la fase primaria, el diagnóstico es exclusivamente clínico para el eritema migratorio. En esta etapa, la serología es innecesaria ya que la producción de anticuerpos aún es insuficiente. Asimismo, los datos biológicos, aún en esta etapa, suelen ser normales. La presencia de un síndrome inflamatorio importante debería sugerir otro diagnóstico.
Durante la fase secundaria, se discuten los exámenes serológicos (ensayos de anticuerpos) según el contexto. Hay dos métodos que se utilizan habitualmente en la práctica: ELISA y Western Blot . La prueba ELISA se utiliza en primera intención, si es positiva o dudosa debe ser confirmada por Western-Blot. La administración de Stevia o Serrapeptase antes de la prueba, por su efecto anti-biofilm, permite la liberación de bacterias al sistema sanguíneo lo que mejora la sensibilidad de la detección.
Esta serología se realiza en sangre (linfocitoma, afectación cardíaca, artritis, etc.), en líquido articular (artritis) o en líquido cefalorraquídeo (neuroborreliosis).
Una serología positiva tiene valor patológico solo en un contexto clínico sugerente. Por el contrario, una serología negativa en el mismo contexto anima a repetir o continuar la investigación.
PCREl propósito de la PCR es detectar la presencia de un fragmento del genoma de una borrelia. Es un examen optativo, en segunda intención, en casos dudosos (contexto clínico y epidemiológico sugerente, pero serología negativa). Se realiza en ubicaciones específicas (muestra de piel, líquido cefalorraquídeo, líquido articular) según el contexto.
La PCR es muy específica, pero no prueba una infección activa, porque el ADN de borrelia puede persistir después de su muerte (eliminación con antibióticos). También en los Estados Unidos como en Europa, la serología sigue siendo, en la práctica actual, el único método inmediatamente disponible para el diagnóstico. En 2019, “ninguna prueba serológica permite (…) diferenciar entre una infección pasada y una infección activa. El papel del internista es doble: pensar en una enfermedad de Lyme frente a síntomas focales y / o generales pero también no atribuir erróneamente a una enfermedad de Lyme síntomas que deberían abrir el campo de los diagnósticos diferenciales ” .
Un estudio ha demostrado que la infección activa se puede detectar mediante el análisis del ADN circulante libre , con mayor sensibilidad que la serología.
Diagnóstico diferencial
En la fase primaria, cuando es atípica, el eritema migratorio puede confundirse con eccema numular , eritema multiforme , dermatofitosis , etc. y, en el sureste de los Estados Unidos, a un STARI (acrónimo de enfermedad eruptiva asociada a garrapatas del sur ).
Cuando el eritema migratorio está ausente o pasa desapercibido, muchos diagnósticos pueden elevarse a la fase secundaria neurológica (encefalitis viral o mielitis, Guillain-Barré , parálisis facial a frigore , esclerosis múltiple ...), reumatológica ( artritis reumatoide , reacción de artritis , artritis juvenil, etc.).
En la fase tardía, la acrodermatitis crónica puede confundirse con trastornos relacionados con insuficiencia venosa o esclerodermia localizada. Los trastornos generales llevan a discutir la fibromialgia o la fatiga crónica .
La diferencia puede ser marcada por la serología y por el hecho de que los síntomas mejoran con la terapia con antibióticos.
La situación más compleja surge cuando un paciente es etiquetado como “ Enfermedad de Lyme crónica ” o Enfermedad de Lyme crónica con CLD . Esta entidad no es reconocida por la comunidad científica debido a la ausencia de definición de estos pacientes y a la imposibilidad de determinar la presencia de gérmenes activos que persisten después del tratamiento estándar.
Diagnóstico de Lyme crónico
En Estados Unidos, estos diagnósticos se realizarían en el marco de una “contracultura” que reúne a asociaciones, laboratorios de pruebas diagnósticas no validadas y médicos autoproclamados especialistas del afecto o “médicos alfabetizados en Lyme” ( LLMD ), con actividades de cabildeo con el Congreso de los Estados Unidos e Internet.
Estos diagnósticos de "enfermedad de Lyme crónica" se dividen en cuatro categorías:
- La categoría 1 es un diagnóstico basado únicamente en síntomas inespecíficos (fatiga, dolor crónico, trastornos cognitivos o del estado de ánimo, etc.) sin ningún trastorno biológico detectable. Estos trastornos inespecíficos están presentes en al menos el 10% de la población general, sin relación con una distribución endémica de la enfermedad de Lyme.
- La categoría 2 son pacientes con otra enfermedad (tengan o no antecedentes de enfermedad de Lyme no comprobada). Por ejemplo, a los pacientes les resulta difícil aceptar el diagnóstico de esclerosis múltiple y encontrar un médico dispuesto a tratarlos por la enfermedad de Lyme crónica.
- La categoría 3 no presenta trastornos clínicos objetivos que sugieran la enfermedad de Lyme, pero tienen anticuerpos contra B. burgdoferi . Los médicos están ofreciendo una prueba empírica de la terapia con antibióticos para tratar sus síntomas.
- La categoría 4 son los pacientes (diagnosticados y tratados con Lyme) con manifestaciones crónicas que llevan a cabo el “síndrome de borreliosis post-Lyme” o síndrome de post-enfermedad de Lyme PLDS . Estos son trastornos subjetivos que pueden persistir durante un año o más después del tratamiento. Estos pacientes plantean el problema más general de estados de fatiga y dolor crónico.
Un estudio reciente (2019) buscó estimar el número de casos de forma crónica de la enfermedad en los Estados Unidos en 2016 y 2020 . Sus resultados muestran una prevalencia "alta y creciente" de formas crónicas en Estados Unidos: según los datos disponibles, entre 69.011 y 1.523.869 personas se vieron afectadas en 2016, y en 2020 la prevalencia podría llegar a 1.944.189 casos.
Tratamiento
Terapia con antibióticos
Principios básicosEl tratamiento antibiótico tiene como objetivo curar las manifestaciones clínicas y evitar la progresión a formas secundarias y terciarias, que se obtiene mediante la erradicación completa de Borrelia. No estamos intentando obtener una serología negativa.
En la práctica, se utiliza una ciclina y, como segunda línea o en casos especiales, un β-lactámico ( cefalosporina ).
En la fase primaria (eritema migratorio), se debe prescribir amoxicilina o doxiciclina durante 14 a 21 días , como mínimo: dentro de las 72 horas si es posible para obtener mejores resultados.
En la fase secundaria y terciaria, para la neuroborreliosis, se utilizan principalmente cefalosporinas , generalmente ceftriaxona , por un período de 21 a 28 días, como mínimo; por vía venosa periférica en caso de meningoencefalitis.
Para las formas terciarias, se pueden ofrecer duraciones más largas según el caso.
En Mayo de 2019 un grupo de sociedades científicas francesas da la siguiente opinión:
“Dado el continuo entre la forma temprana localizada y la borreliosis diseminada y la eficacia de la doxiciclina para tratar la neuroborreliosis, se prefiere la doxiciclina como primera línea de tratamiento para el eritema migratorio (duración 14 días (d). Alternativa: amoxicilina) y neuroborreliosis (duración 14 días) si el tratamiento es temprano, 21 días si se retrasa (Alternativa: ceftriaxona). El tratamiento de las manifestaciones articulares de la borreliosis de Lyme se basa en doxiciclina, ceftriaxona o amoxicilina durante 28 días . Los pacientes con síntomas persistentes después de un tratamiento adecuado no deben recibir un tratamiento prolongado o repetido. Algunos pacientes presentan síntomas persistentes y pleomórficos después de un diagnóstico documentado o sospechado de borreliosis. Otra patología se diagnostica en el 80% de ellos. "
En aproximadamente el 15% de los pacientes, la terapia con antibióticos puede causar una reacción de Jarisch-Herxheimer , relacionada con la lisis de bacterias, con exacerbación de los síntomas. Esta es una reacción leve y transitoria que desaparece en unas pocas horas o en uno o dos días.
EficienciaLas infecciones tratadas en la fase primaria se curan con los antibióticos recomendados. Si la fase primaria pasa desapercibida o no se trata lo suficiente, la enfermedad continúa progresando.
Aproximadamente el 10% de los pacientes tratados, y quizás más en aquellos con neuroborreliosis, continúan teniendo trastornos subjetivos (fatiga, dolor muscular, trastornos cognitivos, etc.). Estos trastornos persisten durante más de 6 meses después de la terapia antibiótica recomendada y hasta más de 10 años, al menos de forma intermitente.
Aunque la mayoría de los pacientes mejoran con el paso de los meses, esta afección tiene un efecto duradero en la calidad de vida. Es el "síndrome post-borreliosis de Lyme", o síndrome de post-enfermedad de Lyme PLDS . En esta situación, los estudios controlados no muestran una diferencia entre la terapia antibiótica prolongada y un placebo, lo que indica que las bacterias no pueden ser responsables de los síntomas.
Tratamientos alternativos
Más o menos reconocidoSi la terapia prolongada con antibióticos no es una solución para estas condiciones crónicas, se deben implementar nuevas estrategias de manejo; sabiendo que casi el 40% de los pacientes crónicos con "borreliosis post-Lyme" mejoran con un placebo . El paciente "post-Lyme" se une a los millones de personas en todo el mundo que sufren de fatiga y dolor crónico de origen indeterminado.
Por lo tanto, los trastornos depresivos deben tratarse de acuerdo con los estándares habituales y el dolor persistente de acuerdo con un enfoque multidisciplinario similar al del tratamiento de la fibromialgia . Por tanto, existen combinaciones de fármacos (analgésicos, antidepresivos, etc.), terapias conductuales , fisioterapia y acupuntura .
Se han desarrollado técnicas de origen neuroquirúrgico , conocidas como neuromodulación por estimulación espinal, para tratar síndromes complejos de dolor crónico o dolor postoperatorio. Parecen ser capaces de reducir el dolor de los pacientes con artritis de Lyme crónica que son resistentes a los tratamientos convencionales (fármacos, fisioterapia).
No reconocido o no recomendadoSe ofrecen muchos tratamientos alternativos en la red. El problema central es que pretenden curar los síntomas de una enfermedad cuando no se prueba su existencia (los estudios citados en el párrafo anterior incluso concluyen que no existe). Sin pruebas de efectividad, lo cual es lógico ya que no se ha validado la existencia misma de la enfermedad, algunos presentan cierto riesgo de efectos adversos.
- No se recomienda la terapia con antibióticos, por ejemplo, de muy larga duración; intermitente; repetido (para el mismo episodio de Lyme); para coinfecciones sin prueba.
- Medicina hiperbárica .
- Terapias de "radiación o energía" (que pertenecen al campo de las pseudociencias)
- Terapias "nutricionales".
- Quelación de metales pesados .
- Piroterapia .
- Diversos fármacos: inmunoglobulinas, hormonas, veneno de abeja ...
Los preparados fitoterapéuticos son ofrecidos o distribuidos por varios laboratorios.
Varias plantas, y especialmente la quinina ghanesa ( Cryptolepis sanguinolenta ) y el nudo japonés (Polygonum cuspidatum), han sido estudiadas por investigadores estadounidenses de la Escuela de Salud Pública Johns Hopkins Bloomberg y probadas in vitro en cultivos de Borrelia:
"Incluso en concentraciones bajas, los extractos de estas dos plantas destruyeron las microcolonias de Borrelia e inhibieron la división celular de la forma libre de la bacteria. En 7 días, una solución al 1% de quinina de Ghana destruyó todas las bacterias, por lo que los antibióticos u otras plantas no pudieron erradicar todas las celdas ".
Un estudio muestra la actividad de ciertos aceites esenciales in vitro contra la biopelícula formada por las bacterias. La Stevia también mostró una reducción de las biopelículas in vitro .
En Francia, uno de ellos, Tic Tox , es una mezcla de aceites esenciales y propóleo desarrollada por Bernard Christophe (1949-2016), farmacéutico alsaciano especializado en fito-aromaterapia . Este producto fue suspendido en 2012, pendiente de su cumplimiento normativo, por la Agencia Nacional para la Seguridad de Medicamentos y Productos Sanitarios (AFSSAPS), que argumentó en particular que contiene salvia oficial (potencialmente tóxica según las dosis ingeridas) y un terpeno. , tuyona , además de una "falta de autorización de comercialización " (AMM).
Sin embargo, según el profesor Christian Perronne , especialista en la enfermedad de Lyme, esta decisión sería cuestionable.
Prevención
Evite la exposición a las garrapatas.
La prevención primaria (actuar directamente sobre el caso: huéspedes y vectores) es difícil debido a la diversidad del reservorio animal. Siempre se discute actuar sobre uno de los factores de emergencia (ver sección epidemiología), porque si se identifican más o menos estos factores, no se conoce bien la forma en que reaccionan entre sí. Por ejemplo, en los Estados Unidos, donde la diversidad de reservorios parece ser menor , se debate la reducción de la población de ciervos ( especialmente ciervos de cola blanca ), como un medio para reducir las enfermedades humanas.
Las medidas recomendadas son evitar la exposición a las garrapatas.
Bosques- Use ropa protectora en el bosque (zapatos cerrados, pantalones largos metidos en calcetines, camisa con cuello cerrado y mangas largas abotonadas en los puños; polainas para trabajadores forestales y recolectores de setas). La ropa de colores claros le permite ver mejor las garrapatas. Prohibir chanclas y sandalias, pantalones cortos y camisetas;
- evite las zonas de muy alto riesgo (matorrales, maleza, etc. especialmente húmedas) permaneciendo en medio de los caminos si es posible;
- limitar el manejo de la caza por parte de los cazadores;
- es posible el uso de repelentes en zonas de riesgo. Por razones toxicológicas, la impregnación de la ropa con insecticidas rara vez se utilizó (molestias y riesgo de efectos secundarios);
nota: se han desarrollado prendas de vestir profesionales y uniformes de combate revestidos con un polímero impregnado de permetrina (algodón, materiales sintéticos y mixtos); reducen el riesgo de mordeduras en más de un 95% si la prenda se lleva correctamente, según un estudio alemán. Esta protección dura al menos un año. Otro estudio (2020) solo pudo comprobar esa protección del 65% en el primer año y del 50% en el segundo año, sin que se detectaran efectos inmediatos en la salud de los portadores de la prenda. Algunas especies de garrapatas (o etapas de desarrollo) son más sensibles a la permetrina que otras. Un estudio de laboratorio (2019) mostró que después de 16 días de uso y 16 ciclos de lavado / secado a máquina , 50-90% de la permetrina empapada en camisas, pantalones y calcetines tratados en fábrica se eliminó de las telas (ahora fuente de contaminación del agua, y haciendo que la prenda sea significativamente menos protectora; después de 1 hora de contacto con la tela, del 31 al 67% de las garrapatas aún mostraban un movimiento normal, en lugar de huir de la tela o permanecer inmovilizadas allí). Por otro lado, los zapatos tratados, usados pero no lavados, han permanecido tan tóxicos para las garrapatas como lo eran originalmente. - inspeccione usted mismo cuidadosamente después de caminar o trabajar en el bosque; en particular las axilas, el ombligo, los genitales, los pliegues de la rodilla, sin olvidar en los niños la cabeza y el cuero cabelludo.
Un estudio de ciencia participativa lanzado en el verano de 2017 en Francia por el INRA , basado en una aplicación ("Señalización de garrapatas") que permite mapear los lugares donde han tenido lugar las picaduras de garrapatas, acaba de demostrar que, contra todas las expectativas, si el 53% de los casos se refieren al bosque, 1/3 (27% exactamente) de las picaduras declaradas voluntariamente tuvieron lugar en los jardines de casas particulares, y "solo el 10% en prados". Se invita a los inscritos a tomar una fotografía de la garrapata y enviarla por correo a los investigadores (54 presentaciones por día en promedio enMayo de 2018). Un sesgo probable juega a favor de las declaraciones sobre los seres humanos y, sin duda, la audiencia de los encuestados no es representativa de toda la población. De los 1.254 informes de mordeduras en animales, 4.198 fueron en humanos. Las picaduras afectan en primer lugar a personas de 20 a 40 años (30% de los casos) y de 40 a 60 años (26%). Esta tasa se reduce al 17% entre los jóvenes de 5 a 20 años. Le siguen las personas mayores de 60 años (15% de los casos) y los niños menores de 5 años (12% de los casos). En el caso de los animales, las declaraciones se refieren principalmente a perros (45% de los casos) y gatos (44%) y, en menor medida, a caballos y bovinos (6 y 5% de los casos).
Entre las medidas a veces recomendadas:
- mantener sus jardines, en particular cortando hierba alta en áreas frecuentadas y destruyendo o quitando hojas muertas;
- la abundancia de garrapatas podría reducirse en algunas áreas (parques y jardines forestales suburbanos ...) mediante una zona de amortiguación libre de basura de hojas muertas (por ejemplo, cubierta con mantillo o grava entre el borde del bosque y las áreas de caza (niños, picnic, etc.) . ) y mediante medidas que prohíban la intrusión de animales como el jabalí o el ciervo), al tiempo que se fomentan los depredadores naturales de las garrapatas: en las zonas rurales, los pollos , que se alimentan de ellas, parecen limitar sus poblaciones.
- Equipe a las mascotas con collares de garrapatas, inspecciónelas con regularidad, especialmente después de regresar de un paseo por el bosque, y elimínelas de las garrapatas. Los insecticidas adecuados se pueden rociar a los perros;
- Los gatos son extremadamente sensibles a los productos químicos. No les aplique insecticidas o repelentes sin el consejo de un veterinario;
- Se creó un modelo predictivo de riesgo para perros combinando factores climáticos, geográficos y sociales, con resultados de pruebas serológicas. Este modelo podría ser útil para ayudar a los veterinarios a evaluar el riesgo para los perros y quizás indirectamente para los humanos.
Estas precauciones no siempre son suficientes y no son 100% efectivas, porque las ninfas de garrapatas están en el límite de visibilidad (1 a 2 mm ) y su picadura es indolora. Además, las mascotas pueden traer garrapatas a casa, lo que resulta en contaminación cruzada con los humanos.
Cuidado de las picaduras de garrapatas
La contaminación requiere un largo tiempo de presencia de la garrapata en la piel. Si el riesgo comienza en la primera hora, es proporcional al tiempo de contacto, con un máximo entre 48 y 72 horas (la comida de sangre de la garrapata dura de 2 a 5 días).
Si la garrapata se quita de la piel dentro de las primeras 36 horas después de que se haya adherido, el riesgo de contaminación se considera bajo; menos del 1%, porque las borrelia aún no se encuentran en las glándulas salivales de la garrapata, sino en su tracto digestivo. Para infectar al huésped, todavía tienen que migrar desde el tracto digestivo a las glándulas salivales, lo que puede demorar de 2 a 3 días , este período puede acortarse en Europa.
Eliminación de garrapatasLos métodos populares, que utilizan una gota de varios productos destinados a adormecer, sofocar o despegar la garrapata son demasiado lentos o corren el riesgo de regurgitar la garrapata: éter, bencina, gasolina, diésel, aceite comestible, esmalte de uñas, calor con un cigarrillo encendido ... No se trata de esperar, por lo que hay que retirar la garrapata lo antes posible, sin tocarla.
En las farmacias se venden varios modelos de pinzas especiales o tipos de pequeñas patas de gallo que permiten extraer las garrapatas girándolas suavemente (con un modelo más pequeño para larvas y ninfas). No debes tirar, sino girar suavemente como para desenroscar, puedes extraer fácilmente la garrapata, al menos si no lleva demasiado tiempo anclada. Esta acción evita el riesgo de dejar la tribuna o la cabeza y su cemento pegados en la piel, lo que puede provocar una infección o incluso un absceso.
En ausencia de un extractor de garrapatas, puede usar unas pinzas finas para tirar de la garrapata sin torcerla ni aplastarla.
Tratamiento de heridaUna vez que se ha eliminado la garrapata (y no antes, no hay producto en una garrapata adherida), la herida debe desinfectarse y controlarse cuidadosamente. En esta etapa, no se recomienda la terapia antibiótica profiláctica para una simple picadura de garrapata, debido a la baja probabilidad de contaminación. Esto se puede discutir en ciertos casos específicos (mujeres embarazadas, persona inmunodeprimida, etc.) o incluso en una zona hiperendémica, cuando la garrapata se retira tarde y se llena de sangre.
Lo mismo ocurre en los Estados Unidos, donde, después de la picadura de una garrapata, los CDC generalmente no recomiendan la profilaxis con antibióticos . Las excepciones son en áreas hiperendémicas donde cualquier persona mayor de 8 años mordida puede recibir una dosis única de 200 mg de doxiciclina dentro de las 72 horas posteriores a la extracción de la garrapata. Para ello, se deben cumplir todas las condiciones siguientes: sin contraindicación para la doxiciclina, garrapata de I. scapularis identificada, garrapata congestionada de sangre con un tiempo de adhesión estimado de más de 36 h .
Después de una picadura de garrapata, el control de la herida es necesario y suficiente. En los días o semanas siguientes, es imperativo consultar a un médico para la terapia antibiótica adecuada, si aparece una mancha y crece gradualmente (eritema migratorio). Lo mismo ocurre en caso de aparición de un estado febril o gripe (más a menudo en América que en Europa).
Vacuna
A partir de 2020, ya no hay una vacuna humana disponible contra la enfermedad de Lyme.
Existen vacunas veterinarias, incluso para perros, basadas en la totalidad de las bacterias muertas o en subunidades ( proteínas de superficie OspA o OspC ).
Primera vacunaUna vacuna (recombinante), Lymerix de Smith-Kline-Beecham , se ha comercializado en los Estados Unidos desdediciembre de 1998 (después de la aprobación de la FDA) en Febrero de 2002. Se dirigió a una de las proteínas de superficie más comunes de B. Burgorferi , OspA . Se ha recomendado para personas en riesgo en áreas endémicas y se han distribuido 1,4 millones de dosis. Los estudios han demostrado que su efectividad está en el rango del 70 al 80% sin efectos secundarios significativos, pero las incertidumbres sobre su efecto protector a largo plazo implican que pueden ser necesarios refuerzos anuales.
En 1999 , los rumores que asociaban la vacuna a la artritis autoinmune , dieron lugar a procesos judiciales, por lo que 121 demandantes iniciaron una acción colectiva . Los estudios de los CDC y la FDA no confirman una relación causal, ya que creen que los beneficios de la vacuna superan los riesgos. Por lo tanto, la vacuna permanece disponible para el público, pero las ventas colapsan debido a la cobertura de los medios de los ensayos en curso y las controversias sobre el riesgo teórico de autoinmunidad.
En 2002 , el fabricante retira su vacuna del mercado por su cuenta, por motivos económicos. En 2003 , se llegó a un acuerdo con los demandantes: suspendieron todos los procesos judiciales a cambio de un millón de dólares para reembolsar los gastos de abogados y tribunal.
La investigación en cursoLa investigación de vacunas busca apuntar a las proteínas de superficie más constantes de las bacterias. Se está preparando una vacuna de este tipo para Europa y Estados Unidos.
Según Stanley Plotkin , la vacuna ideal contra la enfermedad de Lyme debe tener al menos un 80% de efectividad durante dos años, en ambos lados del Atlántico, ser bien tolerada, no contener un determinante antigénico de riesgo teórico y ser utilizable en niños. También debe ser aceptado por el público; Para evitar los errores de comunicación cometidos durante el asunto Lymerix , una nueva vacuna deberá satisfacer una demanda concertada de los actores de la salud pública y del público para que haya un mercado para esta vacuna.
El laboratorio de Valneva está trabajando actualmente En una vacuna para 2025 y comenzará a realizar pruebas en 15.000 sujetos a partir de 2022.
Otra estrategia es romper el ciclo de vida de la bacteria con una vacuna (o vacunas) dirigida a reservorios animales y / o vectores (garrapatas):
- en América del Norte se está considerando la vacunación oral de un reservorio animal como el ratón Peromyscus leucopus , sobre el modelo de vacunación oral de zorros contra la rabia , que ha demostrado ser muy eficaz;
- otras investigaciones apuntan al vector y, más específicamente, a los componentes de la saliva de las garrapatas. Esto, teóricamente, tendría la ventaja de proteger contra todas las enfermedades transmitidas por garrapatas.
Costos económicos
Las enfermedades transmitidas por garrapatas (enfermedad de Lyme en particular) tienen un costo anual que asciende a varias decenas de millones de euros por año para muchos países (por ejemplo, costo estimado de 20 millones de euros / año para los países -Bajo y 80 millones de euros / año para Alemania para mediados de la década de 2010.
Controversia social
Se trata de tesis y argumentos desarrollados por una corriente alterna, contrarios a las recomendaciones oficiales de las sociedades científicas que, por su parte, logran consensos a nivel internacional y que son retomadas por todas las autoridades sanitarias de Norteamérica y Europa.
Esta corriente alterna apareció en los Estados Unidos en la década de 1990, donde los médicos se reunieron en una Sociedad Internacional de Enfermedades de Lyme y Asociadas (ILADS), con el apoyo de asociaciones de pacientes. Esta corriente sostiene que las recomendaciones oficiales son demasiado restrictivas, que la enfermedad está infradiagnosticada y subtratada. Por lo tanto, busca promover nuevas actitudes terapéuticas con las autoridades públicas, en particular mediante el reconocimiento de una “enfermedad de Lyme crónica”, y de una terapia antibiótica de muy larga duración, a veces asociada a terapias no convencionales.
En 2019, una revisión de las recomendaciones europeas y americanas sobre el diagnóstico de la enfermedad de Lyme, muestra que según las directrices de 16 sociedades científicas de 7 países, solo una es diferente de las demás (una sociedad alemana, la Deutsche Borreliose-Gesellschaft, no reconocida como sociedad académica por las autoridades alemanas). La conclusión es "Contrariamente al acalorado debate que tiene lugar en Internet y en los medios europeos y estadounidenses, nuestro análisis muestra que la mayoría de las recomendaciones científicas médicas asociadas con una puntuación cualitativa alta coinciden en los métodos de diagnóstico clínico de la enfermedad de Lyme" .
Supuestos en discusión
El término Lyme crónico (o síndrome postratamiento ) puede referirse a recaídas, síntomas que persisten al suspender el tratamiento con antibióticos o complicaciones crónicas reconocidas atribuidas a la enfermedad de Lyme. También puede referirse a formas crónicas impugnadas por la mayoría de la comunidad médica; o ambos, lo cual es confuso. La forma crónica de la enfermedad ha sido objeto de definiciones, por ejemplo en Suiza en 2005 “(evidencia clínica y de laboratorio documentada de una infección previa por B. burgdorferi , ciclo completo de terapia antibiótica apropiada, síntomas que incluyen fatiga, artralgia, mialgia, disfunción cognitiva o dolor radicular que persiste durante más de 6 meses, asociación oportuna plausible entre la infección documentada por B. burgdorferi y el inicio de los síntomas (es decir, síntomas persistentes o recurrentes que comenzaron dentro de los 6 meses posteriores a la finalización de la terapia con antibióticos recomendada para la borreliosis de Lyme temprana o tardía ) y exclusión de otras causas somáticas o psiquiátricas de síntomas) ” o en los Estados Unidos en 2019.
La naturaleza crónica, inicialmente silenciosa, luego la resistencia a los antibióticos de la enfermedad puede tener varias explicaciones (compatibles entre sí):
- formas "quísticas" persistentes de la bacteria ( pleomorfismo ); ya en 1995 , se detectó que en reacción a la penicilina y la doxiciclina (pero no a la ceftriaxona), la bacteria puede tomar formas particulares que pueden permitir su supervivencia en los tejidos de ciertos pacientes "a pesar de una terapia aparentemente adecuada" ; estas formas persistentes podrían, según los autores, ser la fuente de un "estímulo antigénico continuo que conduzca a quejas de borreliosis de Lyme crónica" .
- una forma L (reversible) de la bacteria (sospechada en 1996 y confirmada en 2008);
- persistencia en una biopelícula , demostrada en 2008.
En 2014, los autores consideraron que no se había demostrado la participación de estas 3 variantes morfológicas en una forma crónica de la enfermedad de Lyme; otros en 2019 creen que la probabilidad de que la enfermedad de Lyme crónica pueda ocurrir como resultado de infecciones persistentes es real.
En 2015, un autor (Paul M. Lantos) cuestiona el concepto de “criptoinfecciones” (ligadas a coinfecciones, cuando la garrapata transmite varias enfermedades), especialmente cuando se sabe que las bacterias no son transmisibles por garrapatas, incluso patógenos fantasiosos. mencionado.
Para ILADS, la enfermedad es ubicua y está muy extendida en formas o transmisiones no reconocidas (por ejemplo, sexual). ILADS en 2019 definió la forma crónica de la enfermedad de Lyme como "enfermedad multisistémica con una amplia gama de síntomas y / o signos que están presentes de forma continua o intermitente durante al menos seis meses" . Los síntomas persistentes son fatiga, dolor, alteraciones del sueño, cognitivas y neurológicas, a tratar con antibioterapia prolongada. La forma crónica resulta de “una infección activa y continua con uno de los muchos miembros patógenos del complejo Borrelia burgdorferi sensu lato (Bbsl). La infección tiene periodos de latencia variables y los signos y síntomas pueden aumentar, disminuir y migrar ” . ILADS distingue entre la forma crónica no tratada y la tratada previamente (en este último caso con manifestaciones de forma crónica que persisten o reaparecen después del tratamiento y se presentan de forma continua o según un patrón de recaída / remisión durante un período de seis meses o más). Estas definiciones se desarrollaron sobre la base de una "revisión sistemática de más de 250 artículos revisados por pares en la literatura internacional" . Según un estudio reciente (2015), los síntomas pueden persistir durante más de 10 años, sin estar asociados con un deterioro funcional del paciente, ni con una cepa particular de B. burgdorferi.
Según un estudio prospectivo que siguió a 174 hombres y 109 mujeres diagnosticados inicialmente con claridad (eritema migratorio y confirmación por cultivo) a los seis meses, 12 meses y posteriormente hasta los 20 años, no hay diferencia en los síntomas entre hombres y mujeres para los síntomas iniciales. , Tasa de serorreactividad de B. burgdorferi o frecuencia de síntomas posteriores al tratamiento, incluidos 71 hombres y 57 mujeres que pudieron ser seguidos durante 20 años, pero "las mujeres tenían muchas más probabilidades que los hombres de regresar para las visitas de seguimiento" .
Para la mayoría de la comunidad médica, la corriente de “Lyme crónica” sería un conjunto de microbiología, inmunología y farmacología “alternativas”, difundidas en Internet y otros medios, mezcladas con testimonios de pacientes. Esta corriente representaría el 2% de los médicos en Connecticut, una de las regiones donde la endémica de Lyme es más fuerte; estas serían actitudes basadas en suposiciones o creencias subjetivas, y no en evidencia científica validada. La forma crónica de la enfermedad se expresa con mayor frecuencia mediante síntomas subjetivos, las diversas pruebas (análisis de orina, recuento de linfocitos CD 57, inmunofluorescencia para mostrar formas L de Borrelia , etc.) han sido desarrolladas por "laboratorios especializados de Lyme" y no estar clínicamente validado o no aprobado por la FDA .
Los argumentos de los defensores de la forma crónica también se basan en el modelo animal ( perros , ponis, etc.) que muestra que las borrelias pueden persistir a pesar de un tratamiento antibiótico adecuado. Pero según sus detractores, esta presencia es frecuente en animales infectados, sin presentar ninguna enfermedad.
Estos argumentos científicos van acompañados de apelaciones a las autoridades públicas, o incluso procesos judiciales contra sociedades médicas eruditas, acusadas de tener vínculos ocultos con compañías de seguros para limitar la duración, por lo tanto, el reembolso de la terapia antibiótica. En Connecticut , se llevó a cabo una investigación sin precedentes sobre la Sociedad Estadounidense de Enfermedades Infecciosas (IDSA ), una sociedad culta acusada de violar la ley antimonopolio , con el argumento de que sus recomendaciones eran las únicas que debían tomar las autoridades sanitarias.
Aparentemente, se encuentra un compromiso temporal con la publicación, en 2011 (revisada en 2014), de las recomendaciones de ILADS en un sitio oficial, pero en realidad es un sitio que solo enumera las recomendaciones sin validarlas. Por lo tanto, las recomendaciones oficiales estadounidenses siguen siendo las publicadas en los sitios de los CDC o NIH .
Según el profesor Lantos, miembro del panel de recomendaciones de la IDSA, tales controversias persistirán "mientras los pacientes sigan padeciendo síntomas inexplicables que afecten a su calidad de vida" .
Situación francesa
La definición, los límites y el valor de los medios de diagnóstico para la "enfermedad de Lyme crónica" siguen siendo objeto de debate. Esta cuestión se ha convertido en un problema social, debido a las controversias que provoca. En Francia, conduciría a una doble pérdida de confianza "para los pacientes que pierden la confianza en su médico, para los médicos que pierden la confianza en sí mismos" en un clima de desconfianza recíproca.
Asociaciones de pacientesLas principales asociaciones son Lyme sans frontières, fundada en 2012, 700 miembros en Francia y Bélgica en 2013, el 90% de los cuales están enfermos; y France Lyme creada en 2008, con 400 miembros en 2014 y 2.700 miembros de la31 de marzo de 2019. Hay otras asociaciones más pequeñas con vocación local. Un informe de 2014 de la Alta Autoridad para la Salud (HAS) afirma que la mayoría de los directivos son mujeres y pertenecen a la categoría de ejecutivos y profesiones intelectuales superiores.
Según el informe HAS de 2014, que cita a un sociólogo, existe un “enconado cara a cara” entre la legitimidad de las asociaciones y la autoridad de la ciencia. Los primeros defienden sus conocimientos mediante la experiencia personal e íntima, los segundos se basan en la observación y la deducción científica ( medicina basada en hechos ). Aún así, según el informe, estas asociaciones están más cerca de la actitud de los anti-vacunas que de la de las asociaciones que luchan contra el VIH, porque "a menudo permanecen tensas por su resentimiento contra la profesión médica y los expertos". Y por tanto, el sistema de actuación en torno al tema de la borreliosis de Lyme ofrece hoy el espectáculo de la legitimidad social sin autoridad ” .
Si estas asociaciones comparten ciertos rasgos con los militantes contra la contaminación por el VIH - orientación “ comunitaria ” (nos apoyamos en una patología específica), ambivalencia de las relaciones con los poderes públicos entre colaboración y confrontación, legitimidad de la “pericia” de los pacientes (la “ Legitimidad incrustada del paciente ”) versus la experiencia de los científicos y la profesión médica, y así sucesivamente. - se distinguen por la ausencia de universalismo (al servicio de la salud pública en un campo de riesgo determinado), la ausencia de profesionalización de activistas tendientes a convertirse en expertos reconocidos consultados por las autoridades públicas, la ausencia de capital social (densidad de redes de relaciones con científicos, medios de comunicación y política).
El informe señala: "Lejos de cualquier 'delirio', la protesta de las asociaciones es por el contrario perfectamente racional, lo que no impide que algunos de sus argumentos sean muy débiles" y "También los activistas defienden una noción esencialista de la ciencia - de base arcana en una experiencia íntima - para reclamar el monopolio de ser las víctimas de la enfermedad y, al menos, quieren creerlo, los únicos que no esconden la verdad (porque están libres de todo conflicto de intereses) ” .
Debates en cursoHasta junio 2018, la atención en Francia se basó en una conferencia de consenso de 2006, que estableció protocolos oficiales.
- En 2014 , la Alta Autoridad Sanitaria (HAS) recordó que “Como el resto de jugadores, las asociaciones deben poder expresarse libremente. También deben ser escuchados. Si bien no les corresponde a ellos hablar sobre la ciencia o las políticas de liderazgo, les corresponde a ellos, por otro lado, hacer que se escuche la voz de los pacientes ”. Para salvar el diálogo y la confianza necesarios, el HAS hace de la borreliosis de Lyme no solo un hecho biomédico, sino también un hecho social . Ofrece una escucha más abierta de las historias y discursos de los pacientes a través de la investigación en ciencias sociales .
- En 2015 , la oposición presentó en febrero un proyecto de ley sobre esta enfermedad, que fue rechazado, pero seguido de varias preguntas sobre el reconocimiento de la enfermedad.
- En 2016 , Matthias Lacoste inició una huelga de hambre en junio para alertar a las autoridades sanitarias y por un “ derecho a la curación ”. En julio, más de cien médicos franceses, incluido Christian Perronne (jefe del departamento de enfermedades infecciosas del hospital Garches ) y asociaciones de pacientes ( France Lyme , Lyme sans frontières , Lymp'act ... se agruparon en la Federación Francesa contra las enfermedades transmitidas por vectores enfermedades, garrapatas) se quejan de una situación que no toma en cuenta su vivencia y su vivencia. Marisol Touraine , entonces Ministra de Asuntos Sociales y Salud,
presentó un plan nacional de control de la enfermedad de Lyme enseptiembre de 2016. - En 2018, las críticas se centraron en la prueba serológica considerada no suficientemente confiable, y en la existencia de una forma crónica que a veces no se cura con 3 semanas de terapia con antibióticos ”; con, por tanto, una subestimación del número de casos crónicos. El reconocimiento no oficial de la forma crónica induciría modalidades de tratamiento que a veces son inadecuadas.
Estas críticas son rechazadas por la SPILF ( sociedad francófona de patología infecciosa ) que considera que las recomendaciones de 2006 siguen siendo válidas a la luz de los conocimientos actuales; lo mismo para la Academia de Medicina .
la20 de junio de 2018, HAS publica nuevas recomendaciones de manejo para la borreliosis de Lyme. Confirman (especificándolos) los protocolos de diagnóstico y tratamiento ya adoptados, pero al igual que en Estados Unidos, se distingue un "síndrome posborreliosis de Lyme" o PLDS Post-Lyme Disease, el HAS distingue "la / la sintomatología / persistente síndrome polimórfico tras posible picadura de garrapata ”o SPPT. Esta denominación de compromiso (falta de consenso) debería mejorar la atención al paciente. la2 de julio de 2018, la Academia de Medicina "expresa claramente su profunda decepción" por este texto. Entonces la19 de julio de 2018, un grupo de sociedades científicas y profesionales se niega a respaldar este nombre de SPPT y a seguir sus recomendaciones.
EnSeptiembre de 2018(tres meses después de la publicación de las recomendaciones HAS), Jérôme Salomon ( Director General de Salud ), todavía en busca de un consenso, pidió a Pierre Tattevin, presidente del SPILF "desarrollar nuevas recomendaciones prácticas para la prevención, el diagnóstico y el tratamiento de la borreliosis de Lyme y otras enfermedades transmitidas por garrapatas ... ". Por su parte, el HAS explicó que antes de publicar sus recomendaciones, intentó en vano llegar a un consenso con el SPILF. Por lo tanto, publicó estas recomendaciones sin la firma de SPILF, porque estaba convencida de que reflejaban el estado de la técnica, pero estableciendo dos reuniones por año para actualizar las recomendaciones a la luz de los avances científicos, esperando dar lugar a recomendaciones. con el SPILF que en 2019 “todavía considera que las pruebas de cribado son efectivas” y que no existe una forma crónica de la enfermedad. - En 2019 , el10 de abril, el Senado debe escuchar a Jérôme Salomon y Dominique Le Guludec (presidente del HAS).
- la 7 de mayo de 2019, el Boletín Epidemiológico Semanal publica un estudio que muestra que en una serie de casos con un diagnóstico de sospecha de Lyme, el diagnóstico se confirmó en menos del 10% de los casos, con un presunto fracaso del tratamiento antibiótico en el 80% de los casos, el 80% de los pacientes tenían otra enfermedad. Según el columnista del boletín, existe un sobrediagnóstico y sobretratamiento significativo de la enfermedad de Lyme, una tendencia que se encuentra en el extranjero. Esto plantea un problema ético de salud pública: al elaborar recomendaciones de tratamiento, ¿se pueden tener en cuenta modelos alternativos en ausencia de hechos convincentes?
Facilidades de ivestigación
En Estados Unidos, donde se estima que a pesar de las acciones de información y prevención, el número de casos de enfermedad de Lyme prácticamente se triplicó de 1990 a 2019 (más de 300.000 casos / año), las acciones de prevención y manejo de la enfermedad se ven frenadas por inadecuadas diagnósticos (con una subestimación del número de casos: 30.000 casos declarados oficialmente de enfermedades transmitidas por garrapatas en los Estados Unidos por año, en comparación con probablemente 300.000 en la realidad), señaló el New England Journal of Medicine . El fabricante de la única vacuna disponible contra la enfermedad de Lyme la retiró en medio de la disminución de las ventas y los problemas de responsabilidad.
En 2018 , los NIH gastaron $ 23 millones solo en la enfermedad de Lyme en 2018, para un total de $ 56 millones asignados a todas las enfermedades transmitidas por garrapatas. En 2019 , luego de la opinión de un grupo asesor por mandato del gobierno de Estados Unidos (opinión alarmante y concluyendo sobre la necesidad de incrementar acciones y recursos financieros para la investigación de enfermedades transmitidas por garrapatas a nivel federal), el NIH elaboró un nuevo plan estratégico para combatir estas enfermedades, y enAbril de 2019, lanzaron una convocatoria de propuestas para la prevención de enfermedades transmitidas por garrapatas, dotada con 6 millones de dólares para 2020. Por su parte, según la revista Science , los científicos esperan obtener aún más dinero para mejorar el diagnóstico de la enfermedad y los medios para tratarla.
Un arma biológica
Ya en 1949 , traído a los Estados Unidos como parte del programa Operación Paperclip , un científico nazi desertor en los Estados Unidos llamado Erich Traub colaboró en Fort Detrick, donde supuestamente infectó ganado, caballos y cerdos con la fiebre aftosa. virus. En 2004, un abogado de Long Island , Michael Carroll, publicó un libro llamado "Lab 257", en el que afirmaba que Erich Traub también habría manipulado las garrapatas aumentando sus cantidades de " Borrelia " para hacerlas más contagiosas en el mundo. Plum. Island Animal Disease Center, un sitio biológico-militar a pocas millas de la costa de la ciudad de Lyme . Las garrapatas se han escapado de la isla, especialmente en aves migratorias.
En la década de 1970, estalló una extraña epidemia de dolor en las articulaciones en el condado de Lyme en los Estados Unidos. La brusquedad de la epidemia y su relativa proximidad geográfica al Centro de Enfermedades Animales de Plum Island han dado lugar a una forma de sospecha.
El representante republicano de Nueva Jersey, Chris Smith, aprobó una enmienda que busca iniciar una investigación sobre las acusaciones de que un laboratorio militar es la fuente de la enfermedad de Lyme. "Varios libros y artículos sugieren que se llevó a cabo una extensa investigación en instalaciones militares de Estados Unidos, incluidas Fort Detrick, Maryland y Plum Island , Nueva York, para utilizar garrapatas y otros insectos como armas biológicas".
Pero la acusación de experimentos en base a la contaminación de moscas, mosquitos y garrapatas, fue revivida por un libro publicado en mayo de 2019: "Bitten, la historia secreta de la enfermedad de Lyme y biológicas" por Kris Newby, un científico de la Universidad de Stanford que tiene a sí misma contrajo la enfermedad de Lyme. En su libro, Kris Newby cita en particular a Willy Burgdorfer , entomólogo y bacteriólogo suizo-estadounidense que en 1981 identificó el germen responsable de la enfermedad de Lyme: Borrelia Burgdoferi , cuyo nombre se deriva del suyo.
Willy Burgdofer dice que trabajó en armas biológicas para el ejército estadounidense durante la Guerra Fría . Sus responsabilidades incluían, dice, criar pulgas, garrapatas, mosquitos y otros insectos chupadores de sangre e infectarlos con patógenos capaces de transmitir enfermedades a los humanos. Y sería según Willy Burgdofer, uno de esos experimentos que habría salido mal y provocado la epidemia de Lyme en Estados Unidos.
El profesor Christian Perronne , presentado en los medios de comunicación como especialista en la enfermedad de Lyme, dijo en 2016 que la explosión de la enfermedad de Lyme, escondida por "los militares y científicos estadounidenses bajo su control" , se debe a una proliferación de garrapatas mal controladas traficadas por los nazis. investigador de virología - Erich Traub - trasladado a los Estados Unidos como parte de la Operación Paperclip al final de la Segunda Guerra Mundial.
Personalidades alcanzadas
- Avril Lavigne
- Shania Twain
- Elena Delle Donne
- Bella hadid
- Ashley Olsen
- Alec Baldwin
- Canal Fabien
- George W. Bush
- Pierrick Fédrigo
- Justin Bieber
- Richard Gere
Notas y referencias
- Gwenaël Vourc'h et al. , Zoonosis: Estas enfermedades que nos unen a los animales , Éditions Quæ , coll. "EnjeuxScience",2021( ISBN 978-2-7592-3270-3 , leído en línea ) , Algunos ejemplos de enfermedades zoonóticas, "Borreliosis de Lyme", p. 79-81, acceso libre.
- (en) Wynne Parry, "La momia del hombre de hielo puede contener la evidencia más temprana de la enfermedad de Lyme " en Live Science (consultado el 13 de marzo de 2020 ) .
- Cosson JF (2019) Ecology de la enfermedad de Lyme ; Salud pública, 1 (HS), 73-87.
- " En los Estados Unidos, los funcionarios electos quieren saber si los militares usaron garrapatas como armas biológicas "
- (en) Owen Dyer , " El Pentágono de los Estados Unidos investigará las afirmaciones que dicen que la enfermedad de Lyme es un arma biológica que se escapó de la guerra fría " , BMJ , vol. 366,19 de julio de 2019, l4784 ( ISSN 0959-8138 y 1756-1833 , PMID 31324616 , DOI 10.1136 / bmj.l4784 , leído en línea , consultado el 20 de julio de 2019 )
- (en) Robert D. Leff, Lyme Borreliosis , Cambridge, Cambridge University Press ,1993, 1176 p. ( ISBN 0-521-33286-9 ) , pág. 852-854en The Cambridge World History of Human Disease, KF Kiple (eds).
- (en) Allen C. Steere , Stephen E. Malawista , David R. Snydman y Robert E. Shope , " Una epidemia de artritis oligoarticular en niños y adultos en tres comunidades de Connecticut " , Arthritis & Rheumatism , vol. 20, n o 1,1977, p. 7–17 ( ISSN 1529-0131 , DOI 10.1002 / art.1780200102 , leído en línea , consultado el 4 de julio de 2021 )
- (en) Johnson RC, FW Hyde GP Schmid y DJ Brenner " Borrelia burgdorferi sp. nov .: agente etiológico de la enfermedad de Lyme » Int J Syst Bacteriol . 1984; 34: 496-497.
- Barbour, AG, W. Burgdorfer, SF Hayes, O. Péter y A. Aeschlimann. "Aislamiento de una espiroqueta cultivable de garrapatas Ixodes ricinus de Suiza" Current Microbiology 1983; 8: 123-126.
- (en) Ryan KJ, Ray CG; Microbiología Médica Sherris ; 4 ª edición (página 434-437) Ed: McGraw Hill, 2004; ( ISBN 978-0-8385-8542-9 )
- E. Pilly, Enfermedades infecciosas y tropicales: todos los elementos de enfermedades infecciosas , París, Alinea Plus,2018, 720 p. ( ISBN 978-2-916641-66-9 ) , pág. 377-378.
- (en) E. Claudia Coipan , Setareh Jahfari Manoj Fonville y G. Anneke Oei , " Presencia desequilibrada del tipo de secuencia multilocus de Borrelia burgdorferi sl en las manifestaciones clínicas de la borreliosis de Lyme " , Infección, Genética y Evolución , vol. 42,agosto de 2016, p. 66–76 ( DOI 10.1016 / j.meegid.2016.04.019 , leído en línea , consultado el 24 de septiembre de 2020 )
- Sylvie De Martino, " La borréliose de Lyme ", La Revue du Praticien , vol. 55,2005, p. 471-477.
- Steere AC & al. (2016) Borreliosis de Lyme . Nature Reviews Disease Primers, 2, 16090. doi: 10.1038 / nrdp.2016.90
- (en) Michael K. Faulde y Martin Rutenfranz , “ patrón de infestación por garrapatas humana, la tasa de picadura de garrapata, y asociado Borrelia burgdorferi sl riesgo de infección durante la exposición ocupacional garrapata en la zona de entrenamiento militar Seedorf, el noroeste de Alemania ” , en garrapatas y enfermedades transmitidas por garrapatas ,septiembre 2014( DOI 10.1016 / j.ttbdis.2014.04.009 , consultado el 24 de septiembre de 2020 ) ,p. 594–599
- Evison J, Aebi C, Francioli P, Peter O, Bassetti S, Gervaix A, Zimmerli S, Weber R, “ Diagnóstico y tratamiento de la borreliosis de Lyme en adultos y niños: recomendaciones de la Sociedad Suiza de las enfermedades infecciosas: Lyme borreliosis 1 st parte: epidemiología y diagnóstico [ Enfermedad de Lyme parte I : epidemiología y diagnóstico ] " Rev Med Suisse , vol. 2, n o 60,2006, p. 919-24. ( PMID 16673723 , leer en línea [html] )
- F. Rodhain, “ Enfermedad de Lyme: epidemiology ”, La Revue du Praticien , vol. 39, n o 15,18 de mayo de 1989, p. 1291-1293.
- Por Le Parisien con AFP El 27 de abril de 2021 a las 7:46 p.m. , " Enfermedad de Lyme: 30% de las garrapatas portadoras de un agente infeccioso, pican en los jardines en aumento " , en leparisien.fr ,27 de abril de 2021(consultado el 28 de abril de 2021 )
- (en) SM Dunham-Ems, MJ Caimano, U. Pal, CW Wolgemuth, Eggers CH, A. Balic y JD Radolf, " Imágenes en vivo revelan una forma bifásica de diseminación de Borrelia burgdorferi dentro de las garrapatas " , J Clin Invest , vol. . 119, n o 12,2009, p. 3652–3665 ( DOI 10.1172 / JCI39401 , leer en línea )
- (en) Tilly K, Rosa PA, Stewart PE. “ Biología de la infección por Borrelia burgdorferi ” Infect Dis Clin North Am . 2008; 22: 217-234.
- INRA , “ Reservorio de investigación, vector de soluciones: el papel clave del INRA en las enfermedades transmitidas por garrapatas ” , en www.inra.fr ,9 de mayo de 2017(consultado el 17 de diciembre de 2017 )
- " Marisol Touraine lanza el Plan Nacional para combatir la enfermedad de Lyme y las enfermedades transmitidas por garrapatas ", Ministerio de Solidaridad y Salud ,29 de septiembre de 2016( leer en línea , consultado el 17 de diciembre de 2017 )
- Allen C. Steere , Frank Strle , Gary P. Wormser y Linden T. Hu “ la borreliosis de Lyme ”, Nature Reviews. Cebadores de enfermedades , vol. 2,15 de diciembre de 2016, p. 3. ( ISSN 2056-676X , PMID 27976670 , PMCID PMC5539539 , DOI 10.1038 / nrdp.2016.90 , leído en línea , consultado el 30 de abril de 2018 )
- (en) Dennis DT, Piesman, JF. “Descripción general de las infecciones transmitidas por garrapatas en humanos” En: Goodman JL, Dennis DT, Sonenshine DE, eds. Infecciones humanas transmitidas por garrapatas . Washington, DC: ASM Press , 2005.
- (en) Allen C. Steere, " La aparición de la enfermedad de Lyme " , J Clin Invest , Vol. 113, n o 8,2004, p. 1093-1101 ( leer en línea )
- Trap D (1996) Aspectos clínicos, epidemiológicos, diagnósticos y de control de la enfermedad de Lyme en animales domésticos . Toro. de GTV., 2, 55-59
- Lamouraux, Cécile (2005), Borreliosis de Lyme en el caballo , tesis de doctorado veterinario defendida en la Facultad de Medicina de Créteil; Escuela Nacional de Veterinaria de Alfort
- Meryl P. Littman , Richard E. Goldstein , Mary A. Labato y Michael R. Lappin , " Declaración de consenso de animales pequeños de ACVIM sobre la enfermedad de Lyme en perros: diagnóstico, tratamiento y prevención ", Revista de Medicina Interna Veterinaria , vol. 20, n o 2Marzo de 2006, p. 422–434 ( ISSN 0891-6640 y 1939-1676 , DOI 10.1111 / j.1939-1676.2006.tb02880.x , leer en línea )
- Moutailler S. et al. (2015) Principales enfermedades transmitidas por garrapatas: epidemiología, clínica y diagnóstico . En: McCoy KD, Boulanger N., eds. Garrapatas y enfermedades transmitidas por garrapatas: biología, ecología evolutiva, epidemiología. IRD Éditions. doi: 10.4000 / books.irdeditions.9047.
- Sara Moutailler , Claire Valiente Moro , Elise Vaumourin y Lorraine Michelet , “ Co-infección de garrapatas: la regla más que la excepción ”, PLoS Neglected Tropical Diseases , vol. 10, n o 3,17 de marzo de 2016( ISSN 1935-2727 , PMID 26986203 , PMCID 4795628 , DOI 10.1371 / journal.pntd.0004539 , leído en línea , consultado el 18 de mayo de 2020 )
- Steere 2016, op. cit., pág. 13 (en formato pdf).
- Djuk-Wasser MA & al. (2016) Coinfección por patógenos transmitidos por garrapatas Ixodes: consecuencias ecológicas, epidemiológicas y clínicas . Trends in Ecology and Evolution, 32, 1, págs. 30-42. doi: 10.1016 / j.pt.2015.09.008
- Muriel Vayssier-Taussat , Maria Kazimirova , Zdenek Hubalek y Sándor Hornok , “ Horizontes emergentes para patógenos transmitidos por garrapatas: de la visión de 'un patógeno - una enfermedad' al paradigma del patobioma ”, Future Microbiology , vol. 10, n o 12,diciembre 2015, p. 2033–2043 ( ISSN 1746-0913 , PMID 26610021 , PMCID 4944395 , DOI 10.2217 / fmb.15.114 , leído en línea , consultado el 18 de mayo de 2020 )
- Johnson y col. (2014) Severidad de la enfermedad de Lyme crónica en comparación con otras afecciones crónicas: una encuesta de calidad de vida . PeerJ, 2, e322. doi: 10.7717 / peerj.322
- M. Alcalay, " Enfermedad de Lyme ", La Revue du Praticien , vol. 44, n o 12,1944, p. 1611-1618.
- (en-US) “ transmisión de la enfermedad de Lyme ” , en www.cdc.gov (visitada 30 de abril 2018 )
- (en-US) “ Preguntas frecuentes sobre la enfermedad de Lyme (FAQ) | Enfermedad de Lyme | CDC ” , en www.cdc.gov (consultado el 14 de agosto de 2017 )
- " Enfermedad de Lyme y donación de sangre | Etablissement francais du sang ” , en dondesang.efs.sante.fr (consultado el 30 de abril de 2018 )
- Vayssier-Taussat M & al. (2015) Cómo un enfoque multidisciplinario de “Una sola salud” puede combatir la amenaza de patógenos transmitidos por garrapatas en Europa. Future Microbiology, vol. 10, págs. 809-818. doi: 10.2217 / fmb.15.15, ver también One Health
- (en-US) “ ¿Cuántas personas contraen la enfermedad de Lyme? | Enfermedad de Lyme | CDC ” , en www.cdc.gov (consultado el 28 de abril de 2018 )
- (En) Sarah E. St. Pierre , Odette N. Gould y Vett Lloyd , " Conocimientos y necesidades de conocimiento sobre la enfermedad de Lyme entre los usuarios ocupacionales y recreativos del aire libre " , Revista internacional de investigación ambiental y salud pública , vol. 17, n o 1,5 de enero de 2020, p. 355 ( ISSN 1660-4601 , PMID 31948017 , PMCID PMC6981950 , DOI 10.3390 / ijerph17010355 , leído en línea , consultado el 24 de septiembre de 2020 )
- (en) NH Ogden , C. Bouchard , J. Badcock y MA Drebot , " ¿Cuál es el número real de casos de enfermedad de Lyme en Canadá? ” , BMC Public Health , vol. 19, n o 1,diciembre de 2019, p. 849 ( ISSN 1471-2458 , PMID 31253135 , PMCID PMC6599318 , DOI 10.1186 / s12889-019-7219-x , leído en línea , consultado el 26 de septiembre de 2020 )
- (en) A Rizzoli , HC Hauffe , G Carpi y GI Vourc'h , “ borreliosis de Lyme en Europa ” , Eurosurveillance , vol. 16, n o 27,7 de julio de 2011( ISSN 1560-7917 , DOI 10.2807 / ese.16.27.19906-en , leído en línea , consultado el 28 de abril de 2018 )
- (en-US) “ LYME ” , en epidemio.wiv-isp.be (consultado el 29 de abril de 2018 )
- Oficina Federal de Salud Pública OFSP , " Enfermedades transmitidas por garrapatas - Situación en Suiza " , en www.bag.admin.ch (consultado el 29 de abril de 2018 )
- Red de centinelas (2018) | URL = https://websenti.u707.jussieu.fr/sentiweb/
- C. Thorin , E. Rigaud , I. Capek y G. André-Fontaine , " La seroprevalencia de la borreliosis de Lyme y la encefalitis transmitida por garrapatas en los profesionales expuestos en el Grand Est de Francia ", Medicina y Enfermedades Infecciosas , vol . 38, n o 10,Octubre de 2008, p. 533-542 ( DOI 10.1016 / j.medmal.2008.06.008 , leído en línea , consultado el 24 de septiembre de 2020 )
- (in) Mathilde De Keukeleire , Annie Robert , Victor Luyasu y Benedict Kabamba , " Seroprevalencia de Borrelia burgdorferi en trabajadores forestales belgas y factores de riesgo asociados " , Parásitos y vectores , vol. 11, n o 1,diciembre 2018, p. 277 ( ISSN 1756-3305 , PMID 29716647 , PMCID PMC5930862 , DOI 10.1186 / s13071-018-2860-2 , leído en línea , consultado el 24 de septiembre de 2020 )
- (en) M. Cinco , F. Barbone , M. Grazia Ciufolini y M. Mascioli , “ La seroprevalencia de infecciones transmitidas por garrapatas en rangers forestales desde el noreste de Italia ” , Clinical Microbiology and Infection , vol. 10, n o 12,diciembre de 2004, p. 1056–1061 ( DOI 10.1111 / j.1469-0691.2004.01026.x , leído en línea , consultado el 24 de septiembre de 2020 )
- Ogden NH, Lindsay LR, Morshed M, Sockett PN, Artsob H. (2009) La aparición de la enfermedad de Lyme en Canadá . CMAJ; 180: 1221-4
- Jacques Exbalin , Calentamiento global y sus impactos , t. II: El caso de Francia , París, ediciones L'Harmattan ,2014, 296 p. , con los testimonios de Jean Jouzel , Nicolas Hulot , Yann Arthus-Bertrand , Yves Cochet y Brice Lalonde ( ISBN 978-2-336-34951-0 y 2-336-34951-5 , OCLC 887816626 , nota BnF n o FRBNF43832179 , leer en línea ) , pág. 230
- Stone, BL, Tourand, Y. y Brissette, CA (2017). Un mundo feliz: el universo en expansión de la enfermedad de Lyme . Enfermedades zoonóticas y transmitidas por vectores | resumen .
- Tougeron K, Perez G, Gillard M, Seimandi-Corda G, Balbi M, et al. (2015) ¿ Biodiversidad bajo prescripción médica? Los efectos de la pérdida de biodiversidad en la salud, el ejemplo de la enfermedad de Lyme en Quebec . Premio de ciencia popular de la Universidad de Montreal, Canadá. (hal-01162524)
- (en) Joshua Lederberg, Infecciones emergentes , National Academy Press ,1992( ISBN 0-309-04741-2 ) , pág. 27-28
- (en) Z. Popović, S. Popović. “Transición forestal y riesgo de zoonosis” Enciclopedia de salud ambiental , p. 803–811 ( resumen )
- Jean-Louis Chapuis, " Borreliosis de Lyme: introducción de un nuevo huésped, la ardilla listada siberiana ", Boletín epidemiológico semanal ,14 de septiembre de 2010, p. 6-8
- Sapi E & al. (2019) Antibióticos: la persistencia a largo plazo de los antígenos y el ADN de Borrelia burgdorferi en los tejidos de un paciente con enfermedad de Lyme ; Antibióticos 2019, 8 (4), 183; https://doi.org/10.3390/antibiotics8040183
- Eppes SC & Childs JA (2002) Estudio comparativo de cefuroxima axetil versus amoxicilina en niños con enfermedad de Lyme temprana . Pediatrics, 109, 1173-1177.
- Preac-Mursic V, Weber K, Pfister HW, Wilske B, Gross B, Baumann A & Prokop J (1989) Supervivencia de Borrelia burgdorferi en pacientes tratados con antibióticos con borreliosis de Lyme . Infección, 17, 355–359.
- Liegner KB, Rosenkilde CE, Campbell GL, Quan TJ, Dennis DT (1992) Fallo del tratamiento confirmado por cultivo de cefotaxima y minociclina en un caso de meningoencefalomielitis de Lyme en los Estados Unidos . En Actas del programa y resúmenes de la Quinta Conferencia Internacional sobre Borreliosis de Lyme, Arlington, VA, EE. UU., 30 de mayo - 2 de junio de 1992; Federación de Sociedades Estadounidenses de Biología Experimental: Bethesda, MD, EE. UU., 1992; Volumen A11.
- Liegner KB, Shapiro JR, Ramsay D, Halperin AJ, Hogrefe W & Kong L (1993) Eritema migrans recurrente a pesar del tratamiento prolongado con antibióticos con minociclina en un paciente con infección persistente por Borrelia burgdorferi . J. Am. Acad. Dermatol, 28, 312-314.
- Steere, AC; Angelis, SM (2006) Terapia para la artritis de Lyme: Estrategias para el tratamiento de la artritis refractaria a los antibióticos . Arthritis Rheum, 54, 3079-3086.
- Klempner, MS, Baker PJ, Shapiro ED, Marques A, Dattwyler RJ, Halperin JJ & Wormser GP (2013) Se revisaron los ensayos de tratamiento para los síntomas de la enfermedad de Lyme . Am. J. Med., 126, 665–669
- Hodzic, E.; Feng, S.; Holden, K.; Freet, KJ; Barthold, SW (2008) Persistencia de Borrelia burgdorferi después del tratamiento con antibióticos en ratones . Antimicrob. Agentes quimioterápicos. | 52, 1728-1736.
- Hodzic, E.; Imai, D.; Feng, S.; Barthold, SW (2014) Resurgimiento de Borrelia burgdorferi no cultivable persistente después del tratamiento con antibióticos en ratones . PLoS ONE 2014, 9, e86907.
- Straubinger, RK; Summers, BA; Chang, YF; Appel, MJ (1997) Persistencia de Borrelia burgdorferi en perros infectados experimentalmente después del tratamiento con antibióticos . J. Clin. Microbiol, 35, 111-116.
- Berndtson, K. (2013) Revisión de evidencia de evasión inmune e infección persistente en la enfermedad de Lyme . En t. J. Gen. Med, 6, 291-306.
- Embers, YO; Barthold, SW; Borda, JT; Bowers, L.; Doyle, L.; Hodžić, E.; Jacobs, MB; Hasenkampf, NR; Martin, DS; Narasimhan, S.; et al. (2012) Persistencia de Borrelia burgdorferi en macacos Rhesus después del tratamiento con antibióticos de una infección diseminada . PLoS ONE 2012, 7, e29914.
- Embers, YO; Barthold, SW; Borda, JT; Bowers, L.; Doyle, L.; Hodžić, E.; Jacobs, MB; Hasenkampf, NR; Martin, DS; Narasimhan, S.; et al. (2012) Persistencia de Borrelia burgdorferi en macacos Rhesus después del tratamiento con antibióticos de una infección diseminada . PLoS ONE, 7, e29914.
- Embers, YO; Hasenkampf, NR; Jacobs, MB; Tardo, AC; Doyle-Meyers, LA; Philipp, MT; Hodzic, E. (2017) Manifestaciones variables, serorreactividad diversa y persistencia postratamiento en primates no humanos expuestos a Borrelia burgdorferi por alimentación de garrapatas . PLoS ONE, 12, e0189071.
- Crossland, NA; Álvarez, X.; Embers, ME Enfermedad de Lyme de diseminación tardía: patología asociada y postratamiento de persistencia de espiroquetas en macacos Rhesus. Am. J. Pathol. 2018, 188, 672–682.
- Hodzic, E.; Imai, DM; Escobar, E. (2019) La generalidad de la persistencia posterior al tratamiento antimicrobiano de las cepas N40 y B31 de Borrelia burgdorferi en cepas de ratón genéticamente susceptibles y resistentes . Infectar. Immun., IAI.00442-19.
- Feng, J.; Cama.; Yuan, Y.; Yee, R.; Zhang, Y. (2019) Las bacterias de la fase biofilm / persistente / estacionaria causan una enfermedad más grave que las bacterias de la fase logarítmica: la biopelícula Borrelia burgdorferi no solo muestra más tolerancia a los antibióticos de Lyme sino que también causa una patología más grave en un modelo de artritis de ratón: implicaciones para comprender la persistencia , PTLDS y fracaso del tratamiento . Discov. Med., 148, 125-138.
- Schmidli, J.; Hunziker, T.; Moesli, P.; Schaad, UB (1988) Cultivo de Borrelia burgdorferi a partir del líquido articular tres meses después del tratamiento de la parálisis facial debida a la borreliosis de Lyme . J. Infect. Decir. 1988, 158, 905–906.
- Häupl, T.; Hahn, G.; Rittig, M.; Krause, A .; Schoerner, C.; Schönherr, U.; Kalden, JR; Burmester, GR (1993) Persistencia de Borrelia burgdorferi en tejido ligamentoso de un paciente con borreliosis de Lyme crónica . Artritis. Rheum., 36, 1621-1626.
- Battafarano, DF; Combs, JA; Enzenauer, RJ; Fitzpatrick, JE (1993) Artritis séptica crónica causada por Borrelia burgdorferi . Clin. Orthop. Relat. Res., 297, 238–241.
- Middelveen, MJ; Sapi, E.; Burke, J.; Filush, KR; Franco, A.; Fesler, MC; Stricker, RB (2018) Infección persistente por Borrelia en pacientes con síntomas continuos de la enfermedad de Lyme . Salud, 6, 33.
- Sylvie de Martino, " Borreliosis europea y enfermedad de Lyme ", Le Concours Médical , vol. 126, n o 33,10 de noviembre de 2004, p. 1919-1924
- (en) Carrie D. Tibbles, " ¿Este paciente tiene eritema migrans-? ” , Revista de la Asociación Médica Estadounidense , vol. 297, n o 23,20 de junio de 2007, p. 2617-2626
- Speere, 2016, op. cit., pág. 9-10.
- Frédéric Blanc, “ Neuroborreliosis: ¿cuándo pensar en ello? », La Revue du Praticien - medicina general , vol. 21, núms . 782-783,2 de octubre de 2007, p. 843-846.
- Christine Tranchant, “ Neurolyme: ¿cómo hacer el diagnóstico? », La Revue du Praticien - medicina general , vol. 33, n o 1022,Mayo de 2019, p. 428-429.
- Steere 2016, op. cit., pág. 10-11.
- (en) Yeung C, Baranchuk A, “Diagnóstico y tratamiento de Lyme carditis” J Am Coll Cardiol . 2019; 73: 717-26. . DOI : 10.1016 / j.jacc.2018.11.035 .
- Pilly 2017, op. cit., págs. 379-380.
- Nicholas A. Crossland , Xavier Alvarez y Monica E. Embers , " Enfermedad de Lyme de diseminación tardía: patología asociada y postratamiento de persistencia de espiroquetas en macacos Rhesus ", The American Journal of Pathology , vol. 188, n o 3,marzo 2018, p. 672–682 ( ISSN 1525-2191 , PMID 29242055 , PMCID 5840488 , DOI 10.1016 / j.ajpath.2017.11.005 , leído en línea , consultado el 9 de mayo de 2020 )
- (in) Johannes Nemeth, " Actualización de las directrices suizas sobre el síndrome de la enfermedad de Lyme postratamiento " , Swiss Medical Weekly ,2016( leer en línea [PDF] )
- (en) Feder HM, Johnson BJ, O'Connell S. et al. " Una evaluación crítica de la" enfermedad de Lyme crónica " " N Engl J Med . 2007; 357 (14): 1422-30. DOI : 10.1056 / NEJMra072023 .
- Paul M. Lantos , " Enfermedad de Lyme crónica ", Clínicas de enfermedades infecciosas de América del Norte , vol. 29, n o 2junio 2015, p. 325–40 ( ISSN 0891-5520 , PMID 25999227 , PMCID PMC4477530 , DOI 10.1016 / j.idc.2015.02.006 , leído en línea , consultado el 3 de mayo de 2018 ).
- François Bricaire , " la enfermedad de Lyme ", La Revue du Praticien - Médecine générale , vol. 29, n o 934,enero 2015, p. 55-57
- HAS 2012 , p. 26.
- Steere, 2016, op. cit., pág. 12 y 32.
- (in) BA Fallon , Sr. Pavlicová , SW Coffino y C. Brenner , " Una comparación de los resultados de las pruebas serológicas de la enfermedad de Lyme de 4 laboratorios en pacientes con síntomas persistentes después del tratamiento con antibióticos " , Enfermedades Infecciosas Clínicas , vol. 59, n o 12,15 de diciembre de 2014, p. 1705-1710 ( ISSN 1058-4838 y 1537-6591 , DOI 10.1093 / cid / ciu703 , leído en línea , consultado el 26 de septiembre de 2020 )
- "2018: Busters de biopelículas para mejorar la detección de Borrelia mediante PCR"
- Steere, 2016, op. cit., pág. 11-12.
- Feyeux D & Fantin B (2019) Noticias sobre el manejo de la enfermedad de Lyme . The Journal of Internal Medicine, 40 (4), 226-231 | resumen .
- "La lanceta, diciembre de 2019: detección de ADN sin células de Borrelia burgdorferi en muestras de plasma humano para un diagnóstico mejorado de la borreliosis de Lyme temprana"
- (en) Eugene D. Shapiro, " la enfermedad de Lyme " , The New England Journal of Medicine , vol. 370, n o 18,1 st de mayo de 2014, p. 1724-1731.
- Paul G Auwaerter , Johan S Bakken , Raymond J Dattwyler y J Stephen Dumler , “ Anticiencia y preocupaciones éticas asociadas con la promoción de la enfermedad de Lyme ”, The Lancet. Enfermedades infecciosas , vol. 11, n o 9,septiembre 2011, p. 713-719 ( ISSN 1473-3099 , PMID 21867956 , PMCID PMC4489928 , DOI 10.1016 / S1473-3099 (11) 70034-2 , leído en línea , consultado el 3 de mayo de 2018 )
- Joanna Ścieszka , Józefa Dąbek y Paweł Cieślik , “ Síndrome post-enfermedad de Lyme ”, Reumatologia , vol. 53, n o 1,2015, p. 46–48 ( ISSN 0034-6233 , PMID 27407225 , PMCID 4847307 , DOI 10.5114 / reum.2015.50557 , leído en línea , consultado el 4 de junio de 2020 )
- (en) Michael T. Melia, " Tiempo para un enfoque diferente a la enfermedad de Lyme y síntomas a largo plazo " , The New England Journal of Medicine , vol. 374, n o 13,31 de marzo de 2016, p. 1277-1278.
- (en) Allison DeLong y Mayla Hsu , " Estimación del número acumulado de casos de enfermedad de Lyme posteriores al tratamiento en los EE. UU., 2016 y 2020 " en BMC Public Health ,diciembre de 2019( ISSN 1471-2458 , PMID 31014314 , PMCID PMC6480773 , DOI 10.1186 / s12889-019-6681-9 , consultado el 24 de septiembre de 2020 ) ,p. 352
- " Conferencia de consenso de Lyme borreliosis 2006 " , en infectiologie.com (consultado el 4 de mayo de 2018 )
- (en) B. Jaulhac, A. Saunier, E. Caumes, K. Bouiller, Gehanno JF et al. , “ Borreliosis de Lyme y otras enfermedades transmitidas por garrapatas. Directrices de las sociedades científicas francesas (II). Biológicos, tratamiento, síntomas persistentes después de una borreliosis de Lyme documentada o sospechada ” , Medicina y Enfermedades Infecciosas ,31 de mayo de 2019( DOI 10.1016 / j.medmal.2019.05.001 )
- Thomas Butler , " La reacción de Jarisch-Herxheimer después del tratamiento con antibióticos de las infecciones por espiroquetas: una revisión de casos recientes y nuestra comprensión de la patogénesis " , The American Journal of Tropical Medicine and Hygiene , vol. 96, n o 1,11 de enero de 2017, p. 46–52 ( ISSN 0002-9637 , PMID 28077740 , PMCID PMC5239707 , DOI 10.4269 / ajtmh.16-0434 , leído en línea , consultado el 4 de mayo de 2018 )
- Steere, 2016, op. cit., pág. dieciséis.
- Steere, 2016, op. cit., pág. 17.
- Simpson EL, Duenas A, Holmes MW, Papaioannou D, Chilcott “Estimulación de la médula espinal para el dolor crónico de origen neuropático o isquémico: revisión sistemática y evaluación económica”; J. Evaluación técnica de la salud. 2009 Mar; 13 (17): iii, ix-x, 1-154. ( resumen )
- Shui Y, Tao W, Huang D, Li Y, Fan B. "Estimulación de la médula espinal para el dolor crónico que se origina en la enfermedad de Lyme" ; Médico del dolor. 2012 Noviembre; 15 (6): 511-4. ( resumen )
- Paul M. Lantos , Eugene D. Shapiro , Paul G. Auwaerter y Phillip J. Baker , " Terapias alternativas poco ortodoxas comercializadas para tratar la enfermedad de Lyme " , Enfermedades infecciosas clínicas: una publicación oficial de la Sociedad de Enfermedades Infecciosas de América , vol. 60, n o 12,15 de junio de 2015, p. 1776-1782 ( ISSN 1058-4838 , PMID 25852124 , PMCID PMC4490322 , DOI 10.1093 / cid / civ186 , leído en línea , consultado el 4 de mayo de 2018 )
- Steere, 2016, op. cit., pág. 17 y 33.
- (en-US) Natalie S. Marzec , Christina Nelson , Paul Ravi Waldron y Brian G. Blackburn , “ Infecciones bacterianas graves adquiridas durante el tratamiento de pacientes con diagnóstico de enfermedad de Lyme crónica - Estados Unidos ” , MMWR. Informe Semanal de Morbilidad y Mortalidad , vol. 66, n o 23,16 de junio de 2017, p. 607–609 ( ISSN 0149-2195 y 1545-861X , DOI 10.15585 / mmwr.mm6623a3 , leído en línea , consultado el 8 de mayo de 2018 )
- (en) Matthew Wood, The Book of Herbal Wisdom , North Atlantic Books , Berkeley, California, 1997 ( ISBN 978-1-55643-232-3 ) .
- Wolf-Dieter Storl ( traducido del alemán por Christophe Bernard), Curar la enfermedad de Lyme de forma natural: tratamiento holístico y usos prácticos , París, Guy Trédaniel ,2013( 1 st ed. 2011 c alemán / o Weltbild bajo el título " Borreliose natürlich heilen: ganzheitliche Behandlung und Anwendungen praktische " y luego en 2012 en holandés bajo el título " De Van ziekte de Lyme " ), 274 p. ( ISBN 978-2-8132-0618-3 y 2-8132-0618-0 , aviso BnF n o FRBNF43668365 , presentación en línea )
- (de) Petra Gutmann , " Borreliose: Natürliche Therapie " , Boletín de A. Vogel , Teufen "9. Heilpflanzen, die helfen" ,2014( lea en línea [Zecken, Borreliose, FSME: Informationen über Begriffe und Behandlung von Lyme Borreliose und FSME]) Ver cardo silvestre ( dipsacus silvestris ), uña de gato ( uncaria tomentosa ).
- (en) Brorson O, Brorson SH, " El extracto de semilla de pomelo es un poderoso agente in vitro contra las formas móviles y quísticas de Borrelia burgdorferi sensu lato " , Infección , vol. 35, n o 3,2007, p. 206-8. ( PMID 17565468 ) [ leer en línea ] : haga clic en la pestaña Mirar dentro para leer las dos primeras páginas del texto.
- https://www.frontiersin.org/articles/10.3389/fmed.2020.00006/full
- https://www.lanutrition.fr/lyme-deux-plantes-qui-tuent-la-bacterie-borrelia
- "Chronimed: algunos aceites esenciales tienen una fuerte actividad contra la fase estacionaria y el biofilm de Borrelia burgdorferi"
- "Fronteras en la medicina: los aceites esenciales selectivos de las especias o las hierbas culinarias tienen una alta actividad contra la fase estacionaria y el biofilm Borrelia burgdorferi"
- "2015, Ncbi: Eficacia del extracto de hoja entera de Stevia Rebaudiana contra las diversas formas morfológicas de Borrelia Burgdorferi in Vitro"
- Guilhem Denis , " Las garrapatas: lo prohibido remedio Tic Tox ", Europa 1 ,27 de enero de 2012( leer en línea ) “La venta de un producto, presentado como remedio preventivo o curativo para las picaduras de garrapatas (enfermedad de Lyme, borreliosis, etc.) por la empresa Nutrivital, acaba de ser prohibida por la Agencia de Productos Sanitarios (Afssaps). La Afssaps señala que este producto es objeto de promoción promocionando sus efectos terapéuticos, mientras que no cuenta con una autorización de comercialización (AMM) para el medicamento y que también presenta riesgos de neurotoxicidad , incluso cuando se toma por vía oral durante un período breve. "
- Decisión de la Afssaps [PDF] , 2012.
- Pryska Ducoeurjoly , " Archivo: la prohibición de Tic Tox llega en un contexto controvertido ", Aperturas: la época del ciudadano "Enfermedad de Lyme",2 de marzo de 2013( leer en línea ) Entrevista al profesor Christian Perronne , especialista en la enfermedad de Lyme, jefe del Departamento de Enfermedades Infecciosas del hospital Raymond-Poincaré de Garches (92), presidente de la Comisión Especializada en Enfermedades Transmisibles del Consejo Superior de Salud Pública (HCSP).
- Rand PW y col. (2004) Abundancia de Ixodes scapularis (Acari: Ixodidae) después de la remoción completa de ciervos de una isla aislada, endémica de la enfermedad de Lyme . J. Med. Entomol. 41, 779–784
- Gilbert, L. et al. (2012) El efecto del manejo de ciervos sobre la abundancia de Ixodes ricinus en Escocia . Escuela. Apl. 22, 658–667
- Levi, T. et al. (2012) Ciervos, depredadores y aparición de la enfermedad de Lyme. Proc. Natl. Acad. Sci. EE. UU. 109, 10942–10947
- KJ Kugeler , RA Jordan , TL Schulze y KS Griffith , “ ¿El sacrificio de ciervos de cola blanca evitará la enfermedad de Lyme? », Zoonosis y salud pública , vol. 63, n o 5,agosto de 2016, p. 337-45. ( ISSN 1863-1959 , PMID 26684932 , PMCID PMC4912954 , DOI 10.1111 / zph.12245 , leído en línea , consultado el 5 de mayo de 2018 )
- (en) Meagan F. Vaughn y Steven R. Meshnick , " Estudio piloto que evalúa la eficacia de la ropa impregnada de permetrina de larga duración para la prevención de picaduras de garrapatas " , Enfermedades zoonóticas y transmitidas por vectores , vol. 11, n o 7,julio 2011, p. 869–875 ( ISSN 1530-3667 y 1557-7759 , DOI 10.1089 / vbz.2010.0158 , leído en línea , consultado el 24 de septiembre de 2020 )
- (en) Robert prosa , Nicole E Breuner , Tammi L Johnson y Rebecca J Eisen , " Contacto irritación y la toxicidad de la ropa tratada-permetrina para Ixodes scapularis, Amblyomma americanum y Dermacentor variabilis garrapatas (Acari: Ixodidae) " , Revista de Entomología Médica ,24 de mayo de 2018( ISSN 0022-2585 y 1938-2928 , PMID 29800259 , PMCID PMC6119117 , DOI 10.1093 / jme / tjy062 , leído en línea , consultado el 24 de septiembre de 2020 )
- (en) Michael K. Faulde Martin Rutenfranz Alexander Keth y Jürgen Hepke , " Estudio piloto que evalúa la eficacia de la ropa impregnada de permetrina de larga duración tratada en fábrica para la prevención de picaduras de garrapatas durante la exposición ocupacional a las garrapatas en áreas de entrenamiento militar altamente infestadas , Alemania ” , Parasitology Research , vol. 114, n o 2febrero de 2015, p. 671–678 ( ISSN 0932-0113 y 1432-1955 , DOI 10.1007 / s00436-014-4232-y , leído en línea , consultado el 24 de septiembre de 2020 )
- (en) Meagan F. Vaughn , Sheana Whelan Funkhouser , Chang Feng Lin y Jason Fine , " Uniformes impregnados con permetrina de larga duración " , American Journal of Preventive Medicine , vol. 46, n o 5,Mayo de 2014, p. 473–480 ( DOI 10.1016 / j.amepre.2014.01.008 , leído en línea , consultado el 24 de septiembre de 2020 )
- (in) Cedar Mitchell , Megan Dyer , Feng Chang Lin y Natalie Bowman , " Eficacia protectora de la ropa impregnada con permetrina de larga duración contra las picaduras de garrapatas en un entorno de enfermedad de Lyme endémica de un año: un ensayo de control aleatorio entre trabajadores al aire libre " , Journal of Medical Entomology , vol. 57, n o 5,7 de septiembre de 2020, p. 1532-1538 ( ISSN 0022-2585 y 1938-2928 , DOI 10.1093 / jme / tjaa061 , leído en línea , consultado el 24 de septiembre de 2020 )
- (en) Neeta P Connally , Dominic A Rose , Nicole E Breuner y Robert prosa , “ Impacto de uso y lavado / secado de la ropa tratada-permetrina en su contacto de irritación y toxicidad para ninfas Ixodes scapularis (Acari: Ixodidae) Garrapatas ” , Revista de Entomología Médica , vol. 56, n o 1,8 de enero de 2019, p. 199–214 ( ISSN 0022-2585 y 1938-2928 , PMID 30165532 , PMCID PMC6326861 , DOI 10.1093 / jme / tjy138 , leído en línea , consultado el 24 de septiembre de 2020 )
- Cuidado con las garrapatas: jardines en riesgo , noticias de TWC Francia;
- (en-US) “ Prevención de picaduras de garrapatas en personas | Enfermedad de Lyme | CDC ” , en www.cdc.gov (consultado el 5 de mayo de 2018 )
- (en) Piesman J, Eisen L. " Prevención de enfermedades transmitidas por garrapatas " Annu Rev Entomol . 2008; 53: 323--43.
- (en) Ginsberg HS, M Butler, Zhioua E. "El efecto de las cercas de exclusión de ciervos se debe a la abundancia de Amblyomma americanum (Acari: Ixodidae) en Fire Island " Nueva York, EE. UU., J Vector Ecol . 2002; 27: 215--21.13,14.
- (en-US) Daphne Cybele , " Control de garrapatas: cómo una bandada de pollos puede ser la mejor opción " , en Wide Open Pets ,11 de mayo de 2019(consultado el 12 de julio de 2019 )
- (en-US) “ La prevención de garrapatas en sus mascotas | Enfermedad de Lyme | CDC ” , en www.cdc.gov ,11 de agosto de 2017(consultado el 5 de mayo de 2018 )
- Watson SC, Liu Y, Lund RB, Gettings JR, Nordone SK, McMahan CS, et al. (2017) Un modelo espacio-temporal bayesiano para pronosticar la prevalencia de anticuerpos contra Borrelia burgdorferi, agente causante de la enfermedad de Lyme, en perros domésticos dentro de los Estados Unidos contiguos. PLoS ONE 12 (5): e0174428. https://doi.org/10.1371/journal.pone.0174428
- Gétaz L, Loutan L, Mezger N, “ Enfermedades transmitidas por garrapatas de aquí y en otra parte [ Enfermedades transmitidas por garrapatas localmente y en el extranjero ] ”, Rev Med Suisse , vol. 8, n o 340,2012, p. 974-6. ( PMID 22662624 , lea en línea [html] )
- (en-US) “ extirpación y el estudio Tick | Enfermedad de Lyme | CDC ” , en www.cdc.gov ,10 de agosto de 2017(consultado el 5 de mayo de 2018 )
- La instrucción de girar lentamente en la dirección REVERSA de las agujas de un reloj está claramente escrita en una caja que contiene dos “removedores de garrapatas”, producidos, vendidos en farmacias, en los laboratorios Clément-Thékan en Montrouge (Francia). De hecho, hay que elegir un sentido de giro y girar el instrumento en ese sentido, dos o tres vueltas o más si es necesario, sin cambiar de sentido durante la operación, para que se salga el tick. En sentido antihorario (como para desenroscar) sería más conveniente para personas diestras, y el otro (como para atornillar) para personas zurdas: preguntas frecuentes sobre tenazas de garrapatas .
- (in) " tick bite prophylaxis (p. 20) " , en cdc.gov (consultado el 5 de mayo de 2018 )
- Monica E. brasas y Sukanya Narasimhan , “ La vacunación contra la enfermedad de Lyme: pasado, presente y futuro ”, Frontiers in Cellular and Infection Microbiología , vol. 3,12 de febrero de 2013( ISSN 2235-2988 , PMID 23407755 , PMCID PMC3569838 , DOI 10.3389 / fcimb.2013.00006 , leído en línea , consultado el 6 de mayo de 2018 )
- (en) Angela K. Shen , Paul S. Mead y Charles B. Barba , " La enfermedad de Lyme Vacuna-A perspectiva de salud pública " , Clinical Infectious Diseases , vol. 52, n o suppl_3,1 st de febrero de 2011, s247 - s252 ( ISSN 1537-6591 y 1058-4838 , DOI 10.1093 / cid / ciq115 , leído en línea , consultado el 24 de septiembre de 2020 )
- L. E. NIGROVIC y KM THOMPSON , “ La vacuna de Lyme: una advertencia ”, Epidemiología e Infección , vol. 135, n o 1,enero 2007, p. 1–8 ( ISSN 0950-2688 , PMID 16893489 , PMCID PMC2870557 , DOI 10.1017 / S0950268806007096 , leído en línea , consultado el 6 de mayo de 2018 )
- (en) Hanner, M., W. Schüler, A. Meinke, U. Lundberg, Plos One Diseño y desarrollo de una nueva vacuna para la protección contra la borreliosis de Lyme , PLoS ONE 9 (11): e113294. Doi: 10.1371 / journal.pone.0113294.
- (en) Stanley A Plotkin, " Necesidad de una vacuna contra la enfermedad de Lyme Nueva " , The New England Journal of Medicine , vol. 375, n o 10,8 de septiembre de 2016, p. 911-913
- Joseph Martin , " Vaccine against Lyme: un laboratorio francés apunta a ser comercializado para 2025 " , en RSE Magazine (consultado el 4 de agosto de 2020 ) .
- Maria Gomes-Solecki , “ Bloqueo de la transmisión de patógenos en la fuente: vacunas basadas en OspA dirigidas al reservorio contra Borrelia burgdorferi ”, Frontiers in Cellular and Infection Microbiology , vol. 4,26 de septiembre de 2014( ISSN 2235-2988 , PMID 25309883 , PMCID PMC4176399 , DOI 10.3389 / fcimb.2014.00136 , leído en línea , consultado el 24 de septiembre de 2020 )
- Cees C Van den Winjngaard y col. (2017) El costo de la borreliosis de Lyme . Revista europea de salud pública, 27, 3, págs. 538-547. doi: 10.1093 / eurpub / ckw269
- Lohr IB (2015) Epidemiología y costo de la atención hospitalaria para la borreliosis de Lyme en Alemania: lecciones de un análisis de la base de datos de utilización de la atención médica . Garrapatas y enfermedades transmitidas por garrapatas, 6, 1, págs. 56-62. doi: 10.1016 / j.ttbdis.2014.09.004
- Alison Tonks , “ guerras de Lyme, ” British Medical Journal , vol. 335, n o 7626,3 de noviembre de 2007, p. 910–912 ( ISSN 0959-8138 , PMID 17974685 , PMCID PMCPMC2048873 , DOI 10.1136 / bmj.39363.530961.AD , leído en línea , consultado el 9 de junio de 2019 )
- C. Eldin , A. Raffetin , K. Bouiller e Y. Hansmann , “ Revisión de las guías europeas y americanas para el diagnóstico de borreliosis de Lyme ”, Medecine Et Maladies Infectieuses , vol. 49, n o 2marzo 2019, p. 121-132 ( ISSN 1769-6690 , PMID 30528068 , DOI 10.1016 / j.medmal.2018.11.011 , leído en línea , consultado el 9 de mayo de 2020 )
- (in) J Nemeth , E Bernasconi , U Heininger y Mr. Abbas , " Actualización de las directrices suizas sobre el síndrome de la enfermedad de Lyme postratamiento " , Swiss Medical Weekly ,5 de diciembre de 2016( ISSN 1424-7860 y 1424-3997 , DOI 10.4414 / smw.2016.14353 , leído en línea , consultado el 24 de septiembre de 2020 )
- (en) Samuel Shor , Christine verde , Beatrice Szantyr y Steven Phillips , " enfermedad de Lyme crónicos: ILADS definición basada en la evidencia Una por el Grupo de Trabajo " , antibióticos , vol. 8, n o 4,16 de diciembre de 2019, p. 269 ( ISSN 2079-6382 , PMID 31888310 , PMCID PMC6963229 , DOI 10.3390 / antibiotics8040269 , leído en línea , consultado el 24 de septiembre de 2020 )
- A. Kersten , C. Poitschek , S. Rauch y E. Aberer , “ Efectos de la penicilina, ceftriaxona y doxiciclina sobre la morfología de Borrelia burgdorferi ”, Agentes antimicrobianos y quimioterapia , vol. 39, n o 5,Mayo de 1995, p. 1127-1133 ( ISSN 0066-4804 , PMID 7625800 , PMCID PMC162695 , DOI 10.1128 / aac.39.5.1127 , leído en línea , consultado el 24 de septiembre de 2020 )
- (in) Vera Preac Mursic Sylvia Reinhardt , Bettina Wilske y U. Busch , " Entrenamiento y cultivo de variantes de forma L de esferoplasto de Borrelia burgdorferi " , Infección , vol. 24, n o 3,Mayo de 1996, p. 218–226 ( ISSN 0300-8126 y 1439-0973 , DOI 10.1007 / BF01781096 , leído en línea , consultado el 24 de septiembre de 2020 )
- (en) Judith Miklossy Sandor Kasas Anne D Zurn y Sherman McCall , " persistente atípica y formas quísticas de Borrelia burgdorferi y la inflamación local en Lyme neuroborreliosis " , Journal of neuroinflamación , vol. 5, n o 1,2008, p. 40 ( ISSN 1742-2094 , PMID 18817547 , PMCID PMC2564911 , DOI 10.1186 / 1742-2094-5-40 , leído en línea , consultado el 24 de septiembre de 2020 )
- Paul M. Lantos , Paul G. Auwaerter y Gary P. Wormser , " Una revisión sistemática de las variantes morfológicas de Borrelia burgdorferi no admite un papel en la enfermedad de Lyme crónica ", Enfermedades infecciosas clínicas: una publicación oficial de la Sociedad de Enfermedades Infecciosas de América , vol. 58, n o 5,1 st de marzo de 2014, p. 663–671 ( ISSN 1058-4838 , PMID 24336823 , PMCID PMC3922218 , DOI 10.1093 / cid / cit810 , leído en línea , consultado el 8 de mayo de 2018 )
- Natalie Rudenko , Maryna Golovchenko , Katerina Kybicova y Marie Vancova , " Metamorfosis de las espiroquetas de la enfermedad de Lyme: fenómeno de las persistencias de Borrelia ", Parásitos y vectores , vol. 12,16 de mayo de 2019( ISSN 1756-3305 , PMID 31097026 , PMCID 6521364 , DOI 10.1186 / s13071-019-3495-7 , leído en línea , consultado el 18 de mayo de 2020 )
- Paul Lantos se presenta como un especialista en el uso de SIG para epidemiología; Autor principal de un informe (2010) del Panel de Revisión de Pautas de Enfermedad de Lyme para la Sociedad Estadounidense de Enfermedades Infecciosas. Copresidió un panel (30 miembros) sobre las pautas de la enfermedad de Lyme (escrito por la Academia Estadounidense de Neurología, el Colegio Estadounidense de Reumatología y la Sociedad Estadounidense de Enfermedades Infecciosas).
- (en) Erica Weitzner , Donna McKenna , John Nowakowski y Carol Scavarda , " Evaluación a largo plazo de los síntomas posteriores al tratamiento en pacientes con enfermedad de Lyme temprana confirmada por cultivo " , Enfermedades infecciosas clínicas , vol. 61, n o 12,15 de diciembre de 2015, p. 1800–1806 ( ISSN 1058-4838 y 1537-6591 , PMID 26385994 , PMCID PMC4657537 , DOI 10.1093 / cid / civ735 , leído en línea , consultado el 24 de septiembre de 2020 )
- (en) Erica Weitzner , Paul Visintainer y Gary P. Wormser , " Comparación de hombres frente a mujeres con enfermedad de Lyme temprana confirmada por cultivo en la presentación y a los 11-20 años después del diagnóstico " , Microbiología diagnóstica y enfermedad infecciosa , vol. 85, n o 4,agosto de 2016, p. 493–495 ( DOI 10.1016 / j.diagmicrobio.2016.04.012 , leído en línea , consultado el 24 de septiembre de 2020 )
- (En) " Eventos pasados de defensa de la enfermedad de Lyme " .
- (in) " Evaluaciones de la evidencia y recomendaciones de las guías en la enfermedad de Lyme: el manejo clínico de picaduras de garrapatas conocidas, erupciones cutáneas y enfermedad de eritema migrans persistente. | National Guideline Clearinghouse ” , en www.guideline.gov (consultado el 8 de febrero de 2017 )
- Y. Hansmann, " ¿Existe la enfermedad de Lyme crónica?" », La Revue du Praticien , vol. 66,septiembre de 2016, p. 711-714.
- TIENE 2014 , p. 41-42
- " Informe de actividad de abril de 2018 a marzo de 2019 " , en francelyme.fr (consultado el 26 de julio de 2019 )
- TIENE 2014 , p. 44.
- HAS 2014 , p. 46.
- " consenso 2006 "
- HAS 2014 , p. 39.
- HAS 2014 , p. 46-47 ..
- " Enfermedad de Lyme: Matthias, en huelga de hambre, exige 'el derecho a ser curado' ", The Obs ,2016( leer en línea , consultado el 11 de mayo de 2018 )
- " Enfermedad de Lyme: el grito de alarma de 100 médicos: 'Hay una emergencia' ", The Obs ,2016( leer en línea , consultado el 11 de mayo de 2018 )
- " Enfermedad de Lyme: la larga lucha del profesor Perronne ", leparisien.fr ,3 de febrero de 2017( leer en línea , consultado el 11 de mayo de 2018 )
- " Enfermedad de Lyme:" Tuve que hacer pasar mi archivo como el de un animal " ", leparisien.fr ,3 de febrero de 2017( leer en línea , consultado el 11 de mayo de 2018 )
- " resumen del plan de 2016 "
- " Enfermedad de Lyme: necesidad urgente de actualizar las recomendaciones " [video] , en Medscape (consultado el 3 de julio de 2020 ) .
- " Enfermedad de Lyme: por qué Francia llega tan tarde ", The Huffington Post ,13 de julio de 2016( leer en línea , consultado el 11 de mayo de 2018 )
- " Enfermedad de Lyme: posición del SPILF - Enfermedad de Lyme: posición de " , en www.infectiologie.com (consultado el 8 de febrero de 2017 )
- " Conclusiones sobre la enfermedad de Lyme " , en academie-medecine.fr (consultado el 7 de mayo de 2018 )
- “ Haute Autorité de Santé - Lyme Borreliosis y otras enfermedades transmitidas por garrapatas ” , en www.has-sante.fr (visitada 05 de julio 2018 )
- " Comunicado de prensa del 2 de julio de 2018:" Actualización de la Haute Autorité de Santé (HAS) sobre la enfermedad de Lyme: reacciones y decepción de la Academia Nacional de Medicina "- Academia Nacional de Medicina | Una institución en su tiempo ”, Academia Nacional de Medicina | Una institución en su tiempo ,2 de julio de 2018( leer en línea , consultado el 4 de agosto de 2018 )
- "Comunicado de prensa de todas las sociedades científicas involucradas en el manejo de enfermedades transmitidas por garrapatas", 19 de julio de 2018 .
- Science et Avenir (2019) Enfermedad de Lyme: la situación se está convirtiendo ubicua ; Olivier Hertel; 08/04/2019
- Ex para literatura médica francófona: con Scholar
- No debe confundirse con la notificación insuficiente, una enfermedad se puede diagnosticar y tratar (correcta o incorrectamente) sin que se informe a los sistemas de vigilancia. Ver https://www.cdc.gov/lyme/stats/humancases.html
- " Boletín epidemiológico semanal, 7 de mayo de 2019 " , en invs.santepubliquefrance.fr (consultado el 9 de junio de 2019 )
- medicalXpress (2018) Brechas en la prevención, manejo de enfermedades transmitidas por garrapatas identificadas publicado el 6 de septiembre de 2018
- Paris Match , " Lyme disease: the masked killer 1/2 " , en parismatch.com (consultado el 25 de junio de 2021 )
- " ¿La propagación de la enfermedad de Lyme se debe a experimentos militares estadounidenses?" » , En www.franceinter.fr (consultado el 26 de junio de 2021 )
- " ¿El ejército de los Estados Unidos creó la enfermedad de Lyme?" » , On Sciences et Avenir (consultado el 25 de junio de 2021 )
- " Podría un mal experimento ido podrían ser la causa de la epidemia de Lyme en los Estados Unidos?" » , En SudOuest.fr (consultado el 25 de junio de 2021 )
- Adrien Sénécat, " ¿Quién es realmente Christian Perronne, médico referente de los conspiradores?" : el jefe del departamento de enfermedades infecciosas del hospital Garches es el respaldo científico del documental Hold-up y seguidor de “teorías alternativas” ”, Le Monde , 18-19 de noviembre de 2020 ( leído en línea , consultado el 6 de abril de 2021 ), cf. sección titulada "Experto en teorías alternativas " .
- Isabelle Léouffre (Artículo actualizado en5 de enero de 2017), " Enfermedad de Lyme: el asesino enmascarado (1/2) ", Paris Match "¿Realidad o leyenda? Se cree que la enfermedad de Lyme se debe a la manipulación genética de las garrapatas ”,14 de junio de 2016( leer en línea , consultado el 7 de abril de 2021 ).
- Anne-Laure Barret, " Enfermedad de Lyme, conspiración aplicada a los ácaros ", Le Journal du dimanche , 18 de septiembre de 2016 con modificación y actualización 21 de junio de 2017 ( leído en línea , consultado el 28 de abril de 2020 ).
- " Lyme, ¿enfermedad imaginaria? », Actu.fr - L'Orne Hebdo , Normandía,26 de mayo de 2016( leer en línea , consultado el 6 de abril de 2021 ).
- ladepeche.fr, " En lágrimas, Avril Lavigne relata su lucha contra la enfermedad de Lyme ", La Dépêche ,30 de junio de 2015( leer en línea , consultado el 3 de julio de 2020 ).
- " Avril Lavigne sobre la enfermedad de Lyme:" Estos fueron los peores años de mi vida "- Elle " , en elle.fr ,12 de septiembre de 2018(consultado el 3 de julio de 2020 ) .
- RTL Newmedia , " Shania Twain con la enfermedad de Lyme se quedó sin palabras: 'Realmente pensé que era el final de mi carrera' ", RTL People ,17 de julio de 2017( leer en línea , consultado el 23 de septiembre de 2018 )
- (en) Steve Ginsburg, "La enfermedad de Lyme nunca está lejos de los pensamientos de la estrella de la WNBA, Delle Donne " , Yahoo,15 de septiembre de 2015(consultado el 15 de septiembre de 2015 )
- (en) http://www.dailymail.co.uk/tvshowbiz/article-3265978/Bella-Anwar-Hadid-battling-Lyme-disease-mom-Yolanda-Foster-reveals.html
- " 8 estrellas víctimas de la enfermedad de Lyme " , en Medicite.fr ,11 de diciembre de 2017(consultado el 5 de julio de 2018 )
- " Enfermedad de Lyme: las estrellas afectadas por la enfermedad " , en Doctissimo.fr (consultado el 5 de julio de 2018 )
- (in) " Alec Baldwin pensó que 'moriría de la enfermedad de Lyme'. Qué saber sobre las enfermedades transmitidas por garrapatas ” , en Health.com (consultado el 25 de diciembre de 2018 )
- " Enfermedad de Lyme: estrellas afectadas por la enfermedad " , en Doctissimo (consultado el 25 de diciembre de 2018 )
- " Enfermedad de Lyme: un ciclista de alto nivel casi se detiene debido a una garrapata " , en www.pourquoidocteur.fr (consultado el 30 de julio de 2019 )
- " bush-fue-tratado-por-la-enfermedad-de-lyme-white-house "
- " Fédrigo sufrió una infección bacteriana " , en velochrono.fr ,27 de julio de 2011(consultado el 27 de julio de 2011 )
- Prisma Media , " Justin Bieber revela que tiene la enfermedad de Lyme - Aquí está " , en Ici.fr (consultado el 9 de enero de 2020 )
- " enfermedad de richard-gere-lyme "
Ver también
Bibliografía
- “ TIENE. Borreliosis de Lyme ' ,2014(consultado el 11 de mayo de 2018 ) .
- Judith Albertat , Enfermedad de Lyme: mi viaje para recuperar la salud , Vergèze, Thierry Souccar ,2012, 224 p. ( ISBN 978-2-36549-001-6 ).
- Chantal Perrin y Roger Lenglet , El caso de la enfermedad de Lyme: una investigación , Arles, Actes Sud ,2016, 155 p. ( ISBN 978-2-330-05800-5 , presentación en línea ).
- Christian Perronne , La verdad sobre la enfermedad de Lyme: infecciones ocultas, vidas destrozadas: hacia una nueva medicina , París, Odile Jacob ,2017, 298 p. ( ISBN 978-2-7381-3509-4 , presentación en línea ).
Filmografia
- Ryszard Hunka, guión y dirección; Erna Buffie & Merit Jensen-Carr, producción; Sandra Moore, gerente de producción; David McGunigal, editorial; Annick Bergeron, narración, El misterio de la enfermedad de Lyme , Canada Media Fund / Rogers Documentary and Cable Network Fund / CBC / France 5 ,10 de octubre de 2013, “Durante la última década, la enfermedad de Lyme, una misteriosa enfermedad transmitida por garrapatas, se ha extendido a un ritmo alarmante en Canadá. El documental explora este flagelo devastador, muchas veces mal diagnosticado y por tanto mal tratado, que sigue generando polémica. Investigación de un misterio médico. » ( Leer en línea [video] )
- Enfermedad de Lyme: ¡cuando atacan las garrapatas! Documental francés emitido sobre France 5 en 2014 y producido en 2014, 52 '. Página web (descripción) .
- Axel en la tierra de los pacientes imaginarios , documental francés emitido sobre France 3 Pays de la Loire, noviembre de 2020, 52 min . “ Axel en la tierra de los pacientes imaginarios ” , en france.tv .
Artículos relacionados
- Ecoepidemiología
- Enfermedad emergente
- Borreliosis
- Enfermedades transmitidas por garrapatas
- Síndrome de activación de mastocitos
enlaces externos
- Encuesta nacional sobre mapeo de mordidas para Francia
- " Enfermedad de Lyme " , sobre el Ministerio de Asuntos Sociales y Salud (Francia) ,18 de enero de 2017(consultado el 26 de enero de 2017 )
- Jean-Paul Krivine , " Enfermedad de Lyme: entre psicosis e información falsa " , SPS n o 321 , en pseudo-sciences.org , AFIS,julio 2017(consultado el 15 de agosto de 2017 )
- Aurélie Haroche , " Enfermedades de" no Lyme ": nuestra sociedad ignoró el sufrimiento de " en Medicine International Journal ,28 de marzo de 2018(consultado el 6 de abril de 2018 )
- https://socialyme.com blog e información sobre la enfermedad de Lyme
- Registros de autoridad :
- Avisos en diccionarios generales o enciclopedias :
- Recursos relacionados con la salud :
- Tesauro del NCI
- Orphanet
- (es) Enfermedades Ontología
- (es) DiseasesDB
- (en + es) Centro de Información sobre Enfermedades Genéticas y Raras
- (es) Encabezados de materias médicas
- (en + es) MedlinePlus
- (cs + sk) WikiSkripta