Proteína
Las proteínas se definieron como macromoléculas biológicas presentes en todas las células vivas , pero estudios recientes muestran que también hay cientos, si no miles, de micro o nano proteínas. Están formados por una o más cadenas polipeptídicas . Cada una de estas cadenas está compuesta por la secuencia de residuos de aminoácidos unidos por enlaces peptídicos .
Las proteínas realizan una multitud de funciones dentro de las células vivas y en los tejidos . Son proteínas enzimáticas ( enzimas ) que catalizan la síntesis química y las reacciones de degradación necesarias para el metabolismo celular. Otras proteínas desempeñan un papel estructural dentro del citoesqueleto o tejidos ( actina , colágeno ), algunas son motores moleculares que permiten la movilidad ( miosina ), otras están involucradas en el acondicionamiento del ADN ( histonas ), regulación de la expresión génica ( factores de transcripción ), energía metabolismo ( ATP sintasa ) o la transmisión de señales celulares ( receptores de membrana ).
Las cadenas de proteínas son sintetizadas en la célula por los ribosomas , a partir de la información codificada en los genes , que determinan el orden en el que se enlazan los 22 aminoácidos, denominados proteinógenos , que se incorporan directamente durante la biosíntesis de los genes . La secuencia de aminoácidos se denomina secuencia polipeptídica. De las modificaciones postraduccionales pueden intervenir una vez la proteína sintetizada, lo que puede tener el efecto de modificar las propiedades físicas o químicas. También es habitual que las moléculas no proteicas, denominadas grupos protésicos , se unan de forma estable a las proteínas y contribuyan de forma decisiva a sus funciones biológicas: este es, por ejemplo, el caso del hemo en la hemoglobina , sin el cual esta proteína no podría transportar oxígeno en la sangre .
Las proteínas adoptan una estructura tridimensional que les permite realizar su función biológica. Esta estructura particular está determinada sobre todo por su secuencia de aminoácidos, cuyas diversas propiedades fisicoquímicas llevan a la cadena proteica a adoptar un plegamiento estable.
En el laboratorio, se pueden separar de otros constituyentes celulares mediante diversas técnicas como ultracentrifugación , precipitación , electroforesis y cromatografía . La ingeniería genética ha introducido una serie de métodos para facilitar la purificación de proteínas. Su estructura puede estudiarse mediante inmunohistoquímica , mutagénesis dirigida al sitio , cristalografía de rayos X , resonancia magnética nuclear y espectrometría de masas .
Las proteínas son un componente importante del alimento animal, se degradan en el tracto digestivo y los aminoácidos liberados son luego reutilizados por el cuerpo.
diferenciamos entre proteínas completas y proteínas incompletas. Una proteína completa contiene los nueve aminoácidos esenciales, mientras que una proteína incompleta que se encuentra en los alimentos de origen vegetal no los contiene todos.
Etimología
Las proteínas fueron descubiertas a partir de 1835 en los Países Bajos por el químico orgánico Gerardus Johannes Mulder (1802-1880), bajo el nombre de wortelstof . Fue su ilustre colega sueco, Jöns Jacob Berzelius , quien le sugirió el nombre de proteína en 1838 .
El término proteína proviene del griego antiguo prôtos, que significa primero , esencial . Esto probablemente se refiere al hecho de que las proteínas son esenciales para la vida y, a menudo, constituyen la mayoría (parte del 60%) del peso seco de las células (animales). Otra teoría es que la proteína se refiere, como el adjetivo proteico, al dios griego Proteus que podía cambiar de forma a voluntad. Las proteínas toman muchas formas y realizan múltiples funciones. Pero esto no fue descubierta hasta mucho más tarde, durante el XX ° siglo .
Bioquímica
Las proteínas se forman a partir de una o más cadenas polipeptídicas , que son biopolímeros lineales, pueden ser bastante largas, compuestas por veinte ácidos L -α-amino diferentes. Generalmente hablamos de proteína con más de cincuenta residuos en la molécula y péptido con hasta unas pocas decenas de residuos.
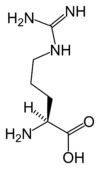
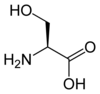
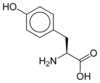
Todos los aminoácidos proteinogénicos , con la excepción de la prolina , comparten una estructura común que consta de una función de ácido carboxílico , una amina primaria en el carbono α y una cadena lateral . Este último tiene una variedad muy amplia de estructuras químicas, y es el efecto combinado de todas estas cadenas laterales de una cadena polipeptídica lo que determina la estructura tridimensional así como las propiedades químicas de este último. El siguiente tablero muestra la estructura química de los 22 aminoácidos proteinogénicos:
|
Estructura de 22 aminoácidos proteinogénicos . El pyrrolysine y selenocisteína (por encima de greyed) son específicos para ciertas proteínas : - la pyrrolysine sólo se encuentran en algunos archaeal metanógenos , - la selenocisteína también está presente entre los eucariotas , pero a priori en decenas de enzimas de la familia de las oxidorreductasas . Por otro lado, los otros 20 aminoácidos, llamados estándares, están distribuidos universalmente en todos los seres vivos conocidos. |
Los aminoácidos en una cadena polipeptídica están unidos por enlaces peptídicos que se establecen entre el carboxilo –COOH de un primer aminoácido y la amina primaria –NH 2 un segundo:
La columna vertebral de la proteína está formada por una cadena lineal de aminoácidos a la que las cadenas laterales están conectadas y unidas por enlaces peptídicos. El enlace peptídico tiene dos formas de resonancia que le confieren en parte las propiedades de un doble enlace , lo que limita las rotaciones alrededor de su eje, de modo que los cuatro átomos del grupo amida - (C = O) NH- son siempre aproximadamente coplanares . Los otros dos enlaces que constituyen la columna vertebral del aminoácido, por otro lado, pueden girar libremente. Los dos ángulos diedros correspondientes a estos dos enlaces internos determinan la geometría local adoptada por la cadena de proteínas.
El extremo carboxilo de la cadena lateral del polipéptido se denomina extremo C -terminal , mientras que el lado amina se denomina extremo N -terminal . Las palabras proteína, polipéptido y péptido son bastante ambiguas y sus significados pueden solaparse. Generalmente hablamos de proteína en referencia a la molécula biológica completa dotada de una conformación estable, mientras que un péptido generalmente designa una molécula más corta sin una estructura tridimensional estable. La línea entre los dos es muy imprecisa y tiene alrededor de unas pocas docenas de residuos de aminoácidos.
Tamaños
Siempre se creyó que las proteínas eran grandes (a escalas biomoleculares); había una sensación desde la década de 1980 y sabíamos desde principios de la década de 1990 que este no era el caso, luego del descubrimiento de una, luego de algunas otras MicroProteínas (a veces llamadas MiP ). Desde entonces, los científicos han demostrado la existencia de cientos y luego miles de microproteínas y nanoproteínas (a veces asociando solo unos pocos aminoácidos, quizás autoensambladas), tan pequeñas que los sistemas de análisis genómico clásicos no pueden detectarlas. Parecen tener funciones clave dentro de las células dentro del complejo de proteínas , al interactuar en las relaciones proteína-proteína. Algunas controlan así la actividad de proteínas más grandes, desempeñando un papel de reguladores postraduccionales, sin interactuar directamente con el ADN o el ARN. Otros promueven el desarrollo muscular y regulan la contracción muscular . Otros más contribuyen a la gestión de los desechos intracelulares (ARN viejo, degradado o defectuoso). En las plantas, podrían participar en la detección de luz y en otros casos desempeñar un papel en la señalización fitohormonal . En los animales, participan en el funcionamiento del reloj biológico .
Se encuentra en particular en venenos (de arañas , escorpiones y otros animales venenosos ). Se pueden crear nanoproteínas complejas in vitro mediante el autoensamblaje de aminoácidos ; quizás podrían usarse para el reconocimiento biomolecular y la catálisis. Ya se ha descubierto que son de interés comercial: algunos insecticidas lo usan. Son de interés médico: se utilizan para marcar tumores cerebrales con el fin de permitir una cirugía más precisa.
Estructura
La naturaleza de las proteínas está determinada sobre todo por su secuencia de aminoácidos, que constituye su estructura primaria . Los aminoácidos que tienen propiedades químicas muy diversas, su disposición a lo largo de la cadena polipeptídica determina su disposición espacial. Esto se describe localmente por su estructura secundaria , estabilizada por enlaces de hidrógeno entre residuos de aminoácidos vecinos, y globalmente por su estructura terciaria , estabilizada por todas las interacciones entre los residuos, a veces muy distantes en la secuencia del péptido pero puestas en contacto espacialmente por el plegamiento. de la proteína , así como entre la proteína misma y su entorno. Finalmente, la estructura cuaternaria de este conjunto describe el ensamblaje de varias subunidades de proteínas para formar un complejo funcional .
También se pueden formar enlaces covalentes adicionales, ya sea dentro de la misma cadena de proteína o entre diferentes cadenas de péptidos dentro de una proteína, en particular a través de la formación de puentes disulfuro entre residuos de cisteína .
La mayoría de las proteínas adoptan una conformación tridimensional única. La forma natural de una proteína in vivo es su estado nativo , que es la forma que toma para ser biológicamente activa y funcional. Muchas proteínas son biológicamente activas a partir de ellas bajo el efecto de la distribución espacial de los residuos de aminoácidos que las constituyen, otras necesitan ayuda para hacer esto mediante proteínas chaperonas para que se plieguen según su estado nativo.
Niveles de organización
En bioquímica , por lo tanto, podemos distinguir cuatro niveles de organización para describir la estructura de las proteínas:
- La estructura primaria corresponde a la secuencia de aminoácidos.
- La estructura secundaria describe la disposición de los residuos de aminoácidos observables a escala atómica. Estabilizados por enlaces de hidrógeno , estos arreglos locales son, por ejemplo , hélices α , láminas β , barriles β o codos. Hay varias variedades y es común que una proteína tenga varios tipos de estructuras secundarias en su conjunto.
- La estructura terciaria corresponde a la forma general de la proteína observable en la escala de la molécula completa. Describe las interacciones entre los diferentes elementos de la estructura secundaria. Se estabiliza mediante un conjunto completo de interacciones que suelen conducir a la formación de un núcleo hidrófobo , posiblemente con enlaces salinos , enlaces de hidrógeno, puentes disulfuro o incluso modificaciones postraduccionales . Una estructura terciaria a menudo se denomina plegamiento de una proteína.
- La estructura cuaternaria describe el complejo resultante del ensamblaje de múltiples moléculas de proteínas (más cadenas de polipéptidos), llamadas en este caso subunidades de proteínas para formar un único complejo de proteínas. Todas las proteínas no constan necesariamente de varias subunidades y, por lo tanto, no siempre tienen una estructura cuaternaria.
Las proteínas no son moléculas completamente rígidas. Es probable que adopten varias conformaciones relacionadas mientras realizan sus funciones biológicas. La transición de una de estas conformaciones a otra se denomina cambio conformacional . En el caso de una enzima, por ejemplo, tales cambios conformacionales pueden ser inducidos por la interacción con el sustrato al nivel del sitio activo . En solución, las proteínas también sufren muchos cambios conformacionales debido a la vibración térmica de la colisión con otras moléculas.
Implicaciones biológicas y determinación de estructuras terciarias y cuaternarias
Hay tres grandes grupos de proteínas según su estructura terciaria o cuaternaria: las proteínas globulares , las proteínas fibrosas y las proteínas de membrana . Casi todas las proteínas globulares son solubles y, a menudo, son enzimas . Las proteínas fibrosas a menudo juegan un papel estructural, como el colágeno , el componente principal del tejido conectivo , o la queratina , un componente proteico del cabello y las uñas . Las proteínas de membrana son a menudo receptores o canales que permiten que moléculas con carga eléctrica o polar pasen a través de la membrana .
El conocimiento de la estructura terciaria, o incluso cuaternaria, de una proteína puede proporcionar información importante para comprender cómo esta proteína realiza su función biológica. La cristalografía de rayos X y la espectroscopia de RMN son métodos experimentales habituales para estudiar la estructura de las proteínas, que pueden proporcionar una y otra información con una resolución a escala atómica . Los datos de RMN proporcionan información a partir de la cual es posible estimar un subconjunto de distancias entre ciertos pares de átomos, lo que permite deducir las posibles conformaciones de esta molécula. La interferometría de polarización dual es un método analítico cuantitativo para medir la conformación general de la proteína y sus cambios conformacionales en función de su interacción con otros estímulos. El dicroísmo circular proporciona otra técnica de laboratorio para resolver ciertos elementos de la estructura secundaria de las proteínas ( hélices α y láminas β particulares). La microscopía crioelectrónica proporciona información estructural a menor resolución sobre proteínas muy grandes, incluidos los virus . La cristalografía electrónica (en) , técnica final de la anterior, permite en algunos casos producir también datos de alta resolución, especialmente para cristales bidimensionales de proteínas de membrana . Las estructuras proteicas resueltas generalmente se depositan en el Protein Data Bank (PDB), una base de datos de acceso abierto que proporciona la estructura de mil proteínas para las que están disponibles las coordenadas cartesianas de cada átomo.
El número de proteínas cuya estructura se ha resuelto es mucho menor que el número de genes cuya secuencia se conoce. Además, el subconjunto de proteínas cuya estructura se ha resuelto está sesgado a favor de proteínas que pueden prepararse fácilmente para su análisis mediante cristalografía de rayos X, uno de los principales métodos para determinar las estructuras de las proteínas. En particular, las proteínas globulares son comparativamente las más fáciles de cristalizar para la cristalografía, mientras que las proteínas de membrana son más difíciles de cristalizar y están subrepresentadas entre las proteínas disponibles en PDB. Para remediar esta situación, se han emprendido enfoques de genómica estructural con el fin de resolver las estructuras representativas de las principales clases de plegamiento de proteínas . Los métodos de predicción de la estructura de la proteína tienen como objetivo proporcionar los medios para generar la estructura plausible de una proteína a partir de estructuras que podrían determinarse experimentalmente.
Síntesis
Los α-amino proteinogénicos ácidos se ensamblan en polipéptidos dentro de las células por los ribosomas a partir de la información genética transmitida por el ARN mensajero del ADN que comprende los genes . Es la secuencia de nucleótidos del ADN, transcrita de manera idéntica en el ARN mensajero, que transporta la información leída por los ribosomas para producir proteínas de acuerdo con la secuencia de péptidos especificada por los genes. La correspondencia entre la secuencia de nucleótidos del ADN y el ARN mensajero, por un lado, y la secuencia de péptidos de las proteínas sintetizadas, por otro lado, está determinada por el código genético , que es esencialmente el mismo para todos los seres vivos conocidos, excepto para un número bastante limitado. variaciones.
Codigo genetico
El código genético establece la correspondencia entre un triplete de bases nucleicas , llamado codón , en el ARN mensajero y un α-aminoácido proteinogénico. Esta correspondencia se realiza in vivo por los ARN de transferencia , que son ARN que comprenden un centenar de nucleótidos como máximo y que llevan un aminoácido esterificando su extremo 3'-OH. Cada uno de los aminoácidos está vinculado a ARN de transferencia específicos, que también llevan codones específicos, de modo que cada uno de los 64 codones posibles puede codificar solo un aminoácido. Por otro lado, cada uno de los 22 aminoácidos proteinogénicos puede estar codificado por varios codones diferentes. Son las enzimas que llevan a cabo la esterificación de los ARN mensajeros con aminoácidos - aminoacil-ARNt sintetasas - las que mantienen el código genético: de hecho, estas enzimas se unen específicamente tanto a un ARN de transferencia dado como a un aminoácido dado, de modo que cada tipo de ARN de transferencia solo se esterifica con un aminoácido específico.
El caso de la selenocisteína y la pirrolisina es algo diferente en el sentido de que estos aminoácidos particulares no están codificados directamente por codones específicos, sino por la codificación de la traducción de los codones de terminación en presencia de secuencias de inserción particulares llamadas el elemento SECIS y el elemento, respectivamente. PYLIS , que recodifica los codones de parada UGA (Opal) y UAG (Ámbar) en selenocisteína y pirrolisina, respectivamente. Además, la selenocisteína no está unida como tal a su ARN de transferencia, porque es demasiado reactiva para existir libremente en la célula; es la serina la que está unida a un ARN de transferencia de selenocisteína Sec tRNA por la serina tRNA ligasa . Los ribosomas no pueden utilizar el seril - tRNA Sec, ya que no es reconocido por los factores de elongación implicados en la biosíntesis de proteínas , por lo que la serina puede incorporarse en selenoproteínas en lugar de selenocisteína. En contraste, serilo-tRNA Sec es un sustrato para ciertas enzimas que su conversión en selenocisteinil - ARNt Sec : conversión directa por la selenocisteína sintasa en bacterias , conversión indirecta a través de la O -phosphoséryl -ARNt Sec sucesivamente por el O - fosfoseril-tRNA Sec quinasa y O -fosfoseril-tRNA: selenocisteinil-tRNA sintasa en arqueas y eucariotas .
Los genes codificados en el ADN se transcriben en primer lugar en ARN premensajero mediante enzimas como las ARN polimerasas . La mayoría de los seres vivos modifican este ARN pre-mensajero a través de un conjunto de procesos llamados modificaciones postranscripcionales que conducen al ARN mensajero maduro. Los ribosomas pueden utilizar este último como modelo durante la biosíntesis de proteínas . En procariotas , el ARN mensajero se puede utilizar tan pronto como se sintetice o se traduzca en proteínas después de salir del nucleoide . Por el contrario, en eucariotas , el ARN mensajero se produce en el núcleo de la célula mientras que las proteínas se sintetizan en el citoplasma , por lo que el ARN mensajero debe atravesar la membrana nuclear .
Biosíntesis
La biosíntesis de una proteína a partir de un ARN mensajero es la traducción de este ARNm. El ARN mensajero se une al ribosoma, que lo lee secuencialmente en tres nucleótidos en cada etapa de síntesis. Cada triplete de nucleótidos constituye un codón en el ARN mensajero, al que se puede unir el anticodón de un ARN de transferencia que proporciona el aminoácido correspondiente. El emparejamiento entre el codón y el anticodón se basa en la complementariedad de sus respectivas secuencias . Es esta complementariedad la que asegura el reconocimiento entre el ARN de transferencia y el codón del ARN mensajero. El aminoácido proporcionado por el ARN de transferencia en el ribosoma establece un enlace peptídico con el extremo C -terminal de la cadena naciente, lo que permite que se extienda por un residuo de aminoácido. Luego, el ribosoma mueve tres nucleótidos en el ARN mensajero para enfrentarse a un nuevo codón, que sigue exactamente al codón anterior. Este proceso se repite hasta que el ribosoma está frente a un codón de parada , en cuyo caso se detiene la traducción.
Se efectúa la biosíntesis de una proteína y el residuo tras residuo, el extremo N -terminal al extremo C -terminal . Una vez sintetizada, la proteína puede sufrir diversas modificaciones postraduccionales como escisión , fosforilación , acetilación , amidación , metilación , glicosilación , lipidación o incluso la formación de enlaces disulfuro . El tamaño de las proteínas así sintetizadas es muy variable. Este tamaño puede expresarse en número de residuos de aminoácidos que constituyen estas proteínas, así como en daltons (símbolo Da), que en biología molecular corresponden a la unidad de masa atómica . Como las proteínas son a menudo moléculas bastante grandes, su masa se expresa a menudo en kilodaltons (símbolo kDa). Por ejemplo, las proteínas de levadura tienen una longitud promedio de 466 residuos de aminoácidos, para una masa de 53 kDa . Las mayores proteínas conocidas son los titins de los sarcómeros que forman las miofibrillas de los músculos esqueléticos estriados : ratón titina contiene algunos 35.213 residuos de aminoácidos compuestas de 551,739 átomos con una masa de más de 3.900 kDa y una longitud de l del orden de 1 m .
Síntesis química
Las proteínas pequeñas también pueden sintetizarse in vitro mediante una variedad de métodos conocidos de síntesis de péptidos , que se basan en técnicas de síntesis orgánica tales como ligación química (en) para producir péptidos de manera eficaz. La síntesis química permite introducir aminoácidos no naturales en la cadena polipeptídica, por ejemplo colocando sondas fluorescentes en la cadena lateral de algunos de ellos. Estos métodos son útiles en el laboratorio en bioquímica y biología celular, pero generalmente no se emplean para aplicaciones comerciales. La síntesis química no es eficaz para sintetizar péptidos de más de aproximadamente 300 residuos de aminoácidos, y las proteínas así producidas pueden no asumir fácilmente su estructura terciaria nativa. La mayoría de los métodos de síntesis química de proteínas proceden del extremo C -terminal al extremo N -terminal , es decir, en la dirección opuesta a la biosíntesis de proteínas por los ribosomas .
Funciones
Entre todos los constituyentes de la célula, las proteínas son los elementos más activos. Aparte de algunos ARN , la mayoría de las otras moléculas biológicas no son lo suficientemente reactivas químicamente y son las proteínas las que actúan sobre ellas. Las proteínas constituyen aproximadamente la mitad de la materia seca de una célula de E. coli , mientras que el ARN y el ADN constituyen un quinto y un 3%, respectivamente. Todas las proteínas expresadas en una célula constituyen su proteoma .
La principal característica de las proteínas que les permite realizar sus funciones biológicas es su capacidad para unirse a otras moléculas de una forma muy específica y muy estrecha. La región de una proteína que se une a otra molécula es su sitio de unión, que a menudo forma una depresión, cavidad o "bolsillo" en la superficie de la molécula. Es la estructura terciaria de la proteína y la naturaleza química de las cadenas laterales de los residuos de aminoácidos del sitio de unión lo que determina la especificidad de esta interacción. Los sitios de unión pueden dar lugar a enlaces particularmente específicos y apretados: Así, el inhibidor de la ribonucleasa se une a humano angiogenina con una sub-femtomolar constante de disociación ( <10 -15 mol L -1 ) pero no se une en absoluto a la Ranpirnase , homóloga de anfibio de esta proteína (constante superior a 1 mol L -1 ). Una ligera modificación química puede alterar radicalmente la capacidad de una molécula para interactuar con una proteína determinada. Por tanto, la aminoacil-tRNA sintetasa específica de la valina se une a esta última sin interactuar con la isoleucina , que sin embargo es estructuralmente muy cercana a ella.
Las proteínas pueden unirse a otras proteínas o a moléculas pequeñas como sustratos . Cuando se unen específicamente a otras proteínas que son idénticas a ellas mismas, pueden polimerizar para formar fibrillas . Esto es común para las proteínas estructurales, formadas a partir de monómeros globulares que se autoensamblan para formar fibras rígidas. De las interacciones proteína-proteína también regulan su actividad enzimática , el progreso del ciclo celular y el ensamblaje de grandes complejos proteicos realizando reacciones muy relacionadas compartiendo una función biológica común. Las proteínas también pueden unirse a la superficie de las membranas celulares y, a menudo, incluso convertirse en una parte integral de ellas. La capacidad de ciertas proteínas para cambiar de conformación cuando se unen a moléculas específicas permite la construcción de redes de señalización celular extremadamente complejas. En general, el estudio de las interacciones entre proteínas específicas es un elemento clave para comprender cómo funcionan las células y su capacidad para intercambiar información.
Enzimas
La parte más visible de las proteínas en la célula es la enzima , es decir, la biomolécula que cataliza las reacciones químicas . Las enzimas son generalmente muy específicas y solo aceleran una o algunas reacciones químicas. La gran mayoría de las reacciones químicas del metabolismo se llevan a cabo mediante enzimas. Además del metabolismo, estos últimos también participan en la expresión génica , la replicación del ADN , la reparación del ADN , la transcripción del ADN en ARN y la traducción del ARN mensajero en proteínas. Algunas enzimas trabajan en otras proteínas para unirse o escindir ciertos grupos funcionales y residuos de otras biomoléculas en ellas, en un proceso llamado modificación postraduccional . Las enzimas catalizan más de 5000 reacciones químicas diferentes. Como todos los catalizadores, no modifican los equilibrios químicos sino que aceleran las reacciones, a veces en proporciones considerables; por tanto, la orotidina-5'-fosfato descarboxilasa cataliza en milisegundos una reacción que de otro modo llevaría varios millones de años.
Las moléculas que se unen a las enzimas y son alteradas químicamente por ellas se denominan sustratos . Aunque las enzimas a veces constan de varios cientos de residuos de aminoácidos, solo unos pocos de ellos entran en contacto con el (los) sustrato (s) de la enzima, y un número muy pequeño, generalmente tres o cuatro, están directamente involucrados en la catálisis. El sitio activo es la región de una enzima involucrada en la reacción química catalizada por esta proteína: agrupa los residuos que se unen al sustrato o contribuyen a su posicionamiento, así como los residuos que catalizan directamente la reacción.
Señalización celular y unión a ligando
Muchas proteínas están involucradas en los mecanismos de señalización celular y transducción de señales . Ciertas proteínas como la insulina pertenecen al entorno extracelular y transmiten una señal desde la célula donde se sintetizan a otras células que a veces se encuentran en tejidos distantes. Otras son proteínas de membrana que actúan como receptores cuya función principal es unirse a moléculas portadoras de señales e inducir una respuesta bioquímica en la célula diana. Muchos receptores de membrana tienen un sitio de unión expuesto al exterior de la célula y un efector de campo (en) en contacto con el medio intracelular. Este dominio efector puede tener una actividad enzimática o puede sufrir cambios conformacionales que actúan sobre otras proteínas intracelulares.
Los anticuerpos son componentes proteicos del sistema inmunológico cuya función principal es unirse a antígenos o xenobióticos para marcarlos para su eliminación del organismo. Los anticuerpos pueden secretarse en el medio extracelular o anclarse en la membrana plasmática de linfocitos B especializados llamados células plasmáticas . Cuando las enzimas son muy específicas para sus sustratos con el fin de acelerar reacciones químicas muy precisas, los anticuerpos no tienen esta limitación; por otro lado, su afinidad por su objetivo es extremadamente alta.
Muchas proteínas transportadoras de ligandos se unen específicamente a moléculas pequeñas y las transportan a sus destinos a través de las células y tejidos de organismos multicelulares . Estas proteínas deben tener una alta afinidad por su ligando cuando la concentración del mismo es alta, pero también deben poder liberarlo cuando su concentración es baja en los tejidos diana. El ejemplo canónico de la proteína portadora de ligandos es la hemoglobina , que transporta oxígeno desde los pulmones a otros órganos y tejidos en todos los vertebrados y tiene contrapartes relacionadas en todos los reinos vivientes. Las lectinas son proteínas que se unen de forma reversible a determinados carbohidratos con una especificidad muy alta. Desempeñan un papel en los fenómenos de reconocimiento biológico que involucran células y proteínas.
Las proteínas transmembrana también pueden desempeñar el papel de ligando transportador. La proteína puede alterar la permeabilidad de la membrana celular a pequeñas moléculas polares e iones . La membrana en sí tiene un núcleo hidrófobo a través del cual las moléculas polares o cargadas eléctricamente no pueden difundirse. Las proteínas de membrana pueden contener así uno o más canales a través de la membrana celular y permitir que estas moléculas y estos iones la atraviesen. Muchos canales de iones son muy específicos del ión por el que circulan. Por tanto, los canales de potasio y los canales de sodio suelen ser específicos para uno de los dos iones potasio y sodio con exclusión del otro.
Proteínas estructurales
Las proteínas estructurales confieren rigidez y rigidez a los componentes biológicos que, sin ellos, serían fluidos. La mayoría de las proteínas estructurales son fibrosas. Este es el caso, por ejemplo, del colágeno y la elastina, que son constituyentes esenciales de los tejidos conectivos como el cartílago , y la queratina presente en estructuras duras o filamentosas como el pelo , las uñas , las plumas , las pezuñas y el exoesqueleto de algunos animales . Ciertas proteínas globulares también pueden jugar un papel estructural, por ejemplo actina y tubulina cuyos monómeros son globulares y solubles pero polimerizan para formar filamentos largos y rígidos que constituyen el citoesqueleto , lo que permite que la célula mantenga su forma y tamaño.
Las proteínas motoras son proteínas estructurales específicas que son capaces de generar fuerzas mecánicas. Estos son, por ejemplo , miosina , quinesina y dineína . Estas proteínas son esenciales para la motilidad de los organismos unicelulares , así como para el esperma de los organismos multicelulares . También ayudan a generar las fuerzas que actúan en la contracción muscular y juegan un papel esencial en el transporte intracelular.
Sin embargo, las manoproteínas parecen tener funciones clave dentro de las células, en particular controlando la porosidad de la pared celular.
Resumen de funciones realizadas por proteínas
Por tanto, las proteínas realizan una amplia variedad de funciones dentro de la célula y el cuerpo:
- las proteínas estructurales que permiten a la célula mantener su organización en el espacio y que son los constituyentes del citoesqueleto ;
- las proteínas de transporte , que proporcionan la transferencia de diferentes moléculas dentro y fuera de las células;
- las proteínas reguladoras , que modulan la actividad de otras proteínas o que controlan la expresión génica ;
- las proteínas de señalización que capturan las señales externas y aseguran su transmisión en la célula u organismo; hay varios tipos, por ejemplo , las proteínas hormonales , que ayudan a coordinar las actividades de un organismo actuando como señales entre las células;
- las proteínas receptoras , que detectan moléculas mensajeras y otras señales para que la célula actúe en consecuencia:
- las proteínas sensoriales detectan señales ambientales y responden transmitiendo señales en la célula (por ejemplo, luz).
- los receptores de hormonas detectan hormonas y envían señales a la célula para que actúe en consecuencia (por ejemplo, la insulina es una hormona que, cuando se recibe, indica a la célula que absorba y use glucosa );
- las proteínas de motor , permitiendo que las células u organismos, o ciertos elementos (cilios) para mover o se deforme (por ejemplo, la. actina y miosina permitir que el músculo a contrato );
- las proteínas de defensa que protegen a la célula contra los agentes infecciosos (por ejemplo, el anticuerpo );
- las proteínas de almacenamiento que permiten la reserva del orden amino ácido biosintetizan otras proteínas (por ejemplo, la ovoalbúmina , la principal proteína de la clara de huevo proporciona almacenamiento para el desarrollo de embriones de pollo );
- las enzimas que modifican la velocidad de casi todas las reacciones químicas en la célula sin transformarse en la reacción.
Métodos de estudio
La estructura y funciones de las proteínas se pueden estudiar in vivo , in vitro e in silico . Los estudios in vivo permiten explorar el papel fisiológico de una proteína dentro de una célula viva o incluso dentro de un organismo en su conjunto. Los estudios in vitro de proteínas purificadas en entornos controlados son útiles para comprender cómo funciona una proteína in vivo : por ejemplo, estudiar la cinética de una enzima permite analizar el mecanismo químico de su actividad catalítica y su afinidad relativa con respecto a diferentes sustratos. . Los estudios in silico utilizan algoritmos informáticos para modelar proteínas.
Purificación de proteínas
Para poder analizarla in vitro , una proteína debe haber sido previamente purificada de los otros componentes químicos de la célula. Esto generalmente comienza con la lisis de la célula, durante la cual se rompe la membrana plasmática para liberar su contenido en una solución para dar un lisado. Esta mezcla se puede purificar mediante ultracentrifugación , lo que permite separar sus constituyentes en fracciones que contienen respectivamente proteínas solubles, lípidos y proteínas de membrana , orgánulos celulares y ácidos nucleicos . La precipitación de las proteínas por liberación permite concentrarlas a partir de este lisado. Entonces es posible utilizar varios tipos de cromatografía para aislar las proteínas que se desea estudiar según sus propiedades fisicoquímicas como su masa molar , su carga eléctrica o incluso su afinidad de unión. El grado de purificación se puede seguir utilizando varios tipos de electroforesis en gel si se conocen la masa molecular y el punto isoeléctrico de las proteínas estudiadas, por espectroscopia si la proteína tiene características espectroscópicas identificables, o por ensayo enzimático (en) si la proteína tiene actividad enzimática. . Además, las proteínas se pueden aislar según su carga eléctrica mediante enfoque isoeléctrico .
Las proteínas naturales eventualmente requieren una serie de pasos de purificación antes de que puedan estudiarse en el laboratorio. Con el fin de simplificar este proceso, se suele utilizar la ingeniería genética para modificar proteínas dotándolas de características que las hacen más fáciles de depurar sin alterar su estructura ni su actividad. Por lo tanto, agrega "etiquetas" reconocibles en la proteína en forma de secuencias de aminoácidos identificados, a menudo una serie de residuos de histidina ( etiqueta de polihistidina o etiqueta de His ) al extremo C -terminal o al ' extremo N -terminal de la cadena polipeptídica . Por lo tanto, cuando el lisado se coloca en una columna cromatográfica que contiene níquel , los residuos de histidina se combinan con el níquel y permanecen unidos a la columna mientras que los constituyentes no marcados la atraviesan sin detenerse. Se han desarrollado varios tipos de etiquetas para permitir a los investigadores purificar proteínas particulares a partir de mezclas complejas.
Localización celular
El estudio in vivo de las proteínas a menudo implica saber con precisión dónde se sintetizan y dónde se encuentran en las células. Aunque la mayoría de las proteínas intracelulares se producen en el citoplasma y la mayor parte de membrana o proteínas secretadas en el medio extracelular se producen en el retículo endoplásmico , es raro que entendemos precisamente cómo las proteínas se dirigen específicamente a ciertas estructuras celulares o ciertas estructuras celulares. Orgánulos . La ingeniería genética proporciona herramientas útiles para hacerse una idea de la ubicación de determinadas proteínas, por ejemplo al vincular la proteína a una proteína estudiada permitiendo la mancha, es decir, realizando una fusión de proteína entre la proteína estudiada y una proteína utilizada como un marcador, como una proteína verde fluorescente . La localización intracelular de la proteína de fusión resultante puede visualizarse fácil y eficazmente mediante microscopía .
Otros métodos de localización intracelular de proteínas implican el uso de marcadores conocidos para ciertos compartimentos celulares como retículo endoplásmico , aparato de Golgi , lisosomas , mitocondrias , cloroplastos , membrana plasmática , etc. Por ejemplo, es posible localizar proteínas marcadas con un marcador fluorescente o dirigidas con anticuerpos contra estos marcadores. Las técnicas de inmunofluorescencia permiten así localizar proteínas específicas. Los pigmentos fluorescentes también se utilizan para etiquetar los compartimentos de las células con un propósito similar.
La inmunohistoquímica generalmente utiliza un anticuerpo dirigido a una o más proteínas diferentes que se conjugan con enzimas que emiten señales luminiscentes o cromogénicas que se pueden comparar con varias muestras, lo que permite deducir información sobre la ubicación de las proteínas estudiadas. También es posible usar técnicas de co-fraccionamiento en un gradiente de sacarosa (u otra sustancia) usando centrifugación isopícnica.
La microscopía inmunoelectrónica combina el uso de microscopía electrónica convencional con el uso de un anticuerpo dirigido contra la proteína estudiada, estando este anticuerpo previamente conjugado a un material de alta densidad electrónica como el oro . Esto permite localizar detalles ultraestructurales así como la proteína en estudio.
Proteómica
El conjunto de proteínas de una célula o de un tipo de célula constituye su proteoma , y la disciplina científica que lo estudia es la proteómica . Estos dos términos fueron acuñados por analogía con genoma y genómica . Sin embargo, si el proteoma se deriva del genoma, no es posible predecir exactamente cuál será el proteoma de una célula a partir del simple conocimiento de su genoma. De hecho, la expresión de un gen varía de una célula a otra dentro del mismo organismo en función de la diferenciación celular , o incluso en la misma célula en función del ciclo celular . Además, el mismo gen puede producir varias proteínas (por ejemplo, poliproteínas virales ) y, a menudo, son necesarias modificaciones postraduccionales para hacer que una proteína sea activa.
Entre las técnicas experimentales utilizadas en la proteómica, observamos electroforesis bidimensional , que permite la separación de un gran número de proteínas, espectrometría de masas , lo que permite una rápida y de alto rendimiento de identificación de proteínas, así como la secuenciación de péptidos. (Con mayor frecuencia después de digestión en gel (en) ), chips de proteínas (en) , que permiten la detección de concentraciones relativas de un gran número de proteínas presentes en una célula, y el enfoque de doble híbrido que también permite la exploración de interacciones proteína-proteína . El conjunto de interacciones proteína-proteína en una célula se denomina interactoma . El enfoque para determinar la estructura de las proteínas entre todas sus posibles conformaciones es la genómica estructural .
Bioinformática
En la actualidad, hay una variedad de métodos informáticos disponibles para analizar la estructura, función y evolución de las proteínas. El desarrollo de tales herramientas se hizo necesario por la gran cantidad de datos genómicos y proteómicos disponibles para un gran número de seres vivos, comenzando por el genoma humano . Es imposible estudiar todas las proteínas de forma experimental, por lo que solo un pequeño número de ellas se estudian en el laboratorio mientras que las herramientas computacionales permiten extrapolar los resultados así obtenidos a otras proteínas que son similares a ellas. Dichas proteínas homólogas se identifican eficazmente mediante técnicas de alineación de secuencias . Las herramientas de generación de perfiles de secuencias de péptidos permiten localizar sitios escindidos por enzimas de restricción , leer marcos en secuencias de nucleótidos y predecir estructuras secundarias . También es posible construir árboles filogenéticos y desarrollar hipótesis sobre la evolución utilizando software como ClustalW (in) para rastrear los ancestros de los organismos modernos y sus genes. Las herramientas bioinformáticas se han vuelto esenciales para el estudio de genes y proteínas expresados por estos genes.
Predicción y simulación de estructuras
Además de la genómica estructural, la predicción de la estructura de las proteínas tiene como objetivo desarrollar medios para construir de manera eficiente modelos plausibles que describan la estructura de las proteínas que no podrían resolverse experimentalmente. La forma más eficaz de predecir la estructura, denominada modelo de homología , se basa en la existencia de estructuras modelo conocidas cuya secuencia es similar a la de la proteína en estudio. El objetivo de la genómica estructural es proporcionar datos suficientes sobre las estructuras resueltas para permitir el esclarecimiento de las que quedan por resolver. Aunque sigue siendo difícil modelar estructuras con precisión cuando solo hay modelos estructurales distantes a los que hacer referencia, se cree que el meollo del problema radica en la alineación de las secuencias porque se pueden encontrar modelos muy exactos. es conocida. Muchas predicciones de estructuras fueron útiles para el campo emergente de la ingeniería de proteínas (en) , que incluyó el desarrollo de nuevos modos de plegamiento . Un problema más complejo de resolver mediante cálculo es la predicción de interacciones intermoleculares, como la predicción del anclaje de moléculas y las interacciones proteína-proteína .
El plegamiento y unión de proteínas se puede simular utilizando técnicas como la mecánica molecular , la dinámica molecular y el método Monte Carlo , que se benefician de cada vez más arquitecturas informáticas de computación paralela y distribuida , como el proyecto Folding @ home o el modelado molecular en un procesador gráfico . El plegamiento de pequeños dominios de proteínas α-helicoidales , como el casquete de villina y la proteína accesoria del VIH se ha simulado con éxito in silico , y los métodos híbridos que combinan la dinámica molecular estándar con elementos de la mecánica cuántica han permitido la exploración de los estados electrónicos de rodopsinas .
Propiedades
Fenotipo
Por tanto, el plan para producir proteínas depende ante todo del gen . Sin embargo, las secuencias de genes no son estrictamente idénticas de un individuo a otro. Además, en el caso de los seres vivos diploides , existen dos copias de cada gen. Y estas dos copias no son necesariamente idénticas. Por tanto, un gen existe en varias versiones de un individuo a otro y, a veces, en el mismo individuo. Estas diferentes versiones se llaman alelos . El conjunto de alelos de un individuo forma el genotipo .
Dado que los genes existen en múltiples versiones, las proteínas también existirán en diferentes versiones. Estas versiones diferentes de proteínas hará que las diferencias de un individuo a otro, tal individuo tiene los ojos azules, sino como otra tienen ojos negros, etc . Estas características, visibles o no, específicas de cada individuo se denominan fenotipo . En el mismo individuo, se dice que un grupo de proteínas con una secuencia similar y una función idéntica es isoforma . Las isoformas pueden ser el resultado del corte y empalme alternativo del mismo gen, la expresión de varios alelos de un gen o la presencia de varios genes homólogos en el genoma.
Evolución
Durante la evolución , las acumulaciones de mutaciones han hecho que los genes diverjan dentro y entre especies . De aquí proviene la diversidad de proteínas asociadas con ellos. Sin embargo, es posible definir familias de proteínas, que a su vez corresponden a familias de genes. Así, en una especie genes muy similares, y por tanto proteínas, pueden coexistir formando una familia. Es probable que dos especies estrechamente relacionadas tengan representantes de la misma familia de proteínas.
Hablamos de homología entre proteínas cuando diferentes proteínas tienen un origen común, un gen ancestral común.
La comparación de las secuencias de proteínas permite demostrar el grado de "parentesco" entre diferentes proteínas, se habla aquí de similitud de secuencias. La función de las proteínas puede divergir a medida que disminuye la similitud, dando lugar a familias de proteínas de origen común pero con funciones diferentes.
El análisis de las secuencias y estructuras de las proteínas ha demostrado que muchas se organizan en dominios , es decir, partes que adquieren estructura y realizan una función específica. La existencia de proteínas con varios dominios puede ser el resultado de la recombinación en un solo gen de varios genes originalmente individuales y, a la inversa, las proteínas compuestas por un solo dominio pueden ser el resultado de la separación en varios genes de un gen originalmente. -proteína de dominio.
Comida humana
Durante la digestión , del estómago, las proteínas de origen vegetal, bacteriano, fúngico o animal son degradadas ( hidrolizadas ) por proteasas ; se descomponen en polipéptidos y luego en aminoácidos útiles para el cuerpo , incluidos los aminoácidos esenciales (que el cuerpo no puede sintetizar). El pepsinógeno se convierte en pepsina en contacto con el ácido clorhídrico del estómago. La pepsina es la única enzima proteolítica que digiere el colágeno , la principal proteína del tejido conectivo .
La digestión de proteínas tiene lugar principalmente en el duodeno . Se absorben principalmente cuando llegan al yeyuno y solo el 1% de las proteínas ingeridas se encuentran en las heces . Ciertos aminoácidos permanecen en las células epiteliales del intestino, utilizados para la biosíntesis de nuevas proteínas, incluidas las proteínas intestinales que son constantemente digeridas, recicladas y absorbidas por el intestino delgado .
La digestibilidad de las proteínas varía considerablemente según su naturaleza y la preparación de los alimentos.
Cantidades recomendadas
La ANSES recomienda una ingesta dietética recomendada (IDR) de 0,83 g · kg -1 · d -1 , para un máximo de 2,2 g · kg -1 · d -1 en adultos con buena salud, 62 g por día para un hombre de 75 kg . Cabe señalar que las ANC son superiores a las necesidades medias que son 0,66 g · kg -1 · d -1 según este mismo informe, lo que daría 49,5 g diarios para el caso anterior.
Las necesidades medias de proteína han sido definidas por la FAO, que recomienda 49 g de proteína para hombres adultos y 41 g para mujeres (47 si está embarazada, 58,5 si está amamantando).
Proteínas animales, fúngicas, vegetales
Según la Asociación Estadounidense del Corazón , no es necesario consumir proteína animal para tener suficiente proteína en su dieta: la proteína vegetal puede proporcionar suficientes aminoácidos esenciales y no esenciales, siempre que las fuentes de proteína de la dieta sean variadas y que las calorías la ingesta es suficiente para satisfacer las necesidades energéticas. No es necesario combinarlos en una misma comida. La Asociación Dietética Estadounidense también recuerda que la proteína vegetal puede satisfacer los requisitos de proteína si la dieta de la planta es variada y cumple con los requisitos energéticos. Además, “un surtido de alimentos vegetales consumidos en el transcurso de un día puede aportar todos los aminoácidos esenciales y asegurar la suficiente retención de nitrógeno y su uso en adultos sanos, por lo que la combinación de proteínas durante la misma comida no es necesaria. "
- Proteínas animales : siempre van acompañadas de lípidos saturados , cuyo consumo suele ser excesivo, y en ocasiones de aditivos alimentarios (como los nitritos de los embutidos , sospechosos de ser cancerígenos). También se cree que las proteínas animales o productos asociados como las aminas heterocíclicas son un factor de riesgo para ciertos cánceres ( colon , vejiga ). Desde 2015 , la OMS y la IARC han clasificado la carne roja (cerdo, ternera, oveja, caballo y cabra) como probable cancerígeno y la carne procesada como cancerígena comprobado (34.000 muertes / año en todo el mundo, según un estudio de Global Burden of Disease Proyecto ; según la OMS: comer 50 gramos de carne procesada al día aumenta el riesgo de cáncer colorrectal en un 18% (se dice que una carne se procesa si se ha sometido a salazón, maduración, fermentación, ahumado u otros procesos destinados a mejorar su calidad). sabor o su conservación) .Por falta de datos, el Grupo de Trabajo de la IARC no pudo clasificar la carne cruda con respecto al riesgo de cáncer, pero recuerda que presenta un riesgo infeccioso . de tener contaminantes bioconcentrados a través de la cadena alimentaria
- Proteínas vegetales : los efectos positivos se asocian a plantas ricas en proteínas. Las legumbres son ricas en proteínas, pero también en fibra , minerales y aportan sensación de saciedad por un índice glucémico bajo. El consumo de frijoles contribuye a reducir los niveles de colesterol y al riesgo de accidentes cardiovasculares y ciertos cánceres ( colorrectal , próstata y páncreas ). Obviamente son una alternativa para veganos o vegetarianos. Los frutos secos, las verduras, los frijoles, la quinua y los cereales contienen altas cantidades de proteínas pero también de energía.
- Proteína fúngica : los hongos comestibles suelen tener un alto contenido de proteínas y, al igual que las plantas, son fuentes de fibra dietética y minerales. Por otro lado, recolectados en la naturaleza o cultivados en sustratos contaminados, tienden a acumular una gran cantidad de metales pesados , metaloides e incluso radionucleidos .
Calidad proteica
Todos los aminoácidos necesarios deben ser aportados por los alimentos, so pena de ser deficientes, lo que implica fuentes diversificadas de proteínas.
La recomendación de combinar proteínas animales y vegetales en cada comida ha sido invalidada desde 1994 a raíz de un artículo de Vernon Young y Peter Pellett que se convirtió en una referencia sobre el metabolismo proteico en humanos, confirmando que la combinación de proteínas en la comida es totalmente innecesaria. Las personas que no desean comer proteína animal no corren el riesgo de sufrir un desequilibrio de aminoácidos de las proteínas vegetales en su dieta. Muchas proteínas vegetales contienen algo menos de uno o más de los aminoácidos esenciales ( especialmente lisina y en menor medida metionina y treonina ), sin que el consumo exclusivo de fuentes de proteínas vegetales impida tener una dieta equilibrada en aminoácidos esenciales.
Las conclusiones del artículo de Young y Pellet sólo deben tenerse en cuenta en el caso muy general en el que los cereales no son la fuente exclusiva de alimento, que se esmeran en precisar, además, donde explican en otros artículos. Así, en algunas regiones desfavorecidas, las raciones de alimentos pueden incluir solo cereales, lo que causa graves problemas de salud para los niños pequeños, por ejemplo en los hogares pobres del estado de Madhya Pradesh en la India (trigo y arroz).
Además, las empresas semilleras buscan obtener o ya han obtenido variedades de cereales con un contenido de aminoácidos modificado ( OGM ), por ejemplo maíz enriquecido en lisina.
Las autoridades sanitarias francesas (AFSSA / ANSES ) siguen negándose a resolver esta cuestión.
Complementos alimenticios
Los complementos alimenticios proteicos existen para deportistas que deseen desarrollar su volumen muscular y para personas con deficiencias proteicas. Las proteínas utilizadas son a menudo proteínas obtenidas de alfalfa ( Alfalfa en forma de extracto de hoja (EFL) ) , habas , guisantes o suero (bajo el nombre de "suero de leche") y aminoácidos ramificados designados con el nombre de "BCAA". .
Alimentos ricos en proteínas
- Los hongos tienen un contenido de proteínas difícil de medir con precisión (contenido previamente sobreestimado en un 70 a 200% a veces) pero a menudo relativamente alto (15 a 35% del peso seco del hongo), mucho más alto que los cereales como el trigo y el maíz. de interés gastronómico. Estos niveles son comparables a los de legumbres como guisantes y lentejas.
Los aminoácidos esenciales a menudo representan una parte significativa de estas proteínas ( p. Ej., 61,8 y 63,3% de los niveles de aminoácidos totales, respectivamente, en Tricholoma portentosum y Tricholoma terreum (en los que la leucina , la isoleucina y el triptófano son los aminoácidos limitantes) Los puntajes de aminoácidos corregidos (PDCAAS) de las proteínas de estos dos hongos son bajos en comparación con los de la caseína, la clara de huevo y la soja, pero más altos que los de muchas proteínas vegetales. El contenido de grasa fue bajo (5.7% para Tricholoma porterosum y 6.6 %). % para Tricholoma terreum ) en ambas especies, con los ácidos oleico y linoleico que representan más del 75% del total de ácidos grasos.
Algunos como el hongo de Paris (3,09 g de proteína por 100 g ) se han cultivado y secado durante mucho tiempo, pero individualmente ( como otros alimentos) pueden ser deficientes en ciertos aminoácidos ( por ejemplo , aminoácidos que contienen azufre, metionina y cistina en el caso de las setas de ostra, por ejemplo) pero son ricas en lisina y leucina que faltan, por ejemplo, en los cereales. Todavía se están descubriendo virtudes ( por ejemplo: una de estas proteínas parece inhibir las alergias alimentarias en ratones ) y defectos ( por ejemplo: se ha demostrado que otra proteína fúngica es cardiotóxica ).
- Los alimentos de origen animal son generalmente más proteínas que los de origen vegetal, y en particular huevos (ricos en albúmina) o queso (caseína, etc.), como el parmesano, por ejemplo, que contiene 39,4 g / 100 g, más que la carne. y pescado. Además de determinadas carnes ( p. Ej., Pechuga de pollo cocida con un contenido medio de 29,2 g / 100 g) como la carne de vacuno que contiene 26 g / 100 g, pescados como el atún blanco o las sardinas también contienen aproximadamente 30 g / 100 g. Los huevos también son una fuente de proteínas (24 g / 100 g por cuatro huevos).
- Ciertas plantas o semillas son muy ricas en proteínas: aceite de semillas ( de almendra , pistacho , lino , etc. ) y legumbres ( garbanzos , judías , lentejas , etc. ). Por lo tanto, 100 g de producto crudo contienen una proporción de proteínas de: 58 g de espirulina , 38 g de soja , 30 g de semillas de calabaza , 25 g de frijoles negros , 24 g de lentejas , 21 g de seitán (gluten) y nueces , 20 g de almendras y sémola , 15 g de avena , 15 g de arroz salvaje, 14 g de quinua .
- Las levaduras , bacterias y cianobacterias rara vez se cultivan para comerlas directamente, pero la levadura o la espirulina (58 g de proteína por 100 g de espirulina) son muy ricas en proteínas.
Notas y referencias
- Descubrimientos de proteínas
- Gregory A. Petsko y Dagmar Ringe ( trad. Del inglés), Estructura y función de las proteínas , Bruselas, Universidad De BoekNoviembre de 2008, 190 p. ( ISBN 978-2-8041-5888-0 , leer en línea )
- (en) Alex Gutteridge y Janet M. Thornton , " Comprensión del conjunto de herramientas catalíticas de la naturaleza " , Tendencias en ciencias bioquímicas , vol. 30, n o 11,noviembre 2005, p. 622-629 ( PMID 16214343 , DOI 10.1016 / j.tibs.2005.09.006 , leer en línea )
- (en) Harvey Lodish, Arnold Berk, Paul Matsudaira, Chris A. Kaiser, Monty Krieger, Matthew P. Scott, Lawrence Zipursky y James Darnell, Molecular Cell Biology , Nueva York, WH Freeman & Company 5 ª edición,agosto de 2003, 973 p. ( ISBN 978-0-7167-4366-8 )
- Garcia Martin S (2015) Dinámica manoproteínas: autoensamblaje de péptidos en monocapa Protegida nanopartículas de oro
- Mitch Leslie (2019) impacto del Outsize ; | Ciencia 18 de octubre de 2019: Vol. 366, número 6463, págs. 296-299 | DOI: 10.1126 / science.366.6463.296 ( resumen )
- Staudt, AC y Wenkel, S. (2011). Regulación de la función de las proteínas por 'microProteínas' . Informes EMBO, 12 (1), 35-42.
- (Wang et al (2009)
- zhang et al, 2009)
- (en) Zhaohui Xu, Arthur L. Horwich y Paul B. Sigler , " La estructura cristalina del asimétrico GroEL-GroES- (ADP) 7complejo de chaperonina ” , Nature , vol. 388, n o 6644,21 de agosto de 1997, p. 741-750 ( PMID 9285585 , DOI 10.1038 / 41944 , leer en línea )
- (en) Lisa J Harris, Eileen Skaletsky y Alexander McPherson , " Estructura cristalográfica de un anticuerpo monoclonal IgG1 intacto " , Journal of Molecular Biology , vol. 275, n o 5,6 de febrero de 1998, p. 861-872 ( PMID 9480774 , DOI 10.1006 / jmbi.1997.1508 , leer en línea )
- (en) W. Bolton y MF Perutz , " Síntesis de Fourier tridimensional de desoxihemoglobina de caballo a una resolución de 2,8 Å " , Nature , vol. 228, n o 5271,7 de noviembre de 1970, p. 551-552 ( PMID 5472471 , DOI 10.1038 / 228551a0 , Bibcode 1970Natur.228..551B , leer en línea )
- (en) Edward N. Baker, Thomas L. Blundell, John F. Cutfield, Susan M. Cutfield, Eleanor J. Dodson, Guy G. Dodson, Dorothy Crowfoot Hodgkin Sr. Roderick E. Hubbard, Neil W. Isaacs, Colin D. Reynolds, Kiwako Sakabe, Norioshi Sakabe y Numminate M. Vijayan , " La estructura de los cristales de insulina de cerdo 2Zn a una resolución de 1,5 Å " , Philosophical Transactions B , vol. 319, n o 11956 de julio de 1988, p. 369-456 ( PMID 2905485 , DOI 10.1098 / rstb.1988.0058 , Bibcode 1988RSPTB.319..369B , leer en línea )
- (en) Michael B. Berry y George N. Phillips Jr. , " Estructuras cristalinas de la adenilato quinasa de Bacillus stearothermophilus con Ap 5 A unido , Mg 2+ Ap 5 A y Mn 2+ Ap 5 Arevelan una posición intermedia de la tapa y seis geometría octaédrica coordinada para el Mg 2+ y Mn 2+ ligados ” , Proteínas: Estructura, Función y Bioinformática , vol. 32, n o 3,15 de agosto de 1998, p. 276-288 ( PMID 9715904 , leer en línea )
- (in) Harindarpal S. Gill y David Eisenberg , " La estructura cristalina de la fosfinotricina en el sitio activo de la glutamina sintetasa ilumina el mecanismo de inhibición enzimática " , Bioquímica , vol. 40, n o 7,20 de febrero de 2001, p. 1903-1912 ( PMID 11329256 , DOI 10.1021 / bi002438h , leer en línea )
- (in) Wojciech R. Rypniewski Hazel Holden e Ivan Rayment , " Consecuencias estructurales de la metilación reductora de residuos de lisina en lisozima de clara de huevo de gallina: Un análisis de rayos X a una resolución de 1.8-Å " , Bioquímica , vol. 32, n o 37,21 de septiembre de 1993, p. 9851-9858 ( PMID 8373783 , DOI 10.1021 / bi00088a041 , leer en línea )
- (en) Tamir Gonen Yifan Cheng, Piotr Sliz, Yoko Hiroaki Yoshinori Fujiyoshi, Stephen C. Harrison y Thomas Walz , " Interacciones lípido-proteína en cristales bidimensionales de doble capa AQP0 " , Nature , vol. 438, n o 7068,1 st de diciembre de de 2005, p. 633-638 ( PMID 16319884 , PMCID 1350984 , DOI 10.1038 / nature04321 , leer en línea )
- (in) Daron M. Standley, Akira R. Kinjo, Kengo Kinoshita y Haruki Nakamura , " Bases de datos de estructura de proteínas con nuevos servicios web para biología estructural e investigación biomédica " , Briefings in Bioinformatics , vol. 9, n o 4,julio 2008, p. 276-285 ( PMID 18430752 , DOI 10.1093 / bib / bbn015 , leer en línea )
- (en) Peter Walian, Timothy A Cross K y Bing Jap , " Genómica estructural de las proteínas de membrana " , Genome Biology , vol. 5, n o 4,2004, p. 215 ( PMID 15059248 , PMCID 395774 , DOI 10.1186 / gb-2004-5-4-215 , leer en línea )
- (en) Roy D. Sleator , " Predicción de funciones de proteínas " , Métodos en biología molecular , vol. 815,2012, p. 15-24 ( PMID 22130980 , DOI 10.1007 / 978-1-61779-424-7_2 , leer en línea )
- Forchhammer K, Bock A, “ Selenocisteína sintasa de Escherichia coli. Análisis de la secuencia de reacción ”, J. Biol. Chem. , vol. 266, n o 10,1991, p. 6324–8 ( PMID 2007585 )
- (en) Yuhei Araiso, Sotiria Palioura, Ryuichiro Ishitani, R. Lynn Sherrer, Patrick O'Donoghue, Jing Yuan, Hiroyuki Oshikane, Naoshi Domae Julian DeFranco, Dieter Söll y Osamu Nureki , " Perspectivas estructurales sobre ARN-dependiente y eucarial formación de selenocisteína ” , Nucleic Acids Research , vol. 36, n o 4,Marzo de 2008, p. 1187-1199 ( PMID 18158303 , PMCID 2275076 , DOI 10.1093 / nar / gkm1122 , leer en línea )
- (en) Sotiria Palioura R. Lynn Sherrer, Thomas A. Steitz Dieter Söll y Miljan Simonovic , " El complejo humano SepSecS-tRNA Sec revela el mecanismo de la educación selenocisteína " , Ciencia , vol. 325, n o 5938,17 de julio de 2009, p. 321-325 ( PMID 19608919 , PMCID 2857584 , DOI 10.1126 / science.1173755 , Bibcode 2009Sci ... 325..321P , leer en línea )
- (en) Alice B. Fulton y William B. Isaacs , " Titina, una proteína sarcomérica enorme y elástica con un papel probable en la morfogénesis " , BioEssays , vol. 13, n o 4,Abril de 1991, p. 157-161 ( PMID 1859393 , DOI 10.1002 / bies.950130403 , leer on-line )
- (in) " Titin (EC 2.7.11.1) (Connectin) Mus musculus (Mouse) " en ProtParam en ExPASy (consultado el 9 de mayo de 2015 )
- (in) Thomas Bruckdorfer Oleg Marder y Fernando Albericio , " De la producción de péptidos en cantidades de miligramos para investigación a cantidades de tonos múltiples para fármacos del futuro " , Biotecnología farmacéutica actual , vol. 5, n o 1,Febrero de 2004, p. 29-43 ( PMID 14965208 , DOI 10.2174 / 1389201043489620 , leer en línea )
- (in) Dirk Schwarzer y Philip A Cole , " Semisíntesis de proteínas y ligadura de proteínas expresadas: persiguiendo la cola de una proteína " , Current Opinion in Chemical Biology , vol. 9, n o 6,diciembre de 2005, p. 561-569 ( PMID 16226484 , DOI 10.1016 / j.cbpa.2005.09.018 , leer en línea )
- (en) Stephen BH Kent , " síntesis química total de proteínas " , Chemical Society Reviews , vol. 38, n o 2Febrero de 2009, p. 338-351 ( PMID 19169452 , DOI 10.1039 / B700141J , leer en línea )
- (en) R. Sankaranarayanan y D. Moras , " La fidelidad de la traducción del código genético " , Acta Biochimica Polonica , vol. 48, n o 22001, p. 323-335 ( PMID 11732604 , leer en línea )
- (en) John A. Copland, Melinda Sheffield-Moore, Nina Koldzic-Zivanovic, Sean Gentry, George Lamprou, Fotini Tzortzatou-Stathopoulou Vassilis Zoumpourlis, Randall J. Urban y Spiros A. Vlahopoulos , " Receptores de esteroides sexuales en la diferenciación esquelética y neoplasia epitelial: ¿es posible una intervención específica de tejido? ” , BioEssays , vol. 31, n o 6,Junio de 2009, p. 629-641 ( PMID 19382224 , DOI 10.1002 / bies.200800138 , leer en línea )
- (in) Stanislav Samarin y Asma Nusrat , " Regulación del complejo de unión apical epitelial por las GTPasas de la familia Rho " , Frontiers in Bioscience , vol. 14,enero de 2009, p. 1129-1142 ( PMID 19273120 , DOI 10.2741 / 3298 , leer en línea )
- (en) Ida Schomburg Antje Chang, Sandra Placzek Carola Söhngen, Michael Rother, Maren Lang, Cornelia Munaretto Susanne Ulas, Michael Stelzer, Andreas Grote, Maurice Scheer y Dietmar Schomburg , " BRENDA en 2013: reacciones integradas, datos cinéticos, función enzimática datos, clasificación mejorada de enfermedades: nuevas opciones y contenidos en BRENDA ” , Nucleic Acids Research , vol. 41, n o D1,enero 2013, D764-D772 ( PMID 23203881 , DOI 10.1093 / nar / gks1049 , leer en línea )
- (en) A. y R. Radzicka Wolfenden , " Una enzima competente " , Science , vol. 267, n o 5194,6 de enero de 1995, p. 90-93 ( PMID 7809611 , DOI 10.1126 / science.7809611 , leer en línea )
- (en) Brian P. Callahan y Brian G. Miller , " OMP descarboxilasa-Un enigma persiste " , Bioorganic Chemistry , vol. 35, n o 6, diciembre 2007, p. 465-469 ( PMID 17889251 , DOI 10.1016 / j.bioorg.2007.07.004 , leer en línea )
- (en) Harold Rudiger, Hans-Christian Siebert, Dolores Solis, Jesús initial Jimenez-Barbero, Antonio Romero, Claus-Wilhelm von der Lieth, Teresa Diaz-Maurino y Hans-Joachim Gabius , " Química medicinal basada en el código del azúcar: Fundamentos de Lectinología y Estrategias Experimentales con Lectinas como Dianas ” , Current Medicinal Chemistry , vol. 7, n o 4,abril 2000, p. 389-416 ( PMID 10702616 , DOI 10.2174 / 0929867003375164 , leer en línea )
- De Nobel, JG, Klis, FM, Priem, J., Munnik, T. y Van Den Ende, H. (1990) L as manoproteínas solubles en glucanasa limitan la porosidad de la pared celular en Saccharomyces cerevisiae . Levadura, 6 (6), 491-499.
- Zlotnik, HINDA, Fernandez, MP, Bowers, BLAIR y Cabib, ENRICO (1984). Las manoproteínas de Saccharomyces cerevisiae forman una capa de pared celular externa que determina la porosidad de la pared . Revista de Bacteriología, 159 (3), 1018-1026.
- Caridi A (2006) Funciones enológicas de manoproteínas de levadura parietal. Antonie Van Leeuwenhoek, 89 (3-4), 417-422 ( resumen )
- Harvey Lodish , Arnold Berk , Paul Matsudaira , Chris A. Kaiser , Monty Krieger , Matthew P. Scott , S. Laurence Zipursky y James Darnell ( traducción de Pierre L. Masson y Chrystelle Sanlaville), Biología molecular de la célula ["Molecular Cell Biology ”], Bruselas, Universidad De Boeck,2005, 3 e ed. , 1096 p. [ detalle de la edición ] ( ISBN 2-8041-4802-5 )
- (en) Julie Hey, Anton Posch, Andrew Cohen, Liu Ning y Adrianna Harbers , " Fraccionamiento de mezclas de proteínas complejas mediante enfoque isoeléctrico en fase líquida " , Métodos en biología molecular , vol. 424,2008, p. 225-239 ( PMID 18369866 , DOI 10.1007 / 978-1-60327-064-9_19 , leer en línea )
- (in) K. Terpe , " Descripción general de las fusiones de proteínas de etiqueta: desde los fundamentos moleculares y bioquímicos hasta los sistemas comerciales " , Microbiología y biotecnología aplicadas , vol. 60, n o 5,enero de 2003, p. 523-533 ( PMID 12536251 , DOI 10.1007 / s00253-002-1158-6 , leer en línea )
- (en) Olesya V. Stepanenko, Vladislav V.Verkhusha Irina Kuznetsova Sr. Vladimir N. Uversky y KK Turoverov , " Proteínas fluorescentes como biomarcadores y biosensores: arrojar luces de color en procesos moleculares y celulares " , Current Protein & Peptide Science , vol. . 9, n o 4,Agosto de 2008, p. 338-369 ( PMID 18691124 , PMCID 2904242 , DOI 10.2174 / 138920308785132668 , leer en línea )
- (in) Rafael Yuste , " Microscopía de fluorescencia hoy " , Nature Methods , vol. 2, n o 12,diciembre de 2005, p. 902-904 ( PMID 16299474 , DOI 10.1038 / nmeth1205-902 , leer en línea )
- (en) William Margolin , " Proteína fluorescente verde como informadora para la localización macromolecular en células bacterianas " , Methods , vol. 20, n o 1,enero 2000, p. 62-72 ( PMID 10610805 , DOI 10.1006 / meth.1999.0906 , leer en línea )
- (in) Terry M. Mayhew y John M. Lucocq , " Desarrollos en biología celular para microscopía inmunoelectrónica cuantitativa basada en secciones delgadas: una revisión " , Histoquímica y biología celular , vol. 130, n o 2Agosto de 2008, p. 299-313 ( PMID 18553098 , PMCID 2491712 , DOI 10.1007 / s00418-008-0451-6 , leer en línea )
- (en) Angelika Görg, Walter Weiss y Michael J Dunn , " Tecnología actual de electroforesis bidimensional para proteómica " , Proteomics , vol. 4, n o 12,diciembre de 2004, p. 3665-3685 ( PMID 15543535 , DOI 10.1002 / pmic.200401031 , leer en línea )
- (en) P. y S. Conrotto Souchelnytskyi , " Enfoques proteómicos en ciencia biológica y médica: principios y aplicaciones " , Oncología experimental , vol. 30, n o 3,septiembre 2008, p. 171-180 ( PMID 18806738 )
- (en) T. J. Joos y Bachmann , " Microarrays de proteínas: potenciales y limitaciones " , Frontiers in Bioscience , vol. 14,enero de 2009, p. 4376-4385 ( PMID 19273356 , DOI 10.2741 / 3534 )
- (in) Manfred Koegl y Peter Uetz , " Mejora de los sistemas de detección de dos híbridos de levadura " , Briefings in Functional Genomics , vol. 6, n o 4,diciembre 2007( PMID 18218650 , DOI 10.1093 / bfgp / elm035 , bfg.oxfordjournals.org/content/6/4/302.full.pdf+html)
- (in) Dariusz y Krzysztof Ginalski Plewczyński , " El interactoma: predicción de las interacciones proteína-proteína en las células " , Cellular and Molecular Biology Letters , vol. 14, n o 1,Marzo de 2009, p. 1-22 ( PMID 18839074 , DOI 10.2478 / s11658-008-0024-7 , leer en línea )
- (en) Chao Zhang y Sung-Hou Kim , " Resumen de la genómica estructural: de la estructura a la función " , Current Opinion in Chemical Biology , vol. 7, n o 1, Febrero de 2003, p. 28-32 ( PMID 12547423 , DOI 10.1016 / S1367-5931 (02) 00015-7 , leer en línea )
- (en) Yang Zhang , " Progreso y desafíos en la predicción de la estructura de la proteína " , Opinión actual en biología estructural , vol. 18, n o 3, junio 2008, p. 342-348 ( PMID 18436442 , PMCID 2680823 , DOI 10.1016 / j.sbi.2008.02.004 , leer en línea )
- (en) Zhexin Xiang , " Avances en la homología del modelado de estructuras de proteínas " , Ciencia actual de proteínas y péptidos , vol. 7, n o 3, junio de 2006, p. 217-227 ( PMID 16787261 , PMCID 1839925 , DOI 10.2174 / 138920306777452312 # sthash.hup2vFsH.dpuf , lea en línea )
- (en) Yang Zhang y Jeffrey Skolnick , " El problema de predicción de la estructura de la proteína podría resolverse utilizando la biblioteca PDB actual " , Actas de la Academia Nacional de Ciencias de los Estados Unidos de América , vol. 102, n o 4, 25 de enero de 2005, p. 1029-1034 ( PMID 15653774 , PMCID 545829 , DOI 10.1073 / pnas.0407152101 , leer en línea )
- (en) Brian Kuhlman, Gautam Dantas, Gregory C. Ireton, Gabriele Varani, Barry L. Stoddard y David Baker , " Diseño de un nuevo pliegue de proteína globular con precisión de nivel atómico " , Science , vol. 302, n o 5649, 21 de noviembre de 2003, p. 1364-1368 ( PMID 14631033 , DOI 10.1126 / science.1089427 , leer en línea )
- (en) David W. Ritchie , " Progreso reciente y direcciones futuras en el acoplamiento proteína-proteína " , Ciencia actual de proteínas y péptidos , vol. 9, n o 1, Febrero de 2008, p. 1-15 ( PMID 18336319 , DOI 10.2174 / 138920308783565741 , leer en línea )
- (in) T. Herges y W. Wenzel , " In Silico Folding of a Three Helix Protein and Caracterización de su paisaje de energía libre en un campo de fuerza de todos los átomos " , Letras soñadas físicas , vol. 94, n o 1, 14 de enero de 2005, p. 018101 ( PMID 15698135 , DOI 10.1103 / PhysRevLett.94.018101 , Bibcode 2005PhRvL..94a8101H , leer en línea )
- (en) Michael Hoffmann, Marius Wanko Paul Strodel, Peter H. König, Thomas Frauenheim Klaus Schulten, Walter Thiel, Emad Tajkhorshid y Marcus Elstner , " Ajuste de color en rodopsinas: el mecanismo para el cambio espectral entre bacteriorrodopsina y rodopsina II sensorial " , Revista de la Sociedad Química Estadounidense , vol. 128, n o 33, 23 de agosto de 2006, p. 10808-10818 ( PMID 16910676 , DOI 10.1021 / ja062082i , leer en línea )
- Proteínas
- " Family Nutrition Guide " (consultado el 26 de noviembre de 2014 )
- (en-US) American Heart Association , " Vegetariana, dieta vegana y salud cardíaca " , Go Red For Women® ,26 de marzo de 2014( leído en línea , consultado el 29 de julio de 2017 )
- (en) " Posición de la Asociación Dietética Estadounidense: dietas vegetarianas " , Revista de la Asociación Dietética Estadounidense ,julio de 2009, p. 1267–1268 ( leer en línea )
- Estudio de Salud Adventista-1 - Resultados cáncer: Algunos Aspectos destacados
- OMS prensa liberación Carcinogénesis del consumo de carne roja y carne procesada de octubre de 2015]
- Formulario de frijoles secos en el sitio web de Health Passport
- consumo de leguminosas distintas de la soja reduce los niveles de colesterol: un metanálisis de ensayos controlados aleatorios
- Consumo de legumbres y riesgo de enfermedad coronaria en hombres y mujeres de EE. UU .: Estudio de seguimiento epidemiológico NHANES I
- V. R. joven y PL Pellett , “ proteínas vegetales en relación a la proteína humana y amino nutrición ácido ”, The American Journal of Clinical Nutrition , vol. 59, n o 5 Suppl,Mayo de 1994, p. 1203S - 1212S ( ISSN 0002-9165 , PMID 8172124 , leído en línea , consultado el 29 de julio de 2017 )
- (in) VR Young y PL Pellett , " Proteínas de trigo en relación con los requisitos de proteínas y la disponibilidad de aminoácidos " , The American Journal of Clinical Nutrition , vol. 41, n o 5,1 st de mayo de 1.985, p. 1077–1090 ( ISSN 0002-9165 y 1938-3207 , DOI 10.1093 / ajcn / 41.5.1077 , leído en línea , consultado el 4 de febrero de 2020 )
- Sophie Landrin, " En India, la religión se invita a sí misma en el plato de los escolares " , en Le Monde ,4 de febrero de 2020(consultado el 4 de febrero de 2020 )
- " Los campos de aplicación de la transgénesis " , sobre pedagogía gnis (consultado el 5 de febrero de 2020 )
- " ESTADOS UNIDOS - Un maíz enriquecido en lisina " , en inf'OGM ,noviembre 2005(consultado el 5 de febrero de 2020 )
- Informe AFSSA / ANSES, páginas 232 y 233
- El contenido de proteínas de los hongos es difícil de medir con precisión porque su quitina y otros compuestos nitrogenados interfieren con el análisis del nitrógeno total (por ejemplo, el método de Kjeldahl ) utilizado anteriormente. Fuente: Danell E. y Eaker D. (1992), Contenido de aminoácidos y proteína total del hongo comestible Cantharellus cibarius (Fries) , Journal of the Science of Food and Agriculture , 60 (3), 333-337.
- Dıez VA y Alvarez A. (2001), Estudios de composición y nutrición en dos hongos comestibles silvestres del noroeste de España , Food Chemistry , 75 (4), 417-422 ( resumen )
- Chang ST y Buswell JA (1996), suplementos nutritivos de la seta , World Journal of Microbiology and biotecnología , 12 (5), 473-476 ( resumen ).
- Peter CK Cheung (2009), Valor nutricional y beneficios para la salud de las setas, las setas como alimentos funcionales , (71-109).
- (en) VA Diez y A. Alvarez, composicional y los estudios nutricionales en dos setas comestibles de noroeste de España . En Química de Alimentos . Banda 75, n o 4, diciembre de 2001, S. 417-422, DOI : 10.1016 / S0308-8146 (01) 00229-1
- Chang ST y Miles PG (1991), Tendencias recientes en la producción mundial de hongos comestibles , The Mushroom Journal , 503, 15-18.
- Shah H., Khalil IA y Jabeen S. (1997), Composición nutricional y calidad proteica del hongo Pleurotus , Sarhad Journal of Agriculture (Pakistán) ( resumen de Agris / FAO ).
- Hsieh, KY, Hsu, CI, Lin, JY, Tsai, CC y Lin, RH (2003), La administración oral de una proteína derivada de hongos comestibles inhibe el desarrollo de reacciones alérgicas a los alimentos en ratones , Alergia clínica y experimental , 33 (11), 1595-1602 ( resumen )
- Lin, JY, Lin, YJ, Chen, CC, Wu, HL, Shi, GY y Jeng, TW (1974), Proteína cardiotóxica de hongos comestibles , Nature , 252 (5480), 235 ( resumen ).
- " Tabla Ciqual de composición nutricional de los alimentos " , en ciqual.anses.fr (consultado el 10 de septiembre de 2018 )
- Albert-François Creff y Daniel Layani, Manual de la dietética en la práctica médica actual , París, Masson,2004, 301 p. ( ISBN 978-2-294-01346-1 , leer en línea ) , pág. 4
Ver también
Bibliografía
- Gregory Petsko, Dagmar Ringe (transl. Chrystelle Sanlaville, Dominique Charmot-Bensimon), Estructura y función de las proteínas , De Boeck, Bruselas, 2009. ( ISBN 978-2-8041-5888-0 ) .
- Lubert Stryer, Jeremy Marcos Berg, John L. Tymoczko (trad. Serge Weinman), Bioquímica , Flammarion, "medicina-Sciences", París, 2008, 6 ª ed. ( ISBN 978-2-257-00003-3 ) .
- Carl-Ivar Brändén, John Tooze (traducción de Bernard Lubochinsky, pref. Joël Janin), Introducción a la estructura de las proteínas , Universidad De Boeck, Bruselas, 1996. ( ISBN 978-2-8041-2109-9 ) .
Artículos relacionados
- Combinación de proteínas (comida - ejemplo: arroz / lentejas)
- Proteínas recombinantes
- Subfamilia de proteínas
- Agregación de proteínas
- Acuaporina
- Proteína Rieske
- Transportador de aminoácidos lisosomales
- Proteína fibrosa
- Proteína globular
- Vicilina
- factores de transcripción
- Proteínas cdx
- Proteína de andamio
- Proteína tau
- Tioproteína
- Selenoproteína
- Manoproteína
- Microproteína
enlaces externos
- ( fr ) Predictor Project Un software informático compartido que utiliza la plataforma BOINC para estudiar el plegamiento de proteínas.
- (es) Servidor MRS Un servidor de banco de datos biológicos, donde la identificación de una entrada en el banco PDB permite visualizar la estructura en pantalla, en modo dinámico (ver por ejemplo lo que produce una búsqueda en el banco PDB de entradas correspondientes a la tripsina).
- ( fr ) Proteins @ home Un proyecto a gran escala para estudiar el plegamiento de proteínas, en el que puede participar con su computadora.