Hemoglobina
La hemoglobina , comúnmente simbolizada como Hb , a veces Hgb es un pigmento respiratorio (familia molecular de metaloproteínas , aquí conteniendo hierro ) presente principalmente en la sangre de los vertebrados , en sus glóbulos rojos y en los tejidos de algunos invertebrados . Su función es transportar oxígeno O 2desde el sistema respiratorio ( pulmones , branquias ) al resto del cuerpo . La cantidad de hemoglobina es un parámetro que se mide durante un hemograma .
Papel
La hemoglobina libera oxígeno en los tejidos para la respiración celular aeróbica que, a través del metabolismo , proporciona energía para los procesos biológicos esenciales para la vida.
En el ser humano , la hemoglobina es una proteína hetero - tetramérica formada a partir de cadenas peptídicas idénticas de dos en dos. La hemoglobina A (HbA) representa aproximadamente el 95% de las moléculas de hemoglobina en adultos, que consta de dos cadenas α y dos cadenas β; también hay una hemoglobina A 2 (HbA 2 ) de fórmula α 2 δ 2, y una hemoglobina F (HbF, fetal) de fórmula α 2 γ 2. Cada uno de los cuatro canales está asociado con un grupo protésico llamado hemo y consiste en un catión de hierro complejado con una porfirina . Por tanto, la hemoglobina es una hemoproteína .
En los mamíferos , la hemoglobina constituye casi el 96% de la masa de materia seca de los glóbulos rojos y aproximadamente el 35% de su contenido total, incluida el agua. Cada molécula de hemoglobina puede unir hasta cuatro moléculas de oxígeno O 2, y la hemoglobina en la sangre puede transportar 1,34 ml de O 2por gramo de proteína, lo que le permite transportar 70 veces más oxígeno que la cantidad de O 2disuelto en sangre. La hemoglobina también participa en el transporte de gases distintos del oxígeno. En particular, asegura el transporte de parte del dióxido de carbono CO 2producido por la respiración celular, y también transporta óxido nítrico NO, que juega un papel importante en la señalización celular de ciertos procesos fisiológicos , y que se libera junto con el oxígeno después de ser transportado sobre un grupo tiol de la apoproteína .
la mayor parte de la hemoglobina se encuentra en los glóbulos rojos, que a su vez son producidos por la médula ósea. Sin embargo, no toda la hemoglobina se concentra en los glóbulos rojos. Se encuentra así, por ejemplo, en las neuronas dopaminérgicas del grupo A9 de la sustancia negra , en los macrófagos , en las células alveolares y, en los riñones , en las células del mesangio . En estos tejidos, la hemoglobina juega un papel antioxidante y regulador del metabolismo del hierro .
La hemoglobina y varias moléculas relacionadas también están presentes en un gran número de invertebrados, hongos y plantas . En estos organismos, la función de la hemoglobina es transportar oxígeno O 2, pero también puede actuar como transportador y regulador de otras especies químicas como el dióxido de carbono CO 2, monóxido de nitrógeno NO, sulfuro de hidrógeno HS y anión sulfuro S 2– . Una variante de la hemoglobina, llamada leghemoglobina , elimina el oxígeno de los sistemas anaeróbicos , por ejemplo, los nódulos de Rhizobium en las fabaceae , antes de que los inactive.
Estructura y funcionamiento
Subunidades
La hemoglobina tiene una estructura cuaternaria característica de muchas proteínas con subunidades globulares . La mayoría de sus residuos de aminoácidos están implicados en hélices α unidas por segmentos no helicoidales. Las secciones helicoidales están estabilizadas por enlaces de hidrógeno que dan a la proteína su estructura tridimensional característica, denominada plegamiento de globina, ya que también se encuentra en otras globinas con un grupo protésico hemo como la mioglobina . Este plegamiento característico tiene una cavidad en la que se inserta firmemente una molécula de hemo que constituye el grupo protésico de la proteína. Por tanto, la hemoglobina contiene una molécula de hemo por subunidad.
-
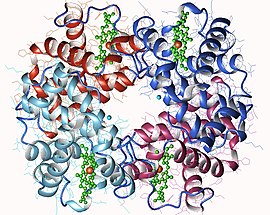
Representación genérica de una molécula de hemoglobina, que muestra las cuatro subunidades, idénticas en pares, cada una con una molécula de hemo insertada en cavidades dentro de las subunidades.
En la mayoría de los vertebrados, la molécula de hemoglobina es un conjunto de cuatro subunidades globulares en una disposición aproximadamente tetraédrica . Estas subunidades se mantienen unidas por enlaces de hidrógeno, por enlaces iónicos y por efecto hidrofóbico . En los seres humanos adultos, el tipo más común de hemoglobina es la hemoglobina A, que consta de dos subunidades α y dos subunidades β, cada una compuesta por 141 y 146 residuos de aminoácidos, respectivamente. Esta estructura está simbolizada por α 2 β 2. Estas subunidades son estructuralmente muy similares y tienen aproximadamente el mismo tamaño. Cada uno tiene un peso molecular de aproximadamente 16 kDa , o 64 kDa ( 64 458 g · mol -1 ) para la proteína de longitud completa. En los niños, la principal hemoglobina se llama hemoglobina F (fetal), de fórmula α 2 γ 2, siendo reemplazadas gradualmente las cadenas γ por cadenas β durante el crecimiento.
Hemo
El hemo está compuesto por un catión de hierro ( II ) coordinado con cuatro átomos de nitrógeno de una porfirina , un tetrapirrol cuya molécula es plana. Este catión Fe 2+ también está unido covalentemente al residuo de histidina F8 de la globina en la que se inserta el hemo; este residuo, llamado histidina proximal , se encuentra debajo del plano del hemo. El Fe 2+ también puede unirse reversiblemente a través de un enlace covalente coordinado a una molécula de oxígeno O 2por encima del plano del hemo, opuesto a la histidina proximal, completando la geometría de coordinación octaédrica de seis ligandos del catión hierro ( II ) en la oxihemoglobina; en ausencia de oxígeno, en la desoxihemoglobina, este sexto sitio está ocupado por una molécula de agua unida muy débilmente.
El hierro ferroso en la desoxihemoglobina se encuentra en un estado de alto espín , es decir que sus cinco orbitales d están ocupados, principalmente por electrones individuales, de ahí un radio iónico del orden de 92 pm , mientras que, en la oxihemoglobina, el hierro ferroso está en un estado de espín bajo , es decir, sus orbitales d están ocupados por seis pares de electrones que están limitados a los tres orbitales de menor energía, por lo tanto, un radio iónico de solo 75 pm . Por esta razón, el ión Fe 2+ se desplaza aproximadamente 40 µm del plano del hemo en la desoxihemoglobina, pero solo 10 µm en la oxihemoglobina. Esta variación está en la base del cambio entre la forma tensa y la forma relajada de hemoglobina.
- Estructura del hemo b , grupo protésico de hemoglobina.
-
(es) Diagrama esquemático de la unión de una molécula de oxígeno O 2en el hemo , simbolizado aquí por una línea gruesa. El ion superóxido O 2• - El resultado está ligado por un lado al catión de hierro ( III ) por un enlace covalente coordinado y por el otro lado a la histidina distal. El catión Fe ( II ) de la desoxihemoglobina se encuentra en el estado de giro alto y se desplazó fuera del plano del hemo hacia la histidina proximal, pero regresa a este plano al pasar al estado de giro bajo por la unión al oxígeno l., Que se desplaza la histidina proximal al hemo y promueve el cambio del resto de la proteína de la forma tensada (T) a la forma relajada (R).
El catión hierro puede encontrarse en el estado de oxidación +2 o +3: en este último caso se trata de metahemoglobina , que se une al oxígeno de forma menos reversible que la hemoglobina y con menor afinidad. De hecho, cuando se une al hemo ferroso, la molécula de oxígeno O 2tiende a reducirse al ion superóxido O 2• - mientras que el catión Fe 2+ tiende a oxidarse a Fe 3+ , un mecanismo que se invierte durante la liberación de oxígeno; por el contrario, la unión de oxígeno al hemo férrico es esencialmente irreversible y tiende a bloquear la proteína en forma de R, lo que evita la liberación de oxígeno e inhibe su funcionalidad transportadora de oxígeno. La citocromo b 5 reductasa o metahemoglobina reductasa es la enzima que asegura la reducción de la hemoglobina funcional de la metahemoglobina mediante la reducción del catión Fe 3+ a Fe 2+ , lo que la convierte en una enzima esencial para mantener las propiedades de la sangre.
Forma tensa (T) y forma relajada (R)
La hemoglobina desoxigenada (desoxihemoglobina) tiene la denominada T, o conformación tensa , mientras que la hemoglobina oxigenada (oxihemoglobina) tiene la denominada R, o conformación relajada . La forma T tiene una baja afinidad por el oxígeno y por lo tanto tiende a liberarlo, mientras que la forma R tiene una alta afinidad por el oxígeno y tiende a unirlo. Varios factores favorecen una u otra de estas conformaciones. Así, la forma T se ve favorecida por un pH bajo ( ácido ), una alta concentración de CO 2y un alto nivel de 2,3-bisfosfoglicerato (2,3-BPG), que promueve la liberación de oxígeno a medida que la sangre circula a través de los tejidos , mientras que la forma R se ve favorecida por un pH alto, una presión parcial baja de CO 2y un nivel bajo de 2,3-BPG, que promueve la captación de oxígeno cuando la sangre circula a nivel de los alvéolos pulmonares .
-
Representación esquemática del cambio de hemoglobina entre las formas T (desoxi) y R (oxi). Los movimientos del hemo y de la histidina proximal son claramente visibles en las subunidades α 1 y β 2 .
-
Tasa de saturación de O 2hemoglobina en función de la presión parcial de O 2 ; a veces llamada curva de Barcroft , es sigmoidea debido al efecto cooperativo que acompaña a la unión del oxígeno a la hemoglobina.
El cambio entre la forma T y la forma R de la hemoglobina es un mecanismo llamado cooperativo , es decir alostérico , porque la unión de una molécula de oxígeno a la forma T induce un cambio conformacional que se propaga parcialmente a subunidades adyacentes, cuya afinidad porque el oxígeno aumenta gradualmente a medida que otras moléculas de oxígeno se unen a la hemoglobina, hasta que toda la proteína asume la conformación R; a la inversa, la liberación de una molécula de oxígeno de la forma R induce un cambio conformacional que se propaga parcialmente a las subunidades adyacentes, cuya afinidad por el oxígeno disminuye gradualmente a medida que la hemoglobina libera oxígeno, hasta que toda la proteína adopta la conformación T. Esta es la razón por la cual la curva de unión del oxígeno a la hemoglobina en función de la presión parcial del oxígeno muestra una forma sigmoidea , mientras que sería hiperbólica en ausencia de alosteria.
Curva de saturación de oxígeno de hemoglobina
Es habitual graficar la tasa de saturación de hemoglobina en oxígeno O 2representado en el eje y en función de la presión parcial de oxígeno O 2, dado en la abscisa . En esta representación, la curva es sigmoidea y tiende a deslizarse hacia la izquierda cuando aumenta la afinidad de la hemoglobina por el oxígeno y hacia la derecha cuando disminuye. La presión parcial de oxígeno a la que la hemoglobina está saturada en un 50% con oxígeno se llama p 50 : cuanto menor es su valor, mayor es la afinidad de la hemoglobina por el oxígeno. Como guía, la p50 de la hemoglobina en un adulto sano es típicamente de 3,5 kPa , a menudo escrita como 26,6 mmHg , mientras que la de la mioglobina suele ser de 130 Pa .
Varios factores aumentan la p 50 y, por lo tanto, deslizan esta curva hacia la derecha:
- una caída del pH , que se vuelve ácido : este es el efecto Bohr ;
- un aumento en el nivel de dióxido de carbono CO 2 : este es el efecto Haldane ;
- un aumento en el nivel de 2,3-bisfosfoglicerato (2,3-BPG);
- un aumento de temperatura, sin embargo, con un efecto relativamente pequeño.
Estos efectos son reversibles y la inversión de la dirección de variación de estos factores hace que la curva se deslice hacia la izquierda.
Otros ligandos transportados por la hemoglobina
Además de oxígeno O 2, que se une a la hemoglobina en un llamado mecanismo cooperativo , esta proteína también transporta otros ligandos , algunos de los cuales son inhibidores competitivos , como el monóxido de carbono CO, y otros son ligandos alostéricos como el dióxido de carbono CO 2y monóxido de nitrógeno NO. CO 2se une reversiblemente a los grupos amina en la apoproteína para formar carbaminohemoglobina , que se cree que proporciona aproximadamente el 10% del transporte de CO 2en mamíferos , el resto se transporta principalmente en forma de iones de bicarbonato HCO 3- . El óxido nítrico se une reversiblemente a los grupos tiol de la apoproteína para formar un S -nitrosotiol . Es posible que el transporte de óxido nítrico medie el transporte de oxígeno por la hemoglobina indirectamente al actuar como vasodilatador en tejidos donde la presión parcial de oxígeno es baja.
Inhibidores por competencia con oxígenoLa unión del oxígeno a la hemoglobina se bloquea eficazmente con el monóxido de carbono CO, por ejemplo, del humo de los cigarrillos , los escapes o la combustión incompleta de una caldera . El monóxido de carbono compite con el oxígeno en el sitio de unión de este último en el hemo. La afinidad de la hemoglobina por el monóxido de carbono es aproximadamente 230 veces mayor que la de la hemoglobina por el oxígeno, por lo que pequeñas cantidades de monóxido de carbono son suficientes para reducir significativamente la oxigenación de la hemoglobina durante la hematosis y, por lo tanto, la capacidad de la sangre para oxigenar el cuerpo. La hipoxia que resulta así de la exposición continua al 0,16% de CO en el aire provoca mareos , náuseas , dolor de cabeza y taquicardia en 20 minutos y conduce a la muerte en menos de dos horas; El 1,28% de CO en el aire provoca pérdida del conocimiento después de solo dos o tres respiraciones y la muerte en menos de tres minutos. Cuando se combina con monóxido de carbono, la hemoglobina es una proteína llamada carboxihemoglobina cuyo color rojo muy brillante probablemente teñirá la piel de rosa de las víctimas que murieron por intoxicación por monóxido de carbono , que de otra manera tendrían la tez pálida o azulada.
De manera similar, la hemoglobina exhibe, en su sitio de unión al oxígeno, una afinidad competitiva por el ion cianuro CN - , el monóxido de azufre SO y el ion sulfuro S 2– , como ocurre con el sulfuro de hidrógeno H 2 S. Estos se unen al catión de hierro del hemo sin modificar su estado de oxidación, pero sin embargo inhiben la unión del oxígeno al hemo, de ahí su alta toxicidad.
Ligandos de hemoglobina alostéricosEl dióxido de carbono CO 2se une más fácilmente a la desoxihemoglobina, lo que facilita su eliminación del organismo. Esto se llama efecto Haldane .
Además, CO 2disuelto en la sangre se convierte en anión bicarbonato HCO 3- por anhidrasa carbónica , dependiendo de la reacción:
CO 2+ H 2 O→ H 2 CO 3→ HCO 3- + H + .De ello se deduce que la sangre rica en CO 2también es más ácido , es decir, su pH se reduce por efecto del ácido carbónico . La unión de protones H + y moléculas de CO 2.la hemoglobina induce un cambio conformacional que favorece la forma T y, por tanto, la liberación de oxígeno. Los protones se unen a diferentes sitios de la hemoglobina, mientras que el dióxido de carbono se une a los grupos α- amino para formar carbaminohemoglobina . La disminución de la afinidad de la hemoglobina por el oxígeno en presencia de CO 2y el pH ácido se llama efecto Bohr .
Las personas aclimatadas a grandes altitudes tienen un aumento del nivel en sangre de 2,3-bisfosfoglicerato (2,3-BPG). Este último es un efector heteroalostérico que tiene el efecto de reducir la afinidad de la hemoglobina por el oxígeno estabilizando la forma T: bajo una presión parcial de oxígeno más baja que al nivel del mar, una caída en la afinidad de la hemoglobina por el oxígeno tiene el efecto de aumentar la eficiencia global del transporte de oxígeno por la hemoglobina. De manera más general, se observa un aumento en el nivel de 2,3-BPG cuando la presión parcial de oxígeno disminuye en los tejidos periféricos, por ejemplo en caso de hipoxemia , enfermedad respiratoria crónica , anemia o incluso insuficiencia cardíaca . Por el contrario , el nivel de 2,3-BPG disminuye en caso de shock séptico e hipofosfatemia (en) .
Biosíntesis y degradación
La biosíntesis de la hemoglobina implica un conjunto complejo de pasos. El hemo proviene de una serie de reacciones que comienzan en las mitocondrias y continúan en el citosol de los eritrocitos inmaduros, mientras que la apoproteína se produce en el citosol de los ribosomas . La producción de hemoglobina ocurre en las primeras etapas de la eritropoyesis , desde la etapa de proeritroblasto hasta la etapa de reticulocitos en la médula ósea . Aquí es donde los eritrocitos de los mamíferos pierden su núcleo , mientras que el núcleo permanece en los eritrocitos de las aves y muchas otras especies . La biosíntesis de la apoproteína sin embargo continúa después de la pérdida del núcleo porque hay restos de la ARN mensajero en la célula, que puede ser traducido por los ribosomas del citosol hasta la activación de los hematíes en el aparato. Cardiovascular .
En los vertebrados , los eritrocitos que han llegado al final de su vida debido a su senescencia o deterioro son eliminados de la sangre por fagocitosis por macrófagos en el bazo y en el hígado . En caso de hemólisis en el torrente sanguíneo , la hemoglobina se une a la haptoglobina , mientras que el hemo libre se une a la hemopexina , lo que limita el efecto oxidativo. Es probable que la hemoglobina degradada o liberada en grandes cantidades por los glóbulos rojos dañados obstruya los vasos sanguíneos , como los capilares de los riñones , lo que puede causar enfermedad renal . La hemoglobina liberada es eliminada de la sangre por la proteína CD163 , que se expresa exclusivamente en monocitos y macrófagos. La hemoglobina se descompone en estas células y el hierro hemo se recicla, mientras que se libera una molécula de monóxido de carbono por molécula de hemo degradada: la descomposición del hemo es uno de los pocos procesos naturales que producen monóxido de carbono en el cuerpo humano y es responsable de la presencia de CO en la sangre de las personas que respiran incluso el aire más puro. Este proceso forma biliverdina , luego bilirrubina , que es de color amarillo. Insoluble, los macrófagos lo liberan al plasma sanguíneo , donde se une a la albúmina sérica , que la transporta a los hepatocitos . Estos últimos lo solubilizan por conjugación con ácido glucurónico y lo secretan en los intestinos con la bilis . Los intestinos metabolizan la bilirrubina a urobilinógeno , que se excreta en las heces como estercobilina y en la orina . Cuando la bilirrubina no puede excretarse, su concentración en sangre aumenta y se elimina principalmente a través de la orina, que se oscurece mientras que las heces se decoloran.
El hierro producido por la degradación del hemo se almacena en las ferritinas de los tejidos y se transporta en el plasma sanguíneo por las β-globulinas como las transferrinas .
Genético
Las moléculas de hemoglobina están formadas por subunidades de tipo globina cuya secuencia difiere según la especie . También existen variantes de hemoglobinas dentro de la misma especie, aunque una de estas variantes suele predominar en gran medida sobre las demás. En los seres humanos , la forma predominante de hemoglobina se llama hemoglobina A; está codificado por los genes HBA1 , HBA2 y HBB ubicados en el cromosoma 16 para los dos primeros y en el cromosoma 11 para el último.
Evolución
Generalmente se acepta que la diferencia entre hemoglobina y mioglobina es posterior a la separación de gnatostomas (de vertebrados a mandíbula ) o con lamprea . La mioglobina se ha dirigido al almacenamiento de oxígeno, mientras que la hemoglobina se ha especializado en el transporte de oxígeno. Las subunidades de la proteína están codificadas por genes de tipo α y β globina . Los predecesores de estos genes surgieron durante una duplicación que ocurrió después de la aparición de los gnatóstomos, hace alrededor de 450 a 500 millones de años. La aparición de los genes α y β abrió el camino a la polimerización de estas globinas y, por tanto, a la formación de una proteína de mayor tamaño compuesta por distintas subunidades . El hecho de que la hemoglobina sea una proteína polimérica es la base del mecanismo alostérico que subyace notablemente a la naturaleza cooperativa de la unión del oxígeno a la hemoglobina. Posteriormente, el gen α ha sufrido una segunda duplicación que conduce a la formación de los genes HBA1 y HBA2 . Estas múltiples duplicaciones y divergencias han creado todo un conjunto de genes relacionados con las globinas α y β, cuya regulación conduce a que se expresen en diferentes etapas de desarrollo.
-
Alineación de las secuencias de las cadenas α, β y δ de la hemoglobina humana (fuente UniProt ).
Mutaciones
Las mutaciones de los genes de la hemoglobina pueden dar lugar a variantes de la hemoglobina. La mayoría de estas variantes son funcionales y no tienen ningún efecto sobre la salud. Algunas mutaciones en la hemoglobina, por otro lado, pueden causar enfermedades genéticas llamadas hemoglobinopatías . La más conocida de estas condiciones es la anemia de células falciformes , que fue la primera enfermedad humana cuyo mecanismo fue dilucidado a nivel molecular. Las talasemias son otro grupo de hemoglobinopatías que implican una alteración de la regulación génica del componente globina de la hemoglobina. Todas estas enfermedades resultan en anemia .
La alteración de la secuencia de aminoácidos de la hemoglobina puede ser adaptativa. Así fue posible demostrar que la hemoglobina se adapta a la caída de la presión parcial de oxígeno observada a gran altura. Entonces, la hemoglobina debe poder unirse al oxígeno a una presión más baja, lo que puede manifestarse por un cambio en la secuencia a nivel de los aminoácidos involucrados en la afinidad de la hemoglobina por el oxígeno, como se ha observado, por ejemplo, en colibríes de la cordillera de los Andes : así, en especies del género Oreotrochilus , en el colibrí de Castelneau , el inca violifera o incluso el colibrí gigante , estas mutaciones reducen la afinidad de la hemoglobina por el ácido fítico , que en estas aves juega el mismo papel que 2, 3-bisfospoglicerato en humanos; esta disminución de la afinidad tiene el efecto de incrementar la eficiencia del transporte de oxígeno cuando se reduce la presión parcial de este último.
La adaptación de la hemoglobina a grandes altitudes también afecta a los humanos. Identificamos así un grupo de mujeres tibetanas cuyo genotipo codifica una hemoglobina cuya afinidad por el oxígeno aumenta a baja presión parcial. Esto tiene el efecto de reducir la mortalidad infantil en estas condiciones extremas, lo que ofrece una ventaja selectiva que favorece a los individuos portadores de estas mutaciones de hemoglobina.
Variantes humanas de hemoglobina
En los adultos, la principal variante de hemoglobina es la hemoglobina A , o HbA , de fórmula α 2 β 2, que representa más del 97% de la hemoglobina total de un adulto sano. La otra variante de la hemoglobina adulta es la hemoglobina A 2 , o HbA 2 , con la fórmula α 2 δ 2, que representa entre el 1,5% y el 3,1% de la hemoglobina total de un adulto sano, pero cuya proporción aumenta en los pacientes drepanocíticos . Además de estas variantes de adultos sanos, hay una docena de otras variantes de hemoglobina humana, que se encuentran en embriones , fetos o pacientes con una o más formas de hemoglobinopatía .
Hemoglobinas embrionarias
Se conocen cuatro tipos de hemoglobina embrionaria en humanos :
- Hb Gower-1 , de fórmula ζ 2 ε 2, es relativamente inestable y se descompone fácilmente;
- Hb Gower-2 , de fórmula α 2 ε 2, más estable que la variante Gower-1, existe en pequeñas cantidades durante la vida embrionaria y fetal; se ha propuesto como tratamiento por reactivación del gen en pacientes que padecen hemoglobinopatías como la β-talasemia en los que la reactivación de la hemoglobina F está contraindicada por motivos de toxicidad;
- Hb Portland-1 , de fórmula ζ 2 γ 2, está presente en pequeñas cantidades durante la vida embrionaria y fetal;
- Hb Portland-2 , de fórmula ζ 2 β 2, es incluso más inestable que la variante Gower-1, pero se ha propuesto como tratamiento de reactivación genética en pacientes con α-talasemia .
La hemoglobina embrionaria a veces se simboliza con Hbε, que no debe confundirse con la hemoglobina E, denominada HbE, que es una variante patológica de la HbA que presenta una mutación deletérea en las subunidades β, denominada β E (la "E" en este caso se refiere a la residuo de glutamato modificado por mutación ).
Hemoglobina fetal
La hemoglobina fetal HbF de fórmula α 2 γ 2, reemplaza la hemoglobina embrionaria después de 10 a 12 semanas de desarrollo. Constituye hasta el 95% de la sangre del recién nacido y se reemplaza gradualmente por hemoglobina HbA adulta a partir del sexto mes después del nacimiento; sin embargo, permanece presente en trazas en adultos, donde no excede el 1% de todas las variantes de hemoglobina detectables. Permanece en los niños producidos durante cierta talasemia en particular, a veces hasta la edad de cinco años, y una condición rara llamada persistencia hereditaria del trastorno de la hemoglobina fetal (en) ( HPFH ) da como resultado la producción de HbF en lugar de HbA más allá del período normal. Además, la producción de HbF se puede reactivar en adultos en un entorno terapéutico para tratar la anemia de células falciformes .
La hemoglobina fetal se caracteriza por una afinidad mayor por el oxígeno que la hemoglobina adulta, que permite que el feto para oxigenar sí mismo a partir de sangre de la madre: de hecho, la p 50 de HbF es de aproximadamente 19 mmHg ( 2,6 kPa ), en comparación con 26,8 mm de Hg ( 3,6 kPa ) para HbA. Esta diferencia de afinidad por el oxígeno resulta de una diferencia de afinidad por uno de los efectores alostéricos de la hemoglobina: el 2,3-bisfosfoglicerato (2,3-BPG), cuya unión con la hemoglobina tiene el efecto de estabilizar la forma T de esta proteína. que corresponde a la desoxihemoglobina, que reduce la afinidad de la hemoglobina por el oxígeno. En el caso de la hemoglobina fetal, la subunidad γ tiene un residuo de serina en la posición 143, donde una subunidad β HbA tiene un residuo de histidina : esta posición se encuentra en el sitio de unión 2,3-BPG, y el reemplazo de un la histidina, cuya cadena lateral lleva una carga eléctrica positiva, por una serina eléctricamente neutra, debilita la interacción de 2,3-BPG con hemoglobina, porque la 2, 3-BPG es una molécula pequeña que lleva cinco cargas eléctricas negativas.
Hemoglobinopatías
Las talasemias se caracterizan por una producción insuficiente de uno de los dos tipos de subunidades de hemoglobina adulta. Por tanto, se hace una distinción entre la talasemia α , que es bastante rara, en la que las subunidades α se producen de manera insuficiente, y la talasemia β , la más común, en la que son las subunidades β las que se producen de manera insuficiente. El primero conduce a la formación de tetrámeros de β-globina llamados hemoglobina H , de fórmula β 4, que son bastante inestables. Los homocigotos α 0 generalmente no sobreviven mucho después del nacimiento debido a una profunda alteración de la hemoglobina fetal HbF, dando en estas condiciones hemoglobina de Barts , de fórmula γ 4.
Las principales mutaciones en la hemoglobina son:
- la hemoglobina C , de fórmula α 2 β C 2, que corresponde a una sustitución E6K, sustitución del residuo de glutamato en la posición 6 por un residuo de lisina . El primero tiene una cadena lateral corta con carga negativa, mientras que el segundo tiene una cadena lateral larga con carga positiva, lo que afecta la plasticidad general de los eritrocitos . Los heterocigotos tienen un 28 a 44% de hemoglobina C, que permanece asintomática, mientras que los homocigotos tienen un 100% de hemoglobina C, lo que causa una anemia hemolítica leve . El gen de la hemoglobina C está presente principalmente en África Occidental , donde se puede tener una ventaja preventiva contra la malaria como otras hemoglobinopatías, así como en el sur de Europa , América Latina y las regiones. Caribe ;
- la hemoglobina E ' de fórmula α 2 β E 2, que corresponde a una sustitución E26K, sustitución del residuo de glutamato en la posición 26 por un residuo de lisina. Esta mutación afecta a alrededor de 1 millón de personas en todo el mundo, principalmente en el sudeste asiático . Afecta la expresión de la β-globina al inducir un corte y empalme alternativo del ARN mensajero en los codones 25-27, por lo tanto, un déficit en la producción de β-globina normal, lo que conduce a la β-talasemia . Además, las subunidades β E interactúan con menos fuerza con las subunidades α, lo que hace que las moléculas de hemoglobina E sean menos estables en presencia de oxidantes ;
- la hemoglobina S , de fórmula α 2 β S 2, que corresponde a una sustitución E6V, sustitución del residuo de glutamato en la posición 6 por un residuo de valina . Esta sustitución, que coloca un residuo de aminoácido hidrofóbico en la superficie de la proteína, crea una zona de adhesión que promueve la precipitación de la hemoglobina S en filamentos largos que extienden los eritrocitos dándoles una hoz ( hoz en inglés, de ahí la "S" de esta variante), de ahí el nombre de anemia de células falciformes que también se le da a esta enfermedad, también llamada anemia de células falciformes . El gen S está presente principalmente en África subsahariana , Oriente Medio y la India central: en 2013 se estimó en 3,2 millones el número de homocigotos que padecían anemia de células falciformes y en 43 millones el número de heterocigotos con rasgo de células falciformes. . Su anemia los protege del paludismo , de ahí una ventaja selectiva que favorece la prevalencia del gen falciforme en las regiones palúdicas.
Moléculas análogas
Existe una amplia variedad de proteínas en plantas y animales que se unen al oxígeno para su almacenamiento o transporte. Las bacterias , los protozoos y los hongos también tienen proteínas relacionadas con la hemoglobina que, por su función conocida o predicha, se unen a ligandos gaseosos de forma reversible. Además de transportar y detectar oxígeno, estas proteínas pueden participar en la eliminación de oxígeno de los medios que se cree que siguen siendo anaeróbicos , como también es el caso de la leghemoglobina .
Dado que muchas de estas proteínas están formadas por globinas y hemo , a menudo se las denomina "hemoglobina", aunque su estructura general es muy diferente de la hemoglobina de los vertebrados . En particular, la distinción entre mioglobina y hemoglobina a menudo es imposible en los animales más simples en ausencia de músculos en este último, mientras que el sistema circulatorio de la mayoría de los insectos no está involucrado en la difusión de oxígeno a través del cuerpo. Varios artrópodos ( arañas , escorpiones , algunos crustáceos ) usan el ojo de la cerradura , que es un hemo libre que contiene cobre pero que usa cationes de cobre coordinados directamente con residuos de histidina , pero esta proteína no es homóloga a la hemoglobina.
La estructura de las hemoglobinas es muy variable según la especie considerada. A menudo es monoglobina en bacterias, protozoos, algas y plantas , mientras que muchos nematodos , moluscos y crustáceos tienen proteínas muy grandes que contienen un número mucho mayor de subunidades que en los vertebrados. Los hongos y anélidos en particular poseen hemoglobinas quiméricas que contienen tanto globinas como otros tipos de proteínas. Así, el gusano tubo gigante de los respiraderos hidrotermales contiene una variedad de hemoglobina que comprende no menos de 144 subunidades de globina, cada una asociada con un grupo hemo, cuya función es capturar oxígeno O 2y sulfuro de hidrógeno H 2 Snecesario para las bacterias que viven en simbiosis con él, así como el dióxido de carbono CO 2necesario para el anabolismo del gusano. Estas estructuras son notables porque pueden transportar oxígeno en presencia de iones sulfuro y transportar estos iones ellos mismos sin ser envenenados por ellos como lo son las hemoglobinas de otras especies.
Entre las proteínas distintas de la hemoglobina capaces de unirse al oxígeno, se pueden retener las siguientes moléculas:
- Mioglobina : se encuentra en los músculos de la mayoría de los vertebrados , incluidos los humanos , y le da a estos tejidos un tinte rojo o gris oscuro. Su estructura es muy similar a las subunidades de globina de la hemoglobina, pero es monomérica y, por lo tanto, no exhibe un efecto cooperativo al unirse al oxígeno. Está más involucrado en el almacenamiento de oxígeno que en su transporte.
- Hemocianina : el segundo transportador de oxígeno más común en la naturaleza después de la hemoglobina, se encuentra en muchos artrópodos y moluscos . Utiliza un grupo protésico que consiste en cobre, no hierro hemo , y exhibe un color azul cuando se oxigena.
- Hemeritrina : algunos invertebrados marinos y algunas especies de anélidos utilizan esta proteína de hierro no hemo para transportar oxígeno. Tiene un color rosa o violeta cuando se oxigena y es transparente cuando no se oxigena.
- Clorocruorina : se encuentra en muchos anélidos, es muy similar a la eritrocruorina, pero su grupo hemo tiene una estructura marcadamente diferente. Es rojo cuando se oxigena y verde cuando se desoxigena (de ahí su nombre).
- Eritrocruorina : se encuentra en muchos anélidos, incluidas las lombrices de tierra , esta es una proteína muy grande que puede contener más de cien subunidades de proteína y unidades de hemo, todas las cuales tienen una masa molecular de hasta 3.600 kDa .
- Leghemoglobina - presente en las vainas , tales como alfalfa y soja , que tiene la función de proteger las bacterias que fijan el nitrógeno de oxígeno para permitir que la nitrogenasa para reducir el nitrógeno , que se puede hacer en la presencia de oxígeno.
Uso clínico
En medicina, varios términos se refieren a la hemoglobina:
- El nivel de hemoglobina se expresa en g / 100 mL . Los valores normales de hemoglobina dependen del sexo y la edad del sujeto. Un nivel de hemoglobina por debajo de la norma define anemia . Los valores de referencia son más altos para los hombres que para las mujeres. Un estudio cuestiona los parámetros de referencia de hemoglobina, argumentando que no se justifica tener diferentes parámetros de referencia de hemoglobina para hombres y mujeres.
- La saturación SaO 2definido en% se calcula por la cantidad de oxihemoglobina dividida por la cantidad total de hemoglobina en la sangre. La saturación SaO 2se puede medir en sangre venosa o arterial. Uno de los parámetros de una prueba llamada gasometría es la saturación de oxígeno de la sangre . El valor de saturación se considera peligroso si es inferior al 90% para la sangre arterial. El valor normal es de aproximadamente el 96-100% para condiciones atmosféricas normales. A este valor, hablamos de capacidad de O 2sangre .
- La cianosis es un signo clínico. Ésta es la coloración azulada de los tegumentos. Aparece cuando la concentración de hemoglobina reducida supera los 5 g / 100 ml de sangre capilar. Puede estar enmascarado por anemia.
Enfermedades genéticas de la hemoglobina.
Como muchas proteínas, las cadenas de hemoglobina presentan diversas mutaciones que, en la mayoría de los casos, no tienen impacto clínico. Se han identificado más de 500 hemoglobinas anormales. Ciertas mutaciones (Hb Köln, Indianápolis, etc.) provocan inestabilidad del tetrámero precipitante en el cuerpo de Heinz o metahemoglobinemia (hemoglobina M).
En ocasiones esta mutación provoca una afinidad anormal por el oxígeno, es decir, como Hb Hope, una disminución de la afinidad con un P50 elevado dando una anemia y cianosis bien toleradas en reposo, estando mal soportado el esfuerzo y la altitud., O, como la Hb Chesapeake, Malmö u Olympia, un aumento de la afinidad con una P50 reducida y una policitemia compensadora que conduce a manifestaciones clínicas a partir de cierta edad.
Otros pueden ser responsables de hemólisis crónica, HbS (por mutación de glutamina a valina que provocará la polimerización de Hb), HbC, o empeorar en el estado heterocigoto otra hemoglobinopatía, HbO Arab, HbD Punjab o Hb Lepore, o β-talasemia, HbE.
Finalmente, el daño genético puede estar relacionado no con la estructura primaria de la proteína, sino con un defecto cuantitativo en su síntesis, o una persistencia anormalmente alta de hemoglobina HbF fetal.
Los defectos de síntesis o la anomalía molecular se describen bajo los nombres de:
Histórico
Se dieron los primeros estudios de la hemoglobina para el XIX ° siglo en Alemania . Descubierta en 1840 por Hünefeld, la hemoglobina fue cristalizada en 1851 por Otto Funke (en) , y fue Felix Hoppe-Seyler quien demostró la fijación reversible del oxígeno en esta proteína en 1866. La naturaleza tetramérica y el peso molecular de la hemoglobina fueron establecidos por Gilbert Smithson Adair (en) en 1925 midiendo la presión osmótica de soluciones de hemoglobina, que también identificó las bases del efecto cooperativo de la unión del oxígeno a esta proteína por la alosteria .
La estructura tridimensional de la hemoglobina fue establecida por Max Perutz en 1959 mediante cristalografía de rayos X , lo que le llevó a compartir el Premio Nobel de Química de 1962 con John Kendrew , quien había realizado un trabajo similar sobre la mioglobina .
Hemoglobina en las artes
En 2005, el artista Julian Voss-Andreae creó la escultura Corazón de acero (hemoglobina) , inspirada en la columna vertebral de la proteína. La escultura está realizada en vidrio y acero corten . El aspecto oxidado de la obra es intencionado y evoca la reacción química fundamental de la unión del oxígeno al hierro contenido en la hemoglobina.
El artista de Montreal, Nicolas Baier, creó la escultura Lustre (Hemoglobina) , una escultura de acero inoxidable pulido que muestra la estructura de la molécula de hemoglobina. La escultura está ubicada en el atrio del centro de investigación del Centro de Salud de la Universidad McGill en Montreal. El tamaño de la escultura es de aproximadamente 10 metros por 10 metros por 10 metros.
Notas y referencias
- (en) G. Fermi, MF Perutz y B. Shaanan , " La estructura cristalina de la desoxihemoglobina humana a una resolución de 1,74 A " , Journal of Molecular Biology , vol. 175, n o 2 15 de mayo de 1984, p. 159-174 ( PMID 6726807 , DOI 10.1016 / 0022-2836 (84) 90472-8 , leer en línea )
- Los valores de la masa y el número de residuos indicados aquí son los de la proteína precursora resultante de la traducción del gen , antes de las modificaciones postraduccionales , y pueden difieren significativamente de los valores correspondientes a la proteína funcional.
- (en) Robert I. Weed, Claude F. Reed y George Berg , " ¿Es el año estructural de la hemoglobina un componente esencial de las membranas de eritrocitos humanos? ” , Revista de Investigación Clínica , vol. 42,Abril 1963, p. 581-588 ( PMID 13999462 , PMCID 289,318 , DOI 10.1172 / JCI104747 , leer en línea )
- (in) E. Domínguez de Villota, MT García Carmona, JJ Rubio y S. Andrés Ruiz , " Igualdad de la capacidad de unión de oxígeno in vivo e in vitro de la hemoglobina en pacientes con enfermedad respiratoria grave " , British Journal of Anesthesia , vol. 53, n o 12,Diciembre de 1981, p. 1325-1328 ( PMID 7317251 , PMCID 289,318 , DOI 10.1093 / bja / 53.12.1325 , leer en línea )
- (En) Connie CW Hsia , " Función respiratoria de la hemoglobina " , The New England Journal of Medicine , vol. 338, n o 4, 22 de enero de 1998, p. 239-247 ( PMID 9435331 , DOI 10.1056 / NEJM199801223380407 , leer en línea )
- (en) Sr. Biagioli, Sr. Pinto, D. et al Cesselli. , “ Expresión inesperada de α- y β-globina en neuronas dopaminérgicas mesencefálicas y células gliales ” , Actas de la Academia Nacional de Ciencias de los Estados Unidos de América , vol. 106, n o 36, 8 de septiembre de 2009, p. 15454-15459 ( PMID 19717439 , PMCID 2732704 , DOI 10.1073 / pnas.0813216106 , leer en línea [PDF] )
- (en) Roy E. Weber y Serge N. Vinogradov, “ hemoglobinas nonvertebrate: funciones y adaptaciones moleculares ” , Physiological Revisión , vol. 81 n o 2, Abril de 2001, p. 569-628 ( PMID 11274340 , leer en línea )
- (en) Ross C. Hardison , " Una breve historia de las hemoglobinas: plantas, animales, protistas y bacterias " , Actas de la Academia Nacional de Ciencias de los Estados Unidos de América , vol. 93, n o 12, 11 de junio de 1996, p. 5675-5679 ( PMID 8650150 , PMCID 39118 , DOI 10.1073 / pnas.93.12.5675 , JSTOR 39604 , Bibcode 1996PNAS ... 93.5675H , leer en línea )
- (En) Mireille Van CP Beekvelt Willy NJM Colier, Ron A. Wevers y Van Engelen Baziel GM , " Rendimiento de la espectroscopia de infrarrojo cercano en el consumo local de O2 y la medición del flujo sanguíneo en el músculo esquelético " , Journal of Applied Physiology , vol. 90, n o 2 Febrero de 2001, p. 511-519 ( PMID 11160049 )
- (en) RD Shannon , " Radios iónicos efectivos Estudios revisados y sistemáticos de distancias interatómicas en haluros y calcogenuros " , Acta Crystallographica Sección A: Física de cristales, Difracción, Cristalografía teórica y general , vol. 32, n o 5 de septiembre de p. 1976 ( DOI 10.1107 / S0567739476001551 , Bibcode 1976AcCrA..32..751S , leer en línea )
- (en) Wray H. Huestis y Michael A. Raftery , " Conformación y cooperatividad en la hemoglobina " , Bioquímica , vol. 14, n o 9,6 de mayo de 1975, p. 1886-1892 ( PMID 235969 , DOI 10.1021 / bi00680a013 , leer en línea )
- (in) Frank B. Jensen , " El doble papel de los glóbulos rojos en el suministro de oxígeno a los tejidos: transportadores de oxígeno y reguladores del flujo sanguíneo local " , Journal of Experimental Biology , vol. 212, n o Pt 21,noviembre de 2009, p. 3387-3393 ( PMID 19837879 , DOI 10.1242 / jeb.023697 , leer en línea )
- (en) D. Nicholas Bateman , " Monóxido de carbono " , Medicina , vol. 31, n o 10, Octubre de 2003, p. 41-42 ( DOI 10.1383 / medc.31.10.41.27810 , leer en línea )
- (in) CL y RL Townsend Maynard , " Efectos sobre la salud de la exposición prolongada a bajas concentraciones de monóxido de carbono " , Medicina ambiental y ocupacional , vol. 59, n o 10, Octubre de 2002, p. 708-711 ( PMID 12356933 , PMCID 1740215 , DOI 10.1136 / oem.59.10.708 , JSTOR 27731796 , leer en línea )
- (en) John Haldane , " La acción del óxido carbónico en el hombre " , The Journal of Physiology , vol. 18, n hueso 5-6, 16 de noviembre de 1895, p. 430-462 ( PMID 16992272 , PMCID 1514663 , DOI 10.1113 / jphysiol.1895.sp000578 , leer en línea )
- (En) Mark Goldstein , " Envenenamiento por monóxido de carbono " , Revista de enfermería de emergencia , vol. 34, n o 6, diciembre de 2006, p. 538-542 ( PMID 19022078 , DOI 10.1016 / j.jen.2007.11.014 , leer en línea )
- (En) Tim Struttmann Amy Scheerer, T. Scott Prince y Linda A. Goldstein , " Intoxicación involuntaria por monóxido de carbono de una fuente poco probable " , Revista de la Junta Estadounidense de Medicina Familiar , vol. 11, n o 6, Noviembre-diciembre de 1998, p. 481-484 ( PMID 9876005 , DOI 10.3122 / jabfm.11.6.481 , leer en línea )
- (En) Edward R. Burka , " Características de la degradación del ARN en la célula eritroide " , Journal of Clinical Investigation , vol. 48, n o 7, Julio de 1969, p. 1266-1272 ( PMID 5794250 , PMCID 322349 , DOI 10.1172 / JCI106092 , leer en línea )
- (en) Goro Kikuchi, Tadashi Yoshida Masato Noguchi , " Hemo oxigenasa y degradación del hemo " , Comunicaciones de investigación bioquímica y biofísica , vol. 338, n o 1, 9 de diciembre de 2005, p. 558-567 ( PMID 16115609 , DOI 10.1016 / j.bbrc.2005.08.020 , leer en línea )
- (en) Ross C. Hardison , " Evolución de la hemoglobina y sus genes " , Cold Spring Harbor Perspectives in Medicine , vol. 2, n o 12, Diciembre 2012, a011627 ( PMID 23209182 , PMCID 3543078 , DOI 10.1101 / cshperspect.a011627 , leer en línea )
- (en) Morris Goodman, William G. Moore y Genji Matsuda , " darwiniana Evolución en la genealogía de hemoglobina " , Naturaleza , vol. 253, n o 5493, 20 de febrero de 1975, p. 603-608 ( PMID 1089897 , DOI 10.1038 / 253603a0 , Bibcode 1975Natur.253..603G , leer en línea )
- (en) Jay F. Storz, Juan C. Opazo y Federico G. Hoffmann , “ La duplicación de genes, la duplicación del genoma, y la diversificación funcional de vertebrados globinas ” , Molecular Phylogenetics and Evolution , vol. 66, n o 2 febrero de 2013, p. 469-478 ( PMID 22846683 , PMCID 4306229 , DOI 10.1016 / j.ympev.2012.07.013 , leer en línea )
- (in) EA Zimmer, SL Martin, Beverley SM, YW Kan y AC Wilson , " Duplicación rápida y pérdida de genes que codifican las cadenas alfa de la hemoglobina " , Actas de la Academia Nacional de Ciencias de los Estados Unidos , vol. 77, n o 4, Abril de 1980, p. 2158-2162 ( PMID 6929543 , PMCID 348671 , DOI 10.1073 / pnas.77.4.2158 , leer en línea )
- (en) Cynthia M. Beall, Kijoung Song, Robert C. Elston y Melvyn C. Goldstein , " Mayor supervivencia de la descendencia tibetana entre mujeres con genotipos de alta saturación de oxígeno que residen a 4.000 m " , Actas de la Academia Nacional de Ciencias de los Estados Unidos. Estados de América , vol. 101, n o 39, 28 de septiembre de 2004, p. 14300–14304 ( PMID 15353580 , PMCID 521103 , DOI 10.1073 / pnas.0405949101 , leer en línea )
- (en) Zhenning Él y J. Eric Russell , “ Expresión, purificación y caracterización de hemoglobinas humanos Gower-1 (ζ 2 ε 2 ), Gower-2 (α 2 ε 2) y Portland-2 (ζ 2 β 2) ensamblados en ratones deficientes transgénicos complejos ” , Blood , vol. 97, n o 4,15 de febrero de 2001, p. 1099-1105 ( PMID 11159543 , leer en línea )
- (en) J. Eric Russell y Stephen A. Liebhaber , " Reversión de α- y β-talasemias letales en ratones por expresión de globinas embrionarias humanas " , Blood , vol. 92, n o 9, Noviembre de 1998, p. 3057-3063 ( PMID 9787139 , leer en línea )
- (en) Sophie Lanzkron John J. Strouse, Renee Wilson, Mary Catherine Beach, Carlton Haywood Park Haesong Catherine Witkop, Eric B. Bass y Jodi B. Segal , " Revisión sistemática: hidroxiurea para el tratamiento de adultos con anemia falciforme " , Anales de Medicina Interna , vol. 148, n o 12, 17 de junio de 2008, p. 939-955 ( PMID 18458272 , PMCID 3256736 , DOI 10.7326 / 0003-4819-148-12-200806170-00221 , leer en línea )
- (in) Amoz I. Chernoff Virginia Minnich, Supa Na Nakorn, Soodsarkorn Tuchinda, Channivat Kashemsant y Renate R. Chernoff , " Estudios sobre hemoglobina S - I. Las características clínicas, hematológicas y genéticas de los síndromes de hemoglobina E " , Revista de Laboratorio y Medicina Clínica , vol. 47, n o 3, Marzo de 1956, p. 455-489 ( PMID 13353880 , leer en línea )
- (en) " Incidencia, prevalencia y años de vida con discapacidad a nivel mundial, regional y nacional por 301 enfermedades y lesiones agudas y crónicas en 188 países, 1990-2013: un análisis sistemático para el Estudio de carga mundial de enfermedades 2013 " , Lancet , vol. 386, n o 9995, 22 de agosto de 2015, p. 743-800 ( PMID 26063472 , DOI 10.1016 / S0140-6736 (15) 60692-4 , leer en línea )
- (en) William E. Royer Jr., Hitesh Sharma, Kristen Strand, James E. Knapp y Balaji Bhyravbhatla , " Lumbricus Erythrocruorin en 3.5 Å Resolución: Arquitectura de un complejo respiratorio megadalton " , Estructura , vol. 14, n o 7, julio de 2006, p. 1167-1177 ( PMID 16843898 , DOI 10.1016 / j.str.2006.05.011 , leer en línea )
- (en) Luc Int Panis, Boudewijn Goddeeris y Rudolf Verheyen , " La concentración de hemoglobina de Chironomus cf. Plumosus l. (Diptera: Chironomidae) larvas de dos hábitats lénticos ” , Netherland Journal of Aquatic Ecology , vol. 29, n o 1, Abril de 1995, p. 1-4 ( DOI 10.1007 / BF02061785 , leer en línea )
- (en) Franck Zal, Francis H. Lallier, Brian N. Green, Serge N. Vinogradov y Andre Toulmond , " El sistema de hemoglobina múltiple del gusano de tubo de ventilación hidrotermal gusano de tubo gigante. II. Composición completa de la cadena de polipéptidos investigada mediante análisis de entropía máxima de espectros de masas ” , Journal of Biological Chemistry , vol. 271, n o 15, 12 de abril de 1996, p. 8875-8881 ( PMID 8621529 , DOI 10.1074 / jbc.271.15.8875 , leer en línea )
- (in) Zoran Minic y Guy Hervé , " Aspectos ioquímicos y enzimológicos de la simbiosis entre el gusano tubular de aguas profundas El gusano tubular gigante y su endosimbionte bacteriano " , The FEBS Journal , vol. 271, n o 15, Agosto de 2004, p. 3093-3102 ( PMID 15265029 , DOI 10.1111 / j.1432-1033.2004.04248.x , leer en línea )
- " ¿Cuál es la evidencia de las diferencias de género en la ferritina y la hemoglobina? » (Consultado el 2 de noviembre de 2019 )
- Hematología de Bernard Dreyfus, Médecine-Sciences- Flammarion1992
- (de) Felix Hoppe-Seyler , " Über die oxidation in lebendem blute " , Med-chem Untersuch Lab , 1866, p. 133–140
- (en) Gilbert S. Adair , " La presión osmótica de la hemoglobina en ausencia de sales " , Actas de la Royal Society de Londres. Serie B, que contiene artículos de carácter biológico , vol. 98, n o 692, Octubre de 1925, p. 524 ( DOI 10.1098 / rspa.1925.0126 , JSTOR 94515 , Bibcode 1925RSPSB..98..524A , leer en línea )
- (en) MF Perutz, Rossmann MG, Ann F. Cullis, Hilary MUIRHEAD, GEORG WILL & ACT NORTH , " Estructura de la hemoglobina: una síntesis de Fourier tridimensional en 5.5-Å. Resolución, obtenida por análisis de rayos X ” , Nature , vol. 185, n o 4711 13 de febrero de 1960, p. 416-422 ( PMID 18990801 , DOI 10.1038 / 185416a0 , leer en línea )
- (en) Max Perutz F. , " Estructura de la hemoglobina " , Simposios de Brookhaven en Biología , vol. 13, 1960, p. 165-183 ( PMID 13734651 )
-
(in) " The Nobel Prize in Chemistry in 1962 " (consultado el 6 de noviembre de 2016 ) :
" El Premio Nobel de Química 1962 fue otorgado conjuntamente a Max Ferdinand Perutz y John Cowdery Kendrew" por sus estudios de las estructuras de las proteínas globulares " . "
- (en) Constance Holden , " Blood and Steel " , Science , vol. 309, n o 5744,30 de septiembre de 2005, p. 2160 ( DOI 10.1126 / science.309.5744.2160d , leer en línea [PDF] )
- (en) Moran L Horton RA Scrimgeour G, Perry M, Principios de bioquímica , Boston, MA, Pearson ,2011, 786 p. ( ISBN 978-0-321-70733-8 y 0-321-70733-8 ) , pág. 127
- (en) Sean Henry, " Eche un vistazo a la colección de arte del MUHC " en CBC News ,7 de agosto de 2014(consultado el 1 st 02 2016 )
- " Lustre (hemoglobina) 2014 " en el arte público de Montreal (consultado el 1 er de febrero de el año 2016 )
- " Nicolas Baier " en la McGill University Health Centre (consultado el 1 er de febrero de el año 2016 )
Ver también
Bibliografía
- Banerjee, R. y Sagaert, L. (1967). Disociación de la hemoglobina humana en un medio ácido . Biochimica y Biophysica Acta (BBA) -Protein Structure, 140 (2), 266-273 ( resumen ).
- Blum, N., Maleknia, M. y Schapira, G. (1970). Α- y β-globinas libres y biosíntesis de hemoglobina. Biochimica et Biophysica Acta (BBA) -ácidos nucleicos y síntesis de proteínas, 199 (1), 236-247.
- Breton-Gorius, J. (1970). Uso de diaminobencidina para la demostración al microscopio electrónico de hemoglobina intracelular . Nuevo Rvdo. P. Hematology, 10, 243-256.
- Caffin, JP, Chauvet, JP y Acher, R. (1969). Hemoglobinas de anfibios: Separación y caracterización preliminar de las cadenas de hemoglobina del sapo Bufo bufo . Cartas FEBS, 5 (3), 196-198 ( resumen ).
- Bardakdjian-Michau, J., Dhondt, JL, Ducrocq, R., Galactéros, F., Guyard, A., Huchet, FX, ... y Wajcman, H. (julio de 2003). Buenas prácticas en el estudio de la hemoglobina . En Annals of Clinical Biology (Vol. 61, No. 4, págs. 401-409).
- Bernard, M., Bordas-Fonfrède, M., Grimaldi, A., Guillemin, C., Stahl, A., Leutenegger, M. y Gillery, P. (1995). Intereses respectivos de los ensayos de hemoglobina glucosilada y fructosamina en el seguimiento de la diabetes mellitus . En Annals of Clinical Biology (Vol. 53, No. 6, págs. 321-327). John Libbey Eurotext.
- Bert, P. (1882). Sobre la riqueza de hemoglobina de la sangre de animales que viven en lugares elevados. CR Acad Sci París, 94, 805-807.
- Bloch-Raphaël, C. (1939). Localización, formación y destrucción de hemoglobina en anélidos poliquetos (Tesis doctoral).
- Eaton, WA y Hofrichter, J. (1990). Polimerización de hemoglobina de células falciformes . Advances in protein chemistry, 40, 263-279.
- Foettinger, A. (1880). Sobre la existencia de hemoglobina en equinodermos . Arco. Biol. París, 1, 405-415.
- Kruh, J., Dreyfus, JC y Schapira, G. (1964). Activación de la síntesis de hemoglobina libre de células por el ácido ribonucleico: III. Acción del ácido ribonucleico hepático total . Biochimica et Biophysica Acta (BBA) -Sección especializada en ácidos nucleicos y temas relacionados, 91 (3), 494-505 ( resumen ).
- Kruh, J., Dreyfus, JC, Rosa, J. y Schapira, G. (1962). Síntesis de hemoglobina por sistemas de reticulocitos libres de células . Biochimica et Biophysica Acta (BBA) -Sección especializada en ácidos nucleicos y temas relacionados, 55 (5), 690-703.
- Lambert, PP, Grégoire, F. y Royers, E. (1955). Hemodinámica glomerular y excreción de hemoglobina . Archivos de fisiología y bioquímica, 63 (1), 7-34 ( resumen ).
- Lena-Russo, D., North, ML y Girot, R. (1992). Epidemiología de las enfermedades genéticas de la hemoglobina en Francia metropolitana . The Practitioner Review, 42 (15), 1867-1872.
- Robert, M. (1975). Afinidad de la hemoglobina por el oxígeno . Hospital cantonal, departamento médico, clínica médica terapéutica.
- Uriel, J. (1958). Detección de las actividades catalasa y peroxidasa de la hemoglobina después de la electroforesis en agar . Boletín de la Sociedad de Química Biológica, 40, 277-280.
- White, CT, Murray, AJ, Smith, DJ, Greene, JR y Bolin, RB (1986). Toxicidad sinérgica de endotoxinas y hemoglobina. J Lab Clin Med, 108 (2), 132-137.