Tirosina
| Tirosina | |
 L o S (-) - tirosina D o R (+) - tirosina 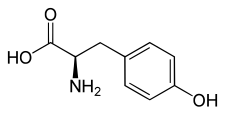 |
|
| Identificación | |
|---|---|
| Nombre IUPAC | ( S ) -2- amino -3- (4-hidroxi fenil ) propanoico |
| Sinónimos |
Y, Tyr |
| N o CAS |
(racémico) (L) oS(-) (D) o R |
| N o ECHA | 100.000.419 |
| N o EC | 200-460-4 |
| DrugBank | DB00135 |
| PubChem | 6057 |
| CHEBI | 18186 |
| FEMA | 3736 |
| Sonrisas |
C ([C @ H] (Cc1ccc (O) cc1) N) (O) = O , |
| InChI |
InChI: InChI = 1 / C9H11NO3 / c10-8 (9 (12) 13) 5-6-1-3-7 (11) 4-2-6 / h1-4,8,11H, 5,10H2, (H, 12,13) / t8- / m0 / s1 |
| Propiedades químicas | |
| Fórmula bruta |
C 9 H 11 N O 3 [Isómeros] |
| Masa molar | 181.1885 ± 0.0091 g / mol C 59.66%, H 6.12%, N 7.73%, O 26.49%, |
| pKa | 2.2 para el ácido; 9.11 para la base y 10.07 para el grupo fenol |
| Propiedades físicas | |
| T ° fusión | 343 ° C ( descomposición ) |
| Solubilidad | 479 mg · l -1 ( agua , 25 ° C ) |
| Termoquímica | |
| S 0 sólido | 214.01 J · mol -1 · K -1 |
| Δ f H 0 sólido | -685,6 kJ · mol -1 |
| C p | 216,44 J · mol -1 · K -1 (sólido, 25 ° C ) |
| Propiedades bioquimicas | |
| Codones | UAU, UAC |
| pH isoeléctrico | 5,66 |
| Aminoácido esencial | Según el caso |
| Ocurrencia en vertebrados | 3,3% |
| Precauciones | |
| WHMIS | |
|
Producto incontroladoEste producto no está controlado de acuerdo con los criterios de clasificación de WHMIS. |
|
| Ecotoxicologia | |
| LogP | -2,26 |
| Unidades de SI y STP a menos que se indique lo contrario. | |
La tirosina (Abreviaturas IUPAC - IUBMB : Tyr y Y ) es un ácido α-amino ácido cuyo enantiómero L es uno de los 20 amino ácidos proteinogénico estándar, codificada en el ARNm por codón UAU y UAC. Su cadena lateral contiene un grupo fenol , cuyo hidroxilo es ligeramente ácido ( pKa = 9,76). Este aminoácido no es esencial en los mamíferos pero, no obstante, el organismo puede producirlo en cantidades insuficientes en determinados casos particulares, por lo que se requiere un aporte alimentario .
La tirosina participa en la síntesis de catecolaminas : adrenalina , noradrenalina , dopamina y DOPA . También es un precursor de la melanina (pigmento que colorea la piel, el cabello, el iris ) y las hormonas tiroideas (formación de tironina a partir de dos tirosinas).
Biosíntesis
En mamíferos, se sintetiza por hidroxilación de fenilalanina , catalizada por fenilalanina hidroxilasa , excepto en un caso más o menos marcado de fenilcetonuria (enfermedad resultante de una acumulación de fenilalanina en sangre, por disminución de la actividad hidroxilasa). Por tanto, es fundamental en presencia de fenilalanina , y se encuentra que es un marcador significativo de la presencia de fenilalanina en el medio ambiente.
En las plantas y la mayoría de los microorganismos, la tirosina se produce a partir del prefenato, un metabolito intermedio de la vía del shikimato . El prefenato sufre una descarboxilación oxidativa para dar p -hidroxifenilpiruvato, que luego se transamina para dar tirosina y 2-cetoglutarato .
Cambios bioquímicos
El núcleo aromático de la tirosina (o parahidroxifenilalanina) comprende un grupo hidroxilo que hace que su cadena lateral sea menos hidrófoba que la de la fenilalanina (pero la tirosina es un aminoácido mucho menos soluble en agua que la fenilalanina). El grupo fenol (benceno + hidroxilo) le da absorción en UV a 277 nm . Su función hidroxilo permite que sea fosforilado por enzimas llamadas quinasas . La fosforilación de un aminoácido muy a menudo tiene la función de regular la actividad de la propia enzima. La treonina y la serina son dos aminoácidos que pueden sufrir la misma fosforilación . La tirosina también puede sufrir sulfatación o hidroxilación.
La tirosina también se puede modificar a (3-) nitrotirosina. Esta reacción de nitración puede afectar a la tirosina como aminoácido libre o como residuo de aminoácido integrado en una cadena polipeptídica. In vivo , esta reacción se debe principalmente a la acción del ácido peroxinitroso (o peroxinitrito , ONOO (-)), pero otras vías de reacción también pueden conducir a la formación de nitrotirosina. In vitro , el tetranitrometano (TNM) también se ha utilizado para este propósito. La nitración de tirosinas se considera generalmente un fenómeno patológico ( por ejemplo, el aumento de la concentración plasmática de nitrotirosina se considera un biomarcador de fenómenos inflamatorios), aunque recientemente se ha sugerido la posibilidad de que esta reacción sea también un fenómeno fisiológico.
Las tirosinas involucradas en enlaces peptídicos dentro de las proteínas pueden formar puentes tirosina tirosina (ditirosina), tirosina-tirosina-tirosina (tritirosina), tirosina-tirosina-tirosina-tirosina (tétratirosina).
Aplicaciones Terapéuticas
Henri Laborit fue uno de los primeros investigadores en utilizarlo y obtener patentes mundiales para su aplicación terapéutica, en el tratamiento de estados de shock, depresión , hipertensión arterial y enfermedad de Parkinson . Tuvo que darse por vencido porque no pudo encontrar a nadie en ese momento para explotarlos.
Desorden de déficit de atención
La administración oral de tirosina, junto con 5-HTP (precursor inmediato de la serotonina) y una serie de cofactores y adyuvantes , provocó una mejora significativa en el 67% de 85 participantes en un ensayo clínico del trastorno por déficit de atención con hiperactividad. Tras el ajuste de la dosis basado en la excreción de metabolitos urinarios en aquellos que no respondieron al tratamiento, la tasa de éxito fue del 77%. Con frecuencia se observó que la administración de tirosina no era suficiente, y que DOPA, en forma de extracto estandarizado al 40% de la planta Mucuna pruniens (guisante arbustivo ) era necesaria para lograr los incrementos de catecolaminas deseados (evaluados por medición de metabolitos urinarios). Los autores del estudio señalan que el grado de seguridad de este protocolo se compara favorablemente con los métodos farmacológicos de uso común (por ejemplo, metilfenidato (ritalina)).
Alimentos que son fuentes de tirosina
Como todos los aminoácidos, la tirosina está presente donde hay proteínas.
Sin embargo, la cantidad de tirosina ingerida no solo dependerá de sus concentraciones en un alimento determinado, sino también de la cantidad total consumida. Por ejemplo, es más raro que consumamos tanta proteína al comer semillas de sésamo o de calabaza como al consumir frijoles : La tirosina se encuentra en particular en los siguientes alimentos:
- de almendras ;
- abogado ;
- plátano ;
- frijol de lima ;
- semilla de calabaza ;
- semilla de sésamo ;
- quesos duros: parmesano , 2328 mg; condado , emmenthal , 1693 mg;
- semillas de soja tostadas, sin sal, 1332 mg;
- jamón crudo.
- Semillas, harina de semilla de algodón , baja en grasas, 1796 mg, etc.
Puede ver pequeñas estrellas blancas visibles en la sección de algunos quesos duros como el parmesano y el comté. Se trata de cristales de tirosina, que dan fe de la proteólisis que tuvo lugar durante la maduración del queso. Esta tirosina, poco soluble en agua, se acumula en finas cristalizaciones.
Acción en el cuerpo humano
La tirosina participa en la síntesis de melanina , el pigmento natural de la piel y el cabello, y en la de la tiroxina , la hormona tiroidea.
Actúa sobre la depresión o la ansiedad y participa en la formación del neurotransmisor epinefrina en la médula suprarrenal .
Un atleta o culturista que entrena intensamente puede beneficiarse de la suplementación con L tirosina que, al afectar directamente los niveles de dopamina , puede ayudar a combatir la fatiga y el estrés asociados con entrenamientos pesados e intensivos. Algunos estudios también parecen indicar que la L tirosina puede ser útil para perder peso.
Notas y referencias
- (en) " Tirosina " , en ChemIDplus , Accessed July 8, 2 009
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- (in) "Tirosina" en NIST / WebBook , Accessed July 8, 2,009 mil
- (en) Francis A. Carey, " Tabla de valores de pK y pH " , en el Departamento de Química de la Universidad de Calgary , 2014(consultado el 26 de julio de 2015 )
- (en) Mr. Beals, L. Gross, S. Harrell, " Amino Acid Frequency " en The Institute for Environmental Modeling (ITSH) de la Universidad de Tennessee (consultado el 26 de julio de 2015 )
- " Tirosina (l-) " en la base de datos de productos químicos Reptox de la CSST (organización de Quebec responsable de la seguridad y salud ocupacional), consultado el 25 de abril de 2009
- (en) Gerald Platzer , Mark Okon y Lawrence P. McIntosh , " Desplazamientos químicos de los aminoácidos ionizables de la bobina aleatoria 1H, 13C y 15N dependientes del pH: una guía para las mediciones de la proteína pK a " , Journal of Biomolecular NMR , flight . 60, n hueso 2-3,20 de septiembre de 2014, p. 109-129 ( ISSN 0925-2738 y 1573-5001 , DOI 10.1007 / s10858-014-9862-y , leído en línea , consultado el 11 de septiembre de 2018 )
- (in) JBA Ross, WR Laws, KW Rousslang y HR Wyssbrod, "Fluorescencia de tirosina y fosforescencia de proteínas y polipéptidos" en JR Lakowicz, Temas de espectroscopia de fluorescencia , vol. 3: Aplicaciones bioquímicas , Nueva York, Springer ( ISBN 978-0-306-47059-2 , DOI 10.1007 / b112909 , leer en línea )
- (in) Svend Olav Andersen, " Los enlaces cruzados en la APROBACIÓN de resilina tienen ditirosina y tritirosina " , Biochimica et Biophysica Acta , vol. 93, n o 1,1964, p. 213-215 ( DOI 10.1016 / 0304-4165 (64) 90289-2 )
- Estos fueron cofactores necesarios para la síntesis de catecolaminas y serotonina, así como moléculas útiles para incrementar la efectividad del tratamiento: vitamina C : 1000 mg ; calcio (citrato): 220 mg ; vitamina B6 : 75 mg ; ácido fólico : 400 μg ; lisina : 500 mg ; cisteína : 4.500 mg en adultos, 2.250 mg en niños; selenio : 400 μg en adultos y 200 μg en niños. Ver tirosina hidroxilasa y triptófano hidroxilasa .
- Marty Hinz , Alvin Stein , Robert Neff y Robert Weinberg , " Tratamiento del trastorno por déficit de atención con hiperactividad con precursores de aminoácidos monoamínicos e interpretación del ensayo de transportadores de cationes orgánicos ", Tratamiento y enfermedad neuropsiquiátrica , vol. 7,2011, p. 31–38 ( ISSN 1176-6328 , PMID 21326653 , PMCID 3035600 , DOI 10.2147 / NDT.S16270 , leído en línea , consultado el 6 de junio de 2020 )
- DOPA y 5HTP son los precursores inmediatos de la dopamina y la serotonina, respectivamente, y las enzimas que las sintetizan (la tirosina hidroxilasa y la triptófano hidroxilasa son limitantes)
- (in) Hinz M, Stein A, Neff R, Weinberg R, T Uncini, " Tratamiento del trastorno por déficit de atención con hiperactividad con Juventa de aminoácidos monoamínicos e interpretación del ensayo de transporte de cationes orgánicos " , Neuropsychiatr Dis Treat , vol. 7,2011, p. 31–8 ( PMID 21326653 , PMCID 3035600 , DOI 10.2147 / NDT.S16270 , leer en línea )
- Ver varias tablas de figuras para el contenido de tirosina (variable) [1] /
- " (no) pregunta estúpida: ¿qué son estos cristales de sal en mi queso?" » , Sobre productos lácteos ,15 de octubre de 2012(consultado el 26 de agosto de 2020 ) .
- (en) McLean A, Rubinsztein JS, Robbins TW, Sahakian BJ. " Los efectos del agotamiento de la tirosina en los voluntarios sanos normales: implicaciones para la depresión unipolar. » , Psicofarmacología , vol. 171, n o 3,2004, p. 286-97. ( PMID 12955284 , leer en línea )