Sacarosa
| Sacarosa | |
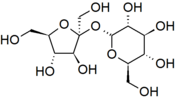 Sacarosa en representación poligonal Sacarosa en proyección de Haworth Estructura 3D de sacarosa  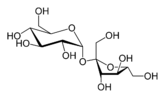 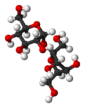  |
|
| Identificación | |
|---|---|
| Nombre IUPAC | α-D-glucopiranosil- (1 → 2) -β-D-fructofuranósido |
| Sinónimos |
neohancósido D |
| N o CAS | |
| N o ECHA | 100.000.304 |
| N o CE | 200-334-9 |
| PubChem | 5988 |
| Sonrisas |
O ([C @@] 1 (O [C @ H] (CO) [C @ H] ([C @@ H] 1O) O) CO) [C @ H] 1O [C @@ H] ([ C @@ H] (O) [C @@ H] ([C @ H] 1O) O) CO , |
| InChI |
InChI: InChI = 1 / C12H22O11 / c13-1-4-6 (16) 8 (18) 9 (19) 11 (21-4) 23-12 (3-15) 10 (20) 7 (17) 5 (2-14) 22-12 / h4-11,13-20H, 1-3H2 / t4-, 5-, 6-, 7-, 8 +, 9-, 10 +, 11-, 12 + / m1 / s1 |
| Apariencia | blanco sólido de forma variable. |
| Propiedades químicas | |
| Fórmula bruta |
C 12 H 22 O 11 [Isómeros] |
| Masa molar | 342,2965 ± 0,0144 g / mol C 42,11%, H 6,48%, O 51,42%, |
| pKa | 12,62 |
| Momento dipolar | 3,1 × 10-18 ° C · m |
| Propiedades físicas | |
| T ° fusión | 185,5 ° C |
| T ° hirviendo | descomposición |
| Solubilidad |
2000 g / L (agua, 25 ° C ) 67,47 % m (agua, 25 ° C ) Moderadamente suelo. en piridina , glicerol , metilpirrolidinona, metilpiperazina, DMSO , DMF ; |
| Densidad | 1,5879 g · cm -3 |
| Propiedades electronicas | |
| Constante dieléctrica | 3,50 - 3,85 |
| Precauciones | |
| WHMIS | |
|
Producto incontroladoEste producto no está controlado de acuerdo con los criterios de clasificación de WHMIS. |
|
| NFPA 704 | |
| 1 1 0 | |
| Ingestión | favorece la aparición de caries , en grandes dosis: vómitos, diarrea, dispepsia |
| Ecotoxicología | |
| DL 50 | 29,7 g · kg -1 (ratas, oral ) |
| LogP | -3,67 |
| Compuestos relacionados | |
| Otros compuestos |
Isomaltulosa , leucrosa , maltulosa , trehalulosa , turanosa |
| Unidades de SI y STP a menos que se indique lo contrario. | |
La sacarosa o sacarosa es un azúcar en el sabor dulce. Extracto de determinadas plantas, principalmente de la caña de azúcar y la remolacha azucarera , es muy utilizado para el consumo humano . Es un disacárido que consta de glucosa y fructosa , cuyo nombre estandarizado es α- D -glucopiranosil- (1↔2) -β- D -fructofuranósido, comúnmente abreviado como Glc-Fru. En inglés, se llama sacarosa , de ahí la abreviatura Suc que a veces se encuentra en la literatura para designar este compuesto.
Los carbohidratos , en particular la sacarosa, antes se denominaban átomos de hidratos debido a la antigua experiencia de deshidratación del azúcar blanco con el concentrado de ácido sulfúrico , en el que la sacarosa, fórmula molecular C 12 H 22 O 11, se descompuso en agua H 2 Oy negro de carbón . Habíamos deducido erróneamente que la fórmula de la sacarosa podría escribirse (H 2 O) 11 C 12, Correspondiente a un hidrato de carbono . Este término se ha convertido en obsoleto como resultado del trabajo de Norman Haworth que estableció al comienzo del XX ° siglo, la estructura de los hidratos de carbono, y ha caído en desuso desde entonces. Sin embargo, el término todavía se usa en el mundo de habla inglesa.
Propiedades
Estructura
La sacarosa es un disacárido formado a partir de una glucosa molécula y una fructosa molécula unidas por un α (1↔2) β osídica de bonos. Su fórmula bruta es C 12 H 22 O 11y su masa molar es 342,3 g mol -1 . A diferencia de la mayoría de los otros diholósidos, la sacarosa resulta de la unión de dos orificios óseos por su extremo reductor, lo que la convierte en un azúcar no reductor. Además, solo el anómero α de la glucopiranosa y el anómero β de la fructofuranosa forman sacarosa.
La sacarosa cristaliza en el sistema de cristal monoclínico de acuerdo con el grupo espacial P2 1 con los parámetros cristalinos a = 1.086 31 nm , b = 0.870 44 nm , c = 0.776 24 nm y β = 102.938 ° .
La pureza de la sacarosa se mide por polarimetría . Más precisamente, se mide la rotación del plano de polarización de la luz polarizada que pasa a través de una solución acuosa de azúcar. La rotación específica ( pulg ) a 20 ° C medida usando la línea D de sodio a 589 nm es + 66,47 °. De esta forma se controla la sacarosa comercial. No se deteriora en condiciones normales.
La sacarosa tiene cinco isómeros naturales que difieren en la posición del enlace osídico :
- Trehalulosa ⇒ Glucosa α (1 → 1) Fructosa
- Turanosa ⇒ Glucosa α (1 → 3) Fructosa ( disacárido reductor )
- Maltulosa ⇒ Glucosa α (1 → 4) Fructosa
- Leucrosa ⇒ Glucosa α (1 → 5) Fructosa (disacárido reductor)
- Isomaltulosa (palatinosa) ⇒ Glucosa α (1 → 6) Fructosa (disacárido reductor)
Reacciones con sacarosa
Son posibles diferentes transformaciones químicas utilizando sacarosa como reactivo :
Descomposición térmicaLa descomposición térmica de la sacarosa se puede representar como una reacción de dos pasos:
- primera deshidratación (por ácido sulfúrico H 2 SO 4) produciendo agua y negro de humo :
- luego la oxidación (con oxígeno del aire) del carbono a dióxido de carbono :
La sacarosa no se derrite cuando se calienta, pero se descompone a alrededor de 186 ° C para formar caramelo .
CombustiónLa sacarosa se quema, en una reacción exotérmica , formando agua y dióxido de carbono, al igual que todos los carbohidratos .
Con ácido clorhídricoCon ácido clorhídrico HClO 3, la sacarosa libera agua, dióxido de carbono y cloruro de hidrógeno (HCl):
8 HClO 3+ C 12 H 22 O 11→ 11 H 2 O+ 12 CO 2+ 8 HCl .Propiedades químicas
La sacarosa es un azúcar no reductor , el carbono hemiacetal de la glucosa y el carbono hemiacetal de la fructosa están involucrados en el enlace osídico . No es higroscópico y no puede realizar mutarrotación .
HidrólisisLa hidrólisis de la sacarosa tiene el efecto de romper el enlace osídico liberando glucosa y fructosa en cantidades equimolares . Sin embargo, esta reacción es tan lenta que una solución acuosa de sacarosa puede permanecer prácticamente estable durante años. Por otro lado, es mucho más rápido en presencia de una sacarasa ( sacarasa-isomaltasa , invertasa , sacarosa alfa-glucosidasa ) o un ácido como HOOC - CHOH - CHOH - COOK bitartrato de potasio o jugo de limón , que son ácidos débiles . Lo mismo ocurre con el jugo gástrico , que participa en la digestión hidrolizando carbohidratos como la sacarosa.
La acción de la invertasa sobre la sacarosa da como resultado el azúcar invertido , que se compone de cantidades iguales de glucosa y fructosa.
Biosíntesis de sacarosaLa biosíntesis de la sacarosa se realiza mediante sacarosa sintasa-fosfato a partir de UDP-glucosa y fructosa 6-fosfato . La energía para esta reacción proviene de la escisión de UDP . La sacarosa es producida por plantas y cianobacterias, pero no por otros seres vivos. Ocurre naturalmente con fructosa en muchas plantas consumidas en la dieta humana . Es el principal carbohidrato de muchas frutas como la piña y el albaricoque ; otras frutas, como la pera y la uva , tienen fructosa como carbohidrato principal.
La síntesis total de sacarosa fue realizada por el químico canadiense Raymond Lemieux en 1953.
Propiedades físicas
Sacarosa caramelize a 160 ° C .
La variación de la solubilidad con la temperatura se muestra en la siguiente tabla:
| Cambio en la solubilidad de la sacarosa en agua en función de la temperatura. | |||
|---|---|---|---|
| temperatura | g de sacarosa por g de agua | porcentaje de masa | porcentaje molar |
| −10 ° C | 1,7615 | 63,79 % m | 8.484 % en moles |
| −5 ° C | 1,7837 | 64,08 % m | 8.582 % en moles |
| 0 ° C | 1.8127 | 64,45 % m | 8,710 % en moles |
| 5 ° C | 1.8489 | 64,90 % m | 8.868 % en moles |
| 10 ° C | 1.8926 | 65,43 % m | 9.059 % en moles |
| 15 ° C | 1,9443 | 66,04 % m | 9.283 % en moles |
| 20 ° C | 2.0047 | 66,72 % m | 9,544 % en moles |
| 25 ° C | 2.0741 | 67,47 % m | 9,842 % en moles |
| 30 ° C | 2.1535 | 68,29 % m | 10.180 % en moles |
| 35 ° C | 2.2435 | 69,17 % m | 10,561 % en moles |
| 40 ° C | 2.3450 | 70,10 % m | 10,986 % en moles |
| 45 ° C | 2.4589 | 71,09 % m | 11,459 % en moles |
| 50 ° C | 2.5863 | 72,12 % m | 11,981 % en moles |
| 55 ° C | 2.7282 | 73,18 % m | 12,556 % en moles |
| 60 ° C | 2.8857 | 74,26 % m | 13,185 % en moles |
| 65 ° C | 3.0598 | 75,37 % m | 13,871 % en moles |
| 70 ° C | 3.2515 | 76,48 % m | 14,613 % en moles |
| 75 ° C | 3.4616 | 77,59 % m | 15,411 % en moles |
| 80 ° C | 3.6901 | 78,68 % m | 16,263 % en moles |
| 85 ° C | 3.9368 | 79,74 % m | 17,164 % en moles |
| 90 ° C | 4.2003 | 80,77 % m | 18,104 % en moles |
| 95 ° C | 4.4775 | 81,74 % m | 19,071 % en moles |
| 100 ° C | 4.7637 | 82,65 % m | 20,046 % en moles |
| 105 ° C | 5.0335 | 83,43 % m | 20,944 % en moles |
| 110 ° C | 5.4499 | 84,50 % m | 22,290 % en moles |
| 115 ° C | 5.9347 | 85,58 % m | 23,801 % en moles |
| 120 ° C | 6.5062 | 86,68 % m | 25,508 % en moles |
| 125 ° C | 7.1895 | 87,79 % m | 27,452 % en moles |
| 130 ° C | 8.0211 | 88,91 % m | 29,685 % en moles |
La solubilidad de la sacarosa en disolventes no acuosos es generalmente menor. Además, la sacarosa no es soluble en disolventes no polares. Se obtienen valores elevados con amoniaco condensado (72%), dimetilsulfóxido (42%) y metilamina (> 25%). Los valores más bajos se obtienen con dióxido de azufre líquido, ácidos fórmico y acético , dimetilformamida , piridina (6%), propilenglicol , glicerol (7%), metanol , etanol , acetona y dioxano .
El nivel de azúcar viene dado por el grado Brix (que corresponde al porcentaje de masa a 20 ° C ). La concentración de una solución acuosa se puede evaluar midiendo la densidad con un mustímetro o el índice de refracción con un refractómetro .
La variación de algunas propiedades de la solución acuosa a 20 ° C se da en la siguiente tabla:
| Variación de algunas propiedades de una solución acuosa de sacarosa a 20 ° C | ||||||
|---|---|---|---|---|---|---|
| porcentaje de masa |
molalidad (moles por kg de agua) |
molaridad (moles por litro de solución) |
densidad | índice de refracción | temperatura de solidificación | viscosidad dinámica |
| 0,5 % m | 0,015 mol kg −1 | 0,015 mol l −1 | 1.000 2 g cm −3 | 1.3337 | −0,03 ° C | 1.015 mPa s |
| 1 % m | 0,03 mol kg −1 | 0,029 mol l −1 | 1,002 1 g cm −3 | 1.3344 | −0,06 ° C | 1.028 mPa s |
| 2 % m | 0,06 mol kg −1 | 0,059 mol l −1 | 1,006 g cm −3 | 1.3359 | −0,11 ° C | 1.055 mPa s |
| 3 % m | 0,09 mol kg −1 | 0,089 mol l −1 | 1,009 9 g cm −3 | 1.3373 | −0,17 ° C | 1.084 mPa s |
| 4 % m | 0,122 mol kg −1 | 0,118 mol l −1 | 1.013 9 g cm −3 | 1.3388 | −0,23 ° C | 1,114 mPa s |
| 5 % m | 0,154 mol kg −1 | 0,149 mol l −1 | 1.017 8 g cm −3 | 1.3403 | −0,29 ° C | 1,146 mPa s |
| 6 % m | 0,186 mol kg −1 | 0,179 mol l −1 | 1.021 8 g cm −3 | 1.3418 | −0,35 ° C | 1,179 mPa s |
| 7 % m | 0,22 mol kg −1 | 0,21 mol l −1 | 1.025 9 g cm −3 | 1.3433 | −0,42 ° C | 1.215 mPa s |
| 8 % m | 0,254 mol kg −1 | 0,241 mol l −1 | 1.029 9 g cm −3 | 1.3448 | −0,49 ° C | 1.254 mPa s |
| 9 % m | 0,289 mol kg −1 | 0,272 mol l −1 | 1.034 g cm −3 | 1.3463 | −0,55 ° C | 1.294 mPa s |
| 10 % m | 0,325 mol kg −1 | 0,303 mol l −1 | 1.038 1 g cm −3 | 1.3478 | −0,63 ° C | 1.336 mPa s |
| 12 % m | 0,398 mol kg −1 | 0,367 mol l −1 | 1.046 5 g cm −3 | 1.3509 | −0,77 ° C | 1.429 mPa s |
| 14 % m | 0,476 mol kg −1 | 0,431 mol l −1 | 1.054 9 g cm −3 | 1.3541 | −0,93 ° C | 1,534 mPa s |
| 16 % m | 0,556 mol kg −1 | 0,497 mol l −1 | 1.063 5 g cm −3 | 1.3573 | −1,1 ° C | 1,653 mPa s |
| 18 % m | 0,641 mol kg −1 | 0,564 mol l −1 | 1.072 2 g cm −3 | 1.3606 | −1,27 ° C | 1,79 mPa s |
| 20 % m | 0,73 mol kg −1 | 0,632 mol l −1 | 1.081 g cm −3 | 1.3639 | -1,47 ° C | 1.945 mPa s |
| 22 % m | 0,824 mol kg −1 | 0,7 mol l −1 | 1.089 9 g cm −3 | 1.3672 | -1,67 ° C | 2.124 mPa s |
| 24 % m | 0,923 mol kg −1 | 0,771 mol l −1 | 1.099 g cm −3 | 1.3706 | −1,89 ° C | 2.331 mPa s |
| 26 % m | 1.026 mol kg −1 | 0,842 mol l −1 | 1,108 2 g cm −3 | 1.3741 | −2,12 ° C | 2.573 mPa s |
| 28 % m | 1,136 mol kg −1 | 0,914 mol l −1 | 1,117 5 g cm −3 | 1.3776 | −2,37 ° C | 2.855 mPa s |
| 30 % m | 1.252 mol kg −1 | 0,988 mol l −1 | 1,127 g cm −3 | 1.3812 | -2,64 ° C | 3,187 mPa s |
| 32 % m | 1.375 mol kg −1 | 1.063 mol l −1 | 1,136 6 g cm −3 | 1.3848 | -2,94 ° C | 3.762 mPa s |
| 34 % m | 1,505 mol kg −1 | 1,139 mol l −1 | 1,146 4 g cm −3 | 1.3885 | −3,27 ° C | 4.052 mPa s |
| 36 % m | 1,643 mol kg −1 | 1.216 mol l −1 | 1,156 2 g cm −3 | 1.3922 | −3,63 ° C | 4.621 mPa s |
| 38 % m | 1,791 mol kg −1 | 1.295 mol l −1 | 1,166 3 g cm −3 | 1.396 | −4,02 ° C | 5.315 mPa s |
| 40 % m | 1.948 mol kg −1 | 1.375 mol l −1 | 1,176 5 g cm −3 | 1.3999 | -4,45 ° C | 6.162 mPa s |
| 42 % m | 2.116 mol kg −1 | 1,456 mol l −1 | 1,186 8 g cm −3 | 1,4038 | −4,93 ° C | 7.234 mPa s |
| 44 % m | 2.295 mol kg −1 | 1,539 mol l −1 | 1,197 2 g cm −3 | 1.4078 | 8.596 mPa s | |
| 46 % m | 2,489 mol kg −1 | 1,623 mol l −1 | 1,207 9 g cm −3 | 1,4118 | 10.301 mPa s | |
| 48 % m | 2.697 mol kg −1 | 1,709 mol l −1 | 1.218 6 g cm −3 | 1.4159 | 12,515 mPa s | |
| 50 % m | 2921 mol kg −1 | 1,796 mol l −1 | 1,229 5 g cm −3 | 1.4201 | 15.431 mPa s | |
| 60 % m | 4.382 mol kg −1 | 2.255 mol l −1 | 1,286 4 g cm −3 | 1,4419 | 58.487 mPa s | |
| 70 % m | 6,817 mol kg −1 | 2,755 mol l −1 | 1,347 2 g cm −3 | 1,4654 | 481,561 mPa s | |
| 80 % m | 11.686 mol kg −1 | 3299 mol l −1 | 1.411 7 g cm −3 | 1.4906 | ||
Propiedades edulcorantes
El poder edulcorante de la sacarosa se utiliza como referencia en la escala de productos edulcorantes, es decir, se considera igual a 1 por convención. El umbral de reconocimiento promedio de sacarosa es 0.017 mol l -1 ( 5.82 g / litro ).
Fuentes de sacarosa
En la naturaleza, la sacarosa está presente en un gran número de plantas y en particular en sus raíces , sus frutos y su néctar , donde se utiliza para almacenar la energía resultante de la fotosíntesis . Muchos mamíferos , aves , insectos y bacterias se alimentan de la sacarosa de las plantas, y algunos la convierten en su principal alimento. Las abejas juegan en este sentido un papel especial en la dieta humana al producir la miel que se consume en todas partes del mundo, a partir del néctar. Sin embargo, los azúcares de la miel son mayoritariamente glucosa y fructosa , con solo trazas de sacarosa.
A medida que la fruta madura , el nivel de sacarosa generalmente aumenta muy rápidamente, pero algunas frutas casi no contienen sacarosa. Este es, por ejemplo, el caso de las uvas , cerezas , arándanos ( arándanos ), moras , higos , granadas , tomates , aguacates , limones y limas .
Usos en la industria alimentaria
Ingrediente alimentario principal del azúcar
La sacarosa es uno de los ingredientes más utilizados en la industria alimentaria . Constituye la base de determinados sectores como la confitería , la pastelería , la industria de las mermeladas y las bebidas.
En la industria farmacéutica se utiliza como excipiente.
Fisicoquímica
La sacarosa es muy soluble en agua y su solubilidad aumenta con la temperatura. Es relativamente estable, sin embargo puede fermentar (un desarrollo indeseable en general, excepto para las bebidas alcohólicas) o hidrolizar (invertir, en el lenguaje de los pasteleros) en glucosa y fructosa , siendo este fenómeno controlable.
Cuando se utiliza en la industria de bebidas, la sacarosa se puede invertir por sí sola durante el tratamiento térmico. Además, al ser el azúcar invertido más soluble que la sacarosa, en su presencia, puede actuar como retenedor de agua y evitar la cristalización de esta última.
La sacarosa reduce la actividad del agua en productos que la contienen en gran cantidad, lo que permite su conservación.
También se puede utilizar como textura coadyuvante, por sus cualidades de apelmazamiento .
Granulometria
Los diferentes tamaños de cristales según las necesidades de la industria:
- azúcar cristalizado;
- azúcar en polvo ;
- azúcar glas ;
- azúcar de grano.
Uso en fermentación
La sacarosa es uno de los sustratos de fermentación más clásicos. Es fermentado por muchos microorganismos, incluido el bien estudiado Saccharomyces cerevisiae .
Uso en agricultura
La sacarosa tiene uso en agricultura. Pulverizar dosis muy bajas de azúcares solubles en arboricultura tiene un efecto insecticida.
Nutrición y salud
Consulte Azúcar / Nutrición y Azúcar / Salud .
Notas y referencias
- SACAROSA , la seguridad de hoja (s) del Programa Internacional para la Seguridad de Sustancias Químicas , consultado el 9 de mayo de 2009.
- (in) " sacarosa " en ChemIDplus , consultado el 5 de octubre de 2009.
- (en) William J. Colonna y Upasiri Samaraweera, Kirk-Othmer Encyclopedia of Chemical Technology: Propiedades de sacarosa , vol. 23, John Wiley & Sons., 4 ª ed. , p. 4.
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- (en) Mohammed Mathlouthi y P. Reiser, Sacarosa: propiedades y aplicaciones , Springer,1995, 294 p. ( ISBN 0-7514-0223-0 , leer en línea ) , pág. 107.
- (en) " Sacarosa " en el banco de datos de sustancias peligrosas (consultado el 18 de febrero de 2010 ) .
- " Sacarosa " en la base de datos de productos químicos Reptox de la CSST (organización de Quebec responsable de la seguridad y salud en el trabajo), consultado el 24 de abril de 2009.
- sacarosa se Spelling propuesto por correcciones de ortografía de los franceses en 1990 : Academia francesa , " sacarosa " en el Diccionario de la Academia Francesa (consultado el 1 er de julio de 2019 ) .
- (in) CA Beevers TRR McDonald JH Robertson y F. Stern , " La estructura cristalina de la sacarosa " , Acta Crystallographica , vol. 5,1952, p. 689-690 ( DOI 10.1107 / S0365110X52001908 , leer en línea ).
- (en) RC Hynes e Y. Le Page , " Sacarosa, una prueba conveniente para estructuras cristalinas absolutas " , Journal of Applied Crystallography , vol. 24,1991, p. 352-354 ( DOI 10.1107 / S0021889891002492 , leer en línea ).
- (en) Peter M. Collins, Diccionario de los hidratos de carbono , Boca Ratón, CRC Press ,2005, 1282 p. ( ISBN 0-8493-3829-8 ) , pág. 538.
- (en) Diccionario de carbohidratos Peter M. Collins , Boca Raton, CRC Press ,2005, 1282 p. ( ISBN 0-8493-3829-8 ) , pág. 948.
- (en) MA Godshall, " El mundo en expansión de los edulcorantes nutritivos y no nutritivos " [PDF] en http://www.sugarjournal.com ,enero 2007(consultado el 7 de noviembre de 2008 ) , pág. 12-20.
- (en) Diccionario de carbohidratos Peter M. Collins , Boca Raton, CRC Press ,2005, 1282 p. ( ISBN 0-8493-3829-8 ) , pág. 537.
- (in) Shmuel Yannai, Dictionary of Food Compounds with CD-ROM: Additives, Flavors and Ingredients , Boca Raton, CRC Press , 2004, 1784 p. ( ISBN 1-58488-416-9 , presentación en línea ) , p. 1243-1244.
- (En) RU Lemieux y G. Huber , " Una síntesis química de sacarosa " , Revista de la Sociedad Química Estadounidense , vol. 75, n o 16, Agosto 1953, p. 4118-4118 ( DOI 10.1021 / ja01112a545 , leer en línea ).
- (in) Food-Info , caramelización .
- (en) Neil L. Pennington y Charles W. Baker, Sugar, una guía del usuario de sacarosa , Springer,1990, 331 p. ( ISBN 0-442-00297-1 , leer en línea ) , pág. 49.
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press ,2003, 84 ª ed. , 2616 p. ( ISBN 0-8493-0484-9 , leer en línea ) , 8 -81.
- (en) RS Shallenberger, Taste Chemistry , Londres, Springer,1993, 613 p. ( ISBN 0-7514-0150-1 , leído en línea ) , “Naturaleza química, psicología y fisiología del gusto” , p. 5-46.
- (en) John E. Lunn , " Metabolismo de sacarosa " , eLS , diciembre de 2008( DOI 10.1002 / 9780470015902.a0021259 , leer en línea ).
- REGLAMENTO (UE) N ° 916/2014 LA COMISIÓN22 de agosto de 2014por el que se aprueba la sustancia de base "sacarosa" de conformidad con el Reglamento (CE) n. ° 1107/2009 del Parlamento Europeo y del Consejo relativo a la comercialización de productos fitosanitarios, y se modifica el anexo del Reglamento de Ejecución (UE) n o 540/2011 de la Comisión
- AZÚCARES SOLUBLES, ¿UNA OPORTUNIDAD PARA LA AGRICULTURA SOSTENIBLE?
Ver también
Artículos relacionados
enlaces externos
- (en) Sustancia sacarosa Base de datos NCBI
- (en) Compuesto: C00089 Sacarosa www.Genome.net
- (en) Glicano: G00370 Neohancoside D www.Genome.net
- (en) Sacarosa en la Biblioteca Nacional de Medicina - Encabezamientos de materias médicas MeSH


