Malaria
Malaria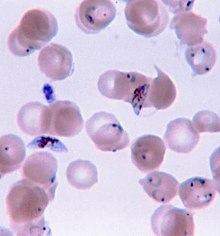 Frotis de sangre que revela la presencia del parásito Plasmodium falciparum que tiene forma de "C" o hoz dentro de los glóbulos rojos humanos.
Frotis de sangre que revela la presencia del parásito Plasmodium falciparum que tiene forma de "C" o hoz dentro de los glóbulos rojos humanos.
| Especialidad | Enfermedad infecciosa |
|---|
La malaria o malaria , también llamada "fiebre de los pantanos", es una enfermedad infecciosa causada por un parásito del género Plasmodium , que se transmite por la picadura de ciertas especies de mosquitos Anopheles .
Con 229 millones de personas enfermas y 409.000 muertes en 2019, la malaria sigue siendo la parasitosis más importante y afecta principalmente a niños menores de cinco años y mujeres embarazadas. El 95% de los casos se registraron en veintinueve países, en particular en el África subsahariana (27% en Nigeria, 12% en la República Democrática del Congo, 5% en Uganda, 4% en Mozambique) ( véase la sección detallada: “ Epidemiología ”) .
El parásito de la malaria se transmite principalmente por la noche cuando es picado por un mosquito hembra del género Anopheles , infectado él mismo después de haber picado a un individuo que padece malaria. El parásito infecta las células del hígado de la víctima y luego circula en la sangre , colonizando los eritrocitos (glóbulos rojos o glóbulos rojos) y destruyéndolos. Muchas especies animales homeotérmicas son parasitadas por Plasmodiidae , que están subordinados a ellas; los humanos no pueden ser parasitados por Plasmodiums animales, con la excepción de Plasmodium knowlesi , un parásito primario de la malaria que se encuentra comúnmente en el sudeste asiático. Causa malaria en los macacos de cola larga, pero también puede infectar a los humanos, ya sea de forma natural o artificial. Plasmodium knowlesi es el sexto parásito principal de la malaria humana. De las 133 especies del género Plasmodium enumeradas, solo cuatro son específicamente humanas: Plasmodium falciparum responsable de una gran mayoría de muertes y otras tres que causan formas "benignas" de malaria que generalmente no son fatales Plasmodium vivax , Plasmodium ovale y Plasmodium malariae . Plasmodium knowlesi, que hasta hace poco se creía que era específico de especies de simios, ahora se cuenta entre los Plasmodiums que también afectan a los humanos, también generalmente benignos ( ver sección detallada: " Causas ").
La causa de la enfermedad se descubrió en 6 de noviembre de 1880en el hospital militar de Constantine ( Argelia ) por un médico del ejército francés, Alphonse Laveran , que recibió el Premio Nobel de Fisiología o Medicina en 1907 . C'est en 1897 que le médecin anglais Ronald Ross (prix Nobel en 1902 ) prouva que les moustiques anophèles étaient les vecteurs de la malaria (jusqu'à cette date, le « mauvais air » émanant des marécages était tenu responsable de la propagation de la enfermedad).
Etimología
El término malaria proviene del latín palus , " pantano ".
La palabra malaria deriva del italiano mal'aria , "mal aire". Este término se usa ampliamente en todo el mundo, especialmente por hablantes de inglés e italiano .
Historia
Desde los orígenes de la humanidad
Los parásitos similares a los de la malaria se encuentran en los chimpancés , el género más cercano a los humanos . Los chimpancés albergan un parásito de la malaria, Plasmodium reichenowi , un pariente cercano de Plasmodium falciparum ; mientras tanto, los gorilas albergan el Plasmodium falciparum, que puede ser la causa del parásito humano (la secuenciación del ADN de Plasmodium falciparum en las heces de un gorila infectado muestra mediante análisis filogenéticos que este parásito primatófilo es el antepasado de la cepa que se encuentra en los humanos).
La malaria ha afectado a los humanos desde el Pleistoceno , hace más de 50.000 años, y ha sido un patógeno desde el comienzo de la historia de nuestra especie. Esto representa varios miles de generaciones de seres humanos, y la malaria se considera una de las enfermedades más mortales de la historia de la humanidad.
Una controvertida especulación estima que la mitad de todos los humanos que han existido han muerto de malaria: se cree que 54 mil millones de humanos murieron de un total de 108 mil millones que han existido o aún existen.
Los parásitos humanos y sus vectores (mosquitos) evolucionaron conjuntamente con grupos humanos que se dispersaban por África y Eurasia. La transmisión de la malaria ha dependido de especies de mosquitos antropofílicos (preferiblemente que pican al ser humano), cuya extensión siempre ha estado limitada por las condiciones ambientales (latitud, altitud, etc.).
Una de las consecuencias de la edad de esta asociación coevolutiva es la existencia biológica, en las poblaciones modernas, de un polimorfismo genético en la sangre. La diversidad de las condiciones de la población ha llevado a una selección natural de genes para la anemia de células falciformes , talasemia , deficiencia de glucosa-6-fosfato deshidrogenasa , eliptocitosis hereditaria (llamada en algunos casos ovalocitosis ). Estas enfermedades, que afectan a los glóbulos rojos, ofrecen una ventaja selectiva contra la malaria ( consulte la sección detallada: " Factores genéticos ").
Hace unos 10.000 años, la propagación de la malaria se vio favorecida por el cambio climático, el inicio de la agricultura ( revolución neolítica ), por lo tanto a la sedentarización con crecimiento demográfico.
Antigüedad y edad media
Las fiebres periódicas , que recuerdan a la malaria, se han informado desde la Antigüedad en textos chinos, indios, asirios y griegos. Las descripciones más detalladas son las de Hipócrates y los autores del Imperio Romano . La teoría medieval de una enfermedad asociada con la miasma de pantanos permanecen en vigor hasta el XIX ° siglo.
En enero 2010, un equipo de científicos egipcios y estadounidenses demostró, mediante análisis de ADN , que Tutankamón tenía malaria en el momento de su muerte (vers.1327 a. C. J.-C.). En la India , desde la antigüedad, los Vedas ("Textos del conocimiento") mencionan las fiebres de la malaria; médico Charaka y Sushruta (probablemente V º siglo aC. ) lo convierten en una descripción y asociarlo ya la picadura del mosquito. Hipócrates describió los síntomas de la fiebre intermitente ; vincula estas fiebres a determinadas condiciones climáticas y ambientales, y las divide en tres tipos: febris tertiana (cada tres días), quartana (cada cuatro días) y dailyiana ou continua (ahora llamada tropica ). Hacia186 a . C. J.-C.Aparece, en ciertas regiones de China , el uso, en té de hierbas , de qing hao su (青蒿素) más tarde llamado artemisinina en Occidente y extraído de una planta medicinal utilizada como antipirético llamada qing hao (青蒿) ( Artemisia annua o " Artemisa anual "). Incluso más antiguas en uso, las raíces de chángshān (常山) ( Dichroa febrifuga ) también tienen indudables efectos medicinales. Así, encontramos referencias a períodos de fiebre malaria en China y síntomas de esta enfermedad en el Huangdi Neijing ( "Canon de la medicina") data de alrededor de la I er siglo antes de Cristo.
La malaria era común en partes del mundo donde ahora ha desaparecido, como la gran mayoría de Europa (la enfermedad de origen africano se había extendido en particular en el Imperio Romano ) y América del Norte.
Edad clásica
En algunas partes de Inglaterra , la mortalidad por paludismo era comparable a la del África subsahariana actual. Aunque William Shakespeare nació al comienzo de un período más frío llamado la " Pequeña Edad del Hielo ", sabía lo suficiente sobre los estragos de esta enfermedad como para citarlos en ocho de sus obras. Plasmodium vivax abundaba hasta 1958 en los pólders de Bélgica y los Países Bajos .
A principios del XVI ° siglo, son los colonos europeos y sus esclavos que probablemente trajeron la malaria en las Américas (sabemos que Colón estaba sufriendo de la enfermedad antes de su llegada a la nueva tierra). Los misioneros españoles jesuitas vieron que los indios que bordean el lago Loxa en Perú usaban la corteza en polvo Cinchona para curar las fiebres. Sin embargo, no hay ninguna referencia a la malaria en la literatura médica de los mayas o los aztecas . El uso de la corteza del "árbol de la fiebre" fue introducido en la medicina europea por los misioneros jesuitas, entre ellos Barbabe de Cobo, quien experimentó con él en 1632 y también lo exportó; de modo que el polvo precioso también se llamó "polvo jesuita". Un estudio en 2012 sobre marcadores genéticos de miles de muestras de Plasmodium falciparum confirma el origen africano del parásito en América del Sur (los propios europeos se vieron afectados por esta enfermedad a través de África): se tomó prestado entre mediados del siglo XVI E y mediados de del siglo XIX E las dos rutas principales de la trata de esclavos , la primera conducía al norte del continente sudamericano ( Colombia ) por los españoles, la segunda conducía más al sur ( Brasil ) por los portugueses.
XVIII XX y XIX XX siglos: primeros estudios científicos
En 1717 , la post mortem de grafito pigmentación del bazo y el cerebro fue publicada por Giovanni Maria Lancisi , el médico del papa Clemente XI , en una obra, publicada en 1717, sobre la malaria De noxiis paludum effluviis eorumque Remediis . Presenta evidencia de que la enfermedad es transmitida por moscas . Lancisi introduce la palabra mal'aria , "mal aire".
En 1820 , Pierre Joseph Pelletier y Joseph Bienaimé Caventou separaron los alcaloides cinconina y quinina de la corteza en polvo del "árbol de la fiebre", lo que permitió la creación de dosis estandarizadas de los componentes activos.
Hacia 1832 , François Clément Maillot perfeccionó el tratamiento curativo y profiláctico de la quinina. Sin embargo, no fue hasta 1881 que su contribución fue reconocida oficialmente en el congreso sobre malaria celebrado en Argel.
En 1848 , Johann Friedrich Meckel (apodado Meckel el Joven) notó una gran cantidad de gránulos de color marrón oscuro en la sangre y el bazo de un paciente que acababa de morir en un hospital psiquiátrico. Probablemente Meckel estaba viendo parásitos de la malaria sin darse cuenta, ya que no mencionó la malaria en su informe, pensando que el pigmento era melanina .
En 1878 , la D r Patrick Manson emite la primera suposición de que la malaria es transmitida por los mosquitos del género Culex , que absorbe el parásito y pone en el agua que los come humanos.
En 1879 , el alemán Edwin Klebs y el italiano Ettore Marchiafava anunciaron que habían encontrado al agente responsable de la malaria Bacillus malariae , hipótesis que los descubrimientos de Laveran nos hicieron olvidar.
En 1880 , Charles Louis Alphonse Laveran estableció, en Argelia , la relación entre las observaciones realizadas por Meckel el joven y el parásito que observó por primera vez en los glóbulos rojos de 44 personas que padecían malaria. Al ver ocurrir la exflagelación , se convence de que los flagelos móviles son microorganismos parásitos (pequeños seres vivos unicelulares que se multiplican vegetativamente a través de la mitosis ). Sin embargo, muchos médicos de la época todavía creían que los protozoos eran, de hecho, solo glóbulos rojos alterados. Laveran tendrá que luchar para que su teoría sea aceptada porque queda por ver cómo estos organismos ingresan al cuerpo humano. Al no haber obtenido un puesto que le permitiera continuar su investigación, Laveran se jubiló y continuó su investigación sobre protozoos en el Institut Pasteur como voluntario. Fue en 1898 cuando publicó su Tratado sobre la malaria . También ve el efecto de la quinina, que destruye estos parásitos. Sugiere que la malaria es causada por este protozoo . Esta es la primera vez que se identifica a un protozoo como la causa de una enfermedad. Este descubrimiento le valió el Premio Nobel de Medicina en 1907 . Los estudios científicos sobre la malaria acaban de realizar su primer avance significativo.
En 1880 , Ettore Marchiafava y Angelo Celli , a pedido de Alphonse Laveran, estudian bajo un microscopio el ciclo reproductivo de los protozoos en la sangre humana, y observan que se dividen más o menos simultáneamente a intervalos regulares y que la división coincide con los ataques de fiebre. En 1885 , llamaron a este protozoo Plasmodium .
En 1881 , Carlos Finlay , médico cubano que trató a pacientes con fiebre amarilla en La Habana , afirmó que eran los mosquitos los que transmitían la enfermedad a los humanos.
En 1886 y 1892 , Camillo Golgi publicó sus hallazgos sobre la frecuencia y periodicidad de las fiebres debidas a la malaria, y mostró que existen varios tipos de malaria causados por diferentes organismos protozoarios.
En 1891 , Paul Ehrlich y Paul Guttman notaron las propiedades antipalúdicas del azul de metileno . Este descubrimiento sigue al de Celli y Guarnieri, que a su vez se basó en trabajos anteriores de Ehrlich que muestran la afinidad de esta sustancia por ciertas células. Ehrlich quiere promover el desarrollo de fármacos aprovechando las diferencias bioquímicas. Era la primera vez que una sustancia sintética era activa contra la malaria (ya en 1849, August von Hofmann ya había subrayado el interés de la síntesis de quinina a partir de alquitrán de hulla ).
En 1895 , la expedición francesa a Madagascar fue un "desastre sanitario": de las 21.600 personas que desembarcaron, 5.731 murieron de malaria y 25 murieron en combate. Tenga en cuenta que este tipo de "desastre" a menudo volverá a ocurrir, como durante la Guerra de Vietnam para los soldados norvietnamitas (ver artículo sobre artemisinina ).
En 1898 , Amico Bignami logró transmitir experimentalmente la malaria a través de mosquitos. No duda en ser mordido y contraer la enfermedad.
En 1898 , fue el británico Ronald Ross , que trabajaba en la India y mantenía correspondencia regular con Laveran y Manson pero que tenía dificultades para imaginar por qué el insecto no transmitía directamente el parásito por picadura, quien finalmente demostró que la malaria se transmitía por esta picadura. Para confirmar su teoría, disecciona, durante dos años, las aves de la malaria que pica por cientos de variedades de mosquitos y es solo después de estos dos años, al borde del desánimo, que nota una especie de mosquito que solo se desarrolla en la superficie. agua y sólo se ve de noche: los anofeles . Luego continúa su investigación; recolecta y cría las larvas y encuentra protozoos de Laveran alrededor del séptimo día en el estómago de los anofeles. La prueba está establecida: es este insecto el que transmite el parásito vivo a su costa. Señala que es necesario un período de incubación de 10 a 14 días entre la picadura y la aparición de los parásitos en la sangre. Acababa de demostrar que ciertas especies de mosquitos transmiten la malaria a las aves, al aislar los parásitos de las glándulas salivales de los mosquitos que se alimentan de las aves afectadas. Esto le valió el Premio Nobel de Medicina en 1902 . Después de renunciar a los servicios médicos indios, Ross trabajó para la entonces recién establecida Escuela de Medicina Tropical de Liverpool , liderando los esfuerzos de erradicación de la malaria en Egipto , Panamá , Grecia y Mauricio . Hasta la década de 1930 , los investigadores hablaban de Anopheles maculipennis en general sin hacer una distinción clara o detallada entre las diferentes variedades.
En 1899 , el zoólogo italiano Giovanni Battista Grassi , basado en el trabajo de Ross (sobre aves), hizo lo mismo con el vector en humanos y demostró que el ciclo de vida del Plasmodium necesita del mosquito como paso necesario. Grassi, Giuseppe Bastianelli y Amico Bignami describen el ciclo de desarrollo de Plasmodium falciparum , Plasmodium vivax y Plasmodium malariae en Anopheles claviger .
Al año siguiente, los hallazgos de Finlay y Ross fueron confirmados por un equipo médico dirigido por Walter Reed ; y las recomendaciones fueron puestas en práctica por William C. Gorgas durante la construcción del Canal de Panamá . Las medidas de salud pública así adoptadas salvaron la vida de miles de trabajadores (ya que muchos miles más habían muerto allí anteriormente) y ayudaron a desarrollar métodos futuros para combatir la enfermedad.
XX XX siglo: en busca del tratamiento
Si bien el conocimiento sobre la enfermedad está aumentando, en particular debido a la práctica de la malaria-terapia, un tratamiento ahora obsoleto, el desarrollo de medicamentos antipalúdicos y el uso de insecticidas para combatir el vector de los parásitos marcan este período. Estos descubrimientos motivaron a la OMS a lanzar el Programa Mundial de Erradicación del Paludismo en 1955. Si bien este programa aún no había logrado su objetivo, y si bien se descubrió una forma latente de parasitosis, la investigación avanza hacia el desarrollo de una vacuna.
DescubrimientosA principios del XX ° siglo, antes de los antibióticos , los pacientes con sífilis fueron intencionalmente "tratado" por infectarlas con la malaria, para darles la fiebre. El tratamiento terapéutico con malaria o malariatherapy es también una oportunidad para aumentar considerablemente el conocimiento acerca de la malaria; allanó el camino para la investigación en quimioterapia y se mantuvo en práctica hasta alrededor de 1950 .
En 1922 , John William Watson Stephens (en) , identifica la 4 ª conocido parásito de la malaria en los seres humanos, P. ovale .
Ya en la década de 1930, los investigadores habían notado la menor sensibilidad de las poblaciones negras a la malaria. En 1949 , Émile Brumpt se sorprendió al no encontrar ningún caso de malaria en Liberia, Gabón, Lagos o Stanleyville cuando había vectores de P. vivax .
En 1949 , JBS Haldane sugirió que los talasémicos heterocigotos serían más resistentes a la malaria. En noviembre, Linus Pauling , Harvey Itano , SJ Singer e Ibert Wells publicaron la primera evidencia de enfermedad humana causada por una proteína anormal en la revista Science . Usando electroforesis , demuestran que los individuos con anemia de células falciformes tienen hemoglobina alterada y que los heterocigotos, que tienen formas de hemoglobina tanto normales como anormales, son más resistentes a las infecciones por malaria. Así también se demuestra que las leyes de Mendel determinan las propiedades físicas de las proteínas, y no solo su ausencia o presencia: este es el comienzo de la genética molecular .
Antipalúdicos (antipalúdicos)A pesar de sus cualidades excepcionales, la quinina, un producto importado de países lejanos, disponible en cantidades limitadas, tenía la desventaja de provocar en ocasiones efectos secundarios; además, su administración tenía que ser diaria: tantos incentivos para adoptar y buscar sustitutos, que William Henry Perkin había intentado hacer en vano ya en 1856 . La Primera Guerra Mundial, que separó a Alemania de India y Java, los principales proveedores mundiales de quinina, llevó a los alemanes a buscar sustitutos basados en la observación de Ehrlich de la acción del azul de metileno .
Así se descubrieron sucesivamente plasmoquina (1926), quinacrina / Sontochin (1930), rodoquina (1931) y certuna (1935). Para ello, la investigación alemana se basó en un modelo animal desarrollado en 1926 por Roehl.
En 1926, investigadores alemanes descubrieron las propiedades antipalúdicas de pamaquin / plasmoquine / paraquine. Sin embargo, la estructura de este primer fármaco antipalúdico derivado de las aminoquinoleínas no se reveló hasta 1928 . Investigadores británicos, franceses y rusos ya han notado la acción antipalúdica de moléculas de la serie 8-aminoquinolina. Empiezan a buscar otros compuestos activos. En 1930 , Ernest Fourneau y su equipo se están desarrollando en el Instituto Pasteur de rodoquina , eficaz en dosis mucho más bajas que la plasmoquina.
En Argelia, los hermanos Edmond y Etienne Sergent lo largo de la primera mitad del XX ° siglo establecieron a petición de Emile Roux doctrina sentar las bases de la lucha contra la malaria en África del Norte. Este trabajo dará como resultado una disminución gradual de la malaria en Argelia y se salvarán muchas vidas.
En el período de entreguerras hay dos modelos animales que apoyan la búsqueda de antimaláricos sintéticos; uno basado en el paludismo de los simios, que no es práctico a gran escala, el otro más comúnmente utilizado, el paludismo aviar, que utiliza principalmente paludismo canario por diferentes tipos de plasmodium.
En la misma década de 1930, en los laboratorios Elberfield de IG Farben en Alemania , Hans Andersag y sus colegas sintetizaron y probaron aproximadamente 12,000 componentes diferentes y lograron producir resoquina , un sustituto de la quinina . Está relacionado con la quinina porque tiene un núcleo de quinolina . Esta resoquina (RESOrcinato de una 4-aminoCHINolina: 7-cloro-4 - [[4- (dietilamino) -1-metilbutil] amino] quinolina) y un componente similar, la estonquina (3-metilresoquina) se sintetizaron en 1934 en cooperación con Empresas estadounidenses, a través de más de 2000 acuerdos entre IG Farben y empresas extranjeras, como Standard Oil de Nueva Jersey , DuPont , Alcoa , Dow Chemical , Agfa , Winthrop Chemical Company y otras empresas estadounidenses. Este fármaco se denomina posteriormente cloroquina . Es un inhibidor de la biocristalización de pigmentos y uno de los mejores antimicrobianos jamás creados. La quinina, como la cloroquina, afecta a los parásitos de la malaria al comienzo de su ciclo de vida, cuando los parásitos forman pigmentos de hematina , derivados de la degradación de la hemoglobina .
El proguanil fue descubierto en 1944 por Curd, Davey y Rose, investigadores británicos de Imperial Chemical Industries . La pirimetamina finalmente es desarrollada entre 1950 y 1952 por el laboratorio Burroughs-Wellcome. Asociado con la sulfadoxina en la década de 1970, formó Fansidar.
En las décadas de 1950 y 1960, los antimaláricos sintéticos, cuyo costo de fabricación era muy bajo, tendían a reemplazar la quinina extraída, que era más cara.
Durante la guerra de Vietnam , en respuesta a una solicitud expresa del “ Việt Cộng ”, se llevó a cabo un estudio sistemático de más de 200 plantas medicinales chinas bajo la dirección de la farmacóloga Tu Youyou y su grupo de investigación en Beijing en 1972 . Qing hao su (青蒿素), llamado artemisinina en Occidente, se extrae a baja temperatura en un medio neutro (pH 7) de plantas de qing hao (青蒿) secas, de acuerdo con las instrucciones de Ge Hong . Éste fue el primero, en el IV ° siglo para recomendar el uso de Qing Hao para el tratamiento de " fiebres intermitentes " en sus necesidades Manual para emergencias médicas . Recomienda remojar las hojas y ramas de artemisa durante la noche, exprimir el jugo amargo y beberlo solo. Actualmente, los derivados se utilizan en combinaciones: arteméter en combinación con lumefantrina , artesunato - amodiaquina , dihidroartemesinina - piperaquina.
Los primeros cultivos in vitro del parásito en su fase sanguínea fueron realizados en 1976 por Trager y Jensen, lo que facilitó considerablemente el desarrollo de nuevos fármacos.
DDTLas propiedades insecticidas del DDT (dicloro difenil tricloroetano) fueron establecidas en 1939 por Paul Hermann Müller, que trabajaba en Geigy Pharmaceutical en Basilea , Suiza, utilizando piretro hecho de piretro dálmata triturado (planta de la familia de los crisantemos ). La difusión de DDT es un método estándar de protección contra insectos. Sin embargo, debido al impacto ambiental del DDT y la resistencia desarrollada por los mosquitos, el DDT se usa cada vez menos, especialmente en áreas donde la malaria no es endémica ( ver sección detallada: " Los medios para combatir o protegerse contra los mosquitos "). Este ha sido el caso en particular desde 1972, cuando Estados Unidos, a través de la AID y el Banco Mundial , amenazó con prohibir las importaciones y recortar los fondos a los países que utilizan DDT.
En 1948, Paul Müller recibió el Premio Nobel de Medicina.
Paludismo en simios y humanosEn la década de 1920, investigadores estadounidenses inyectaron sangre de monos de diferentes especies en humanos para determinar la posibilidad de transmisión de la malaria de monos a humanos.
En 1932-33, Sinton y Mulligan demostraron la presencia de Plasmodium gonderi en Cercopithecidae . Hasta la década de 1960, la infección natural en los monos se había observado sólo excepcionalmente en la India, aunque ya se habían utilizado en grandes cantidades con fines de investigación.
Sin embargo, ya se sabía desde 1932 que P. knowlesi podía transmitirse a los humanos a través de sangre de simio infectada. La cuestión de la transmisibilidad del paludismo de los simios a los humanos, considerada en particular en el contexto de un programa de erradicación, recuperó el interés en 1960 cuando la posibilidad de transmisión (a través de un mosquito) de la malaria de un mono a un humano. En 1969, la cepa Chesson de Plasmodium vivax se adaptó por primera vez a un primate no humano.
Desde 2004, se ha descubierto que P. knowlesi, responsable de la malaria en los simios, es responsable de infecciones humanas que se recomienda tratar como P. falciparum .
Parasitosis latenteAunque diferentes etapas de la sangre y el vector de la malaria (el Anopheles ) se han identificado a partir de la XIX XX siglo, fue sólo en 1980 que la forma latente (ciclos secundarios exo-eritrocitos que va a mantener en el parasitosis hígado durante 3 a 5 años o más para P. vivax , 2 o 3 para P. ovale y de por vida para P. malariae ) del parásito en el hígado . Finalmente, el descubrimiento de esta forma latente del parásito explica por qué los individuos parecen curados de la malaria pero recaen varios años después de que el parásito ha desaparecido de su sangre ( ver sección detallada: “ Fase hepática ”).
Desarrollos y perspectivas contemporáneas
Farmacología- En 2004 , el equipo de D r Jonathan Vennerstrom de la Universidad de Nebraska de Omaha logró sintetizar ácido artemisínico se puede convertir en la artemisinina más eficaz ( in vitro ) como la producida de forma natural. Esta molécula (Arterolane, OZ-277 o RBx11160) se utilizó en combinación con piperaquina en el fármaco Synriam.
- En marzo de 2006 , dos equipos internacionales demostraron la eficacia de varias plantas, incluida Quassia .
- En la misma fecha, investigadores de la Universidad de Lille I desarrollaron una molécula, ferroquina , injertando un ferroceno en una ubicación específica de la molécula de cloroquina . Se dice que la ferroquina es hasta 30 veces más eficaz que la cloroquina. La monoterapia a base de ferroquina y su combinación con artenusato se han probado en 326 sujetos, en su mayoría niños pequeños en áreas palúdicas de África Central. Se han probado 3 dosis de la combinación, que dan lugar a curas en el 97 al 99% de los casos. La monoterapia tuvo una tasa de éxito del 79%, que está en el mismo orden de eficacia que otras monoterapias preexistentes.
- En septiembre de 2006, un equipo francés aísla el principio antipalúdico ( simalikalactona D ) de la infusión de Quassia Amara utilizada en Guyana contra la malaria.
- En 2008 , biólogos del Instituto de Tecnología de Georgia en Atlanta revelaron que ciertos compuestos fungicidas naturales del alga roja Callophycus Serratus inhibían la acción de Plasmodium ; aunque todavía no se comprende el vínculo entre la actividad antifúngica , antibacteriana y antipalúdica.
- En 2009 (publicación febrero 2010), los investigadores del Instituto de Tecnología de Georgia en Atlanta identifican compuestos antiinfecciosos conocidos como “ bromoficólidos ” que son muy eficaces in vitro contra las micosis y contra el plasmodium falciparum .
- En enero 2010, GlaxoSmithKline anuncia que pondrá a disposición de la comunidad científica una lista de más de 13.500 moléculas, y sus estructuras químicas, potencialmente activas contra P. falciparum, con el fin de estimular el desarrollo de nuevos tratamientos contra la enfermedad.
- En 2010, investigadores de la Escuela de Salud Pública Johns Hopkins Bloomberg de la Johns Hopkins Universidad , Baltimore descubrieron que una bacteria perteneciente a la Enterobacter género y que viven en las flora intestinal de Anopheles gambiae muertes por Plasmodium falciparum por medio de radicales libres. . Aproximadamente el 25% de los Anopheles capturados cerca del Instituto de Investigación del Paludismo Johns Hopkins en Macha (sur de Zambia ) contenían esta cepa bacteriana. El estudio demostró que la bacteria inhibió el crecimiento de P. falciparum en cultivos humanos in vitro hasta en un 99%, tal como lo hace en el sistema digestivo de Anopheles.
- En 2010 y 2011, se descubrieron dos nuevas clases de medicamentos antipalúdicos que se encuentran en ensayos clínicos: espiroindolonas e imidazolpiperazinas.
- En septiembre de 2012, la síntesis de artemisinina fue exitosa, lo que permitió que la producción de tratamientos ya no estuviera limitada por la de artemisa.
El Premio Nobel de Medicina 2015 fue otorgado al irlandés William Campbell , al japonés Satoshi Ōmura y a la china Tu Youyou por su trabajo en el tratamiento de enfermedades parasitarias, incluida la malaria.
VacunasLa primera vacuna antipalúdica, SPf66, basada en un péptido sintético, fue desarrollada en enero de 1986 por Manuel Elkin Patarroyo . Sin embargo, su eficacia fue bastante baja o incluso nula contra P. falciparum .
Actualmente, tres tipos de investigación de segunda generación se basan en antígenos de diferentes etapas del ciclo evolutivo parasitario:
- vacunas en etapa anti-eritrocítica: tienen como objetivo evitar que el esporozoito entre o se desarrolle en las células del hígado ;
- Vacunas contra la etapa sanguínea asexual (antimerozoítos): estas evitan que los merozoitos entren o se desarrollen en los glóbulos rojos ;
- vacunas que bloquean la transmisión: inducen anticuerpos que impiden la maduración de las etapas sexuales del parásito en Anopheles.
Desde 1992 , una vacuna antimerozoíto llamada RTS, S ha estado en desarrollo en GlaxoSmithKline Biologicals en Rixensart , Bélgica . En diciembre de 2005 , el Dr. Pedro L. Alonso de la Universidad de Barcelona publicó resultados alentadores ya que la vacuna ha demostrado ser efectiva desde el 1 st inyección en el 30% de los casos y ahorrar la mitad de las crisis. Desde26 de mayo de 2009en 2013, se sometió a ensayos clínicos de fase III que mostraron superioridad de RTS, S / AS01 sobre otros adyuvantes. Se prepara a partir parasitarias sintéticos péptidos y recombinantes proteínas (capaz de intercambiar información genética con otra proteína) o ADN (que se encuentra en las mitocondrias y los apico plástidos de Plasmodium ). Sabiendo que el parásito, para penetrar en los glóbulos rojos , toma la forma de una proteína y es capaz de mutar unas sesenta veces para engañar al sistema inmunológico, esta vía utiliza dos proteínas recombinantes que fusiona:
- parte de la proteína circumsporozoite (CSP = Circum Sporozoite Protein ) de P. falciparum (RTS);
- el antígeno de la superficie del virus de la hepatitis B (S);
- un adyuvante (AS01 o AS02 respectivamente) que se compone de 250 µl de emulsión de aceite en agua, 50 µg de saponina QS21 y 50 µg de inmunoestimulante monofosforico lípido A.
RTS, S / AS01 recibió una opinión favorable de la EMA en julio de 2015 y se comercializa con el nombre Mosquirix. También protege contra la hepatitis B . Está previsto un piloto de la OMS para principios de 2018 con Ghana , Kenia y Malawi .
Otros investigadores apuntan a una solución de vacuna:
- Desde 2002 , la Facultad de Biología y Medicina (FBM) de la Universidad de Lausana en Suiza ha estado estudiando una vacuna antimerozoíto llamada PfCS102 / AS02A basada en un péptido sintético circumsporozoíto (PfCS = Peptide Circum Sporozoïte Protein ) de P. falciparum (PfCS102) reforzado con un adyuvante. Inicialmente, este adyuvante fue Montanide ISA 720 ya que fue reemplazado por AS02A de GSK Bio porque da una mejor respuesta del sistema inmunológico . Los resultados obtenidos son comparables a RTS, S / AS02A. Desde 2005 , ha estado en ensayos clínicos de fase II .
- En noviembre de 2005 , el Institut Pasteur anunció el inicio de los ensayos clínicos de fase I en humanos de un prototipo de vacuna antimerozoíto basada en antígenos y denominada MSP3. Para diseñarlo, los investigadores estudiaron los mecanismos de las personas naturalmente inmunes.
- En 2006 , el Departamento de Defensa de los Estados Unidos (DoD) solicitó al Instituto de Medicina (IOM) de la Academia Nacional de Ciencias (NAS) que reanudara el programa de investigación que inició en 1986 con el objetivo de desarrollar una vacuna contra P. falciparum para los militares. .
- Desde noviembre de 2006 hasta diciembre de 2007, la Facultad de Medicina de la Universidad de Maryland y la Universidad de Bamako probaron conjuntamente en ensayos clínicos de fase I una vacuna FMP2.1 / AS02A. Su principio activo es una proteína derivada de P. falciparum (FMP2.1) que está reforzada por el adyuvante AS02A. Una prueba realizada en Bandiagara ( Malí) en 100 niños de 1 a 6 años mostró que la habituación farmacodinámica al principio activo era segura y que la respuesta inmunitaria un año después de la vacunación seguía siendo alta. Sobre esta base, el mismo equipo pasó a los ensayos clínicos de fase II de mayo de 2007 a julio de 2009 en 400 niños.
- En enero de 2010 , la Universidad de Florida Central en Orlando anunció una vacuna candidata oral o inyectable que es efectiva contra la malaria y el cólera . Se dirige a la inmunidad sistémica y de las mucosas , a través de una construcción antigénica que fusiona los epítopos de la subunidad B de la toxina del cólera (CTB) con los antígenos de la membrana apical (AMA1) y la proteína de superficie (MSP1) de los merozoitos de P. falciparum . Los cloroplastos de tabaco transplastómico y lechuga se probaron como un reactor para producir estas proteínas. Según el estudio, estos últimos, extraídos e inyectados en ratones, lograron protegerlos durante 300 días contra la penetración del parásito en los glóbulos rojos y contra la toxina del cólera. La respuesta inmune sería del tipo Tr1 / Th2. Este proceso ha sido patentado y podría hacer posible, si resulta ser tan efectivo en humanos, producir una vacuna que sea económica y no requiera almacenamiento refrigerado en caso de uso oral.
- En 2015, la vacuna “RTS, S” de GlaxoSmithKline dio resultados prometedores pero decepcionó durante las pruebas de fase III, con una reducción de solo el 40% de las infecciones y menos del 30% para la forma grave (aunque requirió cuatro inyecciones).
- En 2021, la vacuna R21 / Matrix-M diseñada en la Universidad de Oxford y probada en 2019 alcanza una eficacia récord del 77% en un año. La última fase de las pruebas de preaprobación involucra a 4.800 niños de cuatro países diferentes.
Más bien, los genetistas pretenden combatir el parásito, no en los humanos, sino en su vector, el mosquito.
En 2000 , el equipo del profesor Andrea Crisanti del Imperial College London logró crear el primer mosquito modificado genéticamente. En 2003 , reconoció que si el gen marcador persistía durante unas treinta generaciones durante la fertilización entre mosquitos modificados, solo sobrevivía de 4 a 16 generaciones durante la fertilización con un mosquito no modificado.
Desde abril de 2001 , un consorcio internacional es la secuenciación completa del genoma de Anopheles gambiae . Está patrocinado por Tropical Disease Research (TDR). Esta secuenciación fue encomendada a Genoscope en Évry y Celera Genomics en Alameda . El objetivo es identificar los genes implicados en la inmunidad del mosquito a los parásitos Plasmodium o en sus receptores olfativos y gustativos con, en última instancia, el diseño de atraer o repeler moléculas para el mosquito así como apuntar a las proteasas implicadas en su respuesta inmunitaria.
la 15 de julio de 2010El profesor de entomología Michael Riehle anuncia que ha logrado crear con su equipo de la Universidad de Arizona , una hembra genéticamente modificada de Anopheles Stephensi capaz de destruir los parásitos de su cuerpo y, por tanto, incapaz de transmitir la enfermedad. Los investigadores ahora están estudiando cómo reemplazar las poblaciones "normales" de Anopheles en la naturaleza por las producidas en el laboratorio, con la esperanza de que estos mosquitos no se conviertan en invasores transmitiendo otras enfermedades o que el parásito no eluda esta resistencia.
Epidemiología
Distribución en el mundo
Evolución del número estimado de muertes por malaria en el mundo.
En la década de 1990, la malaria fue la causa de 400 a 900 millones de casos de fiebre al año y entre 700.000 y 2,7 millones de muertes, o en promedio, una muerte cada 30 segundos. En 2012, entre 473.000 y 789.000 personas murieron de malaria. La gran mayoría de las víctimas son niños menores de 5 años, las mujeres embarazadas también son particularmente vulnerables porque la placenta es un objetivo donde se pueden acumular los parásitos ( Plasmodium falciparum ). A pesar de los esfuerzos realizados para reducir la transmisión de la enfermedad y mejorar su tratamiento, ha habido pocos cambios desde principios de la década de 1990. La mortalidad parece haber estado disminuyendo desde finales de la década de 2000 y se estima en 1,2 millones de personas en 2010.
La coinfección con el VIH no aumenta la mortalidad, y es un problema menor que la coinfección por malaria / tuberculosis , las dos enfermedades suelen atacar a diferentes grupos de edad: la malaria es más común en los niños, los jóvenes, mientras que la tuberculosis afecta más a los ancianos. Sin embargo, la malaria y el VIH contribuyen a su propagación mutua: la malaria aumenta la carga viral y la infección por VIH aumenta la probabilidad de infección por malaria.
La malaria es endémica en áreas intertropicales de las Américas, en muchas partes de Asia y en la mayor parte de África. Sin embargo, es en África subsahariana donde se encuentran entre el 85 y el 90% de las muertes por paludismo. La distribución geográfica de la enfermedad dentro de grandes áreas es compleja y, por lo tanto, las áreas con paludismo y sin paludismo se encuentran cerca unas de otras. En las zonas secas, los períodos de malaria se pueden predecir sin demasiados errores utilizando mapas de precipitación. A diferencia del dengue , la malaria está más presente en el campo que en las ciudades. Por ejemplo, las ciudades de Vietnam, Laos y Camboya están prácticamente libres de malaria, pero sigue presente en el campo. En 2016, según la Organización Mundial de la Salud , no se registró ningún caso de malaria en Sri Lanka durante tres años consecutivos; por tanto, es el segundo país del sudeste asiático, después de Maldivas, que ha erradicado la malaria. La china se convirtió en el30 de junio de 2021el cuadragésimo territorio habiendo erradicado esta enfermedad. En África, por otro lado, la malaria está presente tanto en áreas rurales como urbanas, aunque el riesgo se reduce en las grandes ciudades. Los niveles endémicos globales de la enfermedad no se han cartografiado desde la década de 1960. Sin embargo, el British Wellcome Trust está financiando el Proyecto Atlas de la Malaria para rectificar esto y evaluar la carga de esta enfermedad en el futuro.
Finalmente, la malaria es la enfermedad parasitaria más común en el mundo. Es la 1 st prioridad para la OMS como sus estragos directos de sus consecuencias socioeconómicas que incluyen: el bajo rendimiento que conduce a la malnutrición y el subdesarrollo.
Europa
Hasta el XIX ° siglo , las epidemias de malaria podrían ocurrir al norte de Europa. La disminución de la malaria en Europa se debe principalmente al secado de las marismas y al drenaje de los humedales . La desaparición de la malaria en Francia sorprendió a los investigadores hasta tal punto que podríamos hablar a este respecto de desaparición espontánea, incluso de desaparición misteriosa. Parece que esta desaparición tuvo múltiples causas. En regiones como Sologne, por ejemplo, diversas innovaciones agronómicas relacionadas en particular con las prácticas de cultivo han podido desempeñar un papel apreciable a este respecto, acumulando cada una su efecto. La enfermedad comenzó a retroceder, como en el resto de Europa, antes del uso de la quinina, que además se usó al principio de manera inapropiada, demasiado tarde o en dosis demasiado bajas. La adopción de la quinina, sin embargo, sirvió para acelerar la desaparición de la enfermedad en áreas donde estaba disminuyendo.
En GreciaEn 2016, el Centro Griego para el Control y la Prevención de Enfermedades prohibió la donación de sangre en 12 municipios de todo el país debido a la malaria, después de que se considerara que la infección había desaparecido durante 40 años.
En FranciaEn Francia continental , la malaria solo ha desaparecido hace relativamente poco tiempo. La enfermedad era todavía común en el XIX ° siglo. Todavía estaba presente en 1931 en las marismas de Poitevin , Brenne , la llanura de Alsacia , Flandes , Landes , en Sologne , Puisaye , en el Golfo de Morbihan , en la Camarga ... A lo largo de la Edad Media y hasta el XV ° - XVI º siglos, la malaria afecta principalmente a las campañas; esto incluso cuando un buen número de ciudades se establecieron a lo largo de los ríos para la comodidad del transporte, ya pesar de las crecidas periódicas de estos ríos en muchos lugares. El Renacimiento vio un recrudecimiento de las fiebres, las Guerras de Religión obligaron a la gente del pueblo a encerrarse en muros rodeados de acequias con agua estancada. También en París al final de la XIX ª siglo, durante las grandes obras de Haussmann : excavaciones importantes de hecho estas obras han causado y largo plazo. Los charcos, estanques y otros puntos de agua estancada persistieron durante mucho tiempo, provocando una proliferación de Anopheles en medio de una gran concentración de humanos. Además, un gran número de trabajadores procedían de regiones infectadas y portaban el plasmodio .
La epidemia de Pithiviers en 1802 , motivó por su gravedad el envío de una comisión de la Facultad de Medicina; se debió a una gran inundación, de inusual magnitud, que había cubierto de agua los prados circundantes durante varias semanas.
Esta enfermedad fue erradicada de Córcega en 1973 . Desconocido en el momento de la presencia romana , la malaria se introdujo allí durante las redadas de vandalismo . Córcega experimentó su última epidemia de casos no importados de Plasmodium vivax de 1970 a 1973 . En particular, en 2006 se produjo un caso autóctono de Plasmodium vivax en la isla. Desde entonces, casi todos los casos observados en Francia han sido malaria importada. Las tropas de las colonias fueron responsables de las últimas epidemias mencionadas.
Los factores críticos que afectan a la propagación o la erradicación de la enfermedad han sido los cambios en el comportamiento humano (métodos agrícolas por encima de todo, los desplazamientos de población, etc.), el nivel de vida ( la pobreza ha sido y sigue siendo la principal causa de mortalidad) y la población de la densidad (la a mayor densidad humana, mayor densidad de mosquitos).
El uso de la quinina y la quinina se convierte en corriente segunda mitad del XIX ° siglo. P. malariae , que es más susceptible, desapareció antes que P. vivax . Pero las dosis utilizadas son insuficientes para prevenir el desarrollo de hematozoides en humanos.
Otro factor determinante: los métodos de cría están cambiando. La vivienda permanente aumenta, lo que permite recuperar los abonos. En 1893 , alrededor de Estrasburgo , solo tres o cuatro municipios tenían todavía más del 12% de su superficie útil reservada para pastos. Las áreas de prados naturales (húmedos) están disminuyendo a favor de la tierra arada (recuperada), principalmente en áreas de agricultura rica. Aumenta el número de animales, lo que disminuye en la misma proporción los ataques de mosquitos a los humanos.
Entra en juego un tercer factor: la ordenación territorial , que tiene varios aspectos. En 1821 se aprobó una ley para el secado de estanques insalubres. Esta ley se ha seguido poco en general; sin embargo, se lanzó la idea, y los estanques más cercanos a las casas fueron los más numerosos para ser llenados (porque eran de más fácil acceso). Sin embargo, los mosquitos adultos no se mueven más de 300 m desde su punto de origen. Por lo tanto, esta desecación fue sin duda una causa importante de la regresión de la enfermedad.
Otro aspecto de la ordenación territorial es el aumento del número de acequias y su mejor mantenimiento, lo que permite un mejor drenaje del terreno.
En las Landas y Sologne, la reforestación también es un factor, los árboles drenan el agua de manera más eficiente que un dosel más pequeño.
El tipo de arado cambia: el doble brabante , que permite un arado plano, da surcos más bajos (por lo tanto, menos agua estancada en el hueco de los surcos en períodos húmedos) y también permite un arado más profundo (por lo tanto, mejor secar la tierra pesada), comenzó a extenderse. a partir de 1850 en Brie , sustituyendo el arado no reversible y sus derivados que daban arado en crestas . También se está extendiendo la práctica del encalado , que aligera los suelos pesados y, por tanto, facilita el secado. La amplitud de las mareas contribuye a la absorción de agua superficial.
Todas estas medidas agronómicas contribuyen en gran medida a reducir las epidemias de malaria y otras fiebres. En el momento de la Primera Guerra Mundial , solo quedaban unos pocos brotes muy localizados.
La malaria endémica desapareció por completo en Francia en 1960.
Cuarenta personas en Francia en veinte años se han infectado en los aeropuertos a causa de los mosquitos que han viajado en aviones desde zonas palúdicas.
En la Isla de la Reunión y la República de Mauricio , el paludismo fue la principal causa de muerte hace 60 años. La erradicación de la enfermedad fue confirmada por la Organización Mundial de la Salud en 1979.
Aumento de la malaria importadaLa malaria importada se observa principalmente en viajeros, migrantes y soldados de países endémicos. Es monitoreado por una red de alrededor de cien hospitales voluntarios en conexión con el Centro Nacional de Referencia (CNR) para la malaria.
Esta malaria es un reflejo de la situación mundial. Por su situación, Francia actúa como “centinela” de lo que está sucediendo en países endémicos, principalmente África subsahariana. Después de una mejora significativa en el período 1990-2010, la situación mundial se está estancando. Según la OMS, once países han registrado un aumento de casos desde 2015.
La Francia metropolitana es el país industrializado con el mayor número de casos de malaria importados, con cerca de 5.000 casos al año. En 2017 se declararon al CNR 2.721 casos de malaria, es decir, alrededor de 5.220 casos estimados según la representatividad de la red de vigilancia, un aumento del 10,3% respecto a 2016.
También en 2017, el 82,8% de los casos notificados fueron en sujetos de origen africano y el 95% en África subsahariana. De un total de 59 países de contaminación, 15 países representan el 92,4% de los casos notificados. Los tres primeros son Costa de Marfil (30%), Camerún (20%) y Guinea (más del 5%). Entre estos países africanos, algunos están disminuyendo o aumentando, dependiendo del número de viajeros o personal militar de áreas donde la malaria está disminuyendo o aumentando.
Se declararon un total de 13 defunciones (letalidad del 0,48% para todos los casos y del 3,4% para las formas graves). El incumplimiento de las recomendaciones de prevención (falta de protección contra mosquitos y quimioprofilaxis) es la causa de la mayoría de los casos. Es necesario un esfuerzo adicional de información con los sujetos originarios de África que visitan sus familiares cercanos en su país de origen.
El migrante, nuevo en un área endémica, rara vez presenta malaria debido a la inmunidad adquirida. Esta inmunidad desaparece en menos de 4 años en Francia. El migrante luego contrae la malaria al regresar al país durante el período de vacaciones en Francia, que generalmente corresponde en África Occidental a la temporada de lluvias, donde la transmisión es más intensa.
Regiones de alto riesgo
Después de haber asolado casi todo el mundo habitado, la malaria afecta a 90 países (99 países según el informe de la OMS de 2011), principalmente a los más pobres de África, Asia y América Latina. En la década de 1950, la malaria se había erradicado de la mayor parte de Europa y gran parte de América Central y del Sur mediante la pulverización de DDT y el drenaje de los pantanos.
La degradación forestal puede promoverlo; “Un estudio realizado en Perú en 2006 reveló que la tasa de picaduras de mosquitos portadores de malaria es 278 veces menor en los bosques intactos que en cualquier otro lugar. "
En 2006 , Europa experimentó un gran número de casos de malaria importados, principalmente en Francia (5.267 casos ), el Reino Unido (1.758 casos ) y Alemania (566 casos). En Francia, 558 casos son soldados, pero la enfermedad también afecta a los turistas: de cien mil de ellos que van a una zona palúdica, tres mil regresan a sus países infectados con una de las formas conocidas de Plasmodium , el resto son casos importados por inmigrantes.
- El África es un continente particularmente afectados por la malaria; se trata del 95% de los casos importados en Francia . El peligro es casi nulo en el norte de África, pero mayor en África oriental , África subsahariana y África ecuatorial, tanto en áreas rurales como urbanas.
- En Asia , la malaria está ausente en las grandes ciudades y es bastante rara en las llanuras costeras. El peligro es mayor en las zonas rurales de Camboya , Indonesia , Laos , Malasia , Filipinas , Tailandia , Birmania (Myanmar) , Vietnam y en China en Yunnan y Hainan .
- En las Indias Occidentales , la malaria está muy extendida en Haití y cerca de la frontera dominicana .
- En Centroamérica hay algunas microzonas, pero el riesgo es relativamente bajo.
- En América del Sur , el riesgo es bajo en las grandes ciudades, pero real en las áreas rurales de Bolivia , Colombia , Ecuador , Perú y Venezuela , y es mayor en toda la región amazónica .
La altitud y la temperatura ambiente son factores importantes para determinar si un área se vuelve palúdica o no.
- Algunos anofeles (como Anopheles gambiae ) apenas pueden vivir por encima de los 1000 metros de altitud, pero otros (como Anopheles funestus ) están perfectamente adaptados para vivir hasta los 2000 m .
- La maduración de Plasmodium dentro Anopheles no puede operar en un rango de temperatura ambiente a partir de 16 a 35 ° C .
OMS lucha contra la malaria
El programa de erradicación mundial de la OMS fue precedido por los proyectos iniciados y gestionados sucesivamente por la Junta Internacional de Salud, luego por la Fundación Rockefeller a partir de 1915 pero especialmente a partir de la década de 1920 . Estas dos organizaciones, emanaciones de la voluntad filantrópica de John D. Rockefeller ya tenían la experiencia de campañas de erradicación de la anquilostomiasis y la fiebre amarilla . Rompiendo con el consenso que aboga por la administración masiva de quinina asociada a medidas para controlar las poblaciones de mosquitos, en particular mediante trabajos de drenaje, los investigadores de la Fundación Rockefeller basaron su estrategia en 1924 en la erradicación exclusiva de los mosquitos. Para ello, cuentan con el Verde de París , una sustancia muy tóxica, sin embargo ineficaz sobre los mosquitos adultos. Italia fue el primer teatro de operaciones desde finales de la década de 1920, seguido de todos los demás lugares de intervención de la Fundación en la región mediterránea y los Balcanes . A pesar de resultados dispares, este curso de acción fue adoptado en la India de 1936 a 1942. Allí, junto con otras, estas medidas produjeron resultados espectaculares pero temporales: en 1941 la situación era similar a la que prevalecía antes del inicio de este programa. La Segunda Guerra Mundial, que suspendió ciertos programas, también les dio expansión: la Comisión de Salud de la Fundación fue creada en 1942 para apoyar los esfuerzos de las fuerzas armadas preocupadas por proteger a sus soldados en las líneas del frente. El desarrollo del DDT , en el que participaron los equipos de la Fundación, y la dispersión de este insecticida desde aviones en la zona inundada al oeste de Roma permitió el lanzamiento de campañas de erradicación de la malaria en Italia a partir del año 1946 . El más famoso de estos programas tuvo lugar en Cerdeña de 1946 a 1951. Basado en el uso masivo de DDT, este programa con métodos y consecuencias ambientales discutibles y debatidos, resultó en la erradicación de los mosquitos y, en consecuencia, de la enfermedad, que sin embargo ya estaba En el declive.
En 1952 , la Fundación Rockefeller puso fin a su programa de salud pública y, por tanto, de lucha contra la malaria, pero después de que la OMS hubiera creado (en 1948 ) un programa destinado a la erradicación del microbio en 1955 en el mundo fuera del África subsahariana y Madagascar. Estados Unidos, al querer protegerse contra la importación de malaria a través de América del Sur, fue un actor importante; consideraciones políticas - la lucha contra el comunismo - también motivaron su compromiso. Tras notables éxitos (España fue el primer país declarado oficialmente libre de paludismo por la OMS en 1964), el programa se enfrentó rápidamente a dificultades; 1969 XXII ª Asamblea Mundial ratifica sus fracasos, pero mantiene sus objetivos globales de erradicación. En 1972, un grupo de países decidió en Brazzaville abandonar el objetivo de erradicación en favor de un objetivo de control. La 31 ª Asamblea Mundial de la Salud está de acuerdo con este cambio en 1978: es no más que apuntar a nivel mundial para la eliminación y la erradicación de la malaria, pero su control. En 1992, la Conferencia Ministerial de Amsterdam adoptó la Estrategia mundial revisada para el control del paludismo. Revisada por otros organismos internacionales, esta estrategia fue definida en 2001 por la OMS.
La OMS abandonó los procedimientos de certificación de erradicación en el decenio de 1980 y los reanudó en 2004.
En 1998, una asociación de RBM (Roll Back Malaria) reunió a la OMS, Unicef , el PNUD y el Banco Mundial .
En 2007, la Fundación Bill y Melinda Gates relanzó un proyecto de erradicación global, estudiado por una multitud de grupos de expertos, artículos científicos y que resultó en proyectos de estrategia de salud pública.
Pero en 2019 , la plausibilidad de la erradicación global sigue siendo objeto de debate. En agosto, la OMS incluso anunció que, según sus expertos, no es posible erradicar la malaria en un futuro próximo, y que fijar un plazo podría socavar los esfuerzos contra la enfermedad, como sucedió cuando la OMS se fijó la misma meta 64 años antes. (El incumplimiento de tales objetivos puede cansar a los donantes y debilitar la voluntad y el compromiso políticos, y el plazo puede orientar insidiosamente los esfuerzos hacia donde es más fácil "hacer números"). Después de 3 años de estudios, un informe del Grupo Asesor Estratégico para la Erradicación del Paludismo (SAGme) de la OMS dice: "No debemos preparar al mundo para el fracaso de otro esfuerzo de erradicación del paludismo" y recomienda desarrollar nuevas herramientas y enfoques contra la malaria, incluso fortaleciendo cobertura sanitaria universal. La Comisión Lancet para la erradicación de la malaria , que reúne a 26 académicos de todo el mundo, desea en cambio fijar una fecha límite (2050), principalmente para mantener el espíritu del desafío.
Se estima que los esfuerzos mundiales para combatir y eliminar la malaria salvaron 3,3 millones de vidas entre 2000 y 2013 al reducir las tasas de mortalidad por la enfermedad en un 45% a nivel mundial y un 49% en África. La lucha contra la malaria es uno de los objetivos del Objetivo de Desarrollo Sostenible 3 de la ONU .
Un estudio publicado el 25 de diciembre de 2019 destaca que ciertas poblaciones de insectos en África han desarrollado resistencia a los insecticidas ampliamente utilizados en los mosquiteros. Demostraron que la sobreexpresión de una proteína llamada SPA2 en las patas de los mosquitos les da resistencia a los insecticidas que contienen piretroides. Las proteínas SPA2 se unen a los piretroides y evitan la propagación del compuesto tóxico en su cuerpo. La proteína SPA2 "proteína de apéndice sensorial" es parte de la familia de proteínas quimiosensoriales "CSP". El descubrimiento del efecto de esta proteína allana el camino para la creación de un insecticida de segunda generación que contiene inhibidores específicos de SPA2. Estos permitirán que continúe la lucha contra la propagación de la enfermedad.
Impacto socioeconómico
La malaria se asocia comúnmente con la pobreza , pero también es una de las principales causas de pobreza y un gran obstáculo para el desarrollo económico y humano . La enfermedad tiene efectos económicos negativos en las zonas donde prevalece. Una comparación del PIB per cápita en 1995, ajustado por paridad de poder adquisitivo, entre los países afectados por la malaria y los no afectados, mostró diferencias de 1 a 5 (1.526 USD contra 8.268 USD). Además, en los países donde la malaria es endémica, el PIB del país creció un 0,4% por año en promedio entre 1965 y 1990, frente al 2,4% de otros países. Sin embargo, esta correlación no muestra que la causalidad y la prevalencia de la malaria en estos países también se deba en parte a la reducción de la capacidad económica para combatir la enfermedad.
El costo económico de la malaria se estima en USD 12 mil millones por año solo para África. Un caso ejemplar es el de Zambia . Si el presupuesto que el país dedicó a la lucha contra esta enfermedad en 1985 fue de 25.000 USD, desde 2008, gracias a la ayuda internacional y al PATH ( Programa de Tecnología Apropiada en Salud ), es de 33 millones distribuidos en un período de nueve años con el objetivo principal de proporcionar mosquiteros a toda la población .
A nivel individual, el impacto económico incluye los costos de atención y hospitalización, días laborales perdidos, asistencia escolar perdida, disminución de la productividad por daño cerebral causado por enfermedad; para los estados, estos impactos se ven agravados por la disminución de la inversión y el turismo. En algunos países particularmente afectados por la malaria, la enfermedad puede ser responsable del 40% del gasto público en salud, del 30 al 50% de los pacientes ingresados en el hospital y hasta el 50% de las consultas.
Causas
La malaria es causada por parásitos del género Plasmodium , ellos mismos transmitidos por mosquitos del género Anopheles .
Plasmodium , el parásito responsable de la malaria.
La malaria es causada por un parásito protozoario del género Plasmodium ( Phylum apicomplexa ). En los seres humanos, la malaria es causada principalmente por P. falciparum (predominante en los trópicos), P. malariae , P. ovale (la especie más rara excepto África occidental) y P. vivax (especie que exige menos temperatura).
P. falciparum es la causa más común de infecciones y es responsable de aproximadamente el 80% de todos los casos de malaria y del 90% de las muertes. El Plasmodium también infecta a aves, reptiles, monos, chimpancés y roedores (animales de sangre caliente). Se han informado infecciones humanas con especies de simios de malaria, incluidas P. knowlesi , P. inui (en) , P. cynomolgi , P. simiovale , P. brazilianum , P. schwetzi y P. simium . Sin embargo, con la excepción de P. knowlesi , estas infecciones siguen siendo limitadas y sin importancia en términos de salud pública. La malaria aviar puede matar pollos y pavos, pero la enfermedad no causa un daño económico significativo a la agricultura. Sin embargo, desde que fue introducida por los humanos, la malaria ha diezmado las especies endémicas de aves de Hawai , que habían evolucionado, en su ausencia, indefensas contra ella.
El Plasmodium tiene la forma de un protozoo muy pequeño (de 1 a 2 micrones según las formas). La tinción con May-Grünwald-Giemsa muestra que se compone de un citoplasma de color azul pálido que rodea una vacuola clara nutricional y que contiene un núcleo rojo y un pigmento marrón dorado o negro ( hemozoína ).
El ciclo evolutivo de Plasmodium es bastante complejo y requiere dos huéspedes, un huésped intermedio: el humano y un huésped definitivo: la hembra hematófaga de un mosquito del género Anopheles (del griego anôphelês que significa: inútil). Desde un punto de vista estrictamente biológico, el verdadero huésped definitivo es el mosquito (la reproducción sexual que parasita a los Anopheles ). El humano solo sería un huésped intermedio en su ciclo de replicación. Sin embargo, por motivos antropocéntricos , se considera que el vector no es el humano sino el mosquito y por tanto esta zoonosis es del tipo zooantroponosis .
Anopheles, vector de la malaria
Interacciones duraderas entre Anopheles y PlasmodiumSolo las hembras de Anopheles chupan sangre . Los machos cuyas únicas actividades son la reproducción de la especie y vuelan de un lado a otro para alimentarse de la savia y el néctar de las plantas no transmiten la enfermedad.
Las hembras de Anopheles se alimentan preferentemente por la noche y comienzan a buscar su comida al anochecer, continuando por la noche hasta que la encuentran.
Al respirar y sudar, los seres humanos y los animales emiten CO 2 , y sus cuerpos emiten constantemente calor y humedad ( transpiración ) así como un cóctel de sustancias potencialmente atractivas ( como el ácido láctico ) presentes en el cuerpo: aliento, sudor o sebo . Los mosquitos hembras (así como otros insectos que pican) pueden detectar algunos de estos humos corporales desde largas distancias (por ejemplo, ± 20 m para el CO 2 ) y son inmediatamente atraídos por estas fuentes. Los mosquitos pueden ser atraídos con más frecuencia después de la ingestión de alcohol o por los colores oscuros y especialmente el negro (que también acumula calor). Se mueven (máximo 2 km) utilizando sus sensores ( quimiorreceptores ).
Durante mucho tiempo se pensó que algunas personas "atraen" a los mosquitos más que otras, y los investigadores en 2011 confirmaron además que los Anopheles masculinos y femeninos no responden a los mismos estímulos químicos y de olor.
Desde un punto de vista ecológico y evolutivo o ecoepidemiológico , para propagarse mejor, este parásito tendría interés en atraer hembras de Anopheles hacia humanos (o animales) enfermos de malaria. Ahora se reconoce que muchos parásitos pueden manipular hasta cierto punto el comportamiento de su huésped, especialmente en especies de interés para la salud pública humana. Varios estudios recientes han demostrado que, durante los procesos de coevolución parásito-huésped, los parásitos han adquirido la capacidad de modificar el olor de su huésped a su favor, atrayendo vectores . Se confirmó en 2004 y 2005 que las personas con malaria atraen más mosquitos que los niños que no están enfermos (un niño con malaria atrae el doble de anofeles picadores que un niño que no está enfermo). Esto también se demostró en 2013 en animales (aves), pero no se sabía por qué proceso.
En 2014 , un estudio mostró que los ratones de laboratorio infectados con un plasmodium ( Plasmodium chabaudii en este caso) tienen un olor corporal que cambia de manera muy significativa (siempre que el ratón siga siendo infeccioso), y que atrae más anofeles que los que no son ratones. infectado.
En 2015 , otro estudio proporcionó una explicación probable para este fenómeno: en el laboratorio, en las células que infectan, los parásitos ( Plasmodium falciparum ) son capaces de sintetizar un atractivo olor a terpeno para las hembras Anopheles, gracias a su apicoplasto (orgánulo heredado - por endosimbiosis - un organismo vegetal, alga o cuerpo intermedio entre las algas y las bacterias ( cianobacterias ..) este orgánulo cercano a los cloroplastos perdió su capacidad fotosintética, pero es capaz de metabolizar terpenos,
esto lo demuestra Audrey R. Odom, de la Facultad de Medicina de la Universidad de Washington en St. Louis, con sus colegas (incluyendo la Universidad de Yale), en un estudio publicado por la revista MBIO. este equipo había trabajado en apicomplexa y la capacidad de apicoplasts demostrado biosynthesize de isoprenoides . un estudio previo no se había detectado la producción de terpenos, pero era basado en ti baja cantidad de plasmodios. El equipo de St Louis tuvo la idea de cultivar esta vez una mayor cantidad de plasmodios, comparable a la que está presente en un organismo infectado. El cultivo se realizó en lotes de glóbulos rojos humanos infectados, cuyas emisiones de gas se compararon con las de lotes idénticos pero no infectados, así como con el gas que se encuentra en las mismas bolsas de plástico pero vacías (controles). Según los resultados de este estudio publicado en 2015, solo los sobres que contenían glóbulos infectados contenían terpenos. Los autores han demostrado que para hacer esto (como algunas plantas), P. falciparum moviliza una vía bioquímica conocida como la " vía de biosíntesis de isoprenoides plastidiales " para sintetizar dos terpenos ( limoneno y pinanediol , que tienen respectivamente un olor a limón y uno que recuerda a pino). ) y otras dos moléculas (cuyo posible papel no se ha identificado). Cada muestra gaseosa de un cultivo de células sanguíneas que contiene células sanguíneas portadoras del parásito contenía al menos uno de estos dos terpenos. Ya sabíamos (demostrado en 2012) que estos dos terpenos (producidos por flores que producen el néctar más atractivo para los machos de Anopheles) atraen a los machos de Anopheles (incluso en dosis muy bajas).
Pruebas adicionales han confirmado que la hembra Anopheles que transmiten la malaria ( Anopheles gambiae ) serán capaces de detectar estos terpenos y que reaccionan a ellas, gracias al hecho de que contienen la "maquinaria celular necesaria para detectar y responder a estos compuestos.» , Según Odom (aunque también se sabe que otras moléculas las atraen; CO 2Por lo tanto, se ha presentado como un factor de atracción importante, pero se ha demostrado (2014) que las cepas de Anopheles gambiae privadas del receptor de CO 2, el calor y el ácido láctico siguen siendo perfectamente capaces de localizar a un huésped humano para que se alimente de su sangre, lo que demuestra que el mosquito "rastrea" otras moléculas y lo guía en la elección del huésped donde alimentarse de sangre.
Esto sugiere que los seres humanos (o animales) infectados con malaria tienen más probabilidades de ser picados por un mosquito, e incluso de ser picados más de una vez, lo que contribuye a la propagación de la epidemia, pero como resultado de esta demostración in vitro, Queda por demostrar in vivo en humanos o animales que estos terpenos son efectivamente liberados por la piel o el aliento y que, en esta forma o en una forma modificada, realmente atraen anofeles, lo que el laboratorio de St. Louis quiere hacer rápidamente.
Esta información abre el camino a nuevas pruebas de diagnóstico no invasivas para la malaria, basadas por ejemplo en el análisis del olor de la piel, el aliento (como un alcoholímetro ) o el sudor. También están surgiendo nuevas vías para combatir la propagación del parásito: manipulando el olor percibido por el mosquito, podría ser posible limitar la atracción de los anofeles hacia los pacientes con malaria o, por el contrario, producir señuelos. ellos muerden.
| Nombre de la zoonosis | Porque | Transmisión | Vector |
|---|---|---|---|
| Chikungunya | Virus | Día noche |
Hembra Aedes hembra Anopheles funestus |
| Dengue | Virus | El día | Aedes hembra |
| La encefalitis japonesa | Virus | La noche | Culex hembra |
| Fiebre amarilla | Virus | El día | Aedes hembra |
| Filariasis linfática | Parásito | La noche | Anopheles femenino |
| O'nyong-nyong | Virus | La noche | Anopheles femenino |
| Malaria | Parásito | La noche | Anopheles femenino |
Ciclo parasitario
En anofeles
El vector del parásito, así como su huésped principal, es la hembra de un mosquito del género Anopheles . Los mosquitos jóvenes ingieren el parásito por primera vez cuando se alimentan de la sangre (que necesita esta hembra para la producción de huevos) de un sujeto humano infectado. Una vez ingeridos, los gametocitos de Plasmodium se diferencian en gametos masculinos y femeninos y se unen para formar un cigoto móvil llamado ookinete que penetra en la pared del estómago del mosquito para convertirse en un oocisto esférico, el núcleo se dividirá en múltiples ocasiones para formar esporozoitos . La duración de esta maduración depende en gran medida de la temperatura exterior. Por ejemplo P. falciparum : no maduración por debajo 18 ° C o por encima de 35 ° C , que es máxima a 24 ° C . Cuando el ooquiste se rompe, libera los esporozoitos que migran a través del cuerpo del mosquito a las glándulas salivales donde pueden, durante una nueva ingestión de sangre, infectar a un nuevo huésped humano, pasando a través de la piel con la saliva .
Ciclo del parásito humano
Fase hepáticaHuso fino de 12 µm / 1 µm, el esporozoíto infeccioso inyectado en humanos, durante esta picadura de una hembra infectada Anopheles, circula rápidamente (menos de media hora) en la sangre hasta el hígado, en el que se encuentra secuestrado en gran parte gracias a los patrones adhesivos. de la proteína principal de su envoltura, la proteína circumsporozoite o CSP = proteína Circumsporozoite , para luego infectar los hepatocitos . Esta crisis hepática preeritrocítica que durará de 7 a 15 días para P. falciparum , de 15 días a 9 meses para P. vivax , de 15 días a X meses para P. ovale y 3 semanas para P. malariae permitirá la parásito para continuar su ciclo. Los esporozoitos que no llegan al hígado serán eliminados por los fagocitos o no podrán continuar su desarrollo si llegan a otros órganos .
Una primera transformación redondea esta forma de "criptozoíto" (del griego κρυπτός (kruptos) que significa "oculto") en un elemento uninucleado (con un solo núcleo) llamado trofozoíto que es la oportunidad para que el parásito se multiplique directamente (siempre lo es. para P. falciparum ), por esquizogonía , durante una semana a quince días dando como resultado un enorme esquizonte (nombre que se le da al protozoo cuando se activa después de la fase de incubación) de 40 a 80 μm . Este cuerpo azul (porque consiste en un citoplasma azul pálido cuando se tiñe con May-Grünwald-Giemsa ) brota , mientras pierde su movilidad, para emitir vesículas , conteniendo los merozoitos jóvenes que serán transferidos a la sangre, iniciando así el eritrocito etapa, es decir, infección de los glóbulos rojos.
Sin embargo, algunos merozoitos de P. ovale o P. vivax pueden permanecer ocultos en el hígado durante varios años, o incluso en la vida de P. malariae , antes de reactivarse en oleadas sucesivas. Estos son ciclos exoeritrocíticos secundarios que mantendrán la parasitosis en el hígado durante dos o tres años para P. Ovale , de 3 a 5 años o más para P. Vivax y durante toda la vida para P. Malariae . Esta fase del parásito se denomina "fase latente". Estos parásitos intrahepáticos latentes se denominan "hipnozoítos" (del griego Ὕπνος, que es Hypnos, el antiguo dios griego del sueño).
Fase de transferenciaLas vesículas se liberan en los sinusoides hepáticos (vasos capilares del hígado que hacen la unión entre este y la red sanguínea) para luego unirse al torrente sanguíneo y esparcir una avalancha de merozoitos " preeritrocíticos " jóvenes listos para infectar los glóbulos rojos . Cada célula hepática infectada contiene aproximadamente 100.000 merozoitos (cada esquizonte es capaz de producir 20.000 merozoitos). Es una verdadera técnica de “ caballo de Troya ” que se utiliza aquí para pasar de las células hepáticas a la sangre . In vivo de imágenes mostró en de 2005 - de 2006 en roedores que merozoitos fueron capaces de producir células muertas que les permite abandonar el hígado para la circulación de la sangre escapando así el sistema inmunológico ). Parece que ambos guían este "vehículo" y se esconden en él, enmascarando las señales bioquímicas que normalmente alertan a los macrófagos . Puede haber una nueva vía para los fármacos activos o una vacuna contra la etapa de exoeritrocitos antes de la etapa de invasión de glóbulos rojos.
Fase de sangreAl comienzo de la fase sanguínea larga: los merozoitos se adhieren a los glóbulos rojos , los invaden, se convierten en trofozoítos y luego se dividen (esquizontes).
En 2011, un equipo internacional descubrió que entre los receptores de superficie del glóbulo rojo que permiten la entrada del parásito, uno de ellos es fundamental para esta penetración (confirmado con todas las cepas analizadas para P. falciparum ); por tanto, este receptor se convierte en un objetivo para futuras investigaciones sobre vacunas.
Al difundirse, los merozoitos hacen que los glóbulos rojos estallen (esto es hemólisis ).
El estallido de esquizontes maduros o "rosetas" pone fin al primer ciclo de eritrocitos esquizogónicos liberando en la sangre una nueva generación de plasmodios, los merozoitos "eritrocitos" capaces de reinfectar otros glóbulos rojos.
Seguirá una sucesión regular de ciclos similares, que serán reemplazados gradualmente (organizando las defensas inmunitarias ) por ciclos de eritrocitos gamogónicos que preparan las formas sexuales. Los trofozoítos dejan de dividirse y cambian su proporción nucleoplasmática. Estas formas de trofozoítos con un núcleo grande y un citoplasma densificado son los gametocitos masculinos y femeninos , que permanecerán en el torrente sanguíneo.
Los parásitos durante esta fase no tienen ninguna posibilidad de supervivencia en los seres humanos: permanecen vivos durante unos veinte días y luego desaparecen. Solo podrán continuar su evolución en el mosquito. En este punto, si una hembra anofeles pica a una persona enferma, este absorbe los gametocitos de la sangre y comienza un nuevo ciclo, esta vez sexual, en el mosquito. Los esporozoitos producidos por esta reproducción pasan a la saliva del mosquito, que puede infectar a un nuevo huésped, y así sucesivamente ...
Fisiopatología
Manifestaciones clínicas
Los hematozoos inoculados por el mosquito se localizan y multiplican primero en el hígado. Esta fase define un período mínimo de incubación, sin ningún síntoma.
Las manifestaciones clínicas de la malaria aparecen al comienzo de la fase sanguínea, cuando la parasitemia supera un umbral, que varía según el individuo. Esta multiplicación asexual de plasmodios dentro de los glóbulos rojos hace que la malaria, literalmente, sea una enfermedad parasitaria de los glóbulos rojos.
La lisis de los glóbulos rojos parasitados (estallido de esquizontes maduros o rosetas) libera nuevos parásitos ( merozoitos ) que a su vez contaminan otros glóbulos rojos. Esta destrucción también conduce a la liberación de desechos del metabolismo plasmodial (pigmentos y restos celulares de los glóbulos rojos, o hemozoína ), estas sustancias pirogénicas interrumpen el funcionamiento del hipotálamo (producción de citocinas como el TNFα ) y provocan fiebres altas .
Los primeros ciclos son primero asincrónicos (malaria primaria, con fiebre continua o anárquica), luego se sincronizan según un ritmo periódico, dependiendo de la especie de Plasmodium. El tiempo que transcurre entre la penetración de un parásito en un glóbulo rojo y el estallido del mismo es bastante constante y alcanza las 48 horas en humanos para P. vivax , P. ovale y P. falciparum (terceras fiebres), 72 horas para P. malariae (cuarta fiebre); y para P. knowlesi , la última especie confirmada en humanos, solo 24 horas.
En casos de parasitismo intenso, la destrucción de los glóbulos rojos es tal que aparecen anemia hemolítica e ictericia . El cuerpo reacciona con hiperplasia (aumento de la producción) de macrófagos , lo que explica el aumento de tamaño del hígado ( hepatomegalia ) y del bazo ( esplenomegalia ).
P. falciparum se distingue de otras especies de Plasmodium por tener la capacidad de realizar su fase sanguínea a nivel de los capilares viscerales, en particular del tejido cerebral. Entonces puede formar "rosetas" (grupos de glóbulos rojos sanos y parasitados), formaciones que se adhieren a las paredes de los capilares. Esta situación puede ir acompañada de hipoxia secundaria, alteraciones metabólicas y electrolíticas , vascular (paredes de pequeños vasos) y daño tisular.
Si no se trata, la malaria por P. falciparum presenta un riesgo inmediato que pone en peligro la vida (riesgo de síndrome de insuficiencia orgánica múltiple, por ejemplo), es probable que las diversas malaria progresen a formas crónicas (formas históricas), con un deterioro progresivo de la afección general que puede conducir a la caquexia .
Inmunidad
Después de varios años de infecciones repetidas, el huésped Plasmodium puede adquirir una inmunidad, llamada premunición (síntomas atenuados de una enfermedad que protege contra una infección de tipo grave posterior). Existe una gran variabilidad en las respuestas a la infección por malaria entre las personas que viven en las mismas áreas endémicas . En áreas de alta transmisión, una gran proporción de niños a menudo son portadores del parásito P. falciparum sin reportar ningún síntoma; es inmunidad clínica. Con la edad y los sucesivos contactos humano / parásito, esta premunición se establece gradualmente, que recurre a mecanismos de resistencia a la infección entre los que las proteínas “ interferón ” metabolizadas y excretadas , entre otras, por el hígado, juegan un papel importante en la lucha antiparasitaria. inmunidad. Hablaremos, entonces, de tolerancia a la infección o inmunidad antiparasitaria. Una hipótesis es que Plasmodium necesita hierro para crecer; la deficiencia de hierro debida a una primera infección proporcionaría una protección relativa y evitaría una "superinfección".
A menudo se dice que esta inmunidad no es esterilizante porque nunca se ha demostrado de manera formal la desaparición total de los parásitos de P. falciparum en ausencia de tratamiento. También se dice que esta inmunidad es lábil porque la premunición desaparece ante la ausencia de contacto frecuente entre el ser humano y el parásito (desaparece a los 12 a 24 meses si el sujeto abandona el área endémica) así como en mujeres embarazadas.
Además, la inmunidad dirigida contra P. falciparum es muy específica para las cepas parasitarias presentes.
Estas peculiaridades de la respuesta inmunitaria contra la malaria están en el origen de las dificultades para desarrollar una vacuna .
Factores genéticos
Los factores genéticos pueden proteger contra la malaria (ver: beneficio heterocigoto ). La mayoría de los que se han descrito están asociados con los glóbulos rojos. Aquí están algunos ejemplos:
- La anemia de células falciformes (en griego Drepanos , "hoz" bajo la forma alargada que tiene una cantidad de glóbulos rojos o glóbulos rojos) también llamada anemia falciforme de la hemoglobina S o anemia falciforme: un cambio en la cadena ß de la hemoglobina causa la las células sanguíneas se deformen , produciendo heterocigotos que protegen mejor contra la malaria. Los glóbulos rojos se deforman y la hemoglobina cristaliza, lo que evita que el parásito ingrese a los glóbulos rojos. Sin embargo, este cambio conduce a una mala oxigenación de los órganos (los glóbulos rojos alargados no pueden pasar a los capilares finos ni a la barrera formada por el filtro del bazo donde se destruyen) y, por tanto, complicaciones graves, hasta la muerte por ellos. sujetos homocigotos (HbS / HbS). La prevalencia de la anemia de células falciformes (HbA / HbS) es alta en las poblaciones africanas sometidas a una gran presión por el paludismo debido a la resistencia que proporciona contra los episodios graves de la enfermedad.
- La talasemia o anemia hereditaria: el sujeto es portador del gen SS que da como resultado un cambio en la tasa de síntesis de las cadenas de globina con la consiguiente mala circulación sanguínea y una fatiga constante.
- La deficiencia genética de G6PD (glucosa-6-fosfato deshidrogenasa) también llamada favismo , que es una enzima antioxidante que normalmente protege contra los efectos del estrés oxidativo en los glóbulos rojos, brinda una mayor protección contra la malaria grave.
- El HLA-B53 está asociado con un bajo riesgo de paludismo grave. Esta molécula del MHC de clase I (complejo principal de histocompatibilidad) presente en el hígado es un antígeno de los linfocitos T (porque están ubicados en el timo ) contra la etapa de esporozoitos. Este antígeno, codificado por IL4 (interleucina-4), producido por las células T (timo), promueve la proliferación y diferenciación de la producción de anticuerpos de células B. Un estudio de los Fulani de Burkina Faso , que tienen menos de dos ataques de malaria con niveles más altos de anticuerpos antipalúdicos que los grupos étnicos vecinos, encontraron que el alelo IL4-524 T estaba asociado con altos niveles de anticuerpos antipalúdicos , lo que plantea la posibilidad de que pueda ser un factor en el aumento de la resistencia a la malaria.
- En la lucha natural contra P. vivax en África, el proceso de selección ha eliminado de la herencia genética un receptor de membrana de los eritrocitos , la glicoproteína DARC (Receptor de antígeno Duffy para quimiocinas), que es el objetivo de entrada de P. vivax. Por lo tanto, los sujetos negativos para el grupo sanguíneo Duffy , abreviado FY (-), no pueden ser contaminados por P. vivax . Esto explica la ausencia de P. vivax en la población de África occidental exclusiva o abrumadoramente del grupo sanguíneo “Duffy-negativo”. Sin embargo, esta inmunidad natural podría cuestionarse, ya que P. vivax logró adaptarse a Madagascar en sujetos Duffy negativos, tras la mezcla genética entre poblaciones africanas y asiáticas. Esto mostraría la existencia de objetivos secundarios del parásito que quedan por determinar.
Existen otros factores genéticos, algunos de los cuales están involucrados en el control de la respuesta inmune.
Clínico
La malaria se manifiesta por episodios de fiebre o "episodios de malaria". Clásicamente, se acostumbra describir el ataque de invasión primaria que ocurre por primera vez en un paciente "ingenuo" (que ya no tiene inmunidad contra la malaria o no ha encontrado el parásito antes), y ataques recurrentes de malaria que ocurren en sujetos ya infectados con Plasmodium .
En la práctica moderna, se hace una distinción entre ataques simples y formas graves. Es probable que los ataques simples se conviertan en formas graves (especialmente aquellos con P. falciparum ), no diagnosticados o tratados, también pueden convertirse en formas crónicas. Además, la sospecha de un ataque de malaria se considera una emergencia diagnóstica y terapéutica.
Acceso simple a la malaria
La incubación es de un mínimo de 7 días hasta 3 meses, dependiendo de los tipos de Plasmodium.
Paludismo de invasión primariaLa invasión primaria por Plasmodium distinto de falciparum puede ser poco o poco sintomática, pasando desapercibida. De lo contrario, el primer ataque de malaria es común a todas las formas de Plasmodium . Ocurre en pacientes no inmunes: adultos que han perdido su inmunidad mientras residían en un área no endémica, o viajeros que llegan a un área endémica, o un niño nacido y afectado por primera vez en un área endémica.
La fiebre es el signo principal en el 90% de los casos, aumenta gradualmente a más de 40 ° C. Se acompaña de un síndrome gripal ( dolor de cabeza , dolores musculares o articulares) y trastornos digestivos ( náuseas , vómitos , diarreas , etc. ). En los niños, los signos digestivos pueden ser dominantes (cuadro de gastroenteritis febril, etc. ).
Esta fiebre es continua o anárquica (sin periodicidad), porque los ciclos eritrocitarios aún no están sincronizados (ciclos asincrónicos).
Acceso recurrenteLa "crisis de la malaria" se caracteriza por ataques febriles intermitentes. Clásicamente, cada acceso tiene 3 fases:
- Fase fría: intensos escalofríos y temblores por sentir un frío extremo, a medida que sube la temperatura, que duran aproximadamente una hora.
- Fase de calor: fiebre en meseta a 40-41 ° C, con una duración de 3 a 4 horas.
- Fase de sudoración intensa: con descenso repentino de la fiebre en 2 a 4 horas.
Estos ataques se repiten con regularidad, dependiendo de los ciclos de eritrocitos. Clásicamente, se hace una distinción entre la fiebre terciaria (es decir, que ocurre cada dos días) causada por Plasmodium vivax y Plasmodium ovale (fiebre terciaria benigna) y Plasmodium falciparum (fiebre terciaria maligna) de la cuarta fiebre (es decir, que ocurre cada 3 días) debido a a Plasmodium malariae (el término "malaria" se refiere específicamente a la fiebre del cuarto).
En ausencia o insuficiencia de tratamiento, estos ataques de malaria pueden repetirse durante meses o incluso años, con P. ovale , P. vivax y especialmente con P. malariae , a menos que sean tratados correctamente y en ausencia de reinfestación (casos de malaria importada, en general).
Con P. falciparum , el curso es más corto, pero con altos riesgos de formas letales.
| |||||||||||||||||||||||||||||||||||
| * Los tiempos de incubación pueden extenderse de varias semanas a varios meses, en caso de profilaxis antipalúdica insuficiente. |
P. ovale y P. vivax están muy cerca y se han confundido durante mucho tiempo.
Hay infecciones mixtas con dos especies de Plasmodium en alrededor del 3 al 4% de los casos. Por ejemplo, una coinfección con P. ovale y P. vivax produce una superposición de ciclos de dos poblaciones de parásitos, manifestada por episodios diarios de malaria o malaria tertiana diaria . También se la llamó fiebre de doble tierce .
De ahí la existencia de muchas variantes con nombres históricos como: fiebre de medio tercio (ataques diarios alternativamente débiles e intensos), fiebre de dos cuartos (acceso en dos días consecutivos separados por un día sin). Las fiebres pseudo-malaria son fiebres intermitentes debidas a causas distintas a la malaria.
Acceso severo a la malaria
La malaria grave es causada de manera abrumadora por P. falciparum y generalmente ocurre de 6 a 14 días después de la infección. Puede aparecer inmediatamente, o después de un tratamiento inadecuado o tardío.
En el XXI ° siglo, se define por criterios clínicos y biológicos Internacional (OMS) o nacional, revisada regularmente. En Francia 2017, los principales criterios para el paludismo grave importado a adultos son:
- Fallo neurológico (de nubosidad al coma).
- Ictericia clínica o bilirrubinemia elevada.
- Hiperparasitemia superior al 4%.
- Insuficiencia renal ( creatinina o uremia elevada).
Otros criterios, menos frecuentes pero indicativos de gravedad, son las fallas respiratorias y cardiocirculatorias y los estados biológicos de acidosis e hiperlactatemia .
La malaria grave que no se trata puede progresar rápidamente y conducir al coma y la muerte en cuestión de días o incluso horas, especialmente en niños pequeños y mujeres embarazadas que son particularmente vulnerables. De ahí el interés de un diagnóstico de urgencia sin demora en el tratamiento. En los casos más graves, la tasa de mortalidad puede superar el 20%, incluso con un tratamiento correcto sin demasiada demora.
Se pueden observar formas graves de P. vivax , especialmente en el sudeste asiático , las principales complicaciones son entonces respiratorias. La malaria por P. knowlesi se presenta con mayor frecuencia como un simple ataque, pero puede progresar a una forma grave (pero sin daño cerebral).
Se puede observar un infarto del bazo o una ruptura del bazo con cualquier especie de Plasmodium , más a menudo P. falciparum y P. vivax .
NeurolariaEs un ataque de malaria grave dominado por manifestaciones neurológicas, estando la malaria cerebral relacionada con el daño a los capilares del cerebro. Es la malaria cerebral de los anglosajones, e históricamente entre los francófonos el pernicioso acceso .
Hacia el final del XX ° siglo, los expertos de la OMS han ampliado el concepto de acceso de la malaria grave como para otros eventos que no sean neurológica, por razones prácticas (incluso peor pronóstico, incluso de la misma el tratamiento de emergencia). También en el XXI ° siglo, las condiciones de acceso o grave (francés), o la malaria grave (Inglés) se utilizan más a menudo como la malaria cerebral o la malaria cerebral, más restrictivo.
El acceso pernicioso se produce de forma gradual o repentina. Asocia fiebre y alteraciones de la conciencia. Las convulsiones se localizan o generalizan a todo el cuerpo, especialmente en niños, y solo en el 50% de los casos en otros adultos. Esto se debe al mal funcionamiento del hígado y al consumo excesivo de azúcar por parte del parásito. Las mujeres embarazadas están particularmente predispuestas a la hipoglucemia y la producción excesiva de ácido láctico que conduce a un aumento de la acidez de la sangre.
Los otros signos neurológicos varían en el tiempo y la ubicación. Pueden ir acompañadas de anemia, insuficiencia hepática e insuficiencia renal funcional y transitoria , o insuficiencia renal aguda más grave.
Un edema pulmonar es una complicación rara pero grave de muy mal pronóstico. Está mal explicado, con una tasa de mortalidad superior al 80%.
Fiebre hemoglobinúrica biliarEsta es una complicación histórica, especialmente observada entre 1910 y 1940, y se convirtió en raras a finales del XX ° siglo. Era un síndrome que se presentaba en expatriados europeos en una zona tropical endémica, con antecedentes de acceso a Plasmodium falciparum y de ingestión irregular de quinina .
Es de origen inmunoalérgico ligado al fármaco, con hemólisis intravascular masiva (estallido de glóbulos rojos dentro de los vasos).
El inicio es repentino, ocurre pocas horas después de tomar el medicamento, con fiebre y dolor lumbar , ictericia y descenso de la presión arterial . La anemia hemolítica causa hemoglobinuria (presencia de hemoglobina en la orina que le da un color oscuro, fiebre de aguas negras para los ingleses u orina roja oportuna para los franceses). La progresión puede conducir a insuficiencia renal aguda por destrucción de los túbulos renales (necrosis tubular aguda).
Hay poca o ninguna parasitemia, lo que distingue este síndrome de un ataque pernicioso.
Esta fiebre biliosa hemoglobinúrica prácticamente ha desaparecido con la sustitución de la quinina por antimaláricos sintéticos como las 4- aminoquinolinas (como la cloroquina ). Sin embargo, se han notificado casos con fármacos químicamente similares a la quinina, como halofantrina o mefloquina . Estos tres fármacos están formalmente contraindicados en sujetos sensibles.
Diagnóstico
Diagnostico clinico
Países desarrolladosCualquier fiebre justifica una búsqueda del historial de viajes; y al regresar de un área donde la malaria es endémica, cualquier fiebre o antecedentes de fiebre es malaria hasta que se demuestre su culpabilidad, debido al riesgo de progresión rápida a una forma grave. En Francia, esto afecta principalmente a los viajeros migrantes que regresan del África subsahariana, incluso en caso de quimioprofilaxis (a menudo mal administrada) o tratamiento en el lugar.
Las trampas clásicas que retrasan el diagnóstico de malaria son la gastroenteritis febril, especialmente en niños; una enfermedad parecida a la gripe en el invierno; la ausencia de fiebre (tratamiento sintomático inadecuado); un cuadro de infección del tracto urinario ; una variedad de dengue .
La sospecha de paludismo implica, en caso de emergencia, un diagnóstico de laboratorio de confirmación.
País en desarrolloEn muchos lugares, ni siquiera un simple diagnóstico de laboratorio es posible, y el interrogatorio de un paciente febril se utiliza como indicación para continuar o no el tratamiento antipalúdico. Pero este método no es el más eficaz: en Malawi , el uso de frotis de sangre teñidos con Giemsa mostró que los tratamientos antipalúdicos innecesarios disminuían cuando se usaban indicadores clínicos (temperatura rectal, palidez del lecho ungueal, esplenomegalia) en lugar de un historial de fiebre informado. (la sensibilidad aumentó del 21% al 41%).
Los cuidadores de primera línea (miembros de la comunidad que han recibido una formación básica que les permite prestar atención básica en ausencia de personal médico calificado) diagnostican erróneamente el paludismo que afecta a los niños (mala historia , uso indebido de las pruebas de diagnóstico rápido); asimismo, está mal evaluado, lo que resulta en un tratamiento inadecuado o insuficiente, impidiendo un tratamiento eficaz.
Diagnóstico biológico
El diagnóstico de malaria se basa en la detección del parásito en la sangre. Este es un diagnóstico de emergencia que debe realizarse dentro de las dos horas posteriores a la extracción de la muestra de sangre.
Análisis de sangre al microscopio (frotis de goteo grueso)El método de diagnóstico más barato (entre US $ 0,40 y US $ 0,70 por portaobjetos), el más confiable y el más utilizado es el examen microscópico óptico de un frotis de sangre y una gota gruesa de sangre.
El frotis permite identificar las características únicas de cada una de las cuatro especies del parásito Homo sapiens porque la apariencia del parásito se conserva mejor con esta muestra. La gota de sangre espesa permite viajar un mayor volumen de sangre para hacer el diagnóstico y no perder Plasmodium . Estos exámenes deben ser realizados por un biólogo calificado e informado.
La información esperada es:
- diagnóstico positivo de malaria (presencia de Plasmodium ).
- diagnóstico de especies (presencia de P. falciparum u otra especie), por gravedad potencial.
- la parasitemia (porcentaje de hematíes infectados o número de parásitos por µl de sangre), útil para el seguimiento del tratamiento.
El valor predictivo negativo de los dos métodos combinados (frotis y película gruesa) no es del 100%. Un examen negativo debe repetirse dentro de las 12 a 24 horas, si persiste la sospecha clínica.
Pruebas de diagnóstico rápidoCuando no se dispone de un microscopio, es posible utilizar pruebas para la detección rápida de antígenos, que solo requieren una gota de sangre y que no requieren conocimientos especiales.
Estas pruebas inmunocromatográficas (también llamadas pruebas de diagnóstico rápido para la malaria o PDR) pueden presentarse en forma de tira reactiva o “tira reactiva”. Las primeras pruebas rápidas usaban glutamato deshidrogenasa (GluDH) de P. falciparum como antígeno diana (pGluDH), pero fueron reemplazadas por las que usaban lactato deshidrogenasa (LDH) (pLDH) de P. falciparum y HRP2 (para la proteína 2 rica en histidina ).
La sensibilidad de las pruebas utilizadas (200 productos disponibles en el mercado) es superior al 95% cuando la parasitemia es superior a 100 por μL de sangre, y al 70% para las parasitemias más débiles e incluso menor para P. ovale. Su especificidad es del 90 al 95%.
En los países desarrollados, estas pruebas rápidas se asocian con el frotis-goteo espeso.
Biología MolecularEste método se basa en la detección de ácidos nucleicos del parásito mediante la reacción en cadena de la polimerasa (PCR), una técnica más sensible y específica que la microscopía. Permite la detección de parasitemias muy débiles y la identificación precisa de las especies de plasmodium (incluida la distinción P. Knowlesi y P. malariae ).
En los países más avanzados, la PCR tiende a convertirse en el método de referencia para el diagnóstico del recurso (situación de dificultades diagnósticas). Los métodos analíticos más rápidos, como la PCR en tiempo real , con resultados en menos de una hora, están disponibles en los laboratorios de referencia y pueden ser compatibles con el diagnóstico de emergencia o de rutina.
Evaluación de la gravedadLa evaluación biológica estándar permite evaluar un nivel de gravedad y ayudar en el diagnóstico diferencial: en particular, el hemograma , la proteína C reactiva , el ionograma , los signos biológicos de hemólisis, el sufrimiento hepático o renal. El análisis de sangre se puede utilizar para detectar otras infecciones, especialmente infecciones virales, según el contexto y según las recomendaciones.
La coinfección con el paludismo siempre es posible, pero la prueba del paludismo es una prioridad dada su mayor frecuencia y su posible gravedad inmediata.
Formas crónicas
Las complicaciones agudas y graves generalmente solo afectan a Plasmodium falciparum , pero no se convierte en formas crónicas.
Las formas subaguda y crónica de malaria se observan durante infecciones por otros plasmodios: P. vivax , P. ovale y especialmente P. malariae . La enfermedad puede reaparecer varios meses o años después de la exposición, debido a la presencia latente de parásitos en el hígado. Por lo tanto, no se puede decir que un sujeto se cura de la malaria simplemente observando la desaparición de los parásitos del torrente sanguíneo. El período de incubación más largo notificado para P. vivax es de 30 años. Aproximadamente uno de cada cinco casos de paludismo por P. vivax en áreas templadas implica la hibernación por hipnozoítos (las recaídas comienzan el año después de la picadura del mosquito).
Evolución de la malaria visceral
Anteriormente denominada caquexia palúdica, esta malaria se observa en niños de 2 a 5 años en áreas endémicas, en sujetos expatriados en áreas endémicas con tratamiento insuficiente y en migrantes que ya no viven en áreas endémicas.
Asocia un deterioro progresivo del estado general, con fiebre intermitente moderada (a veces ausente), anemia crónica con citopenia , esplenomegalia moderada (a veces importante). La parasitemia es muy débil, incluso indetectable.
Esplenomegalia palúdica hiperinmune
Esta malaria crónica, anteriormente confundida en un grupo llamado "esplenomegalias tropicales", corresponde a una respuesta inmunológica anormal. Bastante raro, se encuentra en unas pocas personas que viven en un área donde la malaria es endémica.
Se distingue del paludismo visceral progresivo por una esplenomegalia y hepatomegalia importantes , un aumento de cierto tipo de inmunoglobulina en la sangre (IgM, anticuerpos antipalúdicos) y en el número de linfocitos dentro de los sinusoides hepáticos . La parasitemia suele ser indetectable.
La biopsia del hígado y el examen con microscopio óptico permiten el diagnóstico. El curso muy lento puede ser desfavorable por rotura del bazo , sobreinfección o aparición de un síndrome linfoproliferativo maligno .
Nefritis cuartana
Es una complicación renal grave por infección crónica por Plasmodium malariae (responsable de la fiebre del cuarto, de ahí su nombre). Ocurre con mayor frecuencia en niños en áreas endémicas, después de varios años de desarrollo.
El cuadro es el de un síndrome nefrótico , por depósito de complejos inmunes (asociaciones anticuerpo-antígeno) en los glomérulos renales .
La biopsia de riñón puede identificar la lesión. Este examen revela depósitos de complemento (elementos involucrados en el sistema inmunológico) e inmunoglobulinas (variedad de proteínas que desempeñan el papel de anticuerpos). El laboratorio detecta antígenos de Plasmodium malariae en niños .
La evolución se puede hacer más o menos rápidamente hacia insuficiencia renal crónica , a pesar del tratamiento (antimaláricos y corticoides ).
Formas según el terreno
Mujeres embarazadas
El embarazo con infección de la placenta por Plasmodium tiene un mayor riesgo de complicaciones. En áreas endémicas, el embarazo conduce a una disminución de la inmunidad antipalúdica, mientras que las lesiones placentarias provocan una disminución de la circulación fetal-materna.
En la madre, los ataques de malaria son más frecuentes y graves (riesgo de aborto o parto prematuro ), y en los niños: mortalidad perinatal , anemia, bajo peso al nacer.
En 2018, casi 11 millones de mujeres embarazadas estaban en riesgo de contraer paludismo (en áreas de moderada a altamente endémica) en África subsahariana, con 872.000 bebés con bajo peso al nacer. África occidental es la región con mayor prevalencia de bajo peso al nacer, relacionado con la malaria durante el embarazo.
La frecuencia y gravedad de las infecciones en áreas endémicas dependen del nivel de transmisión de la malaria. En áreas inestables de baja endemia como la India o la región del Sudeste de Asia Pacífico, el riesgo de formas graves en mujeres embarazadas es tres veces mayor que en mujeres no embarazadas. En estas regiones, más del 23% de la mortalidad materna se debe a la malaria.
En regiones con una endémica alta estable como África subsahariana, las formas más graves ocurren durante el primer embarazo o el primer parto (mujer primípara ), mientras que las mujeres que ya han tenido al menos un embarazo presentan menos problemas, incluso con un parásito alto. carga. Este fenómeno podría explicarse por la adquisición de una inmunidad placentaria específica por acumulación selectiva de P. falciparum en la placenta.
El paso transplacentario de Plasmodium de la madre al feto es relativamente común, pero rara vez se manifiesta como una "enfermedad", es decir, malaria congénita que ocurre entre los primeros días y el primer mes después del nacimiento. Su incidencia exacta es debatida: sería muy rara en áreas hiperendémicas (menos de 3 por mil nacimientos de madres infectadas) pero más común en otros lugares.
Niños
En zona endémicaLos niños menores de 5 años son el grupo más afectado por la malaria. En 2018, la OMS estimó el número de niños infectados por P. falciparum en el África subsahariana en 24 millones , incluidos 1,8 millones que padecían anemia grave, y el número de muertes en 272.000, o el 67% de la mortalidad mundial por paludismo.
Clínicamente, los ataques simples de malaria en los niños se presentan en forma de trastornos digestivos y respiratorios, cuya gravedad depende del tipo de Plasmodium y del estado genético, nutricional e inmunológico del niño.
Las formas graves, relacionadas con P. falciparum con más del 4% de parasitemia, pueden combinar paludismo cerebral, dificultad respiratoria , anemia grave, hipoglucemia e infecciones bacterianas secundarias; y con menos frecuencia insuficiencia renal en comparación con los adultos.
La malaria cerebral infantil se manifiesta con mayor frecuencia por convulsiones, una postura anormal en extensión ( opistótonos ), que puede complicarse con hipertensión intracraneal que progresa a un coma con retinopatía específica de la malaria, lo que hace posible distinguir el coma por paludismo de otros coma.
La mayoría de los niños sale del coma en 48 horas sin secuelas, pero el 20% muere a causa de él y el 10% tiene secuelas neurológicas o retrasos cognitivos .
Países desarrolladosEs una malaria importada. En Francia, el país europeo más afectado, los niños representan el 15% del total de casos notificados, o casi mil niños por año, de los cuales el 10% son lactantes. Más del 80% de estos casos infantiles se deben a P. falciparum .
Los bebés afectados suelen ser migrantes de segunda generación que regresaron de vacaciones al país de origen de sus padres, principalmente en el África subsahariana. La malaria en los lactantes es más grave que en los niños. En los años 2000-2009, la ausencia de mortalidad infantil en Francia probablemente indica una atención adecuada en la gran mayoría de los casos.
En 2014, los Estados Unidos notificaron 1.513 casos de malaria importada, incluidos 55 casos de malaria importada en niños menores de 5 años (1 caso de malaria congénita) y 241 casos en menores de 18 años. El 85% de los casos infantiles regresaron de un viaje a África.
Paludismo por transfusión
Los plasmodios , resistente a una temperatura de 4 ° C durante varios días, se pueden transmitir por transfusión de sangre de la sangre almacenada y fortiori un sangre fresca.
Clínicamente, el paludismo por transfusión se asemeja al paludismo de invasión primaria, pero la incubación más prolongada para todas las especies de Plasmodium, P. falciparum y P. malariae está implicada con mayor frecuencia (45 y 30% respectivamente en los casos no endémicos).
MundoEn áreas endémicas, el paludismo por transfusión es frecuente pero benigno debido a la semiinmunidad de los receptores a quienes, además, en ocasiones se les ofrece tratamiento antipalúdico.
La mayor prevalencia de paludismo entre los donantes de sangre se observa en África. Utilizando técnicas moleculares: rondaría el 36% en África, mientras que es del 4% en Asia, del 2% en América y del 1% en Europa.
Los criterios de hemovigilancia de la malaria son propuestos por la OMS y adaptados por cada país de acuerdo con las recomendaciones nacionales. Algunos países, como los Estados Unidos, utilizan un cuestionario para clasificar a los donantes de sangre potencialmente infectados. Otros, como Francia, el Reino Unido o Australia, utilizan pruebas serológicas adicionales sobre la base de este cuestionario.
En la década de 1970, en países no endémicos, se produjeron dos notables "epidemias de transfusión" de paludismo en países no endémicos, en los Estados Unidos por donantes veteranos de Vietnam y en 1971 en España: 54 casos de paludismo por transfusión por P. vivax , vinculado a un único banco de sangre en Barcelona .
FranciaEn la Francia continental (centros de transfusión de Marsella y Niza ), en los años 1960-1970, se produjo un aumento de dicha transmisión, vinculado a un cribado insuficiente de los donantes de sangre. Al principio del XXI ° siglo, este riesgo se considera bajo, advertido por los donantes rechazados después de una estancia reciente en los países endémicos (en menos de 6 meses, de acuerdo con los estándares europeos) y las pruebas biológicas (serología malaria).
Más específicamente en Francia 2019, los candidatos a la donación considerados en riesgo son: 1) personas con antecedentes de malaria, 2) personas con una fiebre no diagnosticada que sugiera un ataque de malaria dentro de los 4 meses posteriores al regreso de una zona de malaria. 3) personas que se han quedado en una región en riesgo, y 4) personas que son nativas o que han vivido durante más de 6 meses consecutivos en una región en riesgo. Los donantes en riesgo se posponen temporalmente para la donación de sangre; el período de ejecución hipotecaria es de 4 meses o 3 años dependiendo de las circunstancias.
Los hemoderivados con mayor riesgo son los concentrados de glóbulos rojos, mientras que el plasma, que no contiene glóbulos rojos, se considera de bajo riesgo. Los donantes asintomáticos conocidos como inmunosilencimiento (ausencia de anticuerpos en ciertos portadores crónicos de parásitos) representan un riesgo residual. En Francia 2019, la probabilidad de paludismo postransfusional es de 0,2 a 0,5 casos por millón de transfusiones, en comparación con 1 a finales de la década de 1990. Entre 2000 y 2019, se notificaron 4 casos de paludismo postransfusional. En Francia, todos relacionados a donaciones de sangre de una persona de una zona endémica. En tres de estos casos, la especie involucrada fue P. falciparum y los receptores infectados murieron.
Paludismo por inoculación
Puede ser una malaria por accidente de exposición a sangre , durante una inyección en el personal de enfermería, o intercambio de jeringas contaminadas entre drogadictos.
La inoculación puede ser voluntaria o "controlada". Históricamente, la inoculación de P. vivax o P. malariae se utilizó como un medio terapéutico contra los neurosífilis en el primer tercio de la XX XX siglo.
Al final de la XX XX siglo, la inoculación de P. falciparum se utiliza en los EE.UU. en voluntarios durante los ensayos de vacunación o estudios de cepas resistentes a los antimaláricos.
En 2018, la inoculación de Plasmodium conocida como Infección de paludismo humano controlado en voluntarios es un medio de investigación experimental de nuevos medicamentos o vacunas contra la malaria.
Tratos
En las zonas endémicas, el tratamiento suele ser insatisfactorio y la tasa global de mortalidad de todos los casos de malaria puede llegar a uno de cada diez. El uso masivo de terapias obsoletas, medicamentos falsos y la mala historia de los síntomas son los responsables de la mala evolución clínica.
Tratamientos antiguos
El endoparásito puede ser combatido por diferentes moléculas tanto en tratamientos curativos como en profilaxis . Estas diferentes terapias son más o menos efectivas según la región y la tasa de resistencia adquirida porque, como el DDT (el insecticida más utilizado en la década de 1960), los medicamentos que eran efectivos hace treinta años, como la cloroquina , ya no lo son. .
Sin embargo, estas formulaciones obsoletas todavía se utilizan ampliamente en los países afectados. Al ser parte del tercer mundo , no tienen los medios para migrar su protocolo de tratamiento a una herramienta más cara como el uso de ACT ( terapia combinada basada en artemisinina ). Durante mucho tiempo, los tratamientos han utilizado cloroquina, quinina y SP (sulfadoxina- pirimetamina ) y en menor medida mefloquina , amodiaquina y doxiciclina .
Estas moléculas fueron armas muy efectivas en la lucha contra los parásitos de la malaria pero su prescripción sin control ha favorecido la aparición de cepas resistentes . Según la Organización Mundial de la Salud (OMS), el tratamiento es eficaz si la tasa de fracaso es inferior al 5%; si supera el 25%, se debe cambiar el protocolo.
Se ha dado prioridad a la cloroquina desde hace mucho tiempo. Al alimentarse de la hemoglobina , el parásito la descompone en aminoácidos , que liberan las moléculas de hemo contenidas en la hemoglobina, tóxicas para el propio parásito, que transforma y almacena en su vacuola digestiva como cristales inertes. La cloroquina entra en la célula infectada y detiene la transformación protectora del hemo en cristales inertes, provocando la acumulación de este hierro tóxico. El parásito muere así por sus propios desechos.
Era un fármaco que tenía muchas ventajas, incluido su bajo costo y la ausencia de efectos secundarios. En la actualidad, más del 25% de la atención basada en cloroquina falla en los países del África subsahariana afectados por la malaria. Sin embargo, todavía están empleados.
Esta resistencia se debe al alelo mutante PfCRT ( Transportador de resistencia a la cloroquina de Plasmodium falciparum ) K76T. Esta mutación drena la cloroquina de la célula infectada, pero conduciría a una peor adaptación del parásito a su entorno. El Malawi es el primer país africano que han abandonado la cloroquina, comenzando en 1993 , lo que lleva a una reaparición de las cepas sensibles a continuación, volver a ser altamente mayoría.
Cuando la cloroquina ya no funciona, se utiliza un medicamento llamado "medicamento de segunda línea": EM (como Fansidar ( sulfadoxina / pirimetamina (en) ) producida por Roche ). Esta molécula evita la resistencia a la cloroquina. Solo cinco años bastaron para que aparecieran cepas resistentes. A continuación, adapta la terapia utilizando un "fármaco de 3 e intención": la quinina , administrada por vía oral en los casos leves o por infusión en los casos agudos. Sin embargo, estos tratamientos también se enfrentan a una nueva resistencia del parásito.
ACTUAR
La terapia de combinación basada en artemisinina en francés terapia de combinación basada en artemisinina y acrónimo ACT , es una terapia y prevención terciaria en casos de malaria no complicada . Está compuesto por la asociación de dos moléculas : una molécula semisintética derivada de la artemisinina y una molécula sintética cuya función es aumentar el efecto de la primera molécula pero también retrasar la aparición de resistencias y, por tanto, tratar mejor la malaria.
Desde la finalización exitosa, en 2001 , de los ensayos clínicos de fase III del primer ACT jamás desarrollado, se ha convertido en el único tratamiento médico recomendado por la Organización Mundial de la Salud para combatir esta enfermedad.
Producidos en cantidades relativamente pequeñas, los fármacos ACT son más caros que la cloroquina . Un tratamiento con cloroquina o con EM cuesta actualmente entre 0,2 y 0,5 dólares por , Mientras que un tratamiento con ACT cuesta entre 1,2 y 2,4 dólares / , O entre cinco y seis veces más. Para muchos pacientes, esta diferencia es el precio de su supervivencia. Un precio que muy pocas personas en África pueden pagar. Solo la fabricación a mayor escala o una mayor asistencia financiera de los países ricos podrían reducir significativamente los costos de producción.
Rutas de investigación
Se exploran nuevas vías, que incluyen:
- Un camino que involucra péptidos y nuevos compuestos químicos.
Las espiroindolonas forman una nueva clase de medicamentos antipalúdicos que se están probando.
La cipargamina pertenece a esta clase con un efecto curativo prometedor por vía oral. - un tratamiento que combina uno o más mecanismos de acción nuevos, que podrían descubrirse probando una colección de compuestos sintéticos con características tridimensionales cercanas a las de los antimaláricos naturales y que aún no se han probado.
Dichos compuestos incluyen, por ejemplo, azetidinas bicíclicas que parecen (por vía oral) ser activas en dosis bajas contra todas las etapas de la vida del parásito, en varios modelos probados in vivo, y que muestran potencial para curar y / o prevenir enfermedades. las poblaciones protegen en riesgo.
Drogas falsas
A partir de medicamentos falsos supuestamente antipalúdicos circulan en Tailandia, Vietnam, Camboya y China; constituyen una causa importante de mortalidad que, no obstante, podría prevenirse. En agosto de 2007, la compañía farmacéutica china Holley-Cotec se vio obligada a retirar veinte mil dosis de su fármaco de artemisinina Duo - Cotecxin en Kenia debido a falsificaciones, originarias de Asia, que contenían muy pocos ingredientes activos e incapaces de ninguna terapia, circulaban en el mercado por un precio cinco veces menor. No existe una manera fácil para que los médicos y los pacientes puedan diferenciar un medicamento real de uno falso sin la ayuda de un laboratorio. Las compañías farmacéuticas están tratando de combatir los medicamentos falsos mediante el uso de nuevas tecnologías para asegurar el producto desde el origen hasta la distribución.
Prevención
Los métodos utilizados para prevenir la propagación de la enfermedad o para proteger a las personas en áreas endémicas incluyen la profilaxis a través de medicamentos, la erradicación de mosquitos y la prevención de las picaduras de mosquitos. Para que la malaria exista continuamente en un solo lugar, se requiere una combinación de factores: alta densidad de población, alta tasa de transmisión de humanos a mosquitos y viceversa. Si alguno de estos factores disminuye, el parásito finalmente desaparece, como en América del Norte y Europa. Por el contrario, el parásito puede reintroducirse en un área y sobrevivir allí si estos factores están presentes allí.
Actualmente no existe una vacuna contra la malaria, pero la búsqueda de una vacuna es un área muy activa.
Algunos investigadores afirman que prevenir la malaria sería más rentable que tratarla a largo plazo; pero los costos incurridos por esto son demasiado altos para los más pobres. El economista Jeffrey Sachs estima que la malaria podría controlarse con tres mil millones de dólares estadounidenses al año. Para alcanzar los Objetivos de Desarrollo del Milenio , el dinero que se asigna actualmente a la lucha contra el SIDA debería reasignarse a la prevención del paludismo, lo que beneficiaría aún más a la economía africana.
Algunos países como Brasil, Eritrea, India o Vietnam han logrado reducir el flagelo de la malaria. El análisis de estos programas muestra que muchos factores tuvieron que unirse para luchar con éxito contra la enfermedad, ya sea mediante la financiación, la acción del gobierno y de las ONG o la acción concreta.
Formas de luchar o protegerse contra los mosquitos
El vector de la malaria (hembra Anopheles) puede combatirse mediante varios medios de prevención, que pueden ser eficaces si se aplican correctamente.
El verdadero problema de esta prevención es el altísimo costo del tratamiento para las poblaciones afectadas. De hecho, puede ser eficaz en los viajeros, pero los países en desarrollo, que son las principales víctimas de esta enfermedad, están luchando por organizar acciones muy eficaces. Podemos dar como prueba el ejemplo de la isla de Reunión, donde la malaria estaba muy extendida como en las otras islas de la región ( Madagascar y Mauricio ) en particular. Al ser la Reunión un territorio francés de ultramar, el problema del costo excesivamente alto no existía y la malaria podía erradicarse de esta isla sin dificultad.
En los países interesados se aplican dos métodos de prevención. Su objetivo es, por un lado, proteger a las poblaciones de las picaduras de mosquitos y, por otro, eliminarlas mediante la implementación de diversos medios. El principal objetivo de esta profilaxis es limitar la población de mosquitos vectores de la enfermedad y así intentar erradicar este flagelo.
En la década de 1960 , el principal método utilizado para erradicar las hembras de Anopheles fue el uso intensivo de insecticidas . El más utilizado fue el DDT (Dicloro-Difenil-Tricloroetano). Este método dio sus frutos en muchas áreas donde la malaria fue completamente erradicada. Sin embargo, el uso intensivo de DDT ha favorecido la selección de mosquitos resistentes. Esta resistencia se ha denominado KDR ( Knock Down Resistance ). Además, puede causar intoxicaciones y enfermedades en la población, como fue el caso en la India, donde se abusaba de ella en la agricultura. Aunque este producto ha sido totalmente prohibido en Europa desde 1972 y que, desde 1992 , ha sido clasificado por la OMS como COP (contaminante orgánico persistente), esta organización parece, no obstante, estar invirtiendo su posición al abogar por nuevas recomendaciones sobre el uso de este plaguicida (uso exclusivo destinado a la lucha contra la malaria en el interior de los edificios). Los cuatro criterios de la OMS son:
- Toxicidad : Se acusa al DDT de ser potencialmente cancerígeno y de ser capaz de modificar el funcionamiento nervioso y hormonal humano (efectos sobre el metabolismo de los estrógenos en las mujeres, efectos antiandrogénicos).
- persistente : su vida media es de quince años, es decir, si pulverizamos 10 kg en un campo, quince años después, quedarán 5 kg , después de treinta años 2,5 kg y así sucesivamente;
- dispersivo : se ha encontrado en las nieves del Ártico ;
- bio acumulativo : los animales que lo absorben no mueren por ello, pero no logran eliminarlo. Lo almacenan en su grasa y se encuentra en altas concentraciones en animales en la parte superior de la cadena alimentaria. Por otro lado, su toxicidad está sujeta a debate aunque una ingestión de 35 g puede ser letal para una persona de 70 kg (como en el caso del ibuprofeno por ejemplo y en comparación con los 225 g de sal o 120 g de café).
Sin embargo, no se ha probado la toxicidad del DDT.
Para reemplazar al DDT, son posibles medios alternativos para combatir el vector de la malaria:
- drenaje de las marismas (sin alterar el sistema ecológico), drenaje de agua estancada donde se desarrollan las larvas de anofeles (un neumático viejo abandonado y lleno de agua por las lluvias es suficiente para que el mosquito ponga sus huevos allí);
- control de larvas mediante la difusión de petróleo o aceite vegetal y el uso de insecticidas solubles esparcidos sobre la superficie del agua estancada, para intentar limitar los nacimientos de anofeles o evitar que las larvas lleguen a respirar en la superficie. Medidas muy indeseables porque son totalmente anti-ecológicas;
- siembra de aguas con depredadores de Anopheles o sus larvas como ciertos moluscos o peces ( tilapia , guppies , gambusies , aphanius );
- reintroducción y protección de variedades de murciélagos insectívoros donde han desaparecido (un murciélago puede tragar casi la mitad de su peso en insectos durante la noche);
- dirigido a la secuenciación del genoma del mosquito. Este genoma ofrece, entre otras cosas, un catálogo del aumento de genes de desintoxicación y genes mutantes que codifican las proteínas a las que se dirigen los insecticidas, así como las variaciones de nucleótidos individuales, llamados polimorfismos de nucleótidos, que se encuentran en el genoma:
- uso de repelentes de insectos e insecticidas dirigidos únicamente contra los anofeles,
- dispersión de machos anofeles estériles en la naturaleza,
- intervenciones genéticas sobre especies de vectores o, en un futuro indefinido, con vacunas que bloqueen la transmisión al inducir anticuerpos que impidan la maduración de las etapas sexuales del parásito en Anopheles.
- Antiparasitario oral. La ivermectina aumenta la mortalidad de los mosquitos cuando pican, durante al menos 28 días.
Estas medidas solo son efectivas en un área limitada. Es muy difícil aplicarlos a la escala de un continente como África.
Todos, individualmente, pueden prevenir las picaduras de anofelino mediante medidas mecánicas, físicas y químicas; Recordemos sobre todo que los anofeles tienen una actividad nocturna, comienzan a picar al anochecer y descansan durante el día en los hogares:
- instalación de mosquiteras (malla inferior a 1,5 mm ) impregnadas de permetrina o derivados piretroides . Cada vez más, estos mosquiteros se proporcionan a precios muy asequibles (máximo USD 1,70 ) o incluso de forma gratuita a las poblaciones de las zonas endémicas. Estas mallas tienen una vigencia de 3 a 5 años según el modelo y las condiciones de uso;
- instalación de mosquiteros en ventanas;
- uso de insecticidas a pequeña escala: rociado de insecticidas de interior (piretroides, DDT, etc. ) en hogares (dormitorios);
- instalación de aire acondicionado en los hogares para bajar la temperatura y agitar el aire (el mosquito detesta los movimientos del aire que lo perturban en sus movimientos y en su facultad sensorial para encontrar su objetivo);
- después de la puesta del sol: llevar ropa holgada, larga y de colores claros y abstenerse del alcohol (los anofeles se sienten tan atraídos por los colores oscuros, especialmente el negro, como por los vapores de alcohol);
- aplicación de crema repelente sobre la piel o la ropa tan pronto como se pone el sol. De todos los repelentes sintéticos, los que contienen DEET (N, N-dietil-m-toluamida) son los más eficaces. El DEET no mata a los insectos, pero sus vapores los disuaden de aterrizar o trepar sobre la persona.
Generalmente, los productos concentrados entre 25 y 30% DEET son los más efectivos durante el período más largo (± 8 horas contra insectos rastreros y de 3 a 5 horas contra Anopheles). También se consideran inofensivos para adultos o niños mayores de dos años si la concentración no supera el 10% para estos últimos. Debe evitarse en mujeres embarazadas y lactantes menores de tres meses. Los productos con una concentración superior al 30% ya no están aprobados.
Los productos vendidos deben aplicarse directamente sobre la piel o sobre la ropa o mosquiteras. Sin embargo, tenga cuidado de que alteren los plásticos, ciertos tejidos sintéticos como el nailon, el caucho, el cuero y las superficies pintadas o barnizadas. También preste atención a los ojos y a la inhalación directa con productos pulverizados, así como a la ingestión. Por tanto, se preferirán los aplicadores provistos de una bola.
La reabsorción transcutánea es del 50% en seis horas y la eliminación será urinaria. La parte no eliminada (30%) se almacenará en la piel y la grasa.
Repelentes
Los estudios han demostrado que los repelentes de eucalipto que contienen aceite de eucaliptol natural son una alternativa eficaz y no tóxica al DEET . Además, las plantas como el limoncillo han demostrado ser eficaces contra los mosquitos. Un estudio etnobotánico realizado en la región de Kilimanjaro ( Tanzania shows) que los repelentes más utilizados, por la gente local, son lamiacées género ocimée la kilimandscharicum Ocimum y suave Ocimum . El estudio sobre el uso de aceites esenciales extraídos de estas ocimeas muestra que la protección contra las picaduras de ciertos vectores anofelinos de la malaria aumenta en un 83 a 91% de los casos e inhibe, en el insecto, su deseo de succionar en un 71,2 a 92,5% de los casos. .
También se recomiendan otras soluciones naturales. Así, según un estudio realizado por el Ministerio de Salud Pública de Camerún, el acto de frotar la piel con especies de plantas herbáceas bianuales de la familia de las Amaryllidaceae , como las cebollas y los ajos, disminuiría la tasa de picadura de 71 en un 79%. Este tipo de tratamiento preventivo se recomienda encarecidamente para personas que siguen una dieta vegetariana y que pueden tener deficiencias de hierro y proteínas, una fuente de succión en el insecto.
Icaridin, también conocido como KBR 3023, es un nuevo repelente de la familia química de las piperidinas y comparable en fuerza al DEET, pero es menos irritante y no disuelve los plásticos. Fue desarrollado por la empresa química alemana Bayer AG y comercializado con el nombre SALTIDIN. La forma de gel con un 20% de producto activo es actualmente la mejor. Tenga cuidado, a pesar de todo, aún no se conocen todos los posibles efectos secundarios con respecto a los niños.
Una prueba de varios repelentes, lanzada al mercado por una organización de consumidores independiente, encontró que los repelentes sintéticos, incluido el DEET, eran más efectivos que los repelentes con sustancias activas naturales.
- uso de permetrina ((3-fenoxifenil) metil) o derivados de piretroides . Son repelentes pero también se pueden clasificar entre los insecticidas. Si repelen e irritan al mosquito, crean una acción de derribo sobre él que lo mata o lo neutraliza directamente.
No usar directamente sobre la piel sino impregnar la ropa o los mosquiteros, cuidando de no irritar las mucosas nasales ni ingerirlos durante la manipulación. La duración de la eficacia es de unos 6 meses (menos en prendas sujetas a roces, lluvia, etc.). La reimpregnación se realiza después de lavar con jabón.
Precaución: No use ropa impregnada con permetrina sobre la piel ya tratada con DEET.
Mujeres embarazadas
El último método implementado es mucho más específico. Efectivamente solo se aplica a mujeres embarazadas, y su finalidad es evitar un embarazo esmaltado con problemas por contracciones prematuras y permitir que los bebés nazcan con buena salud y no con un peso demasiado bajo (sobre todo si se trata de una primípara ) o incluso sufre de muchas enfermedades como la malaria placentaria (infección congénita, o no, está directamente relacionada con la cantidad de parásitos en la placenta ), anemia severa y malformaciones del bebé.
Para prevenir y prevenir complicaciones graves, se ha puesto en marcha una atención integral que incluye la prevención de la malaria y la protección de la salud. Estas acciones tienen como objetivo limitar las infecciones y sus consecuencias que pueden ser muy graves para el niño y la madre. Estos incluyen el uso de mosquiteros tratados con insecticida y el uso de medicamentos contra la malaria, ya sea como profilaxis primaria o como tratamiento intermitente.
Por otro lado, no solo se ha comprobado que el tratamiento intermitente de mujeres embarazadas con la combinación de fármacos SP (sulfadoxina-pirimetamina) una vez en el segundo trimestre y una segunda vez en el tercer trimestre reduce el riesgo de anemia. madre, parasitemia placentaria y bajo peso al nacer, pero también que el tratamiento sistemático con SP de los niños de 2, 3 y 9 meses, durante las vacunaciones, redujo en un 60% los episodios de paludismo clínico y en un 50% los episodios de anemia perniciosa.
En áreas endémicas, se ha demostrado que la prevención eficaz del paludismo durante el embarazo reduce la incidencia de anomalías como bajo peso al nacer o anemia materna grave (disminución de la concentración de hemoglobina en la sangre, por debajo de 0,13 g / ml en hombres y 0,12 g / ml en mujeres). ).
La aplicación de estas pocas reglas sería suficiente para reducir considerablemente el número de personas afectadas por esta enfermedad y, por tanto, el número de víctimas, pero la falta de medios dificulta su aplicación. Muchos residentes ni siquiera pueden pagar los mosquiteros, que pueden reducir el riesgo de infección.
[árbitro. necesario]Profilaxis
Para prevenir cualquier contaminación entre los turistas que viajan a países donde abunda la malaria, los investigadores han implementado una técnica profiláctica . Esta técnica consiste en utilizar un arsenal terapéutico de fármacos preventivos (limitado a la cloroquina, proguanil, la pirimetamina - dapsona combinación, el proguanil- atovacuona combinación, la cloroquina-proguanil clorhidrato de combinación , mefloquina y doxiciclina) para prevenir la infección si el parásito entra en el cuerpo .
Se recomienda tomar tratamiento preventivo con regularidad, especialmente para los niños y las mujeres embarazadas, que tienen un mayor riesgo de padecer paludismo grave, para estancias breves en áreas de transmisión intensa del paludismo. Pero debido al aumento de la resistencia a los medicamentos parasitarios (resistencia de los parásitos a los productos que constituyen el arsenal terapéutico) y los efectos secundarios específicos de los distintos productos, es cada vez más difícil establecer pautas quimioprofilácticas.
Los medicamentos antipalúdicos no garantizan una protección absoluta contra la infección y también es importante protegerse de las picaduras de mosquitos (mosquiteros, repelentes de mosquitos) porque incluso si se ha seguido correctamente un tratamiento adecuado, es posible tener una malaria, a veces de aparición tardía debido a a la forma de hipnozoito que puede tomar Plasmodium .
En Bélgica , cada año se producen casos de muerte por paludismo entre los viajeros que regresan.
Regímenes profilácticos antipalúdicosA partir del 9 de marzo de 2006, la prevención de la malaria se organizó en tres niveles, clasificados según el nivel de quimio-resistencia. Por tanto, cada país en riesgo se clasifica en un grupo. Mucho antes de salir de viaje, es recomendable buscar el consejo de su médico porque estos tratamientos generalmente se inician con anticipación.
País del grupo 0 Zonas libres de malaria: no quimioprofilaxis.- África : Lesotho , Libia , Marruecos , Reunión , Île Sainte-Hélène , Seychelles y Túnez ;
- América : todas las ciudades, Antigua y Barbuda , Antillas Holandesas , Bahamas , Barbados , Bermuda , Canadá , Chile , Cuba , Dominica , Estados Unidos , Granada , Islas Caimán , Islas Malvinas , Islas Vírgenes , Jamaica , Martinica , Puerto Rico , Santa Lucía , Trinidad y Tobago y Uruguay ;
- Asia : todas las ciudades, Brunei , Georgia , Guam , Hong Kong , Isla de Navidad , Islas Cook , Japón , Kazajstán , Kirguistán , Macao , Maldivas , Mongolia , Turkmenistán , Singapur y Taiwán ;
- Europa : todos los países, incluidos Armenia , Azores , Islas Canarias , Chipre , Rusia , Estados bálticos , Ucrania , Bielorrusia y Turquía en Europa;
- Cercano y Medio Oriente : todas las ciudades, Bahrein , Israel , Jordania , Kuwait , Líbano y Qatar ;
- Oceanía : todas las ciudades, Australia , Fiji , Hawái , Islas Marianas , Islas Marshall , Estados Federados de Micronesia , Nueva Caledonia , Nueva Zelanda , Isla de Pascua , Polinesia Francesa , Samoa , Tonga y Tuvalu .
- África : Argelia , Cabo Verde , Egipto , Eritrea y Mauricio ;
- Asia : Azerbaiyán , Norte de Corea , Corea del Sur y Uzbekistán ;
- Cercano y Medio Oriente : Emiratos Árabes Unidos , Omán , Siria y Turquía .
Doxiciclina (ingrediente activo)
un comprimido de 100 mg al día, un día antes de la salida (dos veces el primer día) y hasta 28 días después del regreso o después de salir de la zona endémica de malaria (para tomar sentado con una gran cantidad de líquido o durante la comida ). Las dosis deben reducirse a la mitad para los niños mayores de ocho años. La doxiciclina se puede tomar durante varios meses, pero puede causar fototoxicidad (reacción química causada por la presencia de demasiada sustancia fotorreactiva en la piel y que reacciona bajo la acción de los rayos UV o visibles) e infecciones por hongos orales y genitales; no debe ser utilizado por mujeres embarazadas (trastornos hepáticos) o en período de lactancia, así como en niños menores de 8 años (ralentización reversible del crecimiento óseo y tinción amarilla irreversible de los dientes con mayor riesgo de caries) Es un derivado de la tetraciclina (un antibiótico con cuatro ciclos contiguos capaz de penetrar en las células eucariotas , incluido Plasmodium ) que a veces se usa contra la malaria en combinación con quinina para el tratamiento intravenoso de emergencia.La mefloquina o Lariam ( Roche )
Composición: 250 mg de mefloquina Caja de ocho comprimidos - 34,26 EUR (Precio en Bélgica en 2012) Un comprimido por semana, unas semanas antes de la salida y hasta cuatro semanas después del regreso. Para obtener una concentración sanguínea eficaz de Lariam a la llegada, es necesario iniciar el tratamiento dos o tres semanas antes de la salida. Las personas que nunca hayan tomado este producto antes deben comenzar el tratamiento dos o tres semanas antes de la salida, para verificar posibles efectos secundarios (mareos, insomnio, pesadillas, excitación, ansiedad inexplicable, palpitaciones). No se prescribirá si el médico estima que existe una contraindicación (deseo de embarazo, primer trimestre de embarazo, epilepsia, depresión o arritmias para las que se está en tratamiento con fármacos como betabloqueantes, bloqueantes de los canales de calcio o digitálicos). , o si no ha sido tolerado en el pasado. El tratamiento debe continuarse hasta cuatro semanas después del regreso. Si Lariam se tolera bien, se puede tomar durante meses o incluso años si es necesario. Para estadías prolongadas (duración superior a tres meses), la quimioprofilaxis debe mantenerse el mayor tiempo posible y se recomienda a los viajeros que se comuniquen rápidamente con un médico en el lugar para evaluar la relevancia y el beneficio / riesgo de la quimioprofilaxis.La combinación de atovacuona-proguanil como Malarone ( GlaxoSmithKline ) se puede recomendar como alternativa a la mefloquina.
Composición para adultos: 250 mg de atovacuona + 100 mg de hidrocloruro de proguanil Caja de doce comprimidos - 44,14 EUR (precio en Bélgica en 2012) Composición para junior: 62,5 mg de atovacuona + 25 mg de hidrocloruro de proguanil Caja de doce comprimidos - 18,48 EUR (precio en Bélgica en 2012) Una tableta al día, un día antes de la salida y hasta siete días después de la devolución. Si la primera toma solo comienza durante la estadía, debe tomarse hasta cuatro semanas después del regreso. Para un viaje corto, tomar Malarone, que suele ser muy bien tolerado, es una excelente opción. Se puede utilizar durante varios meses (pero luego habrá que tener en cuenta su elevado coste). Sin embargo, la duración de la administración continua de atovacuona-proguanil en esta indicación debe limitarse a tres meses, por falta de un seguimiento suficiente hasta la fecha en el tratamiento prolongado.En cualquier caso, el consejo de un médico es más que deseable antes de cualquier medicación.
Una tecnología que utiliza SMS acaba de ser probada con éxito en Tanzania .
Esta operación, denominada SMS for Life, consiste en evitar el desabastecimiento de medicamentos contra la malaria, el sida y la tuberculosis en un lugar determinado, incluso el más remoto, mediante la interacción entre un servidor informático y teléfonos móviles .
Para subir
La investigación tanto en farmacología para tratamientos (ver sección detallada " El futuro - Farmacología ") como en vacunación para profilaxis (ver sección detallada " Vacunas ") avanza a un ritmo cada vez más acelerado gracias a patrocinadores como la Malaria Vaccine Initiative u ONG como MSF .
Precauciones a tomar
Tomar medicamentos contra la malaria, incluso con el régimen de tratamiento correcto, no es suficiente para protegerse al cien por cien del riesgo de malaria. También es necesario protegerse de los mosquitos, para evitar que entren en contacto con sus víctimas, para evitar la picadura del insecto:
- evite viajar en zonas de riesgo sin protección, duerma siempre con una mosquitera con malla de menos de 1,5 mm , incluso bajo las estrellas;
- use ropa larga, holgada, blanca, ajustada en las muñecas y los tobillos, con zapatos cerrados, impregnados con repelente (tenga cuidado, el mosquito Anopheles a menudo vuela bajo y puede picar a través de los calcetines);
- aplique repelentes de piel en todas las partes descubiertas del cuerpo (basado en DEET, pero debe evitarse en bebés menores de 3 meses y mujeres embarazadas o en período de lactancia);
- use insecticidas, en interiores, pero también en exteriores;
- dormir con aire acondicionado o debajo de un mosquitero (preferiblemente impregnado con insecticida cuando el cuerpo, por la noche, pueda estar en contacto con este mosquitero): el ser humano actúa así como cebo y además de la barrera mecánica del mosquitero impidiendo la picadura, provoca la muerte del mosquito que ha entrado en contacto con el insecticida;
- proteja todas las aberturas con mosquiteros adecuados.
El uso de repelentes o repelentes de insectos (como DEET o DDT ) y mosquiteros reduce el riesgo de infección, pero la quimioprofilaxis sigue siendo esencial ( Nivaquine , Savarine, Lariam, Malarone). No se recomienda beber alcohol mientras toma estos medicamentos.
Consecuencias económicas
Según la Ligue contre le malaria, una familia afectada solo cosecharía el 40% de su producción agrícola, debido a los días laborales perdidos. La OMS incluso ha calculado que el PIB de África superaría su nivel actual en 115.000 millones de euros, o un 32% adicional, si la malaria se hubiera eliminado hace 35 años.
En cuanto a la lucha, UNICEF estima que el coste medio anual de los programas antimaláricos en cada país africano rondaría los 345.000 euros, o, para un país de cinco millones de habitantes, menos de siete céntimos de euro per cápita.
Las poblaciones ubicadas en áreas palúdicas que viven en su gran mayoría en la pobreza, los nuevos medicamentos, mucho más efectivos pero más costosos que los antiguos, a menudo están más allá de sus posibilidades.
A veces incluso ocurre que un paciente no sigue completamente su tratamiento y, sintiéndose curado, va a vender lo que le queda en el mercado negro, acelerando así la aparición de resistencias a los tratamientos (ver capítulo sobre la resistencia del parásito ).
Según las cifras, el sector privado gastó en 1990 y por víctima 789 dólares en la lucha contra el asma , 3.274 dólares en el sida (cuyo virus afecta tanto a países en desarrollo como desarrollados) y sólo 65 dólares a la malaria. En otras palabras, la cantidad gastada en la investigación de vacunas y el desarrollo de medicamentos antipalúdicos es mínima si consideramos que casi el cincuenta por ciento de la población mundial está en riesgo.
Además, la gran mayoría de los países afectados por la malaria no tienen ni los medios económicos ni los medios tecnológicos para desarrollar una verdadera investigación en el campo médico en su país. Países con medios financieros muy limitados (la mayoría de las veces se derrumban bajo el peso de la deuda externa), falta de voluntad política sólida, un presupuesto de investigación muy por debajo de las expectativas y una ayuda internacional irrisoria en comparación con las necesidades de la población y el número de personas afectadas, recuerde que las desastrosas consecuencias de esta enfermedad del subdesarrollo no se deben enteramente a la naturaleza, que el ser humano tiene mucho que ver con ella.
Sin embargo, en 2001 la OMS fundó un Fondo Mundial para luchar contra la malaria, pero también contra el SIDA y la tuberculosis .
Desde 2003, la Fundación Bill y Melinda-Gates también ha donado varios cientos de millones de dólares, entre otros, a la Iniciativa de Vacuna contra la Malaria , para combatir la enfermedad.
Creado en 2002, el Fondo Mundial de Lucha contra el SIDA, la Tuberculosis y la Malaria , o Fondo Mundial, reúne fondos internacionales para el tratamiento de la malaria.
Diverso
- En Francia , esta enfermedad está en la lista de Enfermedades Infecciosas de notificación obligatoria .
- La malaria se ilustraba a menudo en sellos. El primer ejemplo es un sello benéfico mexicano emitido en 1939 que muestra a un ser humano víctima de un mosquito gigante. Pero lo más espectacular fue el tema realizado en 1962, simultáneamente en cien países celebrando la campaña de la OMS titulada Erradicación del paludismo . La OMS ha hecho de la erradicación del paludismo una de sus principales prioridades.
- La novela El cromosoma de Calcuta de Amitav Ghosh (ed. Seuil 1998, coll. Cadre vert) da un lugar importante al relato, en una atmósfera fantástica, del descubrimiento de Ronald Ross sobre la malaria.
- Una película de televisión anglosajona estrenada en 2013 Mary and Martha: Two Mothers Courage habla de la lucha de dos madres contra la malaria (o malaria).
Notas y referencias
- (fr) Este artículo está tomado parcial o totalmente del artículo de Wikipedia en inglés titulado " Malaria " ( ver la lista de autores ) .
- (en) Organización Mundial de la Salud , informe de la malaria Mundial 2020 , Ginebra, Organización Mundial de la Salud,2020, 300 p. ( ISBN 978-92-4-001580-7 , leer en línea )
- Definiciones lexicográficas y etimológicas de "malaria" de la tesorería computarizada del idioma francés , en el sitio web del Centro Nacional de Recursos Textuales y Léxicos
- Definiciones lexicográficas y etimológicas de “malaria” de la tesorería computarizada del idioma francés , en el sitio web del Centro Nacional de Recursos Textuales y Léxicos
- Gérard Duvallet ( dir. ), Entomología médica y veterinaria , IRD - Quae,2017( ISBN 978-2-7099-2376-7 ) , pág. 210
- (in) AA Escalante OF Freeland, WE Collins y AA Lal, " La evolución de los parásitos de la malaria en primates basada en el gen que codifica el citocromo b mitocondrial del genoma lineal " , PNAS , vol. 95, n o 14,1998, p. 8124-8129 ( leer en línea )
- (en) Weimin Liu, Yingying Li, Learn GH et al. , “ Origen del parásito de la malaria humana Plasmodium falciparum en gorilas ” , Nature , vol. 467,2010, p. 420–425 ( leer en línea )
- (en) Frederick L. Dunn, malaria , Cambridge, Cambridge University Press ,1993, 1176 p. ( ISBN 0-521-33286-9 ) , pág. 860-862.en The Cambridge Word History of Human Disease, KF Kiple (eds).
- (en) Joy D, Feng X, Mu J. et al. "Origen temprano y expansión reciente de Plasmodium falciparum " Science , vol. 300, número 5617, pág. 318-21 , 2003.
- (in) Andreas Nerlich, Paleopatología y Paleomicrobiología de la malaria , ASM Press,2016, 212 p. ( ISBN 978-1-55581-916-3 ) , pág. 155-159en Paleomicrobiología de los seres humanos, M. Drancourt y D. Raoult (eds.).
- (in) La malaria mató a la mitad de las personas que han vivido
- (in) ¿La malaria realmente mató a la mitad de todos los que vivieron?
- (en) F. Cox "Historia de parasitología humana" Clin Microbiol Rev . 2001, vol. 15, n o 4, p. 595-612.
- " Tutankhamon habría sucumbido a la malaria y una enfermedad de los huesos ", Le Monde .fr ,16 de febrero de 2010( leer en línea )
- (en) Z. Hawass, YZ Gad, S. Ismail et al., " Ascendencia y patología en la familia del rey Tutankhamon " , JAMA , vol. 303, n o 7,febrero 2010, p. 638-647 ( DOI 10.1001 / jama.2010.121 )
- (en) Paul U. Unschuld , Medicina en China: una historia de ideas (estudios comparativos de sistemas de salud y atención médica) , University of California Press ,16 de abril de 2010, 2 nd ed. , 464 p. , Edición revisada ( ISBN 978-0-520-26613-1 y 0-520-26613-7 , leer en línea )
- La historia de la malaria, una enfermedad antigua . En el sitio del Centro para el Control y la Prevención de Enfermedades .
- (en) R. Sallares, A. Bouwman, C. Änderung, " La propagación de la malaria al sur de Europa en la antigüedad: nuevos enfoques para viejos problemas " , Historia médica , vol. 48, n o 3,1 er de julio de de 2004, p. 311-28 ( leer en línea )
- (en) " La búsqueda de la quinina: los que ganaron las batallas y los que ganaron la guerra ". Por T. Kaufman y E. Rúveda, en Angew Chem Int Ed Engl , vol. 44, n o 6, p. 854-885 , 2005.
- (en) E. Yalcindag et al , " Múltiples introducciones independientes de Plasmodium falciparum en América del Sur " , PNAS , vol. 109, n o 210 de enero de 2012, p. 511-516 ( DOI 10.1073 / pnas.1119058109 )
- (in) R. Kyle y Mr. Shampe "Descubridores de la quinina" Vuelo JAMA 1974 . 229, n o 4, p. 462 .
- Jean-Paul Bado, Medicina colonial y grandes endemias en África 1900-1960 , Ediciones Karthala ,1996
- (En) " Historia de las contribuciones militares de Estados Unidos al estudio de la malaria " . Por Christian F. Ockenhouse (ed.).
- (en) Biografía de Alphonse Laveran . En la Fundación Nobel .
- Página sobre Ettore Marchiafava .
- Lénaick Ollivier del Instituto de Medicina Tropical del Servicio de Salud del Ejército (IMTSSA Marsella), citado por Le Figaro de 10 de junio de 2008, página 16.
- (en) Biografía de Ronald Ross , en The Nobel Foundation .
- (en) Ross y el descubrimiento de que los mosquitos transmiten los parásitos de la malaria . En el sitio del Centro para el Control y la Prevención de Enfermedades .
- “ Fiebres de ayer, la malaria de hoy. Vida y muerte por enfermedad ”. Por Chantal Beauchamp, en Annales. Economías, Sociedades, Civilizaciones . 43 ª año, n o 1, 1988, p. 252-253 .
- (en) " Plasmodium vivax (Grassi y Feletti, 1890) " .
- (en) L. Pauling, Itano H., SJ Singer e I. Wells, " Anemia de células falciformes, una enfermedad molecular " , Science , vol. 110,Noviembre de 1949( leer en línea [PDF] )
- La quimioterapia de la malaria , bajo la dirección de recursos humanos Negro, Craig J. Canfield, DF Clyde W. Peters y WH Wernsdorfer, 2 ª ed., Organización Mundial de la Salud, Ginebra, 1984, p. 13
- Ernest Fourneau , Jacques y Thérèse Tréfouël y Germaine Benoit , “ Preparativos para ensayos terapéuticos. IV. Derivados quinoléicos y quinolina arsínica ”, Ann. Inst. Pasteur , n o 44,1930, p. 719.
- Ernest Fourneau , Jacques y Thérèse Tréfouël , Georges Stefanopoulo , Yvonne de Lestrange y Germaine Benoit , “ Contribución a la quimioterapia de la malaria: ensayos sobre la malaria canaria ”, Ann. Inst. Pastor , vol. 44,1930, p. 503-533 ( resumen ).
- Ernest Fourneau , Jacques y Thérèse Tréfouël , Daniel Bovet y Germaine Benoit , “ Contribución a la quimioterapia de la malaria: ensayos sobre masillas (segunda tesis) ”, Ann. Inst. Pastor , vol. 50,1933, p. 731-744.
- Marcel Delépine , Aviso sobre la vida y obra de Ernest Fourneau (1872-1949) (extracto de Bull. Soc. Chim. Fr. ), París, Masson et C ie , sd (1950?), 90 p. , p. 61-63.
- (in) " Quimioterapia de la malaria aviar " . Adiós. K. Marshall.
- Difosfato de cloroquina .
- (en) Wall Street y el ascenso de Hitler . Por Anthony Sutton , en The Modern History Project , cap. 2 “ El Imperio de IG Farben ”. 1976.
- (in) " Biocristalización de hemozoína en Plasmodium falciparum y la actividad antipalúdica de los inhibidores de la cristalización ". Por E. Hempelmann, en Parasitol Research , vol. 100, n o 4, p. 671-676 , 2007.
- " Historia de la quinina en la lucha contra la malaria " , en el sitio del CNRS .
- (in) " Parásitos de la malaria humana en cultivo continuo ". Por Trager y Jensen, en Science , vol. 193, n o 4254, p. 673-675 , agosto de 1976.
- “ Desinformación, la malaria y el DDT ” , en afis.org .
- Daniel Vangroenweghe, "El SIDA y la sexualidad en África," OEP 2000, n o 479, p. 124-125 .
- X. Pourrut y V. Robert: "¿Ausencia de infección plasmodial en monos salvajes del norte de Senegal? » En Bull. Soc. Pathol. Exot. 2009, n o 102, 1, pág. 17-18 .
- "Un foco enzoótico de la malaria en simios" . Por SP Ramakrishnan y BN Mohan, Instituto de Malaria de la India.
- (en) G. Robert Coatney "Simian Malaria - Su importancia para la erradicación mundial de la malaria" JAMA 1963; 184 (11): 876-7.
- (en) Ward RA, Rutledge LC, Hickman RL. (1969) "Transmisión cíclica del paludismo de Chesson vivax a primates subhumanos" Nature n o 224, p. 1126-1127 , citado en The American Journal of Tropical Medicine and Hygiene .
- (in) " Demostración de hipnozoitos en una infección por Plasmodium vivax transmitida por esporozoitos ". Por Krotoski W, Collins W, Bray R, et al. , en Am J Trop Med Hyg , vol. 31, n o 6, p. 1291-1293 , 1982. Véase también " Parásitos de la malaria: descubrimiento de la forma hepática temprana ", en Nature . Por Meis J, Verhave J, Jap P, Sinden R, Meuwissen J, vol. 302, n o 5907, p. 424-6, 1983.
- Centro de estudio e investigación de médicos africanos asociado al centro hospitalario universitario y al Laboratoire de Chimie de la Coordination ( CNRS ) de Toulouse
- (en) Held J Supan C., Salazar CL, et al., " Ferroquina y artesunato en adultos y niños africanos con paludismo por Plasmodium falciparum: una fase 2, multicéntrica, aleatorizada, doble ciego, con rango de dosis, no inferioridad estudiar. ” , Lancet Infect Dis. ,2015, p. 15 (12): 1409-19
- Universidad Paul-Sabatier de Toulouse , CNRS , IRD y el Museo Nacional de Historia Natural
- Té de hierbas de quassia: un eficaz antipalúdico . Comunicado de prensa del CNRS del 11 de septiembre de 2006.
- (in) Neurymenólidos antibacterianos del alga roja de Fiji Neurymenia fraxinifolia - Resumen . Por EP Stout, AP Hasemeyer, AL Lane, TM Davenport, S. Engel, ME Hay, CR Fairchild, J. Prudhomme, K. Le Roch, W. Aalbersberg, J. Kubanek. En Org Lett. (2009); 1 de enero de 2011 (1), págs. 225-228.
- (in) " Estructura y actividad antibacteriana de los diterpenos bromados del alga roja Sphaerococcus coronopifolius - Resumen" . Por V. Smyrniotopoulos, C. Vagias, MM Rahman, S. Gibbons, V. Roussis, en Chem Biodivers , 7 de enero de 2010 (1), págs. 186-195.
- (in) Artículo de Microbe Magazine de septiembre de 2009 sobre el potencial antipalúdico de las algas rojas .
- (En) " Bromophycolides bioactivos del Reino Unido del alga roja de Fiji Callophycus serratus - Resumen" Para AS Lin EP Stout, J. Prudhomme K. Le Roch, Fairchild CR, SG Franzblau W. Aalbersberg, ME Hay y J. Kubanek. En J Nat Prod. , 26 de febrero de 2010; 73 (2), págs. 275-278.
- (en) " Comunicado de prensa GlaxoSmithKline " ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? ) (Consultado el 29 de marzo de 2013 ) de 20 de enero de 2010.
- (in) "Se ha demostrado que las bacterias intestinales de los mosquitos matan al parásito de la malaria " . Artículo del 12 de mayo de 2011 en Examiner.com.
- (in) " Refractariedad natural mediada por microbios a la infección por Plasmodium en Anopheles gambiae " - Resumen . En Sciencemag.org, artículo del 13 de mayo de 2011.
- " Malaria: la nueva droga que ataca al parásito en el hígado y en la sangre ". en el sitio santelog.com.
- Marc Mennessier, " Malaria: Sanofi sintetiza artemisinina ", Le Figaro .fr ,14 de septiembre de 2012( leer en línea )
- (in) Cochrane Reviews publicado el 19 de abril de 2006 [ (in) read online ]
- Hoja informativa: RTS, S vacuna contra la malaria ensayos clínicos . Kit de prensa del 17 de octubre de 2007 publicado conjuntamente por The PATH Malaria Vaccine Initiative (PATH / MVI) y GlaxoSmithKline Biologicals (GSK Bio) |.
- (in) Información proporcionada por el profesor Alonso sobre el RTS, S en The Lancet el 10 de diciembre de 2005.
- (in) Malaria Vaccine Initiative - sitios seleccionados para los ensayos clínicos de la fase III de la RTS, S / AS02A .
- (in) Selidji T Agnandji José F Fernandes Emmanuel B & Michael Bache Ramharter, " Desarrollo clínico de RTS, vacuna contra la malaria S / AS: una revisión sistemática de ensayos clínicos de fase I-III " , Future Microbiology ,6 de octubre de 2015( leer en línea )
- (en) R. Audran Lurati F. Ruiz, B. Genton ET Blythman, O. Ofori-Anyinam, C. Reymond, G. y F. Corradin Spertini, " El péptido sintético de Plasmodium falciparum circumsporozoite PfCS102 tiene un candidato a la vacuna contra la malaria: Un ensayo de fase I controlado y aleatorizado ” , PLOS ONE ,2 de octubre de 2009( DOI 10.1371 / journal.pone.0007304 )
- prensa del Institut Pasteur .
- (in) Battling Malaria: Fortalecimiento del programa militar de vacunación contra la malaria de EE. UU . Por Instituto de Medicina - Informe del 25 de mayo de 2006.
- (en) Los ensayos de fase I de FMP2.1 / AS02A en Mali - 1 st edición . Por el Instituto Nacional de Salud de EE. UU. 27 de julio de 2006.
- "Una nueva vacuna experimental" . Artículo del 4 de febrero de 2010 (fuente AFP ). En el sitio guinee24.com.
- (en) Instituto Nacional de Salud de EE. UU . : Ensayos de fase I de FMP2.1 / AS02A en Malí . 1 st edición 12 abril, 2007.
- vacuna podría ser un arma letal contra la malaria y el cólera . Por la Universidad de Florida Central, comunicado de prensa del 26 de enero de 2010.
- (in) " Los antígenos de las vacunas derivadas del cloroplasto confieren inmunidad contra el cólera y la malaria por vía oral o inyectable. "- Resumen . Por A. Davoodi-Semiromi, M. Schreiber, S. Nalapalli, D. Verma, ND Singh, RK Banks, D. Chakrabarti y H. Daniell, en Plant Biotechnol J. , febrero de 2010; 8 (2), págs. 223-242. Epub 28 de diciembre 2009. .
- Una planta transplastómica es una planta cuyos cloroplastos se han transformado genéticamente para multiplicar transgenes por célula.
- (en) " Vacuna contra la malaria de Oxford covid-19 del equipo es más efectiva jamás se ha hecho " , New Scientist ,23 de abril de 2021( leer en línea , consultado el 29 de abril de 2021 ).
- Currículum vitae Profesor Crisanti [ (en) leer en línea ]
- (in) Artículo en Science Daily 21 de febrero de 2003.
- Website Genoscope - Artículo sobre la secuenciación completa del genoma de Anopheles gambiae [ (en) leer en línea ]
- Academia de Ciencias del Institut de France - Artículo del 12 de junio de 2007 “ http://www.academie-sciences.fr/conferences/seances_publiques/pdf/gas_12_06_07_C_Frolet.pdf ” ( Archivo • Wikiwix • Archive.is • Google • Que hacer? )
- Artículo sobre Anopheles gambiae en el sitio web Genoscope .
- (in) " El primer mosquito a prueba de malaria " . Por Daniel Stolte, Universidad de Arizona - Comunicación del 15 de julio de 2010.
- (en) Resumen del Informe mundial sobre el paludismo 2015 ( leído en línea ) , p. 5
- (en) Tabla de datos F: población estimada en riesgo y casos de malaria y defunciones, 2010-2018 ( leer en línea )
- (en) J. Breman, " Las orejas del hipopótamo: manifestaciones, determinantes y estimaciones de la carga de malaria ", en Am J Trop Med Hyg , vol. 64, núms . 1-2, pág. 1-11 , 2001 [ leer en línea ]
- estimación es difícil debido a la falta de fiabilidad de las estadísticas en los países en cuestión; En 2005 , investigadores estimaron en la revista Nature en 515 millones el número de enfermos en 2002 (en un rango que va de 300 a 660 millones), mientras que la estimación de la OMS en 1999 en su informe sobre la salud en el mundo fue de 273 millones. La OMS dijo que revisó esta cifra el año siguiente y desde entonces ha trabajado con un rango de 300 a 500 millones. Cf. el despacho de John Bonner del 10 de marzo de 2005 (15:18), “La fila estalla por el 'error de cálculo' de la OMS sobre la malaria”, en el sitio web de New Scientist [ (en) leer en línea ]
- “ Hoja de datos sobre el Informe 2013 Malaria Mundial ” , en la OMS ,diciembre 2013
- (en) Greenwood BM, Bojang K, Whitty CJ, Targett GA, “ Malaria ”, en The Lancet , vol. 365, pág. 1487-1498, 2005.
- (in) Hay S, C Guerra, Tatem A, Noor A, R Snow, " La distribución global y la población en riesgo de malaria: pasado, presente y futuro " en Lancet Infect Dis , vol. 4, n o 6, pp. 327-36, 2004.
- Murray CJL, Rosenfeld LC, Lim SS et al. Mortalidad mundial por malaria entre 1980 y 2010: un análisis sistemático , Lancet, 2012; 379: 413-431
- (en) Korenromp E, B Williams, S Vlas, Gouws E, C Gilks, Ghys P Nahlen B, " Malaria atribuible a la epidemia del VIH-1, África subsahariana ", en Emerg Infect Dis , vol. 11, n o 9, pp. 1410-1419, 2005 [ leer en línea ]
- (in) Abu-Raddad L, P Patnaik, Kublin J "La doble infección por el VIH y la malaria alimenta la propagación de ambas enfermedades en el África subsahariana ", en Science , vol. 314, n o 5805, pp. 1603-1606, 2006.
- (en) Layne SP, Principios de epidemiología de enfermedades infecciosas , EPI 220, Departamento de Epidemiología de UCLA [ leer en línea ]
- Greenwood B Mutabingwa T, "Malaria en 2002", en Nature , vol. 415, no . 670-2, 2002.
- (in) Grover-Kopec E, M Kawano, Klaver R Blumenthal B Ceccato P, S Connor, "Un recurso de monitoreo de lluvia operativo en línea para sistemas de alerta temprana de malaria epidémica en África" Malar J. 2005, vol. 4, pág. 6. [ leer en línea ]
- (en) Van Benthem B Vanwambeke S Khantikul N, Burghoorn-Maas C Panart K Oskam L Lambin E, Somboon P "Patrones espaciales y factores de riesgo de seropositividad para la infección por dengue", Am J Trop Med Hyg . 2005, vol. 72, n o 2, p. 201-8. [ leer en línea ]
- (in) Trung H, Van Bortel W Sochantha T Keokenchanh K, N Quang Cong L, M Coosemans, "Transmisión de la malaria y principales vectores de la malaria en diferentes áreas geográficas del sudeste asiático" Vuelo de Trop Med Int Health 2004 . 9, n o 2, p. 230-7, 2004.
- Rémi Barroux , " Después de décadas de lucha, Sri Lanka ha conquistado la malaria ", Le Monde.fr ,13 de septiembre de 2016( leer en línea , consultado el 25 de abril de 2017 )
- https://www.france24.com/fr/asie-pacifique/20210630-apr%C3%A8s-70-ans-de-lutte-la-chine-ar%C3%A9ussi-a-%C3%A9radiquer- malaria
- (en) Keizer J, Utzinger J, Caldas de Castro M, Smith T, Tanner M, Singer B, " Urbanización en África subsahariana e implicaciones para el control de la malaria ", en Am J Trop Med Hyg , vol. 71, n o 2, p. 118-27, 2004 [ leer en línea ]
- (in) Hay SI, Snow RW, " El proyecto Atlas de la malaria: desarrollo de mapas globales de riesgo de malaria " en PLoS Medicine , vol. 3, n o 12, p. e473, 2006 [ leer en línea ]
- Callot J .: "Un problema complejo: la regresión de la malaria en Francia" . En: Anales. Economías, sociedades y civilizaciones , 2 º año, n o 3, 1947, p. 330-332.
- Adéa Guillot, " En Grecia, la indigencia y el aislamiento de los migrantes del campo de Frakaport ", Le Monde .fr ,2 de septiembre de 2016( leer en línea )
- Pierre-Olivier Fanica, “ La desaparición de la malaria en Francia rural y la regresión de los humedales: Ejemplo de Sologne ”, Étude et Gestion des Sols , vol. 13, n o 1,2006, p. 53-61 ( leer en línea [PDF] )
- Gilles Bouvenot, Bernard Devulder y Loïc Guillevin, Patología médica , volumen 2: Inmunopatología, alergología, enfermedades infecciosas, parasitología, geriatría, ediciones Masson, Abrégé Médecine, 1994, p. 336.
- Podcast de Figaro .
- mosquitoesinfos.sante.gouv.fr “Malaria en la Isla Reunión y en el mundo” en el sitio web del Ministerio de Sanidad francés.
- (de) Bruno Pradines, “ Epidemiología de la malaria importada en Francia ” , de la opinión del médico , vol. 69,febrero de 2019, p. 150-152
- Olivier Bouchaud y Bruno Pradines, “ Situación de la malaria en el mundo ”, La Revue du Praticien , vol. 69,febrero de 2019, p. 145-149
- G. Brücker, " Patología de la licencia y el regreso ", La Revue du Praticien , vol. 34 "Patología de los migrantes", n o 57,11 de diciembre de 1984, p. 3223-3228
- Simon I. Hay et al. "La distribución mundial y la población en riesgo de malaria: pasado, presente y futuro" The Lancet Infectious Diseases , vol. 4, n o 6, junio de 2004, p. 327-336 [ (en) leer en línea ]
- Informe mundial sobre el paludismo 2011 en el sitio web de la OMS
- Secretaría del Convenio sobre la Diversidad Biológica, “ La Iniciativa LifeWeb ” ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? ) (Consultado el 29 de marzo de 2013 ) (folleto en color de doble cara)
- Le Figaro del 10 de junio de 2008, página 16.
- (in) Braginets OP Minakawa N, Mbogo CM Yan G. "Estructura genética de la población del mosquito africano de la malaria Anopheles funestus en Kenia" The American Journal of Tropical Medicine & Hygiene 2003; 69 (3) 303-8 [ leer en línea ]
- (in) Darwin H. Stapleton "¿Lecciones de historia? » Crónicas de salud pública , marzo-abril de 2004, vol. 119.
- (in) Marcus Hall: "The Rockefeller Foundation in Sardinia: Pesticide Politics in the Struggle Against Malaria - Environmental Values (1991-2002)" , 28 de marzo de 2005.
- Auriane Guilbaud, Malaria - The global fight against a resistente parásito , L'Harmattan, Chaos international collection, 2008, p. 32 .
- Pierre Mouchet et allii, Biodiversidad de la malaria en el mundo , John Libbey Eurotext, 2004.
- OMS (2019) Informe de erradicación de la malaria: beneficios, escenarios futuros y viabilidad. Resumen ejecutivo del informe del Grupo Asesor Estratégico de la OMS sobre Erradicación del Paludismo , 23 de agosto de 2019; CC BY-NC-SA 3.0 OIG; PDF, 172 kB; 13pp
- Martin Enserink (2019) [ https://www.sciencemag.org/news/2019/08/setting-deadline-eradicating-malaria-good-idea-scientists-are-divided (A fecha límite para la malaria final es ¿Es una buena idea? Los científicos están divididos) ] 27 de agosto de 2019
- " Principales avances en la lucha contra la malaria " , sobre OMS ,11 de diciembre de 2013
- (en) Victoria A. Ingham , Amalia Anthousi Vassilis Douris y Nicholas J. Harding , " Una proteína de apéndice sensorial protege los vectores de la malaria de los piretroides " , Nature , vol. 577, n o 7790,enero 2020, p. 376–380 ( ISSN 1476-4687 , PMID 31875852 , PMCID PMC6974402 , DOI 10.1038 / s41586-019-1864-1 , leído en línea , consultado el 31 de mayo de 2020 )
- (en) J. Sachs y P. Malaney, "La carga económica y social de la malaria" , Nature , 2002, vol. 415, pág. 680-5.
- Roll Back Malaria Malaria in Africa , boletín n o 3, [ leer en línea ]
- Sandi Doughton, artículo Seattle Times el 13 de junio de 2008 - " Reviviendo las soluciones de baja tecnología " [ (in) read online ]
- Hacer retroceder la malaria, Costos económicos de la malaria , OMS [ leer en línea ]
- (en) K. Mendis, B. Sina, Marchesini P. y R. Carter, " La carga de la descuidado Plasmodium vivax malaria " , Am J Trop Med , Vol. 64, n hueso 1-2S,2001, p. 97-106 ( leer en línea [PDF] )
- (en) AA Escalante y FJ Ayala, " Filogenia del género Plasmodium de la malaria , derivada de secuencias de genes de ARNr " , PNAS , vol. 91, n o 24,1994, p. 11373-7 ( leer en línea [PDF] )
- (in) PCC Garnham, Parásitos de la malaria y otros hemosporidios , Blackwell Scientific Publications, Oxford, 1996.
- Permin A. y Madsen M., Investing in Animal Health Research to Alleviate Poverty , International Livestock Research Institute, 2001, Apéndice 2: revisión sobre la ocurrencia y el impacto de enfermedades (aves de corral en pequeña escala) [ leer en línea ]
- (in) Atkinson CT, Woods KL, Dusek RJ, Sileo LS Iko WM "Enfermedad de la fauna y conservación en Hawaii patogenicidad de la malaria aviar ( Plasmodium relictum ) en Iiwi ( Vestiaria coccinea ) infectado experimentalmente " Parasitología 1995; 111 Suppl.: S59- 69.
- Science & Vie del 6 de diciembre de 2009: “ Anopheles atrapado por un calcetín sucio ” “ http://mondedurable.science-et-vie.com/2009/12/lanophele-piege-par-une-chaussette-sale/ » ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? )
- (en) Oshikazu Shirai , Takao Tsuda Shinya Kitagawa y Ken Naitoh , " La ingestión de alcohol estimula la atracción de los mosquitos " , Revista de la Asociación Estadounidense de Control de Mosquitos , vol. 18, n o 2Junio de 2002, p. 91–96 ( ISSN 8756-971X , PMID 12083361 , leído en línea , consultado el 26 de junio de 2017 )
- (en) RJ Pitts, CD Rinker, PL Jones, A. Rokas LJ y LJ Zwiebel, " Perfil transcriptómico de apéndices quimiosensoriales en el vector de la malaria Anopheles gambiae Reveals Tissue and sex-specific signatures of olores " , BMC Genomics , vuelo. 12,2011, p. 271 ( DOI 10.1186 / 1471-2164-12-271 )
- (en) T. Lefevre, C. Lebarbenchon, Gauthier-Clerc, Misse D., R. Poulin y F. Thomas, " La importancia ecológica de los parásitos manipuladores " , Trends Ecol Evol , vol. 24, n o 1,2009, p. 41–48 ( leer en línea [PDF] )
- (in) KD Lafferty y Kuris AM, "Consecuencias ecológicas de los parásitos manipuladores" en Host Manipulation by Parasites , eds DP Hughes, J Brodeur, Thomas F (Oxford University Press, Nueva York)2012( leer en línea ) , pág. 158-179
- (en) T. Lefèvre y F. Thomas, " Detrás del escenario, algo más está moviendo los hilos: enfatizando la manipulación parasitaria en enfermedades transmitidas por vectores " , Infect Genet Evol , vol. 8, n o 4,2008, p. 504–519 ( leer en línea [PDF] )
- Poulin R (2010) Manipulación del comportamiento del huésped por parásitos: una actualización y preguntas frecuentes . Avances en el estudio de la conducta, eds Mitani J, et al. (Elsevier, Nueva York) Vol 41, págs. 151–186.
- H. Hurd (2003) Manipulación de insectos vectores de importancia médica por sus parásitos . Annu Rev Entomol 48 (1): 141-161.
- (en) De Moraes CM, Stanczyk NM, Betz SA, Pulido H, Sim DG, Read AF, Mescher MC, “ cambios inducidos por la malaria en los olores de acogida mejorar la atracción mosquito ” , PNAS , vol. 111,2014, p. 11079–11084 ( DOI 10.1073 / pnas.1405617111 , leer en línea [PDF] )
- Ferguson HM, Read AF (2004) El apetito de los mosquitos por la sangre es estimulado por las infecciones por Plasmodium chabaudi en ellos mismos y en sus huéspedes vertebrados . Malar J 3:12.
- (en) R. Lacroix, WR Mukabana, LC Gouagna y JC Koella, “ Malaria infección aumenta el atractivo de los seres humanos a los mosquitos ” , PLoS Biol 3: E298 ,2005( DOI 10.1371 / journal.pbio.0030298 )
- Cornet S, Nicot A, Rivero A, Gandon S (2013) La infección por malaria aumenta el atractivo de las aves para los mosquitos no infectados . Ecol Lett 16: 323–329. doi: 10.1111 / ele.12041.
- Van Dooren GG, Striepen B (2013) "El pasado de algas y el presente de parásitos del apicoplasto". Annu Rev Microbiol 67: 271-289. doi: 10.1146 / annurev-micro-092412-155741 ( resumen ).
- Investigador de microbiología molecular y especialista en malaria infantil en la Facultad de Medicina de la Universidad de Washington en St. Louis
- Sitio web de la Facultad de Medicina de la Universidad de Washington en St. Louis
- Imlay L & Odom AR (2014) Metabolismo isoprenoide en parásitos de Apicomplexan . Informes actuales de microbiología clínica. 1.3-4 (2014): 37-50
- Guggisberg, AM, Amthor, RE y Odom, AR (2014) Biosíntesis de isoprenoides en Plasmodium falciparum . Célula eucariota. 13.11 (2014): 1348-1359 ( resumen )
- Wong RP, Flematti GR & Davis TM (2012) “ Investigación de biomarcadores orgánicos volátiles derivados de Plasmodium falciparum in vitro ”. Malar J 11: 314. doi: 10.1186 / 1475-2875-11-314
- Kelly, M., Su, CY., Schaber, C., Crowley, JR, Hsu, FF., Carlson, JR, Odom, AR (2015) “ parásitos de la malaria producir atrayentes de mosquitos volátiles ” . mBio doi: 10.1128 / mBio.00235-15, vol. 6 no. 2 e00235-15
- (in) VO Nyasembe, PEA Teal, WR Mukabana, JH Tumlinson y B. Torto, " Respuesta conductual del vector de la malaria Anopheles gambiae a compuestos volátiles y sintéticos de plantas hospedadoras " , Parásitos y vectores , vol. 5,2012, p. 234 ( leer en línea [PDF] )
- Dekker T, Geier M & Cardé RT (2005) “ El dióxido de carbono sensibiliza instantáneamente a las hembras de mosquitos de la fiebre amarilla a los olores de la piel humana ”. J Exp Biol 208: 2963-2972. doi: 10.1242 / jeb.01736 ( resumen ).
- (en) CJ McMeniman, RA Corfas, BJ Matthews, SA Ritchie SA y LB Vosshall, "La integración multimodal del dióxido de carbono y otras señales sensoriales impulsa la atracción de los mosquitos hacia los humanos " , Cell , vol. 156,2014, p. 1060–1071 ( DOI 10.1016 / j.cell.2013.12.044 , leer en línea [PDF] )
- Sitio web del laboratorio del Hospital St. Louis
- (en) Talman A Domarle O, F McKenzie, Ariey F Robert V " Gametocitogénesis: la pubertad de Plasmodium falciparum " en Malar J , vol. 3, pág. 24.
- Entomología de la malaria y control de vectores (págs. 7-8), OMS 2003 [ leer en línea ]
- MEDICINE / SCIENCES 2005 (Tráfico de proteínas en los glóbulos rojos infectados por Plasmodium) [ leer en línea ]
- (en) Cécile Crosnier Leyla Y. Bustamante S. Josefin Bartholdson Amy K. Bei Michel Theron, Makoto Uchikawa Souleymane Mboup Omar Ndir Dominic P. Kwiatkowski, Manoj T. Duraisingh, Julian C. Rayner y Gavin J. Wright, Basigin es un receptor esencial para la invasión de eritrocitos por Plasmodium falciparum . leer en línea .
- E. Pilly, Enfermedades infecciosas y tropicales: todos los elementos de enfermedades infecciosas , París, Alinéa Plus,2018, 720 p. ( ISBN 978-2-916641-66-9 ) , pág. 512-514
- Paris Val de Marne University - 2000 - Tesis para el Diploma Estatal de Doctor en Medicina (Título 1.2.2.) [ Leer en línea ]
- (en) Cox-Singh J, Davis TM, Lee KS, Shamsul SS Matusop A Ratnam S, Rahman HA Conway DJ, Singh B, "La malaria por Plasmodium knowlesi en humanos está ampliamente distribuida y potencialmente amenaza la vida " , Clin Infect Say , vol. . 46, n o 22008, p. 165-71. ( PMID 18171245 , PMCID PMC2533694 , DOI 10.1086 / 524888 , leer en línea [html] )
- Marc Gentilini, Medicina Tropical , París, Medicina-Ciencias de Flammarion,1993, 928 p. ( ISBN 2-257-14394-9 ) , pág. 101.
- (in) Resultados de un estudio en ratones DOI : 10.1038 / nm.2368
- NCBI - Explorador de taxonomía (Navegador sobre los códigos genéticos de las diferencias de especies Plasmodium falciparum ) [ (in) read online ]
- P. Bartolucci, " Hemoglobinopatías: una ventaja contra la malaria pero con riesgo de enfermedades graves ", La Revue du Praticien , vol. 64,octubre 2014, p. 1110-1011
- (en) Denis Pierron , Margit Heiske , Harilanto Razafindrazaka y Veronica Pereda-loth , " Fuerte selección durante el último milenio para la ascendencia africana en la población mixta de Madagascar " , Nature Communications , vol. 9, n o 1,2 de marzo de 2018, p. 932 ( ISSN 2041-1723 , PMID 29500350 , PMCID PMC5834599 , DOI 10.1038 / s41467-018-03342-5 , leído en línea , consultado el 8 de noviembre de 2020 )
- CNRS - Malaria - El parásito P. vivax infecta a poblaciones consideradas hasta ahora resistentes - 16 de marzo de 2010 [ (fr) leer en línea ]
- (en) Carolina Lopez, Carolina Saravia et al. “Mecanismos de resistencia a la malaria de base genética” Gene 2010; 467 (1-2): 1-12.
- Nicolas Vignier, " Manejo de ataques simples de malaria, una emergencia terapéutica ", La Revue du Praticien , vol. 69,febrero de 2019, p. 152-158
- Johann Cailhol, “ Malaria ”, de la opinión del médico , vol. 64,diciembre 2014, p. 1457-1468
- De Fritz H. Kayser ( trad. Del alemán), de bolsillo Manual de Microbiología Médica , París, Flammarion Médecine-Sciences,2008, 764 p. ( ISBN 978-2-257-11335-1 ) , pág. 597-599.
- Marc Gentilini 1994, op. cit., pág. 95.
- Marc Gentilini 1993, op. cit., pág. 103-106.
- A. Manuila, Diccionario francés de medicina y biología , t. II, París, Masson,1971, p. 207-210
- Criterios para la malaria grave adoptados por la OMS [ leer en línea ] , p. 15.
- Trampuz A, Jereb M, Muzlovic I, Prabhu R, “revisión clínica: La malaria grave”, en Crit Care , vol. 7, n o 4, p. 315-23, 2003 [ leer en línea ]
- Kain K, Harrington M, Tennyson S, Keystone J, "Malaria importada: análisis prospectivo de problemas de diagnóstico y tratamiento" Clin Infect Dis . 1998, vol. 27, n o 1, p. 142-9.
- Stéphane Jauréguiberry, " Access malaria ", La Revue du Praticien - medicina general , vol. 21, núm . 754/755,16 de enero de 2007, p. 23-28.
- Redd S et al., “Algoritmo clínico para el tratamiento de la malaria por Plasmodium falciparum en niños”, en Lancet , vol. 347, n o 8996, p. 223-7, 1996.
- American Journal of Public Health "Rendimiento del trabajador de salud comunitaria en el manejo de múltiples enfermedades infantiles: distrito de Siaya, Kenia, 1997-2001" en octubre de 2001 [ (in) read online ]
- (en) Pattanasin S. et al. “Evaluación de un nuevo ensayo de lactato deshidrogenasa de Plasmodium (OptiMAL-IT) para la detección de malaria” Transact Royal Soc Trop Med . 2003, vol. 97, pág. 672-4.
- RollBackMalaria - Consumibles y productos no médicos para la malaria - Seminario del 5 al 9 de marzo de 2006 en Dakar [ leer en línea ]
- (en) Ling IT. et al. "Anticuerpos contra la glutamato deshidrogenasa de Plasmodium falciparum " Parasitology 1986, vol. 92, pág. 313-24.
- “ pruebas de diagnóstico rápido para la malaria ” , en medecinetropicale.free.fr ,2018
- (en) Adak T, Sharma V, V Orlov, "Estudios sobre el patrón de recaída de Plasmodium vivax en Delhi, India", en Am J Trop Med Hyg , vol. 59, n o 1, p. 175-9, 1998
- Marc Gentilini 1994, op. cit., pág. 109.
- Marc Gentilini 1994, op. cit., pág. 107-109.
- Bénédicte Girard, " Fiebre y embarazo ", La Revue du Praticien , vol. 57,31 de marzo de 2007, p. 665-669
- “ de la OMS | The World Malaria Report 2019 at a Glance ” , sobre la OMS (consultado el 15 de diciembre de 2019 )
- (en) Athena P. Kourtis, " El embarazo y la infección " , The New England Journal of Medicine , vol. 370, n o 23,5 de junio de 2014, p. 2211-2218.
- (en) Zhi-yong Tao Qiang Fang , Xue Liu y Richard Culleton , " Malaria congénita en China " , PLoS Neglected Tropical Diseases , vol. 8, n o 3,13 de marzo de 2014( ISSN 1935-2727 , PMID 24626148 , PMCID 3953009 , DOI 10.1371 / journal.pntd.0002622 , leído en línea , consultado el 13 de diciembre de 2019 )
- (en) Jane Crawley, " Malaria en niños " , The Lancet , vol. 375,24 de abril de 2010, p. 1468-1481.
- (en) Lauren M. Cohee y Miriam K. Laufer , " malaria en los niños " , las clínicas pediátricas de Norteamérica , vol. 64, n o 4,agosto 2017, p. 851–866 ( ISSN 0031-3955 , PMID 28734514 , PMCID 5733786 , DOI 10.1016 / j.pcl.2017.03.004 , leído en línea , consultado el 15 de diciembre de 2019 )
- Tania Ikowsky, "Importado de la malaria en los lactantes ", La Revue du Praticien - Médecine générale , vol. 23, n o 824,16 de junio de 2009, p. 431-432
- (En) Kimberly E. Mace y el Sr. Paul Arguin , " Vigilancia de la malaria - Estados Unidos, 2014 " , Resúmenes de vigilancia de MMWR , vol. 66, n o 12,26 de mayo de 2017, p. 1–24 ( ISSN 1546-0738 , PMID 28542123 , PMCID 5829864 , DOI 10.15585 / mmwr.ss6612a1 , leído en línea , consultado el 15 de diciembre de 2019 )
- Marc Gentilini 1994, op. cit., pág. 110.
- (en) Federica Verra , Andrea Angheben , Elisa Martello y Giovanni Giorli , “ Una revisión sistemática de malaria transmitida por transfusión en zonas no endémicas ” , Malaria Journal , vol. 17,16 de enero de 2018( ISSN 1475-2875 , PMID 29338786 , PMCID 5771189 , DOI 10.1186 / s12936-018-2181-0 , leído en línea , consultado el 16 de diciembre de 2019 )
- F. Denis, Bacterias, hongos y parásitos transmisibles de madre a hijo , John Libbey Eurotext, 2002, p. 376.
- (en) Ehsan Ahmadpour , Masoud Foroutan-Rad , Hamidreza Majidiani y Sirous Mehrani Moghaddam , “ Transfusion transmitida Malaria: Una revisión sistemática y meta-análisis ” , Enfermedades Infecciosas Foro Abierto , vol. 6, n o 7,11 de junio de 2019( ISSN 2328-8957 , PMID 31334300 , PMCID 6634438 , DOI 10.1093 / ofid / ofz283 , leído en línea , consultado el 16 de diciembre de 2019 )
- J. Ranque: "Paludismo postransfusional: situación actual" .
- François Lefrère, “ Riesgos transfusionales actuales ”, La Revue du Praticien - Médecine générale , vol. 27, n o 894,enero 2013, p. 74-75
- " Malaria: dictamen sobre seguridad de las transfusiones y trasplantes " , en hcsp.fr ,septiembre 2019, p. 7-8
- Nicolas Vignier, " Formas particulares de malaria ", La Revue du Praticien , vol. 69,febrero de 2019, p. 159-161
- (en) Danielle I. Stanisic , James S. McCarthy y Michael F. Bueno , " Controlled infección de la malaria humana: Aplicaciones, Avances y Desafíos " , Infection and Immunity , vol. 86, n o 1,19 de diciembre de 2017( ISSN 0019-9567 , PMID 28923897 , PMCID 5736798 , DOI 10.1128 / IAI.00479-17 , leído en línea , consultado el 16 de diciembre de 2019 )
- (en) Mockenhaupt F. et al. “Manifestación y resultado de la malaria severa en niños en el norte de Ghana” Am J Trop Med Hyg. 2004; 71 (2): 167-72.
- Medicamentos obsoletos retrasan la victoria contra la malaria - Artículo de Daily Nation 30/06/2009 [ (in) read online ]
- Las clínicas privadas siempre están usando tratamientos más antiguos - Artículo del Daily Nation del 23/04/2009 [ (in) read online ]
- BEH - Quimiosensibilidad de la malaria importada a Francia en 2001 y 2002 (artículo del 3 de febrero de 2004) [ (en) leer en línea ]
- (en) Nicholas J. White, " Malaria - Time to Act " , New Eng. J. Med. , vol. 355,9 de noviembre de 2006, p. 1956-1957 ( leer en línea )
- (en) K. Laufer, PC Thesing, ND Eddington, R. Masonga, FK Dzinjalamala, SL Takala, TE Taylor y CV Plowe, " Retorno de la eficacia antipalúdica de cloroquina en Malawi " , New Engl. J. Med. , vol. 355,9 de noviembre de 2006, p. 1959-1966 ( leer en línea )
- (en) Shweta Sinha , Bikash Medhi y Rakesh Sehgal , " Desafíos de la malaria resistente a los medicamentos " , Parasite , vol. 21,2014, p. 61 ( ISSN 1776-1042 , DOI 10.1051 / parásito / 2014059 )
- (en) Brian KS Yeung , Bin Zou , Matthias Rottmann et al. , " Espirotetrahidro Betacarbolinas (espiroindolonas): una nueva clase de compuestos potentes y oralmente eficaces para el tratamiento de la malaria " , J. Med. Chem. , vol. 53, n o 14,22 de junio de 2010, p. 5155-5164 ( resumen ).
- (en) Nicholas J. Blanco , Sasithon Pukrittayakamee Aung Pyae Phyo et al. , " Spiroindolone KAE609 para Falciparum y Vivax Malaria " , N. Engl. J. Med. , N o 376,31 de julio de 2014, p. 404-410 ( resumen ).
- Nobutaka Kato (2016) La síntesis orientada a la diversidad produce nuevos inhibidores antipalúdicos de múltiples etapas ; Naturaleza ; doi: 10.1038 / nature19804, subido: 07 de septiembre de 2016, consultado el 10 de septiembre de 2016
- Lon CT, Tsuyuoka R, Phanouvong S et al. “Medicamentos antipalúdicos falsificados y de calidad inferior en Camboya”, en Trans R Soc Trop Med Hyg , vol. 100, n o 11, p. 1019-24, 2006.
- (en) US Pharmacopeia, antimaláricos falsos encontrados en la provincia de Yunan, China 2004 " http://www.uspdqi.org/pubs/other/FakeAntimalarialsinChina.pdf " ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? )
- (in) Newton PN, Green MD, Fernández FM Day JSP, NJ White, "Medicamentos antiinfecciosos falsificados" en Lancet Infect Dis , vol. 6, n o 9, p. 602-13, 2006
- BBC News, 17 de agosto de 2007 [ leer en línea ]
- Kevin Hull, Malaria: Fever Wars , Documental de PBS, 2006 “ http://www.wgbh.org:81/cgi-bin/nph-algs.cgi/000000A/http/www.wgbh.org/schedules/program- info? program_id = 2682027 & episode_id = 2682029 » ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? )
- Barat, "Cuatro historias de éxito de la malaria: cómo se redujo con éxito la carga de la malaria en Brasil, Eritrea, India y Vietnam", en Am J Trop Med Hyg , vol. 74, n o 1, p.12-16, 2006.
- Posición de la OMS sobre el uso de DDT 2005 [ leer en línea ]
- Prefectura de Reunión - Departamento de Salud y Asuntos Sociales - La lucha contra los mosquitos - 2006 [ leer en línea ]
- Organización Mundial de la Salud , Planificación de programas de control de la malaria: Guía del aprendiz , ed. provisional, OMS , Ginebra , 2003 , pág. 128 [ leer en línea ]
- " ¿Qué es un murciélago?" » , En www.nuitdelachauvesouris.com
- "La secuenciación del genoma del mosquito, publicada en la revista Science, abre el camino a nuevos medios para combatir la malaria" Eurekalert.org , 2 de octubre de 2002 [ leer en línea ]
- (in) Smit MR, Ochomo EO Aljayyoussi G, et al., " Seguridad y eficacia de la ivermectina mosquitocida de dosis alta cuando se coadministra con dihidroartemisinina-piperaquina en adultos kenianos con paludismo no complicado (IVERMAL): un estudio doble ciego aleatorizado , ensayo controlado con placebo ” , The Lancet Infectious Diseases , vol. 18, n o 6,27 de marzo de 2018, p. 615-626 ( DOI 10.1016 / s1473-3099 (18) 30163-4 , leer en línea )
- (en) EJ Kweka F. Mosha Lowassa A. et al., " Estudio etnobotánico de revisiones de algunas de las plantas repelentes de mosquitos en el noreste de Tanzania " , Malaria Journal , vol. 7,2008, p. 152 ( DOI 10.1186 / 1475-2875-7-152 )
- Saltidin - Información técnica (en) “ http://www.bayrepel.com/?501A1 ” ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? )
- Instituto de Medicina Tropical Amberes-Consejo de salud para viajeros, edición destinada a la profesión médica 2007-2008 [[ http://www.itg.be/ITG/Uploads/MedServ/fmedasso.pdf leer en línea]]
- ITG (Instituut voor Tropische Geneeskunde-Your health while travelling-Malaria (versión de agosto de 2008) [ leer en línea ]
- Centro Belga de Información Farmacoterapéutica-Comentarios, dosis de tetraciclinas [ leer en línea ]
- Centro Belga de Información Farmacoterapéutica-Comentarios, dosificación de antimaláricos-Directorio "nombre de la especialidad" que comienza con "L" [ leer en línea ]
- Centro belga de información farmacoterapéutica-Comentarios, dosificación de antimaláricos-Directorio "nombre de la especialidad" que comienza con "M" [ leer en línea ]
- Artículo de The Standard del 8 de mayo de 2010 - Fighting malaria by SMS [ (in) read online ]
Ver también
Bibliografía
- Jacques Verdrager, OMS y malaria: memorias de un médico especialista en malaria . - L'Harmattan, coll. "Actores de la ciencia", París, 2005 ( ISBN 2-7475-8246-9 )
- “Recomendaciones de salud y sanidad del viajero 2005”, Boletín epidemiológico semanal , n o 24-25 / 2005 (14 de junio de 2005) [ leer en línea ]
- (fr) Robert W. Snow y col. “La distribución global de los episodios clínicos de paludismo por Plasmodium falciparum ”, Nature , vol. 434, n o 7030 (10 de marzo de 2005), p. 214-217 [ (en) presentación en línea ]
- Marie Josserand Debacker, Malaria: historia, mitos, creencias e ideas recibidas , tesis de ejercicio, Medicina, París XII , 2000 [ leer en línea ]
- Serge Paul Eholié, Emmanuel Bissagnéné y Pierre-Marie Girard (dir.), Recuerdo terapéutico del paludismo en África , Doin, IMEA, París, 2008, 139 páginas ( ISBN 978-2-7040-1253-4 )
- Christian Lengeler, Jacqueline Cattani y Don de Savigny (eds), A Wall Against Malaria: Something New in Preventing Malaria Deaths , Centro Internacional de Investigaciones para el Desarrollo, Ottawa; Organización Mundial de la Salud, Ginebra, 1997, 220 páginas ( ISBN 0-88936-831-7 )
- Jean Mouchet, Pierre Carnevale, Marc Coosemans y col. Biodiversidad de la malaria en el mundo , J. Libbey Eurotext, Montrouge, 2004, 428 páginas ( ISBN 2-7420-0528-5 )
Filmografia
- Malaria, la hecatombe silenciosa , documental dirigido por Bernard Germain y Jean Vercoutère, producido por Mosaïque Films (París) y distribuido por ADAV, 2000, 54 minutos (VHS)
- Les Faucheurs de Palu , documental de 52 minutos dirigido por Patrice Desenne, producido por Effervescence, France 5, Public Senate, IRD.
- Paludismo: Investigación en el bosque de Gabón una película sobre el origen animal del paludismo (16 min), IRD.
Artículos relacionados
- Martin Shkreli y el escándalo de Daraprim
- Dia mundial de la malaria
- Paludismo aviar
- Control de la malaria
- Fondo Mundial de Lucha contra el SIDA, la Tuberculosis y la Malaria
- DNDi (Iniciativa sobre medicamentos para enfermedades desatendidas)
- Marismas Pontinas
- Atabrine
- Asociación Internacional de Fomento
- Diclorodifeniltricloroetano
enlaces externos
- Registros de autoridad :
- Avisos en diccionarios generales o enciclopedias :
- Recursos relacionados con la salud :
- Tesauro del NCI
- Orphanet
- (en) Clasificación Internacional de Atención Primaria
- (es) Enfermedades Ontología
- (es) DiseasesDB
- (en + es) Centro de Información sobre Enfermedades Genéticas y Raras
- ( fr ) Herencia mendeliana en humanos
- ( fr ) Herencia mendeliana en humanos
- (es) Encabezados de materias médicas
- (en + es) MedlinePlus
- (cs + sk) WikiSkripta
- Página de la OMS
- Proyecto Atlas de la malaria
- (es) Sitio europeo BIOMALPAR, dedicado a la malaria