Etilenglicol
| Etilenglicol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
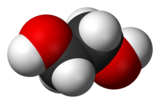 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura del etilenglicol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificación | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre IUPAC | Etano-1,2-diol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinónimos |
1,2-dihidroxietano |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100,003,159 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 203-473-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sonrisas |
C (CO) O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C2H6O2 / c3-1-2-4 / h3-4H, 1-2H2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | líquido incoloro, viscoso e higroscópico. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades químicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fórmula bruta |
C 2 H 6 O 2 [Isómeros] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa molar | 62.0678 ± 0.0026 g / mol C 38.7%, H 9.74%, O 51.55%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusión |
−12,69 ° C puro −26 ° C al 40% vol en agua |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° hirviendo | 197,3 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilidad | Miscible con agua , glicerol , piridina , acetona , aldehídos , ácido acético . Poca tierra en éter (1 en 200). Prácticamente insoluble en benceno , aceites . | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parámetro de solubilidad δ | 29,9 MPa medio ( 25 ° C ); 32,4 J 1/2 cm −3/2 ( 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
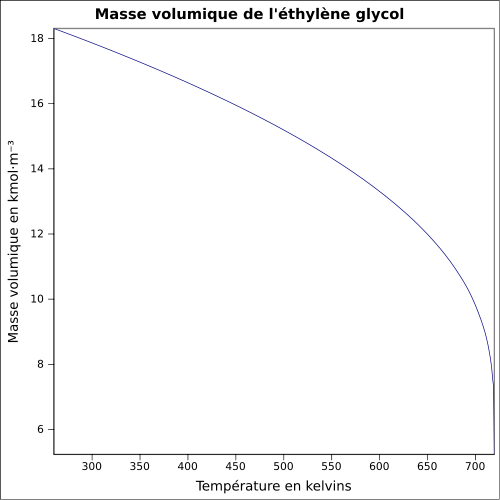
| Densidad |
1,127 4 g cm −3 ( 0 ° C ) 1,120 4 g cm −3 ( 10 ° C ) 1,113 5 g cm −3 ( 20 ° C ) 1,106 5 g cm −3 ( 30 ° C ) ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura de autoignición | 398 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto de inflamabilidad | 111 ° C (copa cerrada). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Límites explosivos en el aire | 3,2–15,3% vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
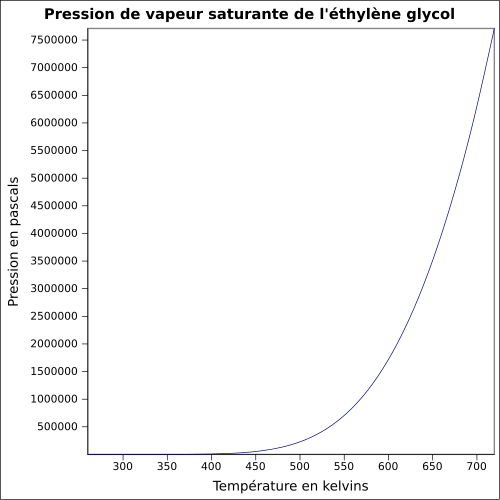
| Presión de vapor saturante | a 20 ° C : 7 Pa
ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Viscosidad dinámica | (16,06 x 10 -3 Pa s a 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto crítico | 8 MPa , 446,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido | 1.658 m s −1 a 25 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termoquímica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gas, 1 bar | 303,8 J mol −1 K −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 líquido, 1 bar | 163,2 J mol −1 K −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gas | −392,2 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 líquido | −460,0 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
ecuación:
ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 1189.2 kJ mol −1 (líquido) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades electronicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re energía de ionización | 10,16 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cristalografía | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Clase de cristal o grupo espacial | P 212121 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parámetros de malla |
a = 5,013 Å b = 6,915 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumen | 321,38 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades ópticas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Índice de refracción | 1,4318 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauciones | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Atención H302, H373, P260, P301, P312, P330, H302 : Nocivo en caso de ingestión H373 : Puede provocar daños en los órganos (indicar todos los órganos afectados, si se conocen) tras una exposición repetida o prolongada (indicar la vía de exposición si se ha demostrado de manera concluyente que ninguna otra vía de exposición causa el mismo peligro) P260 : No respire el polvo / el humo / el gas / la niebla / los vapores / el aerosol. P301 : En caso de ingestión: P312 : Llamar a un CENTRO DE INFORMACIÓN TOXICOLÓGICA oa un médico si no se encuentra bien. P330 : Enjuagar la boca. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 D2A, D2A : Material muy tóxico que provoca otros efectos tóxicos teratogenicidad y embriotoxicidad en animales Divulgación al 0,1% según criterios de clasificación |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 2 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inhalación | Vómitos, parálisis | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotoxicología | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | 8,54 g kg -1 (rata, oral) 6,61 (conejillo de indias, oral) 13,79 ml kg -1 (ratón, oral) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Valor de exposición | 10 ml m −3 , 26 mg m −3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| otro | Se enciende al contacto con KMnO 4después de 10 a 20 s . | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | −1,93 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Umbral de olor | bajo: 0.08 ppm alto: 25 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unidades de SI y STP a menos que se indique lo contrario. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El etilenglicol o glicol o etano-1,2-diol es el compuesto químico más simple de la familia de los glicoles .
Su fórmula estructural es HO - CH 2 —CH 2 —OHy su fórmula cruda C 2 H 6 O 2(es el más simple de los dioles ). El etilenglicol se utiliza con frecuencia como anticongelante en el refrigerante de automóviles . A temperatura ambiente, es un líquido viscoso, incoloro, inodoro y de sabor dulce. El etilenglicol es tóxico y su ingestión requiere atención médica urgente.
apellido
"Etano-1,2-diol" es el nombre sistemático definido por la nomenclatura de química orgánica de la IUPAC para una molécula con dos átomos de carbono (prefijo eth- ) que tienen un enlace individual (sufijo -ane ) y unido a dos grupos hidroxilo en cada uno de los dos carbonos (sufijo -1,2-diol ). "Etilenglicol" es el nombre trivial comúnmente utilizado para etano-1,2-diol.
Historia
El etilenglicol fue sintetizado por primera vez en 1859 por el químico francés Charles Adolphe Wurtz mediante la saponificación del diacetato de etilenglicol por hidróxido de potasio , por un lado, y por la hidratación de óxido de hidrógeno y etileno por otro lado. Se produjo en pequeñas cantidades durante la Primera Guerra Mundial como refrigerante y como componente de explosivos . Su producción industrial comenzó en 1937 , cuando su precursor, el óxido de etileno , se produjo en cantidades industriales a bajo costo.
Provocó una pequeña revolución en el mundo de la aeronáutica al reemplazar el agua en el sistema de refrigeración . Su elevada temperatura de ebullición permitió reducir así el tamaño del radiador y, por tanto, su peso y su resistencia aerodinámica. Antes de que el etilenglicol estuviera disponible, los sistemas de enfriamiento usaban agua a alta presión ; estos sistemas eran engorrosos y poco fiables, y en combate aéreo eran fácilmente alcanzados por las balas enemigas.
Propiedades fisicoquímicas
El etilenglicol es el más simple de los dioles vecinales y tiene propiedades fisicoquímicas particulares debido a su estructura que comprende dos grupos hidroxilo adyacentes a lo largo de la cadena de hidrocarburos.
Es un incoloro, inodoro, de baja volatilidad y higroscópico líquido con una baja viscosidad (16,06 x 10 -3 Pa s a 25 ° C ). Es completamente miscible con muchos disolventes polares , como agua , alcoholes y acetona , y muy poco soluble en disolventes apolares , como benceno , tolueno , dicloroetano o cloroformo .
El etilenglicol tiene una constante molar crioscópica de 3,11 K kg mol -1 y una constante molar ebulloscópica de 2,26 K kg mol -1 .
-
Temperatura muy fría.
-
Viscosidad de la mezcla con agua.
-
Viscosidad en función de la temperatura.
Producción
Se sintetiza a partir de etileno , a través de un intermedio de óxido de etileno que reacciona con el agua , según la ecuación:
C 2 H 4 O + H 2 O → C 2 H 6 O 2
Esta reacción puede catalizarse en un medio ácido o básico , o incluso a alta temperatura. En medio ácido y con exceso de agua, el rendimiento de la reacción puede alcanzar el 90%. Los oligómeros de etilenglicol ( dietilenglicol , trietilenglicol , tetraetilenglicol ) se pueden obtener de la misma manera.
Reactividad y reacciones
El uso de etilenglicol está limitado por algunas precauciones:
- evite el contacto con oxidantes fuertes, aluminio , cloruro de cromilo , hidróxidos alcalinos, ácido perclórico ;
- El etilenglicol es combustible, higroscópico , incompatible con varios materiales sintéticos. Puede explotar en contacto con el aire después de calentarse en forma de vapor o gas.
El etilenglicol se utiliza como grupo protector para los grupos carbonilo durante las reacciones sintéticas de compuestos orgánicos. El tratamiento de un aldehído o cetona con etilenglicol en presencia de un catalizador ácido (por ejemplo, ácido p-toluenosulfónico; trifluoruro de boro) da el correspondiente 1,3-dioxolano, que es resistente a la acción de bases y otros compuestos nucleófilos. Además, el grupo protector 1,3-dioxolano se puede eliminar mediante hidrólisis ácida. En este ejemplo, la isoforona está protegida por etilenglicol y ácido p-toluenosulfónico con bajo rendimiento. El agua se eliminó mediante destilación azeotrópica para desplazar el equilibrio hacia la derecha.
Se utiliza para la protección de las funciones carbonilo en la reacción de acetalización .

usar
El etilenglicol era el más conocido y se utilizaba como anticongelante y refrigerante . Su bajo punto de fusión también se ha utilizado como anticongelante para parabrisas y motores a reacción . El etilenglicol es principalmente una base química en el campo de las industrias petroquímicas , donde permite la producción de fibras textiles y resinas de poliéster , incluido el tereftalato de polietileno , principal material de las botellas de plástico . Sus propiedades anticongelantes también lo convierten en un componente importante de soluciones destinadas a la conservación de tejidos orgánicos a baja temperatura.
La alta temperatura de ebullición del etilenglicol y su alta afinidad por el agua lo convierten en un desecante ideal para la producción de gas natural . En las torres de deshidratación, se hace que el etilenglicol líquido que fluye desde la parte superior de la torre se encuentre con la mezcla de agua e hidrocarburos gaseosos que escapan del fondo. El glicol recoge agua y se drena al fondo, mientras que los vapores de hidrocarburos se recogen en la parte superior. Luego se reinyecta etilenglicol para repetir la operación.
Intoxicación por producto
El principal peligro del etilenglicol proviene de su toxicidad si se ingiere. Debido a su sabor dulce, los niños y las mascotas pueden ingerir grandes cantidades de etilenglicol si se dejan al alcance y los casos no son raros (más de 7,000 presuntas intoxicaciones en los Estados Unidos en 2011). La toxicidad se debe principalmente a sus metabolitos y no al etilenglicol en sí. La progresión de los síntomas del envenenamiento ocurre en varias etapas. El primero es la aparición de síntomas neurológicos. La víctima puede parecer levemente intoxicada, quejarse de mareos y parecer confundida. Luego, el cuerpo convierte el etilenglicol en otra toxina, el ácido oxálico, que se precipitará en los riñones y provocará insuficiencia renal aguda .
En caso de intoxicación, puede producirse un aumento significativo de los niveles de lactato en sangre, que es, de hecho, un falso aumento debido a la proximidad química entre el lactato y los productos de degradación del glicol: glicolato y glioxilato . Estos últimos de hecho dan reacciones cruzadas con ciertos sistemas para medir la concentración de lactato. También hay un "agujero osmolar" con una osmolalidad medida mucho más alta que la evaluada por la medición de natremia, glucemia y uremia .
El etilenglicol puede ser fatal para los adultos. De cualquier manera, se necesita atención médica urgente. Si la víctima aún está consciente, si es posible, dele 100 ml (un vaso) de alcohol fuerte a 45 ° para beber. El etanol sustituye efectivamente al etilenglicol por enzimas que degradan estos últimos compuestos más tóxicos, lo que limita la producción de toxinas (conocido como inhibidor competitivo). La persona también debe ser trasladada a un hospital donde se le puedan administrar, en lugar de etanol, otros inhibidores de la alcohol deshidrogenasa, la enzima responsable en los humanos de convertir el etanol en etanol , etanal y etilenglicol en aldehído oxálico, que transformará (gracias a otras deshidrogenasas) finalmente en oxalato, que es tóxico para él. Uno de estos inhibidores es el fomepizol .
Debido a su toxicidad, ya se ha hablado del etilenglicol en los medios:
- en 2007 , se descubrió glicol en pastas dentales de China. Los fabricantes que aceptaron responder a los periodistas explicaron que el glicol permite que la masa tenga la consistencia adecuada. En principio, no se traga pasta de dientes mientras se cepilla los dientes, pero en la práctica puede suceder muy bien, especialmente con los niños.
seguridad
Inflamabilidad
No muy inflamable en estado líquido, el etilenglicol puede ser explosivo en estado gaseoso. Por tanto, es fundamental manipularlo en locales bien ventilados (concentración inferior a 100 mg m −3 ).
La electrólisis de etilenglicol con un ánodo de plata produce una reacción exotérmica .
Precauciones
Los vapores de etilenglicol son irritantes antes de ser peligrosos. Sin embargo, la exposición crónica es la fuente de patologías reconocidas en Francia como enfermedades profesionales por el código de la Seguridad Social .
Notas y referencias
- ETILENGLICOL , hoja (s) de seguridad del Programa Internacional de Seguridad Química , consultado el 9 de mayo de 2009
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- D. R. Lide, 2007 , cap. 3 (“Constantes físicas de compuestos orgánicos”), pág. 232.
- (en) James E. Mark, Manual de propiedades físicas del polímero , Springer,2007, 2 nd ed. , 1076 p. ( ISBN 978-0-387-69002-5 y 0-387-69002-6 , leer en línea ) , pág. 294
- (en) Yitzhak Marcus, Las propiedades de los solventes , vol. 4, Inglaterra, John Wiley & Sons Ltd,1999, 239 p. ( ISBN 0-471-98369-1 )
- (en) Robert H. Perry y Donald W. verde , de Perry Ingenieros Químicos Handbook , EE.UU., McGraw-Hill,1997, 7 ª ed. , 2400 p. ( ISBN 0-07-049841-5 ) , pág. 2-50
- D. R. Lide, 2007 , cap. 15 ("Datos prácticos de laboratorio"), pág. 17.
- DR Lide, 2007 , cap. 6 ("Propiedades de los fluidos"), pág. 49.
- DR Lide, 2007 , cap. 14 (“Geofísica, astronomía y acústica”), p. 40.
- D. R. Lide, 2007 , cap. 5 ("Termoquímica, electroquímica y cinética"), pág. 22.
- (en) Carl L. Yaws, Manual de diagramas termodinámicos: compuestos orgánicos C8 a C28 , vol. 1, Huston, Texas, Pub del Golfo. Co.,1996, 396 p. ( ISBN 0-88415-857-8 )
- (en) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 de junio de 2002, 83 ª ed. , 2664 p. ( ISBN 0849304830 , presentación en línea ) , p. 5-89
- DR Lide, 2007 , cap. 10 ("Física atómica, molecular y óptica"), pág. 213.
- " glicol de etileno " , en reciprocalnet.org (visitada 14 de junio 2012 )
- SDS establecido por Sigma-Aldrich [1]
- " Etilenglicol " en la base de datos de productos químicos Reptox de la CSST (organización de Quebec responsable de la seguridad y salud ocupacional), consultado el 24 de abril de 2009
- " Etilenglicol " en hazmap.nlm.nih.gov (consultado el 14 de noviembre de 2009 )
- "Ethane-1,2-diol" , en ESIS , consultado el 20 de febrero de 2009
- CA Wurtz , " Memorias sobre glicoles o alcoholes diatómicos ", Annal. Chim. Phys. , 3 Serie E , vol. 55,1859, p. 400-478 ( leer en línea ).
- CA Wurtz , “ Síntesis de glicol con óxido de etileno y agua ”, CR Hebd. Sesiones Acad. Sci. , vol. XLIX, n o 21,1859, p. 813-815 ( leer en línea ).
- H. Yue, 2012 .
- DR Lide, 2007 , cap. 15 (“Datos prácticos de laboratorio”), pág. 28.
- DR Lide, 2007 , cap. 15 (“Datos prácticos de laboratorio”), pág. 27.
- http://xotxim.ru/etilenglikol/
- Bronstein AC, Spyker DA, Cantilena LR, Rumack BH y Dart RC, Informe anual 2011 del Sistema Nacional de Datos de Venenos (NPDS) de la Asociación Americana de Centros de Control de Envenenamientos: 29o informe anual , Clin. Toxicol. (Phila), 2012, 50: 911-1164
- Guo C, Cenac TA, Li Y y McMartin KE, el oxalato de calcio, y no otros metabolitos, es responsable de la toxicidad renal del etilenglicol , Toxicol. Letón. , 2007, 173: 8-16
- Oostvogels R, Kemperman H, Hubeek I y ter Braak EW, La importancia de la brecha de la osmolalidad en la intoxicación de etilenglicol , BMJ, 2013, 347: f6904
- INRS , “toxicologique Ficha n ° 25” , Septiembre 2016
- Brent J, McMartin K, Phillips S et al. , Fomepizol para el tratamiento de la intoxicación por etilenglicol , N. Engl. J. Med. , 1999, 340: 832-838
Ver también
Bibliografía
- (en) H. Yue , Y. Zhao et al. , “ Etilenglicol: propiedades, síntesis y aplicaciones ” , Chem. Soc. Rvdo. , vol. 41,2012, p. 4218-4244 ( ISSN 0306-0012 , DOI 10.1039 / C2CS15359A ).
- (en) DR Lide ( dir. ), CRC Handbook of Chemistry and Physics , Boca Raton, FL, CRC Press ,2007, 88 ª ed. , 2640 p. ( ISBN 978-0-8493-0488-0 ).
Artículos relacionados
enlaces externos
- INRS, "Ficha toxicológica n ° 25" ,septiembre de 2016.
- Tarjeta de seguridad internacional .