Miastenia gravis
Miastenia gravis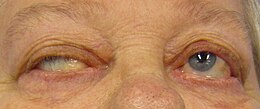 Ptosis en una persona con miastenia gravis que intenta abrir los ojos.
Ptosis en una persona con miastenia gravis que intenta abrir los ojos.
| Especialidad | Neurología |
|---|
| ICD - 10 | G70.0 |
|---|---|
| CIM - 9 | 358,0 |
| OMIM | 254200 |
| Enfermedades DB | 8460 |
| MedlinePlus | 000712 |
| eMedicina | 1171206, 793136, 261815 y 1216417 |
| eMedicina |
neuro / 232 emerg / 325 (emergencia), med / 3260 (embarazo), oph / 263 (ojo) |
| Malla | D009157 |
| Droga | Piridostigmina , neostigmina , ciclosporina , ciclofosfamida , prednisona , azatioprina , rituximab , eculizumab , micofenolato de mofetilo ( d ) , prednisolona , tacrolimus , distigmina ( d ) y piridostigmina |
| Paciente del Reino Unido | Miastenia-gravis-pro |
El gravis (griego μύς "músculo" y ἀσθένεια "debilidad"), en latín gravis es una enfermedad neuromuscular autoinmune crónica , que se manifiesta en diversos grados por debilidad y cansancio excesivo del músculo estriado esquelético , es decir, aquellos que se activan voluntariamente. Debe su nombre al neurólogo alemán Friedrich Jolly (1844-1904) y también tiene un nombre epónimo : Enfermedad de Erb - Goldflam , en honor a los dos clínicos que dieron la descripción más completa. Es causada por anticuerpos circulantes que, en más de tres de cuatro casos, se dirigen a receptores de acetilcolina en la unión neuromuscular , inhibiendo así el efecto excitador de este neurotransmisor .
Histórico
Probablemente fue Thomas Willis quien describió por primera vez a un paciente con miastenia gravis. Jolly nombra la enfermedad acuñando el término “ miastenia gravis pseudoparalytica ” y destaca el deterioro electrofisiológico. Mary Walker propuso en 1934 el tratamiento con fisostigmina . Las anormalidades del timo con respecto a la MG son conocidos, y la timectomía practicadas desde el principio de la XX XX siglo , antes de la comprensión de la fisiopatología y la identificación de génesis autoinmune.
Epidemiología
Su prevalencia varía de 5 a 10 por 100.000 habitantes y su incidencia entre 2 y 20 por año y por millón de habitantes según las series. Puede ocurrir a cualquier edad, su incidencia máxima se refiere al grupo de edad de 20 a 30 años. La proporción de sexos de los pacientes, 3 mujeres por 2 hombres, varía según el grupo de edad (2 mujeres por 1 hombre para los menores de 50 años, 1 mujer por 1 hombre para los mayores de 50 años). Enfermedad esencialmente esporádica, las formas familiares son excepcionales.
Fisiopatología
La fisiopatología putativa de la miastenia gravis consiste en el daño de las proteínas de la membrana postsináptica de la unión neuromuscular por los autoanticuerpos circulantes . El objetivo principal del anticuerpo coincidía con el receptor de acetilcolina (un neurotransmisor ), actuando como un inhibidor competitivo de la acetilcolina y acelerando la degradación del receptor por modulación antigénica. Esto da como resultado un aumento en el número de cuantos de acetilcolina requeridos para producir la despolarización de la membrana postsináptica, lo que conduce a un agotamiento más rápido y profundo de las reservas de acetilcolina presinápticas y clínicamente resulta en fatiga muscular.
A medio plazo, la presencia de estos anticuerpos puede inducir, a través de la activación del sistema del complemento , alteraciones anatómicas de la membrana postsináptica, reduciendo aún más su excitabilidad. En esta etapa, en las formas más graves, pueden aparecer déficits permanentes.
Con la excepción de la D-penicilamina y el trasplante alogénico de médula ósea, no se ha identificado ningún agente exógeno que promueva la aparición de miastenia gravis. Existe una ligera predisposición genética, en particular los grupos HLA B8 (en) y DR3 (en) con el DR1 (en) más específico para la miastenia gravis ocular. Recientemente se han identificado muchos otros autoanticuerpos como patógenos, todos dirigidos a un componente de la membrana postsináptica: anticuerpos anti-MuSK ( quinasa específica de músculo ), anticuerpos anti-agrina, anticuerpos anti-LRP4. Se demuestra el papel del timo en la patogénesis. Es el asiento de la maduración de los linfocitos T . Bajo la estimulación de este último, los linfocitos B se transforman en células plasmáticas que secretan anticuerpos.
Manifestaciones clínicas
Las características clínicas se pueden describir de la siguiente manera:
el síntoma cardinal y fundamental para el diagnóstico es la fatiga de esfuerzo. Por tanto, los síntomas son fluctuantes, se intensifican con el esfuerzo y mejoran en reposo. Suelen ser más marcadas al final del día y pueden empeorar en situaciones estresantes: infección, cirugía, calor… Finalmente, por tanto, el examen clínico puede ser estrictamente normal o poco perturbado, realizando pruebas de estrés que permiten desenmascarar anomalías.
La localización muscular y los síntomas resultantes son variables:
- en el 50% de los casos, el síntoma inicial es ptosis , diplopía o ambas. Estos síntomas suelen ser fluctuantes, por lo general aparecen o empeoran al final del día o al leer o conducir un vehículo. Esta es la queja más evocadora del diagnóstico y permite la única prueba diagnóstica clínica específica. Es característica la aparición de una ptosis con oftalmoparesia (párpados caídos con dificultad de convergencia) a la fijación excéntrica de la mirada durante unos minutos en un paciente asintomático de antemano. En un paciente sintomático, la prueba de cubitos de hielo (mejoría de la ptosis después de colocar hielo durante unos minutos en el párpado sintomático) es menos específica pero muy sugerente;
- en el 20% de los casos, la queja inicial se refiere a una fatiga de las extremidades, con mayor frecuencia en sus partes proximales, lo que puede llevar al diagnóstico a una miopatía. Las pruebas de estrés repetidas pueden desenmascarar la fatiga segmentaria, pero no son muy específicas;
- en el 10% de los casos, el síntoma inicial consiste en astenia aislada (fatiga generalizada, a menudo confundida con debilidad muscular real), lo que no debe sugerir el diagnóstico como tratamiento de primera línea a menos que un médico haya demostrado debilidad muscular real y permita fatigabilidad. estar en primer plano. Ésta es la queja más inespecífica y las pruebas clínicas son de poca utilidad;
- muy raramente, las molestias iniciales consistirán en trastornos fluctuantes de masticación, deglución o debilidad de los extensores del cuello;
- la observación de una afectación óculocefálica global que produce la "facies miasténica" es rara pero muy sugerente (ptosis palpebral asimétrica, labio inferior caído, borrado de arrugas de la frente, posibles trastornos oculomotores extrínsecos y debilidad de los extensores del cuello). La naturaleza fluctuante de esta facies permite distinguirla de muchas otras causas de diplejía facial y confirmar el diagnóstico.
Por definición, los síntomas son solo motores y están ausentes las molestias sensoriales. Sin embargo, debido a esfuerzos compensatorios excesivos, el paciente puede resaltar quejas sensibles y dolorosas (mialgia, artralgia, parestesia) que conducen al diagnóstico de patología reumática, miopatía, trastorno metabólico, polineuropatía o mielopatía.
En el examen, los reflejos miotáticos son normales y la atrofia se observa solo en formas avanzadas graves.
Se distingue entre formas generalizadas, formas bulbares y formas oculares puras. Se pueden formar varias combinaciones (formas óculo-bulbares). Las formas oculares puras se limitan al deterioro de la oculomotricidad extrínseca y la ptosis. De diez a veinte por ciento (10 a 20%) de las formas oculares permanecerán en esta etapa, una forma incapacitante pero leve de la enfermedad, y las otras progresarán a miastenia gravis generalizada.
Las formas bulbares iniciales (15%) incluyen voz nasal con dificultad para articular, debilidad masticatoria con tendencia a dejar caer la mandíbula, dificultad para tragar (disfagia) con comida falsa o vías salivales.
El curso de la enfermedad ocurre típicamente a través de una sucesión de agravamientos y remisiones, posiblemente intercaladas con verdaderas "crisis miasténicas" para las formas generalizadas. Estas crisis, verdaderas urgencias médicas, se definen por un agravamiento brusco con insuficiencia respiratoria aguda, disnea con congestión, trastornos de la deglución con riesgo de aspiración o debilidad severa generalizada con impotencia que no cede al reposo.
La etapa de máxima gravedad se alcanza en tres años en más de las tres cuartas partes de los pacientes.
En 1 a 5% de los casos, la enfermedad se declara por una crisis miasténica inaugural. El diagnóstico es entonces extremadamente difícil y debe evocarse en caso de una desproporción entre la presunta patología causal y la gravedad clínica o en el caso de fallos repetidos inexplicables en los intentos de destete de la ventilación mecánica, el otro diagnóstico a evocar en tales situaciones. siendo una polirradiculoneuritis aguda.
Clasificación clínica de Osserman o MGFA (Myasthenia Gravis Foundation of America)
Esta clasificación describe varias etapas:
- estadio I : debilidad de un músculo del ojo, posible ptosis. Sin otra debilidad muscular
- estadio II : debilidad de los músculos oculares de cualquier gravedad, debilidad leve de otros músculos
- estadio IIa : músculos predominantemente débiles de las extremidades o músculos del tronco
- estadio II b: debilidad predominante en los músculos respiratorios o trastornos de la deglución
- estadio III : debilidad de los músculos oculares de cualquier gravedad, debilidad moderada de otros músculos
- estadio IIIa : músculos predominantemente débiles de las extremidades o músculos del tronco
- estadio III b: predominantemente debilidad de los músculos respiratorios o trastornos de la deglución
- estadio IV : debilidad de los músculos oculares de cualquier gravedad, debilidad grave de otros músculos
- estadio IV a: predominantemente debilidad en los músculos de las extremidades o del tronco
- estadio IV b: debilidad predominante en los músculos respiratorios o trastornos de la deglución. También puede incluir la necesidad de una sonda nasogástrica sin intubación.
- etapa V : intubación necesaria para mantener la respiración
Formas especiales
Las diferentes formas de miastenia grave merecen ser individualizadas por su presentación y su manejo particular.
Miastenia grave autoinmune fetal y neonatal
La placenta es permeable a los anticuerpos. Del diez al veinte por ciento (10 al 20%) de los hijos de madres con miastenia gravis tienen miastenia gravis neonatal que se presenta dentro de los primeros 3 días y generalmente se resuelve en unas pocas semanas (máximo 3 meses). Los síntomas que varían de un niño a otro incluyen: hipotonía, llanto débil, dificultad para succionar o tragar, ptosis, diplejía facial y problemas respiratorios. El tratamiento se basa en el manejo sintomático en una unidad de cuidados intensivos neonatales hasta la resolución y la administración de fármacos anticolinesterásicos. La evolución es en general favorable. En las formas más graves se puede realizar una exanguinotransfusión.
Las formas fetales son más raras y pueden provocar un retraso del crecimiento intrauterino. Excepcionalmente, se producen manifestaciones clínicas graves (hidramnios, artrogriposis, muerte en el útero).
Miastenia gravis autoinmune infantil y juvenil
La miastenia gravis que comienza antes de los 15 años, esta forma merece ser individualizada debido a la difícil distinción de la miastenia gravis congénita no autoinmune y la necesidad, en vista de la edad, de restringir al máximo el uso de corticoides e inmunosupresores.
Miastenia gravis iatrogénica autoinmune
Excepcional, su diagnóstico es generalmente evidente sobre la base de la historia clínica. Implican los mismos autoanticuerpos y responden a los mismos tratamientos que la miastenia gravis clásica. Sin embargo, es probable que respondan a un tratamiento específico. Hasta el momento, solo se han demostrado:
- Miastenia gravis inducida por D-penicilamina. Afecta al 1% de los pacientes tratados con D-penicilamina. La recuperación después de suspender la D-penicilamina dentro de los 6 meses es la regla;
- miastenia gravis inducida por trasplante alogénico de médula con enfermedad de injerto contra huésped.
Patologías asociadas
Ciertas patologías, debido a la frecuencia de su asociación con miastenia gravis o la gravedad de su pronóstico espontáneo inherente, deben ser investigadas sistemáticamente.
Tumores tímicos
En el 10 al 15% de los casos de miastenia gravis, con anticuerpos anti-receptor de acetilcolina, se encuentra un timoma . Los timomas son tumores del mediastino anterior, a menudo benignos, asociados de forma variable con miastenia gravis.
Un marcador de la existencia de estos timomas en pacientes menores de 60 años es el antititina, la indicación quirúrgica es fundamental. Permite especificar si el timoma es benigno (2/3 casos) o maligno según su carácter invasivo o no.
En el 50-70% de la forma joven de miastenia gravis con anticuerpo anti-receptor de acetilcolina, se encuentra hiperplasia tímica. Esta anomalía siempre debe considerarse benigna (lo que no excluye la ablación del timo).
Entre el 15 y el 20% de los pacientes con timoma también muestran signos clínicos de miastenia gravis, y el 25% de los pacientes tienen anticuerpos anti-receptor de acetilcolina (anticuerpos anti-ACh-R) sin mostrar síntomas. Cualquier paciente con un timoma con signos de miastenia gravis tiene anticuerpos positivos, y cualquier masa mediastínica asintomática asociada con anticuerpos anti-ACh-R es un timoma. Si bien la asociación estadística sugiere una correlación entre las dos patologías, el mecanismo exacto de causa y efecto sigue siendo debatido y se están considerando varias hipótesis:
- selección de linfocitos T defectuosos dentro del timoma, responsables de la hipersecreción del autoanticuerpo;
- presentación defectuosa de autoantígenos a las células tímicas, lo que conduce a la no eliminación de los linfocitos T que los reconocen;
- presencia de centros germinales específicos dentro del parénquima tímico que producen autoanticuerpos con mayor facilidad;
- en ancianos, presencia de autoinmunidad inespecífica.
No todos los tipos histológicos de timomas se asocian de la misma manera con la miastenia gravis, y algunos ni siquiera se asocian con ella:
- tipo A: 0%
- tipo AB: 6,8%
- tipo B1: 40%
- tipo B2: 55,6%
- tipo B3: 10%
- carcinoma tímico: 0%
Enfermedades autoinmunes
En el 5 al 15% de los casos, según la serie, se identifica al menos otra enfermedad autoinmune en los miasténicos. Se trata de informes de asociaciones significativas, sin que se haya demostrado ningún vínculo fisiopatológico aparte de la hipótesis de un "terreno disinmune". Estas patologías son distiroidismo autoinmune, artritis reumatoide, lupus eritematoso sistémico, síndrome de Sjögren, polimiositis, enfermedad inflamatoria intestinal crónica, anemia de Biermer, anemia hemolítica autoinmune, insuficiencia suprarrenal.
Exámenes adicionales
Las exploraciones complementarias, además de las destinadas a descartar diagnósticos alternativos, tienen como objetivo confirmar o excluir el diagnóstico y, en caso de confirmación diagnóstica, buscar patologías asociadas. Estos exámenes son:
Para fines de diagnóstico
BiologíaEn la práctica clínica sólo se buscan anticuerpos anti-receptor de acetilcolina y, si están ausentes, anticuerpos anti-MuSK. Su especificidad es del 99%. Su sensibilidad global es superior al 90%, por lo que menos del 10% de la miastenia gravis se define como “seronegativa”. Más precisamente, la sensibilidad de los anticuerpos anti-receptor a la acetilcolina es del 90% para la miastenia gravis generalizada y del 50% para la miastenia grave ocular. Siempre que la prueba de anticuerpos anti-receptor de acetilcolina sea negativa, la sensibilidad de los anticuerpos anti-MuSK es del 40% para la miastenia grave generalizada y marginal para la miastenia grave ocular.
Sus excelentes especificidades los convierten en la mejor prueba para confirmar el diagnóstico en caso de fuerte sospecha clínica (valor predictivo positivo de solo el 1% para la población general).
Recientemente, en caso de miastenia gravis doble negativa, también es posible analizar anticuerpos LRP4.
Exámenes electrofisiológicosSon necesarios dos exámenes electrofisiológicos:
- un estudio electromiográfico que incluye:
- un electromiograma de rutina que suele ser normal. Sin embargo, se pueden observar actividades de reinervación en casos avanzados graves,
- un estudio electromiográfico con estimulación repetitiva supra-máxima de un nervio motor. La prueba se considera positiva cuando la disminución de la amplitud del potencial de la unidad motora (PUM) es superior al 10%. Esta prueba es inespecífica y tiene una sensibilidad del 79% para la miastenia gravis generalizada y del 50% para la miastenia grave ocular.
- un estudio electromiográfico de "fibra única" con medición de un jitter (variación de la latencia entre la estimulación y el potencial de la unidad motora para una fibra determinada durante la estimulación repetitiva de un nervio motor) significa en el estudio de muchas fibras que requieren un examinador experimentado y especializado equipo. La prueba se considera positiva cuando se observa un aumento en este jitter por encima de los estándares de laboratorio para el músculo estudiado. Esta prueba no es específica y tiene una sensibilidad del 98% para la miastenia gravis generalizada y del 80% para la miastenia grave ocular.
- un estudio de las velocidades de conducción nerviosa. Este examen debe ser normal para que las anomalías del electromiograma se consideren relevantes.
La excelente sensibilidad de la electromiografía la convierte en la mejor prueba para descartar el diagnóstico en caso de baja sospecha clínica (valor predictivo negativo indeterminado si la proporción de pacientes en el grupo de estudio es superior al 1%).
Prueba farmacológicaLa prostigmina se utiliza bien como prueba terapéutica por vía oral, bien por vía intramuscular o especialmente por vía intravenosa ante un síntoma clínico que no hablaba del plan electrofisiológico o de urgencia (ptosis, diplopía, trastornos del habla o respiratorios). se considera positivo si produce una mejoría de los síntomas o signos electrofisiológicos. A veces se compara con una prueba de placebo.
En busca de patologías asociadas
BiologíaSe medirán sistemáticamente los marcadores de patologías autoinmunes potencialmente asociadas con la miastenia gravis. Esto incluye marcadores de inflamación, hormonas tiroideas y anticuerpos anti-piroperoxidasa, factores anti-nucleares, anticuerpos anti-nucleares, hematograma, ionograma, función hepática y renal, vitamina B12 y folato.
Escáner de tomografía computarizada torácicaRealizado sistemáticamente para buscar timoma (sensibilidad del 99%, especificidad del 95%) e hiperplasia tímica (sensibilidad del 50%, especificidad del 95%).
Diagnóstico diferencial
El diagnóstico diferencial es amplio y depende de la presentación clínica. Podemos mencionar en particular:
- otros síndromes miasténicos: congénita miastenia Gravis , síndrome miasténico de Lambert-Eaton , botulismo , ciertos venenos de serpiente , de organofósforo o envenenamiento de magnesio;
- miopatías;
- neuropatías periféricas;
- patologías reumáticas;
- alteraciones de líquidos y electrolitos;
- endocrinopatías;
- anemia;
- ptosis adquirida, congénita y traumática;
- estrabismo descompensado;
- trastornos funcionales, trastornos psiquiátricos y síndrome de fatiga crónica.
Pronóstico
El pronóstico es específico para cada paciente. Sin embargo, podemos describir algunas generalidades:
La gravedad de la miastenia gravis está relacionada con la aparición de crisis miasténicas con dificultad respiratoria y potencialmente mortales. Este riesgo es más alto al comienzo de la enfermedad, con el 75% de las convulsiones que ocurren en los primeros dos años de desarrollo.
Si no se trata, el curso de la miastenia gravis generalizada puede ser fatal. El pronóstico vital de las formas que permanecen oculares no está involucrado.
En casos muy raros, hay remisiones espontáneas de la enfermedad, cuya duración es variable.
Del 10 al 20% responderá poco o no al tratamiento y desarrollará impotencia motora variable. Los factores de mal pronóstico y mala respuesta terapéutica son: la presencia de un timoma, la presencia de anticuerpos anti-MuSK y formas sero-negativas.
Cuidado terapéutico
El manejo de la miastenia gravis se puede dividir esquemáticamente en tratamiento sintomático, tratamiento de mantenimiento y tratamiento de crisis de la enfermedad, tratamiento de patologías asociadas y medidas generales. Los principios generales son:
Tratamientos sintomáticos para la miastenia gravis
Medicamentos anticolinesterasaInhibidores de la acetilcolinesterasa, una enzima que degrada la acetilcolina , constituyen el tratamiento sintomático de primera línea. Los más utilizados son la piridostigmina (Mestinon) y el cloruro de ambenonio (Mytelase). El uso de otros fármacos anticolinesterásicos (como la neostigmina ) se ha vuelto marginal aparte de la crisis miasténica. No se ha demostrado su eficacia en la miastenia gravis seronegativa o con anticuerpos anti-MuSK.
Tratamiento a largo plazo para la miastenia gravis
Corticosteroides e inmunosupresores.Los corticosteroides, como un régimen progresivo de prednisona (Cortancyl) o prednisolona (Solupred), los inmunosupresores, la azatioprina (Imurel), que tiene la mayor eficacia demostrada, y el micofenolato de mofetilo (Cellcept) son el segundo tratamiento más importante. Los corticosteroides pueden iniciarse en dosis muy bajas y con una reevaluación clínica cercana, siendo común un empeoramiento clínico transitorio.
Ahora se ha demostrado que la adición de un tratamiento combinado con corticosteroides e inmunosupresores para la miastenia gravis generalizada insuficientemente controlada con fármacos anticolinesterasa mejora el estado clínico a los dos años en comparación con la adición de corticosteroides o inmunosupresores por separado. Algunos expertos recomiendan su uso como tratamiento de primera línea para formas seronegativas o con anticuerpos anti-MuSK.
Los inmunosupresores no son muy eficaces para las formas oculares.
De forma marginal, los tratamientos biológicos como el rituximab (Mabthera), un anticuerpo monoclonal quimérico dirigido a la molécula CD20 expresada específicamente por los linfocitos B , se han utilizado con cierto éxito en formas graves.
Plasmaféresis e inmunoglobulinas intravenosasEstos tratamientos tienen poco lugar aparte de las crisis miasténicas ( ver más abajo ). Sin embargo, se utilizan excepcionalmente para las formas más severas resistentes a otros tratamientos o en caso de degradación clínica rápida.
Tratamientos de patologías asociadas
Timectomía y tratamientos adyuvantesEl descubrimiento de un timoma es una indicación absoluta de timectomía y requiere un seguimiento radiológico prolongado en busca de recurrencias neoplásicas. En caso de resección incompleta, infiltración de tejidos vecinos o descubrimiento de metástasis, se debe ofrecer un tratamiento adyuvante consistente en radioterapia y / o quimioterapia según corresponda.
El beneficio clínico de la timectomía en ausencia de timoma aún se debate. Sin embargo, se recomienda en caso de descubrimiento de hiperplasia tímica con presencia de anticuerpos anti-receptor de acetilcolina en pacientes menores de 40 años. Un estudio aleatorizado de 2016 también encontró una mejoría clínica en los síntomas de la miastenia gravis después de la timectomía, incluso en ausencia de hiperplasia tímica.
Es posible un empeoramiento sintomático posquirúrgico transitorio. En los primeros meses posteriores a la timectomía, se puede intentar la suspensión del fármaco si aparece una mejoría sintomática o incluso una remisión.
Otros tratamientosSon necesarios tratamientos específicos en caso de descubrimiento de una patología autoinmune asociada.
Manejo de crisis miasténicas
Cuidados de apoyoCualquier aparición rápida de insuficiencia respiratoria, disnea con congestión bronquial, trastornos de la deglución o debilidad generalizada objetivada por un médico justifica el traslado médico a una institución hospitalaria con unidad de cuidados intensivos. Al ingreso se realizará una evaluación de las vías respiratorias, respiración, circulación y neurología, así como una medición de la capacidad vital (CV). Una alteración de la conciencia, una capacidad vital inferior al 25% del valor teórico o un agotamiento respiratorio clínico justifican la intubación y el traslado a una unidad de cuidados intensivos para ventilación mecánica y posible estabilización hemodinámica. En otros casos, es suficiente la atención ordinaria con una evaluación periódica de la capacidad vital.
Corrección de factores desencadenantes y promotores reversiblesEstos factores deben investigarse y corregirse tan pronto como se realicen maniobras vitales. Se trata principalmente de causas iatrogénicas (ver Contraindicaciones de medicamentos), infecciones, descompensación de otras patologías crónicas del paciente y aumentos de temperatura, endógenos o exógenos.
El caso de las convulsiones que ocurren durante el embarazo es especial y la posibilidad de que ocurran debe haber sido discutida previamente con la paciente. Las convulsiones graves que no responden al tratamiento sintomático requieren un tratamiento adecuado.
Descartar una sobredosis de anticolinesterasasEl principal diagnóstico diferencial de la crisis miasténica es la sobredosis de anticolinesterasa. Se sospecha sistemáticamente ante la ingesta diaria de más de 480 mg de piridostigmina o síntomas muscarínicos: bradicardia, miosis bilateral, hipersecreciones, degradación fecal, etc. En caso de duda, el empeoramiento clínico tras la administración de neostigmina confirmará el diagnóstico de sobredosis. El tratamiento es entonces puramente de apoyo, además de la administración de atropina por sus efectos antimuscarínicos.
Tratamientos sintomáticosLa administración de neostigmina es el tratamiento sintomático de primera línea. Si aparecen síntomas muscarínicos, se debe agregar atropina.
En caso de empeoramiento clínico durante el tratamiento, se debe considerar una sobredosis de fármacos anticolinesterasa.
En caso de mala respuesta terapéutica (fracaso de la detubación), el tratamiento de segunda línea se basa en la repetición de plasmaféresis y / o curas con inmunoglobulinas intravenosas.
Si esto falla, los corticosteroides y los inmunosupresores son el tratamiento de tercera línea. Sin embargo, sus indicaciones deben preguntarse cuidadosamente, siendo común un empeoramiento clínico transitorio.
Medidas generales y cuidados paramédicos
Contraindicaciones de medicamentos. Tarjeta miasténicaEl Ministerio de Sanidad francés ha publicado una tarjeta de atención y emergencia para personas con miastenia gravis. Se recomienda encarecidamente que el paciente lleve esta tarjeta en la que se mencione su enfermedad, su tratamiento, sus últimas vacunas y la lista de medicamentos contraindicados en la miastenia gravis. Pueden obtenerlo de las consultas de referencia o contactando con la AFM-téléthon].
Higiene de vidaComo ocurre con cualquier patología crónica, la miastenia gravis requiere que el paciente sea educado sobre su enfermedad y, en particular, sobre los factores que favorecen las crisis miasténicas. Se debe fomentar la participación en ejercicio físico moderado, adaptado al estado del momento, con descansos frecuentes.
Atención paramédicaEn formas severas o resistentes al tratamiento en profundidad, puede ser necesario el apoyo social y por parte de especialistas en fisioterapia, logopedia, terapia ocupacional, rehabilitación o psicología, así como la derivación del paciente a una combinación de terapias.
Prepárese para embarazos y cirugíasEn general, el embarazo y la cirugía son una de las principales causas de convulsiones miasténicas, que ocurren en el 30% de los casos. Para minimizar los riesgos, algunos autores recomiendan la realización preparto y prequirúrgica de sesiones de plasmaféresis o curas con inmunoglobulinas, así como una evaluación que incluya pruebas funcionales respiratorias. Un parto siempre debe tener lugar en una institución hospitalaria con una unidad de cuidados intensivos y una unidad de reanimación neonatal. La detubación nunca debe realizarse hasta que se confirme la capacidad del paciente para participar.
Durante el embarazo, los corticosteroides y los inmunosupresores deben usarse en consulta con un ginecólogo.
Notas y referencias
- (in) MB Walker , " Tratamiento de la miastenia gravis con fisostigmina " , Lancet , vol. 1,1934, p. 1200-1201 ( DOI 10.1016 / S0140-6736 (00) 94294-6 )
- (en) Phillips LH, "La epidemiología de la miastenia gravis " Ann NY Acad Sci. 2003; 998: 407-12
- Colegio de Profesores de Neurología. Miastenia gravis
- (En) Carr AS, Cardwell CR, PO McCarron, J McConville, "Una revisión sistemática de estudios epidemiológicos basados en la población en miastenia gravis" BMC Neurol. 2010; 10:46.
- (en) Bradley et al. Neurología en la práctica clínica , 5 ª ed., Butterworth-Heinemann, 2007
- Goulon-Goeau et al. “Miastenia gravis y síndromes miasténicos” EMC-Neurologie , 17-172-B-10, 2002, Elsevier, resumen en línea
- B. Eymard “Los anticuerpos en la miastenia grave” opinión Neurológica 2009; 165 (2): 125-205 DOI : 10.1016 / j.neurol.2008.11.020
- (en) Zhang B, C Shen, Bealmear B, Ragheb S, Xiong inodoro, Lewis RA, Lisak RP, Mei L. " Autoanticuerpos a la agrina en la miastenia gravis pacientes ' PLoS One , 2014; 3: e91816 DOI : 10.1371 /journal.pone.0091816
- (en) W. Allan. “La patogénesis de la miastenia” Up-to-Date 2012
- (en) Howard et al. "Correlaciones clínicas de anticuerpos que se unen, bloquean o modulan los receptores de acetilcolina humanos en la miastenia gravis " Ann NY Acas Sci. 1987
- (en) SJ Bird "Las manifestaciones clínicas de la miastenia gravis " Up-to-Date, 2013
- (en) Bershad et al. “ Crisis de miastenia gravis ” South Med J. 2008; 101 (1): 63-9. DOI : 10.1097 / SMJ.0b013e31815d4398
- Gaumond "Trastornos oculares de la miastenia gravis" EMC-Neurología , 2005 DOI : 10.1016 / j.emcn.2005.08.002
- (en) Pelak y cuándo "Ocular miastenia" Fecha Hasta a la de 2013
- (en) Spillane J, E Higham, Kullmann DM. “ Miastenia gravis ” BMJ 2012; 345: e8497
- (en) Jaretzki A, Barohn RJ, Ernstoff RM et al. , “ Miastenia gravis: recomendaciones para estándares de investigación clínica. Grupo de trabajo del Consejo Asesor Científico Médico de la Fundación Estadounidense de Miastenia Gravis ” , Neurología , vol. 55, n o 1,2000, p. 16-23 ( PMID 10891897 , leer en línea )
- (en) Finnis MF Jayawant S, " Miastenia gravis juvenil: una perspectiva pediátrica " , Autoinmune Dis , vol. 2011,2011, p. 404101. ( PMID 22110902 , PMCID PMC3206364 , DOI 10.4061 / 2011/404101 , lea en línea [html] )
- Anticuerpo antititina en la miastenia gravis de aparición temprana y tardía. Szczudlik P, Szyluk B, Lipowska M, Ryniewicz B, Kubiszewska J, Dutkiewicz M, Gilhus NE, Kostera-Pruszczyk A. Acta Neurol Scand. 2014 (junio). Doi: 10.1111 / ane.12271. [Publicación electrónica antes de la impresión]
- El timo, timoma y miastenia gravis Fujii Y, Surg Today 2013 May; 43 (5): 461-6. doi: 10.1007 / s00595-012-0318-2
- clínica y funcional de la clasificación de la OMS sobre neoplasias epiteliales tímicas humanas: un estudio de 146 tumores consecutivos. Okumura M, Miyoshi S, Fujii Y, Takeuchi Y, Shiono H, Inoue M, Fukuhara K, Kadota Y, Tateyama H, Eimoto T, Matsuda H, Am J Surg Pathol 2001 Enero; 25 (1): 103-10.
- (en) Mercelis et al. “Utilidad diagnóstica de la electromiografía estimulada de una sola fibra del músculo orbicular de los ojos en pacientes con sospecha de miastenia ocular” Muscle Nerve 2011; 43 (2): 168-70.
- (en) Preston et al. Electromiografía y alteraciones neuromusculares. Correlaciones clínico-electrofisiológicos , 2 ª ed., Elsevier, 2005
- (en) Taraldsen Heldan. “Miastenia grave seropositivo. Un estudio epidemiológico nacional » Neurología 2009
- (en) Trakas et al. “Desarrollo de un ensayo de diagnóstico de alta sensibilidad para autoanticuerpos de tirosina quinasa específica de músculo (MuSK) en miastenia gravis” J Neuroimmunol . 2011; 240-241: 79-86.
- (en) Vincent et al. “Anticuerpo del receptor de acetilcolina como prueba de diagnóstico para la miastenia gravis : resultados en 153 casos validados y 2967 ensayos de diagnóstico” J Neurolo Neurosurg Psych. 1985; 48 (12): 1246-52.
- (en) Witoonpanich et al. “Estudio electrofisiológico e inmunológico en miastenia gravis : sensibilidad diagnóstica y correlación” Clin Neurophysiol. 2011; 122 (9): 1873-7.
- (en) Zambelis et al. “Estimulación nerviosa repetitiva de los músculos faciales e hipotenares: sensibilidad relativa en diferentes subgrupos de miastenia gravis” Eur Neurol. 2011; 65 (4): 203-7.
- (en) Lindstrom et al. "Anticuerpo contra el receptor de acetilcolina en la miastenia gravis. Prevalencia, correlatos clínicos y valor diagnóstico » Neurología 1976.
- (en) Bird "Diagnóstico de la miastenia gravis " Up-to-Date , 2013
- Autoanticuerpos contra la proteína 4 relacionada con las lipoproteínas en pacientes con miastenia gravis doble seronegativa. Zhang B1, Tzartos JS, Belimezi M, Ragheb S, Bealmear B, Lewis RA, Xiong WC, Lisak RP, Tzartos SJ, Mei L. Arch Neurol. Abril de 2012; 69 (4): 445-51. doi: 10.1001 / archneurol.2011.2393. Epub 2011 12 de diciembre
- (en) Bird "diferencial Diognosis de miastenia gravis" Up-to-Date 2012
- (en) Bird "El tratamiento de la miastenia" Up-to-Date , 2013
- (en) Howard et al. Miastenia gravis. Un manual para el proveedor de atención médica , Myasthenia Gravis Foundation of America, 2008
- (en) Oro R, Schneider-Gold C, “ Las normas actuales y futuras en el tratamiento de la miastenia gravis ” , Neurotherapeutics , vol. 5, n o 4,2008, p. 535-41. ( PMID 19019304 , PMCID PMC4514693 , DOI 10.1016 / j.nurt.2008.08.011 , leer en línea [html] )
- (en) Mandawat et al. “Análisis comparativo de la opción terapéutica utilizada para la miastenia gravis ” Ann Neurol. 2010; 68 (6): 797-805.
- " cloruro de ambenonio " en www.vidal.fr (consultado el 1 st 08 2015 )
- (en) Collongues N, O Casez, Lacour A. et al. "Rituximab en miastenia refractaria y no refractaria: un estudio multicéntrico retrospectivo " Muscle Nerve 2012; 46: 687-91
- (en) Gil I. Wolfe, Henry J. Kaminski, Inmaculada B. Aban et al., " Ensayo aleatorio de miastenia grave en timectomía " , New England Journal of Medicine (NEJM \ / MMS), vol. 375, n o 6,11 de agosto de 2016, p. 511-522 ( ISSN 0028-4793 , DOI 10.1056 / nejmoa1602489 , leer en línea ).
- (en) Goldenberg, WD y Shah, AK , " Myasthenia Gravis " , eMedicine (consultado el 5 de mayo de 2012 )
- (fr) Este artículo está tomado parcial o totalmente del artículo de Wikipedia en inglés titulado " Myasthenia gravis " ( ver la lista de autores ) .