Enfermedad del sueño
Tripanosomiasis africana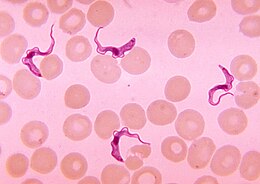 Trypanosoma brucei en la sangre de un paciente con tripanosomiasis africana, comúnmente conocida como enfermedad del sueño.
Trypanosoma brucei en la sangre de un paciente con tripanosomiasis africana, comúnmente conocida como enfermedad del sueño.
| Especialidad | Enfermedad infecciosa |
|---|
| ICD - 10 | B56 |
|---|---|
| CIM - 9 | 086,5 |
| Enfermedades DB | 29277 13400 |
| MedlinePlus | 001362 |
| eMedicina | 228613 |
| eMedicina | med / 2140 |
| Malla | D014353 |
| Incubación min | 7 días |
| Incubación máxima | 21 días |
| Síntomas | Signo de Winterbottom ( en ) , fiebre periódica ( d ) , dolor de cabeza , malestar general , anemia , artralgia , trastornos del sueño , mareos , foco primario de infección ( d ) , taquicardia , hinchazón , caquexia y sopor ( en ) |
| Enfermedad transmitida | Transmisión vectorial ( d ) |
| Causas | Trypanosoma brucei , Trypanosoma gambiense ( d ) y Trypanosoma brucei rhodesiense ( d ) |
| Droga | (RS) -eflornithine , Nifurtimox , la suramina y la pentamidina |
| Paciente del Reino Unido | Tripanosomiasis africana |
La tripanosomiasis africana , comúnmente conocida como enfermedad del sueño , es una forma de tripanosomiasis , una enfermedad parasitaria causada por tripanosomas ( flagelado de protozoos ), que se transmite por la picadura de la mosca tsetsé o mosca tsetsé y que afecta a animales y humanos. Dos subespecies de un tripanosoma ( Trypanosoma brucei ) generan diferentes patologías en el ser humano: Trypanosoma brucei ssp. gambiense ( África Occidental ) y Trypanosome brucei ssp. rhodensiense ( África Oriental ).
La enfermedad es endémica en partes del África subsahariana , cubre alrededor de 36 países y amenaza a 60 millones de personas. Se estima que entre 50.000 y 70.000 personas están infectadas actualmente por año, y el número ha disminuido ligeramente en los últimos años.
Tres grandes epidemias se han producido en los últimos cien años, uno de cada 1896 - 1906 (que se dice que han matado a cerca de un millón de personas en la cuenca del Congo ) y los otros dos en 1920 y 1970 . La tripanosomiasis del ganado se llama nagana ("estar deprimido" o "debilidad" en zulú ).
Características clínicas
Además de la picadura de la mosca tsetsé, la enfermedad se puede contraer de la siguiente manera:
- De madre a hijo: el tripanosoma puede atravesar la barrera placentaria e infectar al feto , con riesgo de muerte perinatal.
- En el laboratorio: Infecciones accidentales, por ejemplo, durante la manipulación de la sangre de una persona infectada o mediante un trasplante de órgano, aunque esto es raro.
- Sexualmente: tener sexo sin protección con una persona afectada podría transmitirlo pero los casos comprobados son anecdóticos.
Los síntomas comienzan con fiebre, generalmente intermitente, dolor de cabeza y dolor en las articulaciones. Un chancro (hinchazón en el punto de inoculación) se ve en uno de cada cinco casos en la forma de Rhodesia, pero es excepcional en la forma de Gambia. A medida que los parásitos ingresan al cuerpo a través de la sangre y el sistema linfático , los ganglios linfáticos a menudo se inflaman y crecen hasta alcanzar tamaños enormes. Puede aparecer el signo de Winterbottom , linfadenopatía cervical posterior (ganglios linfáticos detrás del cuello). Si no se trata, la enfermedad abruma gradualmente las defensas de la persona infectada y aparecen nuevos síntomas, como anemia , problemas endocrinos , cardíacos y renales . La enfermedad entra en su fase de trastornos neurológicos cuando el parásito cruza la barrera hematoencefálica . Los síntomas de esta segunda fase dan nombre a la enfermedad; Además de la confusión mental y los trastornos de la coordinación, el ciclo del sueño se interrumpe, lo que provoca episodios de fatiga que se alternan con períodos de inquietud maníaca que aparecen durante el día con somnolencia y por la noche con insomnio . Si no se trata, la enfermedad es fatal, con un deterioro mental progresivo que conduce al coma y la muerte. El daño causado en la fase neurológica puede ser irreversible.
La duración de la enfermedad varía según el parásito involucrado. La evolución es más rápida en el caso de Trypanosomia rhodesiense (de unas pocas semanas a unos meses). Puede llegar a varios años en el caso de Trypanosomia gambiense .
La afectación cardíaca se puede ver en la forma de Gambia, esencialmente como una anomalía en el electrocardiograma sin consecuencias. Este ataque permanece en un segundo plano, a diferencia de la forma americana de tripanosomiasis ( enfermedad de Chagas ). La forma de Gambia también puede ser completamente asintomática.
Distribución geográfica y epidemiológica
La enfermedad se presenta en dos formas, dependiendo del parásito involucrado, Trypanosoma brucei gambiense o Trypanosoma brucei rhodesiense . TBgambiense se encuentra en África central y occidental; provoca un daño crónico que puede continuar de forma pasiva durante meses o años antes de que aparezcan los síntomas. La tuberculosis de Rhodesia está provocando una forma aguda de la enfermedad, pero sus efectos son mucho más limitados. Se encuentra en el sur y este de África; la infección comienza en unas pocas semanas, es más virulenta y se desarrolla más rápidamente. Según estimaciones recientes , La enfermedad del sueño es responsable de la pérdida de la esperanza de vida (9 a 10 años) de 2 millones de personas. Evaluaciones recientes Indican que más de 60 millones de personas en alrededor de 250 hogares están en riesgo de contraer la enfermedad, y hay alrededor de 300,000 casos nuevos cada año. En 2011, un informe de los CDC predijo que al ritmo del calentamiento global actual, algunas regiones templadas podrían convertirse en áreas en riesgo de contaminación; si actualmente están expuestas 75 millones de personas, estiman que en 2090, de 40 a 77 millones más de personas estarán expuestas al riesgo de transmisión de enfermedades.
La enfermedad se ha encontrado en 36 países, todos en África subsahariana . Los seres humanos son el principal reservorio de Trypanosoma brucei gambiense , pero también se pueden encontrar otras especies en los cerdos y otros animales. Los animales salvajes y el ganado son el principal reservorio de TB rhodesiense .
Los tábanos ( Tabanidae ) y Stomoxydinae probablemente pueden desempeñar un papel en la transmisión pasiva (en situaciones especiales) no solo de nagana (la forma animal de la enfermedad del sueño) sino también de la forma humana de la enfermedad.
Ciclo parasitario
La mosca tsetsé es grande, marrón y sigilosa. La picadura se siente como una aguja caliente clavada en la carne. Durante una ingestión de sangre en el mamífero huésped, una mosca tsetsé infectada (del género Glossina ) inyecta los tripomastigotes metacíclicos en el tejido de la piel. Los parásitos ingresan al sistema linfático y pasan al torrente sanguíneo (1). Dentro del hospedador, se convierten en tripomastigotes que circulan en la sangre (2) y son transportados a otros lugares del cuerpo, alcanzando otros fluidos biológicos (p. Ej., Linfa , líquido cefalorraquídeo ) y continúan replicándose por escisiparidad (3). El ciclo parasitario del tripanosoma africano está representado por etapas extracelulares. Una mosca tsetsé se infecta con tripomastigotes circulantes al ingerir sangre de un huésped mamífero infectado (4) (5). En el intestino de la mosca, los parásitos se transforman en tripomastigotes procíclicos, se multiplican por fisiparidad (6), abandonan el intestino y se convierten en epimastigotes (7). Los epimastigotes llegan a las glándulas salivales de la mosca y continúan multiplicándose por fisión (8). El ciclo en la mosca dura aproximadamente 3 semanas.
Diagnóstico de laboratorio
El diagnóstico se basa en la evidencia de tripanosomas mediante el examen microscópico del líquido de un chancro, líquido de la punción de un ganglio linfático , sangre, médula ósea o, en las últimas etapas de la infección, líquido cefalorraquídeo recolectado por punción lumbar . Los tripanosomas móviles se buscan en una preparación húmeda y luego se fija una preparación y se tiñe con el método de Giemsa . Se pueden utilizar técnicas de concentración antes del examen microscópico. Para las muestras de sangre, se utiliza la centrifugación, para otras muestras, como el líquido cefalorraquídeo , las técnicas de concentración incluyen la centrifugación seguida del examen del sedimento. El aislamiento del parásito por inoculación en ratas o ratones es un método sensible, pero su uso se limita a la tuberculosis rhodesiense . La detección de anticuerpos tiene una sensibilidad y una especificidad demasiado variables para sacar conclusiones clínicas. Además, en las infecciones por TB rhodesiense , la seroconversión ocurre después del inicio de los síntomas clínicos y, por lo tanto, tiene un beneficio limitado.
Se encuentran disponibles tres pruebas serológicas similares para la detección del parásito de Gambia: micro-CATT, wb-CATT y wb-LATEX. El primero utiliza sangre coagulada, mientras que los demás utilizan muestras de sangre completa. Estas pruebas consisten en hacer reaccionar una gota de sangre sobre un reactivo de una tarjeta. Son fáciles de usar y constituyen un medio eficaz de detección. La serología es, en cambio, de poca utilidad en las formas rodesianas, debiendo privilegiarse y ser más fácil el diagnóstico parasitológico, debido a una mayor concentración de parásitos.
En las formas neurológicas, la punción lumbar muestra, además del parásito, un aumento del nivel de proteínas así como la presencia de glóbulos blancos .
Tratamiento
El tratamiento estándar actual para la primera etapa de la enfermedad es pentamidina por vía intravenosa (para Tb gambiense ) o intramuscular, durante una semana, siendo los principales efectos secundarios hipoglucemia y dolor en el lugar de la inyección; seguido de suramina intravenosa (para Tbrhodesiense ) durante un período más largo.
El tratamiento estándar actual para la segunda etapa de la enfermedad (fase neurológica) es melarsoprol por vía intravenosa a 2,2 mg / kg por día durante 10 días consecutivos.
La primera línea de terapia alternativa incluye 0,6 mg / kg de melarsoprol por vía intravenosa el día 1, 1,2 mg / kg de melarsoprol por vía intravenosa el día 2 y 1,2 / día por vía intravenosa combinada con 7,5 mg / kg por vía oral de nifurtimox dos veces al día los días 3 a 10 o eflornitina por vía intravenosa 50 mg / kg cada seis horas durante 14 días.
En áreas resistentes al melarsoprol o en pacientes que han recaído después de la monoterapia con melarsoprol, el tratamiento debe ser melarsoprol y nifurtimox o eflornitina.
Los siguientes protocolos tradicionales ya no deben usarse:
- Antiguo "régimen" terapéutico de 26 días de melarsoprol (3 series de 3,6 mg / kg / día por vía intravenosa durante 3 días, con un descanso de siete días entre series) (este protocolo es menos fácil y los pacientes están menos dispuestos a completar el tratamiento completo );
- Tratamiento gradual con melarsoprol: ciclo de diez días de melarsoprol (0,6 mg / kg IV el día 1, 1,2 mg / kg IV el día 2 y 1,8 mg / kg los días 3 a 10). Se suponía que este protocolo reduciría el riesgo de encefalopatía inducida por tratamiento, pero ahora se sabe que está asociado con un mayor riesgo de recaída y una mayor incidencia de encefalopatía ;
Todos los pacientes deben ser seguidos durante dos años con punciones lumbares semestrales para detectar recaídas.
Historia de tratamiento
En 1910, el mismo año del descubrimiento de Bruce , se introdujo el primer fármaco activo contra la enfermedad del sueño, Salvarsan ( arsfenamina ), desarrollado por Paul Ehrlich y Sahachiro Hata . Sin embargo, el uso de este derivado del arsénico presenta graves riesgos, incluida la ceguera . Unido a una toxicidad que lo vuelve difícil de manejar, la eficacia de Salvarsan fomenta más investigaciones en la dirección de los derivados del arsénico, y otras moléculas se obtendrán por derivación del ácido aminofenolarsinoso: triprsamida (it) y melarsen, ácidos arsínicos, con núcleo de arsénico pentavalente. ; arsenofenilglicina, óxido de melarseno y melarsoprol, óxidos de ácidos arsínicos, con un anillo trivalente.
Sin embargo, no fue hasta 1919 que se completó el trabajo de Walter Jacobs y Michael Heidelberger , lo que permitió a Wade Brown y Louise Pearce introducir la triparsamida. A partir de entonces aparecieron tres tripanocidas durante los años 1920, suramina (no arsenical), orsanina y triparsamida, se utilizan en vastas campañas de detección y tratamiento masivo. La suramina (Bayer 205), sintetizada en 1917, pero cuya fórmula, mantenida en secreto, no fue dilucidada por Ernest Fourneau hasta 1924 en el Institut Pasteur , fue introducida en 1920. Se utilizó en la primera etapa de la enfermedad. O en caso de arseno-resistencia. Su administración por vía intravenosa y en dosis elevadas limita su uso. Sin embargo, ya pesar de su importante toxicidad, todavía se utilizaba en 2001 en la fase de sangre linfática. La triparsamida (it) , derivada del atoxilo, se introduce en 1921 y se comercializa en 1930 con el nombre de Tryponarsil. Es el primer fármaco activo en la fase cerebroespinal. Sin embargo, incluso reducido en una dosis progresiva, su toxicidad ocular afecta al 2% de los pacientes tratados durante la campaña dirigida por Jean Laigret en la República del Congo a mediados de la década de 1920, y el 4,4% de los tratados por Eugène Jamot en Camerún. En el misma época. Y en pacientes administrados en un estadio avanzado, la tasa de letalidad iatrogénica es del 6,6%. La orsanina sódica (Fourneau 270) se utilizó a partir de 1925 y durante unos quince años, ya sea sola en pacientes "en período dudoso", o en combinación con triparsamida en pacientes en la segunda etapa.
Desde principios de la década de 1930, en el Congo Belga , aparecieron los primeros casos de arsenorresistencia y, a partir de 1934, la triparsamida se asoció con otras moléculas, entre ellas la suramina y la orsanina sódica.
Orsanine fue abandonado con el descubrimiento, en 1939, de pentamidina , una molécula muy eficaz en la primera fase de la enfermedad, que se utiliza comúnmente en África occidental como un agente profiláctico, y que durante la década de 1950 reducen las tasas de infección. Tan importante que creen que es posible erradicar la enfermedad. La suramina, generalmente asociada a la triparsamida, siguió siendo el fármaco más utilizado en el tratamiento de la enfermedad del sueño hasta finales de la década de 1960, reemplazado gradualmente a partir de 1949 por el melarsoprol , desarrollado por Friedheim, y que tiene una toxicidad menor que todos los arsenicales utilizados hasta entonces.
La eflornitina finalmente (difluorometilornitina o DFMO), el tratamiento más moderno, fue desarrollado en la década de 1970 por Albert Sjoerdsmanot y ha sido objeto de ensayos clínicos en la década de 1980 La molécula fue autorizada a Estados Unidos por la Administración de Alimentos y Medicamentos en 1990, pero Aventis , la compañía farmacéutica responsable de su fabricación, dejó de producir en 1999. Sin embargo, en 2001, Aventis, en asociación con Médicos Sin Fronteras y la Organización Mundial de la Salud , firmó un acuerdo a largo plazo para fabricar y distribuir el medicamento. Su eficacia ha sido demostrada, su tolerancia es mejor que la del melarsoprol. Sin embargo, hay recaídas bajo este tratamiento, en poco menos del 10% de los casos, pero la mayoría de las veces son fatales. El fexinidazol podría ser una alternativa a este tratamiento.
Los tratamientos combinados podrían reducir este riesgo de recaída, entre los que la combinación eflornitina- nifurtimox parece particularmente prometedora.
El megazol, una molécula biológicamente activa con actividad tripanocida, fue objeto de estudios científicos hace algunos años. De hecho, esta molécula, activa en forma de pastilla (vía oral) elimina el 100% del parásito en dos días (pruebas in vitro e in vivo en chimpancés y cerdos). Sin embargo, se sospecha que esta molécula es cancerígena y su desarrollo se ha detenido.
Perspectivas y vías de investigación
Se ha decodificado el genoma del parásito y se han identificado varias proteínas como posibles dianas para el tratamiento farmacológico. La decodificación del ADN también ha arrojado luz sobre por qué ha sido tan difícil producir una vacuna para esta enfermedad. T brucei tiene más de 800 genes que producen proteínas que utiliza para evitar la detección por parte del sistema inmunológico. (Berriman, et al. , 2005)
Un equipo de investigación internacional que trabaja en la República Democrática del Congo , Sudán y Angola, en el que participan Immtech International y la Universidad de Carolina del Norte en Chapel Hill, realizó los ensayos clínicos de fase I y comenzó un ensayo de fase III en 2005 para probar la eficacia del primer tratamiento oral para la enfermedad del sueño, actualmente conocido como "DB289".
Los resultados recientes indican que el parásito no puede sobrevivir en el torrente sanguíneo sin su flagelo . Este descubrimiento brinda a los investigadores un nuevo ángulo de ataque para eliminar el parásito.
Los investigadores han encontrado un mecanismo inmunológico que creen que están utilizando para crear nuevos tratamientos. Una proteína relacionada con la haptoglobina ( Hpr ) descubierta en 2006 y unida a los lípidos en el sistema sanguíneo puede capturar hemoglobina y transportarla al cuerpo graso al que están unidas, que contiene una toxina fatal para el tripanosoma. Este mecanismo podría ser una solución inmune utilizando la dependencia de los tripanosomas de la hemoglobina. Cuando este último ha sido capturado previamente por una proteína Hpr, los tripanosomas también se adhieren a la partícula grasa que luego envenena al parásito.
Prevención y control
No hay prevención de vacunas o drogas. La prevención y el control se centran, cuando sea posible, en la extirpación del huésped parásito, la mosca tsetsé . Se han empleado alternativamente dos estrategias para intentar reducir la tripanosomiasis africana. Una de las tácticas es principalmente médica o veterinaria y se dirige directamente a la enfermedad mediante la profilaxis, el tratamiento y la vigilancia para reducir la cantidad de organismos portadores de enfermedades. La segunda estrategia es generalmente entomológica e implica interrumpir el ciclo de transmisión al reducir el número de moscas.
Hay ejemplos de cómo reducir la enfermedad del sueño mediante el uso de técnicas de esterilización de insectos. La vigilancia activa regular, que incluye la detección de casos y el tratamiento, además del control de la mosca tsetsé, es la columna vertebral de la estrategia de control de la enfermedad del sueño. El cribado sistemático en comunidades donde se han identificado brotes es el mejor enfoque, ya que el cribado caso por caso no es prácticamente posible en áreas altamente endémicas. El cribado sistemático puede adoptar la forma de clínicas móviles o centros de cribado fijos donde los equipos viajan diariamente a los hogares. La naturaleza de la enfermedad de Gambiense es tal que los pacientes no buscan tratamiento lo suficientemente temprano porque los síntomas en esta etapa no son lo suficientemente obvios o graves como para justificar una consulta médica, debido a la lejanía de las pocas áreas afectadas. Además, el diagnóstico de la enfermedad es difícil y la mayoría de los trabajadores de la salud no pueden detectarla. El cribado sistemático permite detectar y tratar una enfermedad temprana antes de que la enfermedad progrese y reduce el reservorio humano.
Para el viajero, se aconseja el uso de ropa protectora así como repelentes contra la mosca responsable.
Historia y epidemiología
En África, la presencia de la enfermedad del sueño es atestiguado desde el XIV ° siglo .
Sin embargo, no fue hasta principios del XX ° siglo , en 1901 y 1903 , que Sir David Bruce descubre y confirma el agente parasitario de esta enfermedad, a la que dio su nombre: Bruce tripanosoma ( Trypanosoma brucei ), y en 1910 que él identificó con precisión su insecto vector, la mosca Glossina palpalis
Ha habido tres epidemias graves en África durante el siglo pasado. El primero, entre 1896 y 1906, afectó principalmente a Uganda y la cuenca del Congo .
Una gran epidemia se produce después de que el comienzo de la colonización, de paso, el XX ° siglo, probablemente matando a aproximadamente un millón de personas en la cuenca del Congo , lo que contribuye a despoblar el país de la cuenca africana; Además, es probable que el aumento y, a menudo, los movimientos forzados en esta cuenca, la promiscuidad entre los niños reunidos en las escuelas, entre los portadores de diferentes tribus y orígenes (voluntarios o reclutados por la fuerza, si querían encontrar a sus esposas en campos de detención por los franceses). autoridad , campamentos donde las muy difíciles condiciones de vida también condujeron a una disminución de la inmunidad y las epidemias). La administración colonial establece una Asistencia Médica nativa y unidades móviles de salud en todas sus colonias, incluidas Marruecos y Argelia, África Occidental Francesa y Camerún, que se confían rápidamente a los médicos militares .
Una segunda epidemia estalló a partir de 1920 en varios países africanos. Es detenido por equipos móviles que examinan sistemáticamente a millones de personas en peligro. Habiendo casi desaparecido la enfermedad entre 1960 y 1965, la detección y vigilancia se debilitó tras la salida de las autoridades coloniales y, en 1970, estalló la tercera gran epidemia.
Desde entonces, la enfermedad ha seguido progresando de forma endémica en varios focos.
Diverso
De 1951 a 1953 , mientras se lograban importantes avances en la farmacología y en el conocimiento de las psicosis , el profesor Pierre Gallais, jefe del departamento de psiquiatría del hospital Lévy de Marsella , experimentó con un método terapéutico inspirado en la malaroterapia , que denomina tripanoterapia, hace testea directamente en 12 pacientes durante dos años, estimando que "la fase nerviosa de la enfermedad podría ser un momento saludable para los pacientes psicóticos y esquizofrénicos, en fracaso terapéutico , acomodados en su departamento"
La molécula secretada por el parásito responsable de las repercusiones sintomáticas en el estado de vigilia es el triptofol .
Notas y referencias
- Documental Los médicos militares en la época de las colonias , Arté France, 2011, dirigido por Farnçois Caillat & Silvia Radelli.
- Futura Sciences [1]
- (in) G. Rocha , A. Martins , G. Gama , F. Brandão y J. Atouguia , " Posibles casos de transmisión sexual y congénita de la enfermedad del sueño " , Lancet , vol. 363,17 de enero de 2004, p. 247 ( PMID 14738812 , leer en línea [PDF] )
- (en) R. Brun, J. Blum J, F. Chappuis y C. Burri, " Tripanosomiasis africana humana " , Lancet , vol. 375,2010, p. 148-159 ( leer en línea )
- Odiit M, Kansiime F, Enyaru JC, Duración de los síntomas y letalidad de la enfermedad del sueño causada por Trypanosoma brucei rhodesiense en Tororo, Uganda , East Afr Med J, 1997; 74: 792-795
- Checchi F, Filipe JA, Haydon DT, Chandramohan D, Chappuis F, Estimaciones de la duración de la etapa temprana y tardía de la enfermedad del sueño gambiense , BMC Infect Dis, 2008; 8:16
- Blum JA, Zellweger MZ, Burri C, Hatz C, Participación cardíaca en la tripanosomiasis africana y americana , Lancet Infect Dis, 2008; 8: 631–641.
- Datos y estadísticas de salud y mortalidad de la OMS , consultado el 10 de febrero de 2009.
- (en) Organización Mundial de la Salud (Ginebra) , Informe sobre la salud en el mundo 2000: Sistemas de salud que mejoran el rendimiento ,2000( leer en línea )
- (in) Comité de Expertos de la OMS en Control y Vigilancia de la tripanosomiasis africana (Ginebra) , Serie de Informes Técnicos de la OMS, No 881 ,1998( leer en línea )
- (en) Sean Moore, Surya Shrestha, Kyle W. Tomlinson y Holly Vuong, Predicción del efecto del cambio climático en la tripanosomiasis africana: integración de la epidemiología con la biología de parásitos y vectores . leer en línea
- (en) T. Cherenet , RA Sani , JM Panandam S. Nadzr N. Speybroeck y Pé van den Bossche , " Prevalencia estacional de tripanosomiasis bovina en una zona infestada de mosca tsetsé y una zona libre de mosca tsetsé de la región de Amhara, en el norte Etiopía occidental ” , Revista de investigación veterinaria Onderstepoort , vol. 71, n o 4,2004, p. 307–312 ( leer en línea )
- Lutumba P, Robays J, Miaka C y Als. Eficiencia de diferentes estrategias de detección de tripanosomiasis africana humana en T. B. gambiense , Trop Med Int Health, 2005; 10: 347–356
- (en) C. Burri , S. Nkunku , A. Merolle y al. , “ Eficacia de un programa nuevo y conciso para el melarsoprol en el tratamiento de la enfermedad del sueño causada por Trypanosoma brucei gambiense: un ensayo aleatorizado ” , Lancet , vol. 355, n o 9213,2000, p. 1419-25 ( PMID 10791526 )
- (en) Sylvie Bisser , François-Xavier N'Siesi , Veerle Lejon et al. , “ Ensayo de equivalencia de melarsoprol y Nifurtimox en monoterapia y terapia combinada para el tratamiento de la enfermedad del sueño por Trypanosoma brucei gambiense de segunda etapa ” , Revista de Enfermedades Infecciosas , vol. 195,2007, p. 322–29 ( leer en línea ).
- (en) S. van Nieuwenhove , PJ Schechter , J. Declercq y al. , “ Tratamiento de la enfermedad del sueño gambiense en Sudán con DFMO oral (DL-alfa-difluorometil ornitina) un inhibidor de la ornitina descarboxilasa: primer ensayo de campo ” , Trans R Soc Trop Med Hyg , vol. 79, n o 5,1985, p. 692–8.
- (en) J. Pepin y B. Mpia , “ ensayo controlado aleatorio de tres regímenes de melarsoprol en el tratamiento de Trypanosoma brucei gambiense tripanosomiasis ” , Trans R Soc Trop Med Hyg , vol. 100,2006, p. 437-41.
- El 19 de abril de 1910, en el Congreso de Medicina Interna en Wiesbaden , Ehrlich y Hata informan sobre el descubrimiento de la arsfenamina y los alentadores resultados de los primeros ensayos clínicos.
- “Quimioterapia de infecciones por tripanosomas y espiroquetas. Química del ácido N-fenilglicineamida-p-arsónico ”, Journal of Experimental Medicine , vol. 30, n o 5, 1 st de noviembre de 1919, p. 411 ; L. Pearce y WH Brown, “Acción terapéutica en la tripanosomiasis experimental de ratones, ratas y cobayas”, ibid. , p. 437 ; "Acción tóxica", ibid. , p. 417 ; “Acción terapéutica en la tripanosomiasis experimental de conejos”, ibid. , p. 455 ; "Acción sobre las infecciones por espiroquetas", ibid. , p. 483 .
- H. Jonchère "Quimioprofilaxis de tripanosomiasis humana en AOF", en Boletín de la Sociedad de Patología Exótica , 44 (1951), 83-93.
- S. Abbatucci, "Con respecto al tratamiento de la enfermedad del sueño con triparsamida", en Bulletin de la Société de pathologie exotique , 19 (1926), 271-279.
- Ernest Fourneau , “ Sobre el uso de ácido oxiaminofenilarsínico y ácidos arilarsínicos en general en el tratamiento de la espirilosis y tripanosomiasis ”, Annales de Institut Pasteur , vol. 35,1921, p. 571-574.
- Ernest Fourneau , Jacques y Thérèse Tréfouël e Yvonne de Lestrange-Trévise , “ Derivados del ácido fenilarsénico (como pentavalente) en el tratamiento de la tripanosomiasis. II ”, Ann. Inst. Pastor , vol. 40,1926, p. 933.
- Ernest Fourneau , Jacques y Thérèse Tréfouël y Germaine Benoit , " En los isómeros de para-oxi-3-amino-fenil-arsinic ácido y su derivado de acetilo ( stovarsol ) ", Bulletin de la Société Chimique de France , 4 º serie, vol. 41,1927, p. 499-514.
- J. Dutertre y R. Labusquière, "La terapia de la tripanosomiasis", en Tropical Medicine , 26 (1966), 342-356.
- J. Burke, "Historia de la lucha contra la enfermedad del sueño en el Congo", en Annales de la Société belge de medicine tropique , 51 (1971), 465-477.
- EAHFriedheim, "Mel B en el tratamiento de la tripanosomiasis humana", Am. J. Trop. Medicina. Hig. , 29 (1949) 173-180.
-
J. Hardenberg, N. Claverie GP Tell, "el tratamiento de eflornitina (Ornidyl) de Trypanosoma brucei gambiense enfermedad de dormir: informe de 711 pacientes tratados hasta marzo de 1991", 21 ª Reunión del Consejo Científico Internacional para la Investigación y la lucha contra la tripanosomiasis (CSILRT), Yamoussoukro, Côte d'Ivoire , 1991;
FJ Louis, J. Keizer, PP Simarro, C. Schmid, J. Jannin, "Eflornitina en el tratamiento de la enfermedad del sueño", Med. Demasiado. , 63 (2003), 559-563. - Priotto G., Pinoges L., Fursa IB et al., “Seguridad y eficacia de la eflornitina de primera línea para la enfermedad del sueño por Trypanosoma brucei gambiense en Sudán: estudio de cohorte” , BMJ , 2008, 336 , 705-708.
- Kande Betu Ku Mesu V, Mutombo Kalonji W, Bardonneau C et al. Fexinidazol oral para la tripanosomiasis africana por Trypanosoma brucei gambiense en etapa tardía: un ensayo pivotal multicéntrico, aleatorizado y de no inferioridad , Lancet, 2018; 391: 144-154
- Priotto G., Kasparian S., Ngouama D. et al., “Terapia de combinación de nifurtimox-eflornitina para la enfermedad del sueño de segunda etapa por Trypanosoma brucei gambiense: un ensayo clínico aleatorizado en el Congo” , Clin. Infectar. Decir. , 2007, 45 , 1435-42.
- Gérard Chauvière, Bernard Bouteille, Bertin Enanga, Cristina de Albuquerque, Simon L. Croft, Michel Dumas, Jacques Périe, Journal of medicinal chemistry , vol. 46, n o 3, 2003, p. 427-440 .
- (in) David Williamson , "El compuesto podría vencer a la enfermedad del sueño africana, ensayo clínico a partir de este mes " , Servicio de noticias de la Universidad de Carolina del Norte ,25 de agosto de 2005( leer en línea )
- (in) staff , " Clinical Trials Update " , Genetic Engineering News ,15 de septiembre de 2005, p. 5
- " Avance de la enfermedad africana del sueño " (consultado el 7 de abril de 2006 )
- equipo de la Universidad de Aarhus y la Université Libre de Bruxelles, estudio publicado en la revista Science a mediados de 2008
- B. Vanhollebeke et al., “ Un receptor de haptoglobina-hemoglobina transmite inmunidad innata a Trypanosoma brucei en humanos ”, Science , vol. 320,2008( resumen )
- " dirección estratégica para la tripanosomiasis africana Investigación " ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? ) , Programa Especial de Investigaciones y Enseñanzas sobre Enfermedades Tropicales (consultado el 1 er de marzo de de 2006 )
-
D. Bruce, "Nota sobre el descubrimiento de un nuevo Trypanosoma", Actas de la Real Sociedad de Física de Edimburgo , IXIX, 1902, p. 496 ;
“ La etiología de la enfermedad del sueño (con placa especial). El tripanosoma y su insecto portador ”, informe de la conferencia impartida por el coronel D. Bruce a la Sociedad Biológica de Liverpool sobre la enfermedad del sueño en Uganda, British Medical Journal , 21 de noviembre de 1903, pág. 1343-1350 . - D. Bruce, AE Hamerton, HR Bateman, FP Mackie, " El alimento natural de Glossina palpalis ", Actas de la Royal Society de Londres, Serie B (publicaciones biológicas), 15 de junio de 1910.
- Vassal J. (1923). Panorama general de la asistencia médica indígena en África . Rvdo. medicina Angola, 1, 205-206.
- Chatinières P (1919) En el Gran Atlas marroquí: extractos del libro de registro de un médico asistencial indígena 1912-1916 . Plon-Nutre.
- Cilleuls, JD (1959). La participación de médicos de grupos móviles de salud en la Asistencia Médica Indígena y en la conquista de Marruecos. Historial médico, 9, 5-39.
- Raynaud L, Soulié H & Picard P (1932) Higiene y patología del norte de África: Asistencia médica para europeos en Argelia, por P. Picard . Asistencia médica a los nativos de Argelia, a cargo de H. Soulié. Consideraciones generales sobre la organización y funcionamiento de los servicios asistenciales e higiénicos de la colonia , por H. Soulié, L. Raynaud, P. Picard (Vol. 2). Masson.
- Heckenroth F. (1923). El trabajo de la asistencia médica indígena en el África Occidental Francesa. Rvdo. medicina Angola, 1, 207-219
- (in) Centro de prensa de la OMS , Hoja informativa N o 259: Tripanosomiasis africana o enfermedad del sueño ,2001( leer en línea )
- http://www.chs-savoie.fr/france/MENU5/news/index.html/quand-1317420000 ver también: Souvenirs (JDTR)
- Blanc F (2012) Tripanoterapia, contribución a la historia de la psiquiatría biológica ; PSN 2012/1 (Volumen 10); Ediciones de materiales ; ( ISBN 9782919694150 ) pág. 77 a 94.
- (en) EM Cornford, WD Bocash, Braun LD, PD Crane, WH y Oldendorf MacInnis AJ. "Distribución rápida de triptofol (3-indol etanol) al cerebro y otros tejidos" J Clin Invest. 1979; 63 (6): 1241-8.
Apéndices
Bibliografía
- Gaëlle Ollivier y Dominique Legros , " Historia de la tripanosomiasis africana humana ", Tropical Medecine International Health , vol. 6, n o 11,Noviembre de 2001, p. 855-863 ( leer en línea )
- ( fr ) MP Barrett y col. , " Las tripanosomiasis " , Lancet , vol. 362, n o 9394,1 st de noviembre de de 2003, p. 1469-80 ( PMID 14602444 , leer en línea )
- (en) M. Berriman et al. , “ El genoma del tripanosoma africano Trypanosoma brucei ” , Science , vol. 309, n o 5733,2005, p. 416–22 ( PMID 16020726 , leer en línea )
Artículos relacionados
- Mosca tsetse
- Lista de enfermedades infecciosas
- Enfermedad de Chagas , otra enfermedad humana causada por tripanosoma
- DNDi (Iniciativa sobre medicamentos para enfermedades desatendidas)
- Epidemia de enfermedad del sueño en la cuenca del Congo
enlaces externos
- Médicos Sin Fronteras / Médicos Sin Fronteras Página de información sobre la enfermedad del sueño
- Instituto de Investigaciones para el Desarrollo
- Última actualización de la OMS "Tripanosomiasis humana africana (enfermedad del sueño)" Marzo del 2014, http://www.who.int/mediacentre/factsheets/fs259/fr/