Picolina
La picolina o metilpiridina es un heterocíclico aromático de fórmula empírica C 6 H 7 N. Consiste en un núcleo piridina sustituido por metilo , y está en forma de tres isómeros dependiendo de la posición relativa del grupo metilo en el ciclo con respecto a el átomo de nitrógeno .
Propiedades
| Picolina | |||
| apellido | 2-metilpiridina | 3-metilpiridina | 4-metilpiridina |
| Otros nombres | 2-picolina α-picolina o picolina orto picolina |
3-picolina β- picolina m -picolina meta picolina |
4-picolina γ-picolina p -picolina para picolina |
| Fórmula estructural |

|

|
|
| número CAS | |||
| (mezcla) | |||
| PubChem | 7975 | 7970 | 7962 |
| Fórmula bruta | C 6 H 7 N | ||
| Masa molar | 93,13 g mol -1 | ||
| Estado ( CNTP ) | líquido | ||
| Apariencia | líquido incoloro olor desagradable y acre |
líquido incoloro a amarillento |
olor a piridina líquida amarillenta |
| Punto de fusión | −70 ° C | −18 ° C | 3 ° C |
| Punto de ebullición | 128 ° C | 144 ° C | 145 ° C |
| Densidad ( 20 ° C ) | 0,94 g · cm -3 | 0,96 g · cm -3 | 0,96 g · cm -3 |
|
Presión de vapor saturante ( 20 ° C ) |
12 hPa | 5,9 hPa | 5,8 hPa |
| punto de inflamabilidad | 27 ° C (copa cerrada) | 36 ° C (copa cerrada) | 39 ° C (copa cerrada) |
| Punto de autoencendido | 535 ° C | > 500 ° C | |
| Límites explosivos | 1,4-8,6% vol. 54-330 g / m³ |
1,3-8,7% vol. 55-335 g / m³ |
1,3-8,7% en volumen 50-335 g / m³ |
| Solubilidad en agua | soluble | ||
|
pK A (del ácido conjugado BH + ) |
5,94 | 5.63 | 6.03 |
| LogP | 1,11 | 1.2 | 1,22 |
| SGH |
 
Peligro |
||
| Frases H y P |
H226 , H302 y H311
H226 : Líquido y vapores inflamables H302 : Nocivo en caso de ingestión H311 : Tóxico en contacto con la piel H319 , H332 y H335 H319 : Provoca irritación ocular grave H332 : Nocivo en caso de inhalación H335 : Puede irritar las vías respiratorias |
H226 , H302 y H311
H226 : Líquido y vapores inflamables H302 : Nocivo en caso de ingestión H311 : Tóxico en contacto con la piel H314 y H332 H314 : Provoca quemaduras graves en la piel y lesiones oculares graves H332 : Nocivo por inhalación |
H226 , H311 y H302 + H332
H226 : Líquido y vapores inflamables H311 : Tóxico en contacto con la piel H302 + H332 : Nocivo en caso de ingestión o inhalación. H315 , H319 y H335 H315 : Provoca irritación cutánea H319 : Provoca irritación ocular grave H335 : Puede irritar las vías respiratorias |
|
P261 y P280.3
P261 : Evite respirar el polvo / humo / gas / niebla / vapores / aerosoles. P280.3 : Use protección para los ojos. P312 y P305 + P351 + P338 P312 : Llame a un CENTRO DE INFORMACIÓN TOXICOLÓGICA oa un médico si no se encuentra bien. P305 + P351 + P338 : En caso de contacto con los ojos: Enjuagar cuidadosamente con agua durante varios minutos. Quítese los lentes de contacto si la víctima los usa y se pueden quitar fácilmente. Continúe enjuagando. |
- |
P210 , P280 y P302 + P352
P210 : Mantener alejado de fuentes de calor, chispas, llama abierta o superficies calientes. - No fumar. P280 : Use guantes de protección / ropa protectora / protección para los ojos / protección facial. P302 + P352 : En caso de contacto con la piel: lavar con abundante agua y jabón. P305 + P351 + P338 y P308 + P310 P305 + P351 + P338 : En caso de contacto con los ojos: Enjuagar cuidadosamente con agua durante varios minutos. Quítese los lentes de contacto si la víctima los usa y se pueden quitar fácilmente. Continúe enjuagando. P308 + P310 : En caso de exposición probada o sospechada: llamar a un CENTRO DE INFORMACIÓN TOXICOLÓGICA oa un médico. |
|
Las picolinas son líquidos incoloros que tienen un olor similar a la piridina . Son miscibles con agua, etanol y éter dietílico . Los tres isómeros tienen puntos de fusión muy distantes, respectivamente -70, -18 y 3 ° C , pero puntos de ebullición relativamente cercanos.
Como en la 2- y 4-picolina, los grupos metilo se conjugan directamente con el átomo de nitrógeno que atrae electrones, los grupos metilo de estos dos isómeros pueden desprotonarse con relativa facilidad con bases fuertes como diisopropilamida de litio o butillitio y luego sustituirse.
Síntesis
Hoy en día, la 2-picolina se produce principalmente por dos vías sintéticas: la condensación de acetaldehído o formaldehído y amoniaco , o por ciclación de nitrilos y acetileno ( ciclación de Bönnemann ). A continuación se muestra el ejemplo de la reacción entre acetaldehído y amoníaco:

En 1989 se produjeron alrededor de 8.000 tonos en todo el mundo.
La 3-metilpiridina puede prepararse haciendo reaccionar la acroleína con amoniaco:
pero el método más eficiente utiliza acroleína, propanal y amoníaco:
En 1989 se produjeron alrededor de 9.000 tonos en todo el mundo.
Utilizar
Los tres isómeros tienen propiedades bastante similares a la piridina en sus propiedades y pueden reemplazarla fácilmente en aplicaciones donde la estructura molecular exacta no es importante, por ejemplo, como disolventes . De lo contrario, sirven como base sintética para productos farmacéuticos y agroquímicos y para la producción de tintes .
Se pueden citar, por ejemplo, 2-vinilpiridina y nitrapirina , un producto agroquímico que se puede producir a partir de 2-picolina. La 3-picolina se puede utilizar como materia prima para la síntesis de clorpirifos y niacina , y la 4-picolina se utiliza para producir el agente antituberculoso isoniazida .
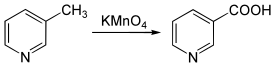
La oxidación de picolinas, por ejemplo mediante permanganato de potasio (KMnO 4 ), produce los ácidos carboxílicos equivalentes, respectivamente ácido picolínico , ácido nicotínico y ácido isonicotínico .

Medio ambiente
Las picolinas son más volátiles y se degradan más lentamente que sus homólogos de ácido carboxílico. La volatilización es mucho menor en el suelo que en el agua, debido a la absorción de compuestos en las arcillas del suelo y la materia orgánica. La degradación de las picolinas parece estar mediada principalmente por bacterias, la mayoría de las cepas pertenecientes a actinobacterias . La 3-metilpiridina se degrada más lentamente que los otros dos isómeros, posiblemente debido al impacto de la resonancia en el anillo heterocíclico. Como la mayoría de los derivados de piridina simples, las picolinas contienen más nitrógeno del necesario para el crecimiento de microorganismos, y el exceso de nitrógeno generalmente se excreta al medio ambiente como amonio durante el proceso de degradación.
Historia
La picolina fue aislada por primera vez, en forma impura, en 1826 por el químico alemán Otto Unverdorben (1806 - 1873), quien la obtuvo por pirólisis de huesos y la llamó “ Odorina ” por su olor desagradable. En 1849, el químico escocés Thomas Anderson (1819-1874) preparó picolina pura a partir de alquitrán de hulla y mediante pirólisis de huesos. Anderson luego lo denomina "picolina" mediante una combinación de las palabras latinas pix (alquitrán) y oleum (aceite), siendo el aceite de alquitrán de hulla el material del que lo había extraído. Alrededor de 1870, el químico alemán Adolf von Baeyer sintetizó la picolina de dos formas: por destilación en seco de " acroleïnammoniak " (CH 2 = CH-CH = N-CHOH-CH = CH 2 ), y calentando " tribromallyl " ( 1,2 , 3-tribromopropano ) con amoniaco en etanol .
En 1871, el químico y físico inglés James Dewar planteó la hipótesis de que la picolina era metilpiridina. Sin embargo, si la estructura de la piridina propuesta por el químico Garmano-italiano Wilhelm Körner en 1869 es correcta, es decir que la piridina es un análogo del benceno (un anillo hexagonal con enlaces simples y dobles alternos), esto significa que hay tres isómeros de metilpiridina. Hacia 1879, el químico austriaco Hugo Weidel logró aislar y caracterizar tres isómeros de picolina, a los que denominó α–, β– y γ - picolina, siendo la α - picolina el componente principal de la picolina impura, acompañada de pequeñas cantidades de β - picolina y γ - picolina obtenibles mediante destilación en seco de Baeyer de acroleinamoniaco .
Luego, Weidel somete cada isómero de picolina a oxidación por permanganato de potasio , transformándolos en un ácido carboxílico . Luego llama a la forma ácida de α- picolin Picolinsäure ( ácido picolínico ). Reconoció en la forma ácida de la β- picolina Nicotinsäure ( niacina o ácido nicotínico), un compuesto que había descubierto en 1873.
Cuando Weidel descarboxila la forma de ácido carboxílico de cada isómero, mediante la destilación en seco de su sal de calcio con óxido de calcio , obtiene piridina, lo que demuestra que la picolina era una mezcla de los tres isómeros de metilpiridina, como esperaba. Sin embargo, Weidel nunca determinó para ninguno de los isómeros la posición del grupo metilo en relación con el átomo de nitrógeno del anillo piridico. La estructura de la niacina, y por lo tanto la de la β-picolina, se determinó en 1883 cuando el químico checo-autichiano Zdenko Skraup y Albert Cobenzl oxidaron repetidamente la β-naftoquinolina y encontraron niacina entre los productos, lo que demostró que la β-picolina era 3-metilpiridina.
Notas y referencias
- (en) / (de) Este artículo es parcial o totalmente extraído de artículos titulados en inglés " Picoline " ( ver lista de autores ) y en alemán " Picoline " ( ver lista de autores ) .
- Entrada "2-Picoline" en la base de datos química GESTIS de la IFA (organismo alemán responsable de la seguridad y salud en el trabajo) ( alemán , inglés ), consultado el 2 de enero de 2021 (Se requiere JavaScript) .
- entrada "2-picolina" en la base de datos químicos GESTIS del IFA (organismo alemán responsable de la seguridad y salud) ( alemán , Inglés ), accede 02/01/2021 ( Se requiere JavaScript) .
- Entrada "4-Picoline" en la base de datos química GESTIS de la IFA (organismo alemán responsable de la seguridad y salud en el trabajo) ( alemán , inglés ), consultado 2021-01-02 (Se requiere JavaScript) .
- CRC Handbook of Tables for Organic Compound Identification , 3 e ed. , 1984 ( ISBN 0-8493-0303-6 ) .
- (de) metilpiridina entrada en Römpp Online . Georg Thieme Verlag, consultado el 25 de noviembre de 2014.
- M. Sainsbury, M. Berry, JD Hepworth, C. Drayton, EW Abel, D Phillips, JD Woollins, AG Davies, Química heterocíclica , Royal Society of Chemistry,2009, 1 st ed. ( ISBN 0-85404-652-6 ) , pág. 30
- (en) Shinkichi Shimizu , Nanao Watanabe , Toshiaki Kataoka , Takayuki Shoji , Nobuyuki Abe , Sinji Morishita y Hisao Ichimura , Enciclopedia de química industrial de Ullmann , Weinheim, Wiley-VCH, 2005( DOI 10.1002 / 14356007.a22_399 ).
- (de) A. Behr, Angewandte homogene Katalyse , Weinheim, Wiley-VCH,2008( ISBN 3-527-31666-3 ) , pág. 722
- (en) Eric Scriven y FV Ramiah Murugan, Enciclopedia Kirk-Othmer de Tecnología Química , XLI,2005( DOI 10.1002 / 0471238961.1625180919031809.a01.pub2 ) , "Piridina y derivados de piridina".
- GK Sims y LE Sommers , " Degradación de derivados de piridina en el suelo ", J. Calidad ambiental , vol. 14, n o 4,1985, p. 580–584 ( DOI 10.2134 / jeq1985.00472425001400040022x )
- GK Sims y LE Sommers , “ Biodegradación de derivados de piridina en suspensiones de suelo ” , Toxicología y Química Ambiental , vol. 5, n o 6,1986, p. 503–509 ( DOI 10.1002 / etc.5620050601 )
-
Para conocer la historia de las primeras investigaciones sobre la picolina, consulte:
- Manual de Química , vol. Vuelo. 11, Londres, Inglaterra, Cavendish Society,1857, 263–272 pág. ( leer en línea )
- (de) Neues Handwörterbuch der Chemie [“Nuevo diccionario de química”], vol. Vuelo. 5, Braunschweig, Alemania, Friedrich Vieweg und Sohn,1890, 575–584 pág. ( leer en línea )
- (de) Arthur Calm y Karl Buchka , Die Chemie des Pyridins und seiner Derivate [“La química de la piridina y sus derivados”], Braunschweig, Alemania, Friedrich Wieweg und Sohn, 1889–1891, 62–68 p. ( leer en línea )
- (de) Richard Wolffenstein , Die Pflanzenalkaloide ["Los alcaloides de las plantas"], Berlín, Alemania, Julius Springer,1922, 40–42 pág. ( ISBN 9783642924491 , leer en línea )
- (de) Otto Unverdorben , “ Ueber das Verhalten der organischen Körper in höheren Temperaturen ” [“Sobre el comportamiento de sustancias orgánicas a altas temperaturas”], Annalen der Physik und Chemie , vol. 8,1826, p. 253-265; 477–487 ( leer en línea ) Unverdorben nombró picolina Odorin en la p. 255.
- Thomas Anderson , " Sobre la constitución y propiedades de la picolina, una nueva base orgánica de alquitrán de hulla ", Transacciones de la Royal Society de Edimburgo , vol. 16, n o 21849, p. 123–136 ( DOI 10.1017 / S0080456800024984 , leer en línea )
- Thomas Anderson , “ Sobre los productos de la destilación destructiva de sustancias animales. Part I. ”, Transactions of the Royal Society of Edinburgh , vol. 16, n o 4,1849, p. 463–474 ( DOI 10.1017 / s0080456800022432 , leer en línea )
- (Anderson, 1849), pág. 124.
- (Fehling & Hell, 1890), pág. 575.
- (Wolffenstein, 1922), pág. 42.
- (De) Adolf Baeyer , “ Untersuchungen über die Basen der Pyridin- und Chinolinreihe. I. Ueber die Synthese des Picolins ” [“ Investigaciones sobre las bases de las series piridina y quinolina. I. Sobre la síntesis de picolina ”], Annalen der Chemie und Pharmacie , vol. 155, n o 3,1870, p. 281–294 ( DOI 10.1002 / jlac.18701550304 , leer en línea )
- James Dewar , " Sobre los productos de oxidación de la picolina ", Chemical News , vol. 23,27 de enero de 1871, p. 38–41 ( leer en línea ) Desde p. 40: "Si consideramos la picolina como con toda probabilidad metilpiridina, ..."
- W. Koerner , " Síntesis de una base isomérica con toluidina ", Giornale di Scienze Naturali ed Economiche (Revista de Ciencias Naturales y Economía (Palermo, Italia)) , vol. 5,1869, p. 111-114 ( leer en línea )
- (en) H. Weidel , " Studien über Verbindungen aus dem animalischen Theer " ["Sobre el estudio de compuestos de alquitrán animal"], Berichte der Deutschen Chemischen Gesellschaft , vol. 12, n o 21879, p. 1989–2012 ( DOI 10.1002 / cber.187901202207 , leer en línea ) pag. 2008: “Eine vollständige Trennung gelingt nur durch die Platindoppelsalze. Das des α-Picolins (wie ich es nennen will) ist schwerer löslich als jenes des β-Picolins. " (La separación completa [los dos isómeros] solo es posible a través de sus sales de sales dobles de platino. Esta [sal doble] de α-picolina (llamada I) es menos soluble que la β-picolina). P. 2011: " Es kann daher Baeyer's aus Acroleïnammoniak gewonnene Base vielleicht als das dritte, nach Koerner's Auffassungsweise mögliche γ-Picolin betrachtet werden ". (Por lo tanto, la base de Baeyer que se obtuvo a partir de acroleinammoniak quizás pueda considerarse, según la interpretación de Körner, como el tercer [isómero] posible, γ-picolina).
- (Weidel, 1879), pág. 1994.
- (Weidel, 1879), pág. 2004.
- H Weidel , " Zur Kenntniss des Nicotins " ["[Contribución] a nuestro conocimiento de la nicotina"], Annalen der Chemie und Pharmacie , vol. 165, n o 21873, p. 328–349 ( DOI 10.1002 / jlac.18731650212 , leer en línea )
-
Ver:
- en (Weidel, 1879), págs. 2000-2001, Weidel muestra que la descarboxilación del ácido picolínico produce piridina;
- en (Weidel, 1873), pág. 343, Weidel muestra que la descarboxilación de niacina produce piridina;
- en (Weidel, 1879), pág. 2000, Weidel describe la picolina como piridina con un grupo metilo (CH _ {3} -), C _ { 5} H _ { 5} N --- CH _ {3} ;
- en (Weidel, 1879), pág. 2008, Weidel describe que su muestra de picolina contiene al menos dos isómeros de picolina: “… ein Gemisch von zwei Isomeren…” (… una mezcla de dos isómeros…).
- En (Weidel, 1879), p. 2011: “Die mitgetheilten Thatsachen reichen noch nicht aus, um endgültige teoretische Erklärungen namentlich der Isomerien, die offenbar in der relativas Stellung der CH 3 -, resp. COOH-Gruppe zum Stickstoff ihren Grund haben, zu geben. " (Los hechos informados aún no son suficientes para proporcionar explicaciones teóricas definitivas, especialmente sobre la isomería, que obviamente se debe a la posición relativa del CH 3 - COOH respectivamente. - en relación con el nitrógeno)
- (de) Zd. H. Skraup y A. Cobenzl , “ Über α– y β - Naphthochinolin ” [“Sobre α– y β - naftoquinolina”], Monatshefte für Chemie , vol. 4,1883, p. 436–479 ( DOI 10.1007 / BF01517985 , S2CID 96180283 , leer en línea ) Ver ilustración de Nicotinsaur (ácido nicotínico o niacina) p. 455.
Ver también
- Piridina
- Lutidina (dimetilpiridina)
- Collidina (trimetilpiridina)

