Acetileno
| Acetileno | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura tridimensional de acetileno. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificación | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre IUPAC | ethyne | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.743 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 200-816-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6326 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sonrisas |
C # C , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / C2H2 / c1-2 / h1-2H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | gas incoloro disuelto en acetona a presión | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades químicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fórmula bruta |
C 2 H 2 [Isómeros] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa molar | 26.0373 ± 0.0017 g / mol C 92.26%, H 7.74%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusión | −80,7 ° C ( punto triple ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° hirviendo | −84,7 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilidad | 1,185 g l −1 (agua, 20 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad |
ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura de autoignición | 305 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto de inflamabilidad | Gas inflamable | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Límites explosivos en el aire | 2,3 - 100 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presión de vapor saturante | a 20 ° C : 4460 kPa
ecuación:
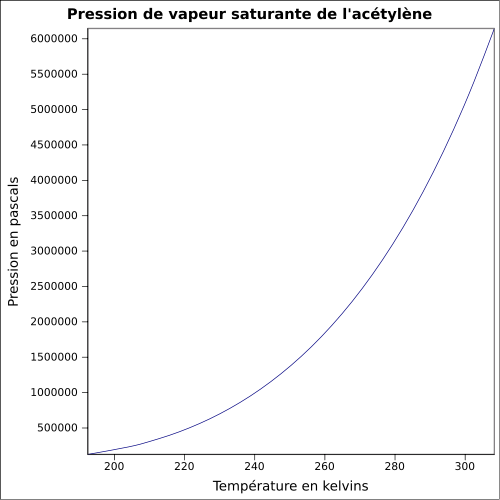
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto crítico |
35,2 ° C 61,38 bar 0,1122 l / mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Triple punto | −80,8 ° C a 1,2825 bar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termoquímica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gas, 1 bar | 200,93 J mol −1 K −1 ( 1 bar ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gas | 226,73 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
44.04 J mol −1 K −1 a 25 ° C
ecuación:
ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 1301,1 kJ · mol -1 ( 25 ° C , gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades electronicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re energía de ionización | 11.400 ± 0.002 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cristalografía | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Clase de cristal o grupo espacial | Pa 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parámetros de malla |
a = 6.140 Å b = 6.140 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumen | 231,48 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauciones | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Peligro H220, EUH006, H220 : Gas extremadamente inflamable EUH006 : Peligro de explosión en contacto o sin contacto con el aire |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   A, B1, F, A : Temperatura crítica del gas comprimido = 36,3 ° C B1 : Límite inferior de inflamabilidad del gas inflamable = 2,5% F : Material peligrosamente reactivo sujeto a una reacción de descomposición violenta Divulgación al 1,0% según los criterios de clasificación Comentarios: Consulte también la clasificación WHMIS de acetileno disuelto . |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 0 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transporte | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
239 : gas inflamable, que puede producir espontáneamente una reacción violenta. Número ONU : 1001 : ACETILENO DISUELTO Clase: 2.1 Código de clasificación: 4F : Gas disuelto a presión, inflamable; Etiqueta: 2.1 : Gases inflamables (corresponde a los grupos designados con una F mayúscula); 
- Número ONU : 3374 : ACETILENO SIN DISOLVENTE Clase: 2.1 Código de clasificación: 2F : Gas licuado, inflamable; Etiqueta: 2.1 : Gases inflamables (corresponde a los grupos designados con una F mayúscula);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotoxicología | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 0,37 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Umbral de olor | bajo: 226 ppm alto: 2,584 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unidades de SI y STP a menos que se indique lo contrario. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El acetileno (llamado etino por la nomenclatura IUPAC ) es un compuesto químico clase de hidrocarburos de alquinos de fórmula empírica C 2 H 2. Fue descubierto por Edmund Davy en Inglaterra en 1836 . Es el alquino más simple, que consta de dos átomos de carbono y dos de hidrógeno . Los dos átomos de carbono están conectados por un triple enlace que contiene la mayor parte de su energía química.
Descripción
Berthelot , en 1862 , fue el primero en sintetizar acetileno, en un aparato llamado "huevo de Berthelot", al producir un arco eléctrico entre dos electrodos de grafito bañados en una atmósfera de hidrógeno : 2 C + H 2 → C 2 H 2
El acetileno es un gas incoloro, prácticamente inodoro cuando está puro (pero generalmente se le atribuye un olor característico a ajo que proviene de las impurezas, especialmente la fosfina cuando se produce a partir del carburo de calcio ).
El acetileno es extremadamente inflamable a temperatura y presión normales . Es endoenergético con respecto al carbono y al hidrógeno, pudiendo descomponerse de forma espontánea, explosiva cuando la presión es superior a 100 kPa , y hasta unos pocos bares donde inevitablemente se produce esta descomposición espontánea . Es por ello que se almacena disuelto en acetona o dimetilformamida (DMF), incluidas ellas mismas en un material estabilizador poroso.
usar
Aplicaciones de acetileno:
- El alto contenido de carbono da una llama muy luminosa que se utiliza, por ejemplo, en lámparas de acetileno (calabomb) para mineros o espeleólogos.
- El elevado calor de combustión del acetileno alcanza altas temperaturas ( 3200 ° C en oxígeno puro), lo que lo convierte en un candidato ideal como combustible para soldadura. Una de las peculiaridades de la combustión del acetileno es su combustión en dos etapas: el acetileno primero reacciona con el oxígeno para dar monóxido de carbono e hidrógeno , luego estos productos reaccionan en una segunda etapa para formar dióxido de carbono y agua. El monóxido de carbono y el hidrógeno son gases reductores, lo que los convierte en reactivos populares en la soldadura de acero para reducir los óxidos de hierro resultantes de la reacción entre el hierro y el oxígeno a alta temperatura, permitiendo así una mejor homogeneización de la soldadura y por tanto una mejor calidad de esta última. La soldadura con acetileno permite el ensamblaje de varios metales ( aceros , acero inoxidable, aleaciones de cobre ), pero también bajo ciertas condiciones aluminio aleado con silicio .
- El acetileno también se utiliza como combustible en dispositivos analíticos. En efecto, en la espectrometría de absorción atómica (AAS), asociada a diversos oxidantes (aire, oxígeno puro, óxido nitroso), permite la ionización de elementos típicamente alcalinotérreos y determinar su concentración gracias a la ley de Beer-Lambert .
- El acetileno también se usa en sopletes de oxi-corte. Sin embargo, se prefiere el propano porque es menos costoso. Pero para cortes muy gruesos, el acetileno es esencial para calentar suficientemente el acero e iniciar el corte con llama en un ancho pequeño.
- La reacción de acetileno con ácido clorhídrico es una forma de producir cloruro de vinilo (monómero de cloruro de polivinilo ).

Propiedades fisicoquímicas
Las propiedades químicas del acetileno se explican en gran medida por la presencia en su molécula de un triple enlace resultante de la superposición de un enlace simple s (resultante de la fusión de dos orbitales sp ) y dos enlaces p resultantes de la fusión de dos orbitales 2p . Este enlace, de 0,124 nm de longitud y caracterizado por una energía de 811 kJ , es menos estable que los enlaces simples (614 kJ ) y dobles (347,3 kJ ) y, por tanto, más reactivo.
Las reacciones del acetileno
- El acetileno y los monoalquilacetilenos son los únicos hidrocarburos que tienen hidrógeno de carácter ácido y que pueden intercambiarse por un metal.
- Algunos acetilenidos detonan con el impacto.
- El acetileno reacciona con ácido cianhídrico para formar acrilonitrilo , un monómero de acrilonitrilo butadieno estireno (ABS) y estireno-acrilonitrilo (SAN).
- El acetileno da benceno por polimerización bajo la acción del calor.
- Por dimerización en presencia de catalizadores se obtiene vinilacetileno al que se le añade cloruro de hidrógeno para obtener cloropreno, un monómero de policloropreno o neopreno .
Producción y síntesis
El acetileno no existe de forma natural (en ocasiones existen otros alquinos en los hidrocarburos). Los principales métodos industriales para producir acetileno son:
Método carboquímico
La piedra caliza y el coque o el carbón vegetal se utilizan como materias primas . En un horno de alta temperatura ( 1700 ° C mínimo) calentado por una corriente eléctrica que pasa a través del medio de reacción fundido, se produce carburo de calcio de acuerdo con las reacciones: CaCO 3 → CaO + CO 2, CaO + 3 C + 108,300 calorías → CaC 2 + CO.
En el usuario, el carburo reacciona con el agua para producir acetileno, combinándose 1 kg de carburo con 562,5 g de agua para liberar 350 l de acetileno: CaC 2 + 2 H 2 O → C 2 H 2 + Ca (OH) 2 + 31.000 calorías.
Combustión parcial de metano
La combustión parcial de metano también produce acetileno: 3 CH 4 + 3 O 2 → C 2 H 2 + CO + 5 H 2 O.
Deshidrogenación de alcanos
Los alcanos más pesados del petróleo y el gas natural se descomponen en moléculas más ligeras que se deshidrogenan a altas temperaturas: C 2 H 6 → C 2 H 2 + 2 H 2.
Notas y referencias
- ACETILENO , hoja de seguridad (s) del Programa Internacional para la Seguridad de Sustancias Químicas , consultado el 9 de mayo, 2009
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- (en) David R. Lide , CRC Handbook of Chemistry and Physics, 89ª Edición , Boca Ratón, CRC Press / Taylor y Francis,2009, "Constantes físicas de compuestos orgánicos"
- Entrada "acetileno" en la base de datos química GESTIS de la IFA (organismo alemán responsable de la seguridad y salud) ( alemán , Inglés ), consultado el 14 de abril de, 2009 (Javascript required)
- (en) Robert H. Perry y Donald W. verde , de Perry Ingenieros Químicos Handbook , EE.UU., McGraw-Hill,1997, 7 ª ed. , 2400 p. ( ISBN 0-07-049841-5 ) , pág. 2-50
- Clark, AM; Din, F., Equilibrios entre fases sólida, líquida y gaseosa en sistemas binarios de baja temperatura acetileno - dióxido de carbono, acetileno - etileno y acetileno - etano, Trans. Faraday Soc., 1950, 46, 901.
- Tsonopoulos, C.; Ambrose, D., Propiedades críticas de vapor-líquido de elementos y compuestos. 6. Hidrocarburos alifáticos insaturados, J. Chem. Eng. Datos, 1996, 41, 645-656.
- " acetileno " , en http://www.nist.gov (visitada 14 de abril 2009 )
- (en) Carl L. Yaws, Manual de diagramas termodinámicos , vol. 1, 2 y 3, Huston, Texas, Gulf Pub. Co.,1996( ISBN 0-88415-857-8 , 978-0-88415-858-5 y 978-0-88415-859-2 )
- (en) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 de junio de 2002, 83 ª ed. , 2664 p. ( ISBN 0849304830 , presentación en línea ) , p. 5-89
- (en) David R. Lide, Manual de química y física , CRC,2008, 89 ª ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , pág. 10-205
- " acetileno " , en www.reciprocalnet.org (visitada 12 de diciembre 2009 )
- Número de índice en la tabla 3.1 del apéndice VI del reglamento CE N ° 1272/2008 (16 de diciembre de 2008)
- " Acetileno " en la base de datos de productos químicos Reptox de la CSST (organización de Quebec responsable de la seguridad y salud en el trabajo), consultado el 24 de abril de 2009
- " Acetylene " , en hazmap.nlm.nih.gov (consultado el 14 de noviembre de 2009 )
- Nowak Ph. (1999) - "L ' acétylène ", " Le P'tit Usania n o 7 " , en USAN (consultado el 5 de enero de 2021 ) ( ISSN 1292-5950 ) , USAN, Nancy, p. 1
Ver también
Artículos relacionados
- Acetileno hidratasa
- Alcyne
- Lámpara de acetileno
- Louis Bleriot
- Coronilla Frédéric
- Henri moissan
- Walter Reppe











