Fibrilación auricular
Fibrilación auricular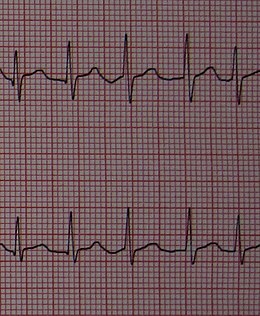 ACFA en V4 V5
ACFA en V4 V5
| Especialidad | Cardiología |
|---|
| CISP - 2 | K 78 |
|---|---|
| ICD - 10 | I48 |
| CIM - 9 | 427,31 |
| OMIM | 611819 y 615770 613120, 611819 y 615770 |
| Enfermedades DB | 1065 |
| MedlinePlus | 000184 |
| eMedicina | 151066 |
| eMedicina | med / 184 emerg / 46 |
| Malla | D001281 |
| Síntomas | ES PC DE Angina |
| Complicaciones | Carrera de IC |
| Riesgos | HA Enfermedad cardíaca valvular CMO CMNO congénita Tabac SAS |
| Diferencial | Otras arritmias |
| Tratamiento | Control de frecuencia o ritmo |
| Droga | Metoprolol , warfarina , disopiramida , dofetilida ( en ) , diltiazem , procainamida , ibutilida ( en ) , digoxina , deslanósido ( en ) , quinidina , digitoxina , atenolol , sotalol , propafenona ( en ) , verapamil , fondaparinux , atenolone ( en ) , clopidogrel , Dabigatrán , edoxabán , dabigatrán etexilato ( d ) , amiodarona , dronedarona , bisoprolol / hidroclorotiazida ( d ) , rivaroxabán , carvedilol , apixabán , flecainida y ácido acetilsalicílico |
| Frecuencia | ~ 2.5% países "desarrollados" |
| Paciente del Reino Unido | Fibrilación auricular pro |
La fibrilación auricular , también llamada fibrilación auricular (con frecuencia abreviada como "FA") es la arritmias cardíaca más común . Forma parte de los trastornos del ritmo supraventricular.
Corresponde a una acción descoordinada de las células del miocardio auricular , provocando una contracción rápida e irregular de las aurículas del corazón .
El término fibrilación auricular es de uso frecuente, pero desde 1998 el nombre académico ha sido "fibrilación auricular", y las aurículas han sido rebautizadas como "aurículas" en la nueva nomenclatura anatómica . También se encuentran otros nombres: arritmia completa por fibrilación auricular ( AC / FA o ACFA ) y, a veces, taquiarritmia completa por fibrilación auricular ( TAC / FA ).
La fibrilación auricular a veces se denomina "arritmia"; sin embargo, este término es sinónimo de "arritmia", un concepto más amplio, que por lo tanto incluye la fibrilación auricular.
Epidemiología
En raison de son développement rapide, lié au vieillissement de la population (pour sa forme non valvulaire), elle est parfois considérée comme l'une des grandes épidémies du troisième âge et du nouveau millénaire (avec par exemple plus de 660 000 personnes concernées en Francia). Esta arritmia se ha convertido en la más común en la práctica clínica. Su incidencia y prevalencia han aumentado constantemente durante varias décadas, junto con la obesidad (tan rápida y similar en frecuencia), y en parte por razones que aún no se conocen bien en 2020. A menudo no es muy sintomático en los ancianos y puede ser subdetectado. Es la fuente de una "carga creciente de morbilidad y mortalidad cardiovascular"
Histórico
La fibrilación auricular se describió por primera vez en humanos en 1906 , tras la observación de un síndrome similar en animales, y esto sin el uso del electrocardiograma , una herramienta de diagnóstico que aún no existe. Willem Einthoven , el inventor del electrocardiograma, publicó el primer trazo de fibrilación en el mismo año. El carácter común de los síndromes observados inicialmente se reconoció ya en 1909 .
Terminología
Hablamos de fibrilación auricular:
- paroxística: duración inferior a siete días (habitualmente 48 h ), finalizando espontáneamente o con cardioversión;
- persistente: dura más de siete días, se detiene espontáneamente o por cardioversión ;
- persistente prolongada: duración superior a un año para la que se considera una estrategia de control del ritmo;
- permanente: si se acepta la arritmia y no se hacen más intentos para detenerla.
- Las formas paroxísticas o persistentes pueden ser recurrentes.
Epidemiología
Es el trastorno del ritmo cardíaco más común, especialmente en los adultos mayores.
La incidencia y la prevalencia de FA aumentan drásticamente con la edad:
- incidencia: menos de "un nuevo caso por mil por año" antes de los 40 años , "cinco por mil por año" alrededor de sesenta (aumento mayor que un factor de 5) y "quince a veinte por mil por año" después de los 80 (incidencia multiplicada por 20 entre los 40 y los 80 años);
- prevalencia: alrededor del 1% de la población antes de los 60 años y alrededor del 10% o más después de los 80 años (teniendo en cuenta las respectivas longevidades de hombres / mujeres en este último grupo de edad). A nivel mundial, la fibrilación auricular afecta a más de 33 millones de personas (datos de 2010, con mayor prevalencia en Norteamérica y menor en Asia) y su incidencia tiende a aumentar.
Factores de riesgo
Varias patologías cardíacas pueden asociarse con la aparición de fibrilación auricular:
- Aumento crónico de la presión arterial en la aurícula izquierda, por ejemplo, secundario a estenosis mitral o insuficiencia mitral
- La presión sanguínea
- La insuficiencia cardiaca
- El infarto de miocardio
- Después de una cirugía de corazón
Aparte de las patologías cardíacas, buscaremos sistemáticamente las circunstancias patológicas, agudas o crónicas, que favorezcan la aparición del síndrome: hipertiroidismo , embolia pulmonar , consumo agudo o crónico de alcohol, apnea del sueño, infección aguda ( sepsis ), anomalías iónicas, etc. .
Tomar ciertos narcóticos ( cocaína y crack ), ciertos medicamentos (todos neuroestimulantes, simpaticomiméticos ), tomar tratamientos para el resfriado, tomar teofilina (para el asma) o ácido zoledrónico (tratamiento adyuvante de ciertos cánceres u osteoporosis).
También se sabe que la presencia de un bloqueo auriculoventricular de primer grado cuadriplica el riesgo de desarrollar fibrilación auricular.
Finalmente, existen factores genéticos que predisponen a la fibrilación auricular. Varios genes, independientemente de los que son directamente factores de patologías cardíacas, han sido identificados como factores de riesgo independientes de fibrilación auricular: mutación en el gen del péptido natriurético auricular, gen SCN5A , gen KCNH2 , gen MYL4 o mutación en un locus del cromosoma 4q25 .
Se discute el papel del tabaquismo , y el aumento del riesgo de fibrilación auricular parece ser pequeño.
Por último, los cardiólogos deportivos también son conscientes de la existencia de episodios de FA paroxística asociados a un hábito de entrenamiento intenso y muy regular en resistencia (ciclistas, maratonistas, esquiadores de fondo, etc.). Este contexto particular multiplicaría el riesgo de FA espontánea por dos o tres:
- el riesgo de FA idiopática de hecho parece estar correlacionado con el aumento del diámetro y volumen de la aurícula izquierda (aquí abreviado como OG), cambios funcionales ellos mismos ligados a la sobrecarga crónica del OG debido a un entrenamiento intenso y regular;
- el desacondicionamiento progresivo, es decir la exigencia de una práctica física regular de resistencia muy limitada en intensidad, podría (hipótesis controvertida) reducir paulatinamente este riesgo según algunos autores;
- Varias observaciones clínicas sugieren que ciertos episodios de FA paroxística, en particular los que afectan a sujetos con sobrecondicionamiento de resistencia aeróbica, podrían paradójicamente ser tratados con ejercicio físico de intensidad y duración adecuadas.
Fisiopatología
Normales Los resultados de contracción cardiaca de una despolarización cíclico (inversión de la polaridad eléctrica de la celda de membrana ) de un grupo de células situadas en el nivel de la parte superior de la aurícula derecha y que constituye el nodo sinusal (o sinoauricular nodo - NSA) . Esta despolarización se propaga muy rápidamente (en menos de una décima de segundo), de arriba a abajo y paso a paso, a todas las células de las dos aurículas, desencadenando su contracción casi sincrónica, así como en la dirección del nodo. atrioventricular (NAV). La activación del NAV por los potenciales de acción de la aurícula desencadenará a su vez la contracción de ambos ventrículos, pero de una manera ligeramente retardada en relación con la de las aurículas. Como recordatorio, la contracción de las aurículas permite un llenado adicional de los ventrículos (del orden del 20 al 30% según la edad del sujeto), justo antes de la sístole: esta es la llamada fase de llenado activo .
Durante la fase de inicio de la fibrilación auricular (FA), aparecen retrobucles de la corriente de despolarización (los llamados circuitos de reentrada ), que volverán a excitar las fibras musculares tempranas que recién emergen de su período refractario, generando luego una activación eléctrica inapropiada y desincronizada de estas fibras. La generalización de este mecanismo a todo el tejido auricular conducirá entonces a la fibrilación de las aurículas. La activación del NAV por trenes de potenciales de acción desincronizados tendrá lugar entonces de manera anárquica, el NAV luego transmitirá a los ventrículos una onda de despolarización (a través del haz de His ) de frecuencia muy irregular y con mayor frecuencia anormalmente rápida (pero no siempre) : este es el fenómeno clásico de taquiarritmia . En este fenómeno de inicio de FA incriminamos también la intervención de los denominados focos ectópicos, centros de hiperexcitabilidad con una frecuencia de alta muy rápida. Estos focos ectópicos pueden localizarse en muchos lugares diferentes de las aurículas, pero principalmente a nivel de las aberturas de las venas pulmonares en la aurícula izquierda. Estos dos tipos de mecanismos podrían actuar de forma más o menos sinérgica en el fenómeno desencadenante de la fibrilación. Finalmente, una anomalía primaria o secundaria, es decir, una enfermedad aguda o crónica, por ejemplo, de las fibras de las aurículas, caracterizada entonces por un acortamiento patológico de su período refractario, acentuará aún más el mecanismo de reentrada descrito anteriormente. En este sentido, numerosos autores han demostrado que, en caso de fibrilación auricular permanente, el período refractario de las fibras auriculares tiene "naturalmente" una tendencia a acortarse progresivamente, remodelando tejido permanente que de por sí contribuirá a la sostenibilidad de las fibras auriculares. la fibrilación auricular, estado de fibrilación. La vocación natural de AF es, por tanto, reforzarse en una especie de "círculo vicioso". Se dice que "la FA provoca FA", por lo que si el tratamiento médico no consigue reducir rápidamente el estado de fibrilación (mediante tratamiento farmacológico), después de cierto tiempo se hace difícil la cardioversión , sean cuales sean las consecuencias eléctricas o farmacológicas. medios utilizados.
Esta desaparición de la sincronización de contracción de las fibras musculares auriculares tiene dos tipos de consecuencias o riesgos:
- consecuencias hemodinámicas: las aurículas se volverán mecánicamente ineficaces: ya no se contraen (pérdida de la sístole fisiológica); por tanto, desaparece el llenado ventricular activo al final de la sístole, lo que provoca una disminución mecánica del gasto ventricular y, por tanto, del gasto cardíaco . Además, debido a la taquicardia asociada con mayor frecuencia a la fibrilación auricular, el llenado pasivo de los ventrículos durante la diástole también estará limitado por la reducción significativa de la duración diastólica;
- Riesgos embólicos: la ausencia de contracción auricular favorece un cierto estancamiento de la sangre en las aurículas, estado de estasis sanguínea que se sabe que favorece la aparición de trombos (o trombos) por el fenómeno de coagulación espontánea (a nivel del lado izquierdo). aurícula en particular). En presencia de FA, y mientras no se realice cardioversión, es por tanto recomendable administrar tratamiento anticoagulante heparínico (en forma aguda) o en forma de antivitamina K (AVK) para la FA permanente irreducible. Si los anticoagulantes están contraindicados, el tratamiento con agentes antiplaquetarios puede constituir una solución alternativa para el tratamiento de la FA permanente (consulte los detalles a continuación en la sección “Tratamiento”).
| Conducción | ||
Ritmo sinusal 
|
Fibrilación auricular 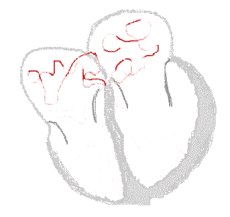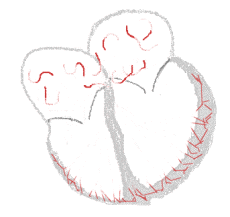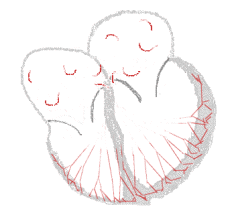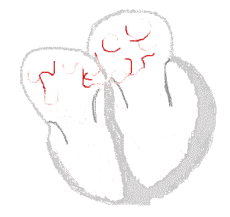
|
|
Generalmente se favorece la aparición de un estado de fibrilación auricular:
- cuando la aurícula izquierda está dilatada (diámetro superior a 5 cm en la ecografía);
- cuando las fibras auriculares están sometidas a un aumento permanente del nivel de tiroxina o catecolaminas .
Durante la fibrilación auricular, la frecuencia auricular puede alcanzar los 300 latidos por minuto. Debido a la presencia del nódulo auriculoventricular , se filtra toda la señal eléctrica auricular, lo que resulta en una limitación marcada de la frecuencia cardíaca ventricular basal. El ventrículo late entonces a una frecuencia mucho más baja que las aurículas, aunque permanece bastante rápido, permitiendo así, en general, gracias al tratamiento farmacológico asociado, una buena tolerancia de la patología por parte del paciente (en particular en reposo).
Diagnóstico
Síntomas
El paciente puede estar completamente asintomático y la fibrilación se descubre durante un EKG de rutina o se realiza por alguna otra razón.
- El paciente a veces siente que las palpitaciones pasan desapercibidas, pero a veces son muy irregulares.
- El paciente puede quejarse de fatiga ( astenia ), malestar ( desmayo ), dificultad para respirar ( disnea ), sensación de hundimiento en algunos casos.
- Finalmente, puede quejarse de dolor en el pecho , en particular en el caso de angina funcional.
- El cuestionario busca un déficit neurológico transitorio (ataque isquémico transitorio ) o crónico ( accidente cerebrovascular ), un signo de una complicación grave y urgente de la fibrilación auricular.
Examen físico
- El latido del corazón es irregular, más o menos rápido. En este caso, la frecuencia cardíaca debe estimarse mediante auscultación cardíaca y no midiendo solo el pulso . De lo contrario, la cifra encontrada podría estar equivocada por subestimación.
- De forma rutinaria buscamos signos de insuficiencia cardíaca .
- Finalmente, buscamos signos a favor de una causa particular: hipertensión , soplo cardíaco , signos de hipertiroidismo , embolia pulmonar , pericarditis (fricción pericárdica) ...
Exámenes adicionales
ECGEste examen es necesario para hacer el diagnóstico. Observamos la ausencia de actividad auricular organizada con desaparición de las ondas P a favor de la vibración de la línea isoeléctrica. La frecuencia ventricular (QRS) es irregular. Los QRS están bien (excepto el bloqueo de rama preexistente). El electrocardiograma también permite en algunos casos señalar determinadas causas.
El diagnóstico a veces es menos fácil ya que un estudio de 2007 muestra que el software de interpretación de ECG computarizado ignora este diagnóstico en casi el 20% de los casos.
El diagnóstico también se puede realizar mediante un registro electrocardiográfico prolongado ( holter cardíaco ).
En ocasiones, la apariencia puede confundirse con la de aleteo auricular o taquicardia auricular , especialmente si la conducción auriculoventricular es irregular. Si la arritmia es rápida y regular, la línea isoeléctrica no es visible y, por lo tanto, se puede hacer un diagnóstico de taquicardia de la unión por error. Entonces es importante tener un rastro de duración suficiente para desenmascarar las irregularidades que firman la fibrilación. En los raros casos contenciosos, una inyección de trifosfato de adenosina permite bloquear temporalmente el nódulo auriculoventricular, lo que permite desenmascarar las oscilaciones irregulares de la línea de base, indicadoras de fibrilación auricular.
EcocardiografíaLa ecocardiografía permite visualizar el corazón y sus cavidades mediante técnica ultrasónica. De este modo, permite buscar la causa de una arritmia y evaluar su impacto en el músculo cardíaco:
- estudio de las válvulas cardíacas , búsqueda de anomalías de la válvula mitral que puedan apuntar a la causa de la arritmia;
- estudio de las cámaras cardíacas: búsqueda de hipertrofia ventricular izquierda (HVI), trombo de la aurícula izquierda, dilatación auricular, siendo esta última posiblemente la causa de la arritmia pero también la consecuencia de la misma, sobre todo si es antigua;
- características de la insuficiencia cardíaca (sistólica o diastólica) si existe.
Al mínimo :
- evaluación biológica estándar, que comprende una evaluación de la coagulación , pudiendo prescribirse un tratamiento anticoagulante;
- Prueba de TSH para el hipertiroidismo .
Exámenes adicionales que se deben realizar según sea necesario:
- radiografía de tórax para evaluar el tamaño del corazón y buscar sobrecarga vascular indicativa de insuficiencia cardíaca ;
- Holter cardíaco (registro de ECG de 24 horas) si la arritmia es paroxística.
- Telemetría (registro continuo de ECG durante la hospitalización)
Evolución y complicaciones
La fibrilación auricular suele controlarse con el tratamiento adecuado. Sin embargo, su tendencia "natural" es evolucionar hacia la cronicidad: de lo paroxístico a ser progresivamente persistente, luego permanente. Esta afección crónica es potencialmente la fuente de múltiples complicaciones posibles, lo que lleva a una mayor tasa de mortalidad.
- aumento de la mortalidad cardiovascular (riesgo multiplicado por 2 en promedio) y la mortalidad general;
- Accidentes tromboembólicos: el riesgo de accidente cerebrovascular se multiplica en particular por un factor de 5 en ausencia de un tratamiento anticoagulante o antiagregante adecuado. Este riesgo se puede estimar sistemáticamente mediante el cálculo de una puntuación de riesgo embólico ;
- insuficiencia cardíaca por "miocardiopatía rítmica";
- Enfermedad rítmica de la aurícula ('enfermedad sinusal'): disfunción del nódulo sinusal que se caracteriza por la alternancia de episodios iterativos de bradicardia (transición a ritmo ventricular lento) o, por el contrario, fibrilación paroxística, FA paroxística que puede volverse permanente término.
- complicaciones iatrogénicas (secundarias a tratamientos farmacológicos o médico-quirúrgicos);
- en el caso particular (y muy raro) del síndrome de Wolff-Parkinson-White : un episodio de fibrilación auricular paroxística de conducción rápida expone un riesgo importante de fibrilación ventricular y, por tanto, de muerte súbita .
El pronóstico de las formas paroxísticas y no paroxísticas sigue siendo debatido: las recomendaciones estadounidenses estipulan que el riesgo tromboembólico es idéntico en las dos formas, pero ciertos datos muestran el carácter más peyorativo de las formas no paroxísticas.
Manejo de la fibrilación auricular
Ha sido objeto de varias publicaciones de recomendaciones : la última versión europea data de 2020 y las estadounidenses, de 2014, con una actualización en 2019.
La exclusión de ciertos estimulantes (alcohol y cafeína) a menudo puede ayudar a espaciar las convulsiones paroxísticas. La dieta mediterránea combinada con suplementos de aceite de oliva puede reducir el riesgo de que ocurra este trastorno rítmico. El tratamiento médico se basa en varios puntos:
- reducción de la fibrilación (fármaco o cardioversión), es decir, para obtener un retorno a un ritmo sinusal , normal;
- reducir el riesgo de recurrencia;
- ralentizar la frecuencia cardíaca durante la arritmia, lo que permite una mejor tolerancia de esta última;
- prevención de complicaciones embólicas especialmente.
Reducción de la fibrilación
Consiste en un retorno a un llamado ritmo sinusal normal . También se llama cardioversión .
Puede lograrse mediante la administración de medicamentos o mediante descarga eléctrica externa . En caso de fibrilación auricular que dure menos de 48 horas, se puede intentar de inmediato, sin precauciones especiales. Si se desconoce la fecha de inicio o es anterior, debe ir precedida de un tratamiento anticoagulante eficaz durante al menos 3 semanas, o después de una ecografía transesofágica de control destinada a verificar la ausencia de trombos formados en las aurículas.
La cardioversión parece tanto más rentable desde un punto de vista médico como la fibrilación es reciente, con una antigüedad de menos de seis meses. El riesgo de recurrencia a corto plazo de la FA parece ser tanto más limitado cuanto que el estado de fibrilación fue muy breve y controlado desde el principio, ya que no hubo intentos previos repetidos y fallidos de reducción y, por supuesto, no existe la noción de ya vieja condición patológica del corazón.
La reducción de fármacos se puede lograr mediante la administración de fármacos antiarrítmicos como amiodarona o flecainida , por vía oral o intravenosa. En algunos casos, esta reducción puede realizarla el propio paciente de forma ambulatoria (sin hospitalización), mediante la administración oral de una dosis única de un antiarrítmico al inicio de los síntomas ( método de píldora en el bolsillo ).
La reducción eléctrica ( desfibrilación ) se realiza bajo anestesia general breve, mediante la aplicación de una descarga eléctrica a corto plazo en el pecho del paciente. Posiblemente no se prescriba una sobredosis de digital durante la realización de la descarga.
Mantener el ritmo sinusal
Después de la reducción, se lleva a cabo mediante la prescripción de fármacos antiarrítmicos por vía oral (ejemplos de moléculas que se pueden utilizar: amiodarona , dronedarona , propafenona , disopiramida , sotalol ( betabloqueante con efecto estabilizador de membrana - ASM), flecainida y quinidina ). Sin embargo, la tasa de recurrencia sigue siendo alta.
La prescripción de tratamiento con fármacos antiarrítmicos no es obligatoria si se trata de un primer ataque, de rápida resolución, con correcta tolerancia y ausencia de cardiopatía de base.
La pérdida de peso (en obesos) puede reducir sustancialmente el riesgo de recurrencia. Asimismo, el ejercicio físico ayuda a estabilizar el ritmo.
Control de frecuencia cardiaca
Cuando los intentos de reducción no han tenido éxito, o existe una contraindicación para la reducción, la frecuencia cardíaca se ralentizará para evitar la aparición de síntomas debilitantes y mala tolerancia cardíaca. Simplemente ralentizar la arritmia sería más efectivo, en términos de estancias hospitalarias y mortalidad, que tratar de regular el ritmo o evitar que el trastorno rítmico reaparezca. Asimismo, en caso de insuficiencia cardíaca , una actitud agresiva dirigida a reducir la fibrilación y mantener el ritmo sinusal por medios medicinales no parece ser superior en cuanto a morbimortalidad y evolución en el tiempo respecto a una actitud contenido en ralentización y control. la frecuencia cardíaca.
Se pueden utilizar medicamentos como betabloqueantes , bloqueantes de los canales del calcio bradicardial ( diltiazem y verapamilo ), así como digoxina y, en menor medida , amiodarona , debido a sus múltiples efectos secundarios a largo plazo.
El objetivo es mantener la frecuencia cardíaca en reposo por debajo de 80 latidos por minuto, pero un control menos estricto (frecuencia en reposo inferior a 110 / min) parece igualmente eficaz.
En caso de falla, es posible lograr una "desconexión" entre las aurículas y los ventrículos del corazón mediante una técnica de radiofrecuencia que destruirá el haz de His . Este método requiere la colocación de un marcapasos permanente.
Prevención de la formación de trombos en la aurícula.
Cuando se inicia el tratamiento anticoagulante como parte de la prevención de accidentes tromboembólicos cerebrales, no es necesario organizar un relevo con una heparina ( heparina no fraccionada ), a diferencia del tratamiento de la enfermedad tromboembólica venosa ( flebitis o embolia pulmonar ).
Como regla general, la terapia anticoagulante se continúa durante al menos 1 mes después de la reducción y luego se suspende si la arritmia se ha resuelto y existe una alta probabilidad de que no vuelva a aparecer.
Si la arritmia persiste o si el mantenimiento del ritmo sinusal parece incierto (fibrilación auricular paroxística), se debe discutir el mantenimiento de la anticoagulación de acuerdo con el riesgo estimado de complicación tromboembólica . En 2001, se creó el puntaje CHADS2 para este propósito , iniciales de "Insuficiencia cardíaca" (insuficiencia cardíaca), "Hipertensión", "Edad" (más de 75 años), "Diabetes" y "Accidente cerebrovascular" (antecedentes de accidente vascular). -cerebral). La presencia de cada ítem cuenta como un punto, excepto el último (accidente neurológico), contando como dos puntos (explicando el “2” en el nombre de la puntuación). Esta puntuación se correlaciona con el riesgo de complicaciones trombóticas. Esta puntuación se completó en 2010, denominada CHA2DS2-VASc , que incluye otros criterios: sexo femenino, presencia de enfermedad vascular y edad intermedia (entre 65-75 años). En la práctica, una puntuación de 1 o 0 indica una puntuación baja y la ausencia de necesidad de tratamiento anticoagulante. En caso de enfermedad valvular mitral significativa ( estenosis mitral o insuficiencia mitral ), el riesgo trombótico es alto, independientemente del puntaje CHADS2 y está indicado el tratamiento anticoagulante. El riesgo también varía según el tipo de fibrilación: es más importante si esta última es permanente o persistente que si es solo paroxística. Asimismo, no está claro si el riesgo aumenta más allá de un umbral ("carga de fibrilación auricular") o si este aumento de riesgo es continuo con la duración de la arritmia.
En algunos casos, el riesgo del tratamiento anticoagulante parece ser mayor que el beneficio esperado; entonces se prefiere utilizar agentes antiplaquetarios : esencialmente aspirina . Esta última molécula ha demostrado cierta eficacia en la prevención de accidentes embólicos, pero en un grado significativamente menor que el tratamiento anticoagulante. La adición de clopidogrel reduce significativamente el riesgo vascular pero aumenta el riesgo de hemorragia.
El ximelagatrán , un inhibidor de la trombina , sería al menos tan eficaz como la vitamina K, pero su desarrollo se detuvo debido a los efectos secundarios del hígado. Otra molécula del mismo tipo, el dabigatrán , parece prometedora con una eficacia al menos comparable a las antivitaminas K y un menor riesgo de hemorragia. Otras moléculas de la clase de inhibidores del factor Xa como rivaroxaban y apixaban tienen resultados equivalentes. Estos medicamentos tienen la ventaja de no requerir un control regular del INR mediante muestras de sangre repetidas. Sus desventajas son la ausencia de un antídoto (pero se están desarrollando) en caso de hemorragia (pero la corta vida media de las moléculas consideradas en principio limita este riesgo) así como su coste nada despreciable.
Uno de los principales problemas de este tipo de tratamiento, sea el que sea, es la estimación empírica del riesgo hemorrágico. Se puede ayudar calculando una puntuación HAS-BLED en función de varios criterios: hipertensión arterial no controlada (1), insuficiencia renal (1) o hepática (1), antecedentes de accidente cerebrovascular (1), antecedentes de hemorragia (1), INR inestable (1), mayor de 65 años, consumo de drogas (1) o alcohol (1). Esta puntuación es 9. Es un acrónimo de " hipertensión, función renal o hepática anormal, accidente cerebrovascular, hemorragia, INR lábil, vejez, drogas o alcohol " . Sin embargo, cabe señalar que ciertos criterios de riesgo hemorrágico son los mismos que los del riesgo de accidente embólico. Una puntuación HAS-BLED alta no contraindica la prescripción de AVK, todo depende del balance riesgo beneficio. Los pacientes con una puntuación HAS-BLED alta deben ser monitoreados más de cerca si están en tratamiento.
Una alternativa, en caso de contraindicación de los anticoagulantes, es el cierre de la aurícula izquierda , una pequeña bolsa en el fondo de saco de la aurícula izquierda donde se forman con mayor frecuencia los trombos . Esta técnica se realiza mediante cateterismo transeptal (paso a la aurícula izquierda atravesando el tabique interauricular), bajo fluoroscopia y control por ecografía transesofágica en un paciente bajo anestesia general. Conduce a la instalación de un dispositivo que permite ocluir el pabellón auricular. Da resultados equivalentes a los de las antivitaminas K.
Tratamiento de la causa
Si se ha determinado una causa, tratar esta última, cuando sea posible, suele ser la forma más fácil de tratar de forma permanente la arritmia: tratamiento del hipertiroidismo , cirugía de válvulas, etc.
Técnicas ablativas
La mayoría de las fibrilaciones auriculares tienen su origen en focos de activación situados a nivel de la llegada de las venas pulmonares a la aurícula izquierda: el aislamiento eléctrico de las venas pulmonares por vía endocavitaria (ablación por radiofrecuencia) permite reducir de forma muy apreciable el riesgo de recurrencia en comparación con el tratamiento antiarrítmico convencional y se ha practicado desde finales de la década de 1990 . Sin embargo, esta es una técnica larga y compleja (que requiere el paso de un catéter especial a la aurícula izquierda a través del tabique interauricular: cateterismo transeptal), con un riesgo de complicaciones un poco más altas en un 5% con, principalmente, estrechamiento de las venas pulmonares y derrames pericárdicos compresivos ( taponamiento ). El riesgo embólico sigue siendo controvertido después del procedimiento y generalmente se recomienda continuar con los anticoagulantes durante algunos meses. Finalmente, la recurrencia de la arritmia es una posibilidad frecuente, incluso a largo plazo, que puede derivar en una nueva intervención. Por tanto, no es posible, en estas condiciones, hablar de "curación" .
En la actualidad, estas técnicas se utilizan principalmente en caso de fibrilación auricular recurrente mal tolerada a pesar de un tratamiento antiarrítmico óptimo. Sin embargo, pueden discutirse como una opción de primera línea en determinados casos (CA / FA paroxística en corazones sanos, especialmente en sujetos deportivos, o miocardiopatía rítmica). Su uso en la insuficiencia cardíaca parece ser más interesante para la comodidad de los pacientes afectados.
Notas y referencias
- http://www.sfcardio.fr/seignement/cardiologues-en-formation/documents-de-travail/cardiologie/ p. 168
- " ¿Sabías que la fibrilación auricular (FA) es una epidemia emergente del nuevo milenio?" » , Sobre Cardiología Práctica ,19 de septiembre de 2019(consultado el 14 de octubre de 2020 )
- " Fibrilación auricular: ¿la epidemia del siglo?" » , Sobre Cardiología Práctica ,28 de marzo de 2017(consultado el 14 de octubre de 2020 )
- Henri Kulbertus y Patrizio Lancellotti , “ La fibrilación auricular: una epidemia de la tercera edad? » , En Revue Médicale de Liège ,2014( ISSN 0370-629X , consultado el 14 de octubre de 2020 )
- J.-M. Davy y F. Roubille , “ La fibrilación auricular en 2010: un peso creciente en la morbilidad y mortalidad cardiovascular ” , en Annales de Cardiologie et d'Angéiologie ,diciembre de 2010( DOI 10.1016 / S0003-3928 (10) 70002-0 , consultado el 14 de octubre de 2020 ) , S4 - S13
- Cushny AR, Edmunds CW, Irregularidad paroxística del corazón y fibrilación auricular , En: Bulloch W, ed. Estudios en patología. Aberdeen, Escocia: Universidad de Aberdeen, 1906: 95-110
- Einthoven W. El telecardiograma. Arch Int Physiol 1906; 4: 132-164
- Lewis T, Fibrilación auricular: una condición clínica común , BMJ, 1909; 2: 1528-1528
- Kirchof P, Benussi S et al. "Guía ESC 2016 para el manejo de la fibrilación auricular desarrollada en colaboración con EACTS". Eur Heart J. 2016. doi: 10.1093 / eurheartj / ehw210. Próximo.
- (en) Furberg CD, Psaty BM, Manolio TA, Gardin JM, Smith VE Rautaharju PM Prevalencia de la fibrilación auricular en sujetos de edad avanzada (el Estudio de salud cardiovascular) , Am J Cardiol 1994; 74: 236-241
- (en) Miyasaka Y, Barnes ME, Gersh BJ et al. Tendencias seculares en la incidencia de fibrilación auricular en el condado de Olmsted, Minnesota, 1980 a 2000, e implicaciones en las proyecciones de prevalencia futura , Circulation, 2006; 114: 119-125
- (en) Chugh SS Havmoeller R, K Narayana et al. Epidemiología mundial de la fibrilación auricular: circulación de un estudio de 2010 sobre la carga global de enfermedad . 2014; 129: 837–847
- Larsson SC, Drca N, Wolk A, Consumo de alcohol y riesgo de fibrilación auricular: un estudio prospectivo y un metanálisis de respuesta a la dosis , J Am Coll Cardiol, 2014; 64: 281-289
- Kunal Pradip Verma y Michael Wong , " Fibrilación auricular " , Australian Journal of General Practice , vol. 48, n o 10,octubre de 2019, p. 694-699 ( ISSN 2208-7958 , PMID 31569325 , DOI 10.31128 / AJGP-12-18-4787 , leído en línea , consultado el 14 de noviembre de 2020 )
- (en) Cheng S, Keyes MJ, Larson MG , et al. “ Resultados a largo plazo en individuos con intervalo PR prolongado o bloqueo auriculoventricular de primer grado ” JAMA , 2009; 301: 2571–7
- (en) Fox CS, Parise H, D'Agostino RB Sr et al. “ La fibrilación auricular parental como factor de riesgo de fibrilación auricular en la descendencia ” JAMA . 2004; 291: 2851-2855.
- (en) Hodgson-Zingman DM, Karst ML, Zingman LV et al. Mutación por desplazamiento del marco del péptido natriurético auricular en la fibrilación auricular familiar , N Engl J Med, 2008; 359: 158-165
- Olson TM, Michels VV, Ballew JD et al. Mutaciones del canal de sodio y susceptibilidad a insuficiencia cardíaca y fibrilación auricular , JAMA, 2005; 293: 447-454.
- Sinner MF, Pfeufer A, Akyol M et al. La variante del canal IKr de codificación no sinónima KCNH2-K897T está asociada con la fibrilación auricular: resultados de un análisis sistemático basado en genes candidatos de KCNH2 (HERG) , Eur Heart J, 2008; 29: 907–914
- Gudbjartsson DF, Helgason H, Gudjonsson SA et al. Secuenciación del genoma completo a gran escala de la población islandesa , Nat Genet, 2015; 47: 435–444
- Gudbjartsson DF, Arnar DO, Helgadottir A et al. Variantes que confieren riesgo de fibrilación auricular en el cromosoma 4q25 , Nature, 2007; 448: 353–357
- (en) Kaab S, Darbar D, van NC et al. Replicación a gran escala y metanálisis de variantes en el cromosoma 4q25 asociadas con la fibrilación auricular , Eur Heart J, 2009; 30: 813-19
- Zhu W, Yuan P, Shen Y, Wan R, Hong K, Asociación del tabaquismo con el riesgo de fibrilación auricular incidente: un metanálisis de estudios prospectivos , Int J Cardiol, 2016; 218: 259–66
- (in) Molina L, Mont L, J Marrugat, Berruezo A, Brugada J, J Bruguera, Rebato C Elosua R. " La práctica de deportes de resistencia a largo plazo aumenta la incidencia de fibrilación auricular solitaria en hombres: un estudio de seguimiento » Europace . Mayo de 2008; 10 (5): 618-23
- (in) Mozaffarian D, Furberg CD, Psaty BM, Siscovick D. [ Actividad física e incidencia de fibrilación auricular en adultos mayores: el estudio de salud cardiovascular. ], Circulación. 19 de agosto de 2008; 118 (8): 800-7
- (en) Ragozzino W, Snyder J, Nayak. [ Autocardioversión de la fibrilación auricular solitaria paroxística con ejercicio ], N Engl J Med, 2002; 347,25: 2085
- (en) The Heuzey JY, Copy X, Henry P et al. [ Mecanismos de fibrilación auricular. ], Presse Med. 6 de abril de 1996; 25 (12): 590-4. Revisar
- (en) Mant J, Fitzmaurice DA, Hobbs FDR y als. Precisión del diagnóstico de fibrilación auricular en el electrocardiograma por médicos de atención primaria y software de diagnóstico interpretativo: análisis de datos del ensayo de detección de fibrilación auricular en ancianos (SAFE) , BMJ, 2007; 335: 380-2
- (en) Wolf PA, Abbott RD, Kannel WB. La fibrilación auricular como factor de riesgo independiente de accidente cerebrovascular: el estudio de Framingham , accidente cerebrovascular, 1991; 22: 983-988
- enero CT, Wann LS, Alpert JS et al. Guía de 2014 AHA / ACC / HRS para el tratamiento de pacientes con fibrilación auricular: informe del Grupo de trabajo del American College of Cardiology / American Heart Association sobre las guías de práctica y la Heart Rhythm Society , JACC, 2014; 64: e1 - e76
- Ganesan AN, Chew DP, Hartshorne T et al. El impacto del tipo de fibrilación auricular en el riesgo de tromboembolismo, mortalidad y hemorragia: una revisión sistemática y metanálisis , Eur Heart J, 2016; 37: 1591-1602
- Hindricks G, Potpara T, Dagres N et al. Guía de la ESC 2020 para el diagnóstico y tratamiento de la fibrilación auricular desarrollada en colaboración con la Asociación Europea de Cirugía Cardio-Torácica (EACTS): Grupo de Trabajo para el diagnóstico y tratamiento de la fibrilación auricular de la Sociedad Europea de Cardiología (ESC) Desarrollado con la contribución especial de la European Heart Rhythm Association (EHRA) de la ESC , Europ Heart J, 2021; 42: 373–498
- Enero CT, Wann LS, Calkins H et al. Actualización centrada en la AHA / ACC / HRS de 2019 de la Guía de la AHA / ACC / HRS de 2014 para el tratamiento de pacientes con fibrilación auricular: un informe del Grupo de trabajo del Colegio Estadounidense de Cardiología / Asociación Estadounidense del Corazón sobre Guías de Práctica Clínica y la Sociedad del Ritmo Cardíaco en Colaboración con la Sociedad de Cirujanos Torácicos , Circulación, 2019; 140: e125 - e151
- Martínez-González MA, Toledo E, Arós F et al. El consumo de aceite de oliva extravirgen reduce el riesgo de fibrilación auricular: Ensayo PREDIMED (Prevención con Dieta Mediterránea) , Circulación, 2014; 130: 18-26
- Directrices para el tratamiento de la fibrilación auricular: Grupo de trabajo para el tratamiento de la fibrilación auricular de la Sociedad Europea de Cardiología (ESC) , Eur Heart J, 2010; 31: 2369-2429
- Frick M, Frykman V, Jensen-Urstad M et al. Factores que predicen la tasa de éxito y la recurrencia de la fibrilación auricular después de la primera cardioversión eléctrica en pacientes con fibrilación auricular persistente , Clin Cardiol, 2001; 24: 238–244
- Paolo Alboni, MD, Giovanni L. Botto, MD y col. Tratamiento ambulatorio de fibrilación auricular de inicio reciente con el enfoque de “píldora en el bolsillo” , N Engl J Med 2004; 351: 2384-2391.
- Hohnloser SH, Crijns HJ, van Eickels M et al. Investigadores de ATHENA, Efecto de la dronedarona sobre los eventos cardiovasculares en la fibrilación auricular , N Engl J Med, 2009; 360: 668-78
- Pathak RK, Middeldorp ME, Meredith M et al. Efecto a largo plazo del control de peso dirigido por objetivos en una cohorte de fibrilación auricular: un estudio de seguimiento a largo plazo (LEGACY) , J Am Coll Cardiol; 2015; 65: 2159-2169
- Malmo V, Nes BM, Amundsen BH, Tjonna AE, Stoylen A, Rossvoll O, Wisloff U, Loennechen JP, El entrenamiento con intervalos aeróbicos reduce la carga de la fibrilación auricular a corto plazo: un ensayo aleatorizado , Circulation, 2016; 133: 466 –473
- (in) Los investigadores de AFFIRM, Una comparación del control de la frecuencia y el control del ritmo en pacientes con fibrilación auricular , N Engl J Med 2002; 34: 1825–1833
- (en) Roy D, Talajic M, Nattel S et al. [358: 2667-2677 Control del ritmo versus control de la frecuencia para la fibrilación auricular y la insuficiencia cardíaca ], N Eng J Med, 2008; 358: 2667-2677
- Van Gelder IC, Groenveld HF, Crijns HJ et al. Control de frecuencia indulgente versus estricto en pacientes con fibrilación auricular , N Engl J Med, 201; 362: 1363-1373
- Wigle P, Hein B, Bloomfield HE, Tubb M, Doherty M. Pautas actualizadas sobre anticoagulación ambulatoria , Am Fam Physician, 15 de abril de 2013; 87 (8): 556-66. PubMed .
- Gage BF, Waterman AD, Shannon W, Boechler M, Rich MW, Radford MJ, Validación de esquemas de clasificación clínica para predecir accidentes cerebrovasculares: resultados del Registro Nacional de Fibrilación Auricular , JAMA, 2001; 285: 2864-2870
- (in) Lip GY, Nieuwlaat R Pisters R, Lane DA, Crijns HJ, " Refinando la estratificación del riesgo clínico para predecir el accidente cerebrovascular y la tromboembolia en la fibrilación auricular mediante un enfoque novedoso basado en factores de riesgo: la encuesta Euro Heart es la fibrilación auricular " Chest . 2010; 137: 263-272
- (en) Steinberg BA, Hellkamp AS Lokhnygina Y et al. “ Mayor riesgo de muerte y accidente cerebrovascular en pacientes con persistencia vs. fibrilación auricular paroxística: resultados del ROCKET-AF Trial " Eur Corazón J . 2015; 36: 288-296
- (en) Vanassche T Lauw MN, Eikelboom JW et al. " Riesgo de patrón de trazo selon isquémica de la fibrilación auricular: análisis de 6563 pacientes tratados con aspirina en ACTIVE-A y AVERROES" Eur Corazón J . 2015; 36: 281-288.
- Chen LY, Chung MK, Allen LA et al. Carga de la fibrilación auricular: más allá de la fibrilación auricular como entidad binaria: declaración científica de la American Heart Association , Circulation, 2018; 137: e623-e644
- (en) Hart RG, Pearce LA, MI Aguilar, Meta-análisis: Terapia antitrombótica a prevenir el accidente cerebrovascular en pacientes que tienen fibrilación auricular no valvular , Ann Int Med, 2007: 146: 857-867
- (in) The ACTIVE Investigators, Efecto del clopidogrel agregado a la aspirina en pacientes con fibrilación auricular , N Engl J Med 2009; 360: 2066-2078
- (en) Connolly SJ, Ezekowitz MD, Yusuf S et al. Dabigatrán versus warfarina en pacientes con fibrilación auricular , N Eng J Med, 2009; 361: 1139-1151
- Mahaffey KW, Fox KAA, Rivaroxaban Inhibición directa del factor Xa por vía oral una vez al día en comparación con el antagonismo de la vitamina K para la prevención del accidente cerebrovascular y el ensayo de embolia en fibrilación auricular
- Granger BC, Alexander JH, McMurray J JV et al. para los comités e investigadores de ARISTOTLE, apixaban versus warfarina en pacientes con fibrilación auricular , N Engl J Med, 2011 (10.1056 / NEJMoa1107039)
- (in) Pisters R, Lane DA, Nieuwlaat R to your CB, Crijns HJ, Lip GY, " Una puntuación novedosa y fácil de usar (HAS-BLED) para evaluar el riesgo de hemorragia grave a 1 año en pacientes con fibrilación auricular: el Euro Heart Survey » Chest . 2010; 138: 1093-1100
- (in) Stoddard MF Dawkins PR, Prince CR Ammash NM " Los trombos de la orejuela auricular izquierda no son infrecuentes en pacientes con fibrilación auricular aguda y eventos embólicos recientes: un estudio ecocardiográfico transesofágico " J Am Coll Cardiol 1995; 25: 452-459
- (en) Reddy VY, Doshi SK, H Sievert et al. “ Cierre percutáneo de la orejuela auricular izquierda para la profilaxis del ictus en pacientes con fibrilación auricular: seguimiento a 2,3 años del ensayo PROTECT AF (sistema Watchman de la orejuela izquierda para la protección embólica en pacientes con fibrilación auricular) ” Circulación . 2013; 127: 720-729
- (en) Haissaguerre M, Jais P, Shah DC et als. Inicio espontáneo de la fibrilación auricular por latidos ectópicos que se originan en las venas pulmonares , N Engl J Med, 1998; 339: 659-66
- (en) Pappone C, Augello G, S Sala et al. " Un ensayo aleatorizado de ablación circunferencial de la vena pulmonar versus tratamiento con fármacos antiarrítmicos en la fibrilación auricular paroxística: el estudio APAF " J Am Coll Cardiol . 2006; 48: 2340-7
- (en) Cappato R, Calkins H, Chen SA et al. Encuesta mundial sobre los métodos, la eficacia y la seguridad de la ablación con catéter para la fibrilación auricular humana , Circulation, 2005; 111: 1100-5
- (en) Calkins H, Brugada J, Packer DL, Cappato R, Chen S, Crijns HJ, et al. Declaración de consenso de expertos de HRS / EHRA / ECAS sobre ablación quirúrgica y con catéter de la fibrilación auricular: recomendaciones para el personal, la política, los procedimientos y el seguimiento. Un informe del Grupo de Trabajo de la Heart Rhythm Society (HRS) sobre ablación quirúrgica y con catéter de la fibrilación auricular , Heart Rhythm, 2007; 4: 816-61
- (in) Calkins H, Información adicional sobre los aspectos técnicos y los resultados de la ablación con catéter "curativa" de la fibrilación auricular , Arrhythmia Electrophysiol Circ 2008; 1: 238-239
- (en) Natale A, Raviele A, Arentz T et al. Documento de consenso internacional Venice Chart sobre ablación de la fibrilación auricular , J Cardiovasc Electrophysiol, 2007; 18: 560-80
- (en) Khan MN, Jaïs P, Cummings J et al. Aislamiento de la vena pulmonar para la fibrilación auricular en pacientes con insuficiencia cardíaca , New Eng J Med, 2008; 359: 1778-1785