Vanilina
| Vanilina | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  representaciones de la molécula de vainillina |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificación | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre IUPAC | 4-hidroxil-3- metoxibenzaldehído | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinónimos |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100,004,060 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 204-465-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o RTECS | YW5775000 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 1183 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 3107 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sonrisas |
O = CC1 = CC (OC) = C (O) C = C1 , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / C8H8O3 / c1-11-8-4-6 (5-9) 2-3-7 (8) 10 / h2-5.8H, 1H3 InChIKey: MWOOGOJBHIARFG-UHFFFAOYSA-N |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia |
sólido blanco (generalmente en agujas) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades químicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fórmula bruta |
C 8 H 8 O 3 [Isómeros] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa molar | 152.1473 ± 0.0079 g / mol C 63.15%, H 5.3%, O 31.55%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| pKa | 7,40 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusión | 353–354 K ( 81,5 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° hirviendo | 558 K ( 285 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilidad |
10 g · l −1 en agua ( 25 ° C ) Molido libremente. en cloroformo , éter, CS 2 , ácido acético glacial , piridina . |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad | 1.056 g · cm -3 (sólido) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto de inflamabilidad | 147 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termoquímica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauciones | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Atención H319, P305 + P351 + P338, H319 : Provoca irritación ocular grave. P305 + P351 + P338 : Si entra en contacto con los ojos: Enjuagar cuidadosamente con agua durante varios minutos. Quítese los lentes de contacto si la víctima los usa y se pueden quitar fácilmente. Continúe enjuagando. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Directiva 67/548 / CEE | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Frases R : R22 : Nocivo por ingestión. Frases S : S24 / 25 : Evítese el contacto con la piel y los ojos. Frases R : 22, Frases S : 24/25, |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotoxicología | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 |
1580 mg · kg -1 (rata, oral ) 3925 mg · kg -1 (ratón, oral ). |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Consideraciones terapéuticas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Clase terapéutica | Antioxidantes | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Compuestos relacionados | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isómero (s) | Salicilato de metilo , ácido mandélico | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Otros compuestos | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unidades de SI y STP a menos que se indique lo contrario. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
La vainillina es un aldehído aromático natural que se desarrolla en las vainas de la vainilla en la preparación de la misma como especia .
Se utiliza para elaborar sabores naturales.
Origen
La vainillina es el más importante y característico de los muchos componentes del aroma natural de la vainilla . Representa del 0,75% al 2% de la masa de la vaina. Por tanto, una vaina que pesa alrededor de tres gramos contiene sólo de 22 a 60 mg .
Fue extraído por primera vez en estado puro por el químico Théodore Nicolas Gobley mediante maceración de vainilla en alcohol a 85 ° , seguido de extracción con éter . La sustancia marrón muy fragante que obtiene después de la evaporación se lleva a ebullición en agua y luego se filtra en caliente. La vainillina se aísla finalmente después de varias recristalizaciones sucesivas en forma de largas agujas incoloras.
La vainillina fue sintetizada por primera vez en 1874 por Wilhelm Haarmann y Ferdinand Tiemann , a partir de la coniferina, un derivado de isoeugenol que se encuentra en la corteza de pino. Karl Reimer propuso dos años después, en 1876, una nueva ruta sintética a partir del guayacol .
Propiedades físicas y químicas
La molécula es un aldehído aromático , de ahí sus otros nombres de vainillaldehído o aldehído vanílico. En solución, en presencia de hierro y otro compuesto alcalino , el aldehído adquiere un color rojo y pierde su poder oloroso.
La vainillina tiene un olor similar a la vainilla con un sabor dulce. Sin embargo, su intensidad aromática es de 2 a 4 veces menos potente que la de la etil vainillina .
Producción y síntesis
La vainillina se puede fabricar de forma económica mediante varios procesos, mientras que la vainilla es muy cara de producir y preparar. Así, la producción industrial de vainillina y su uso en alimentos y perfumes se han vuelto mucho más importantes que la producción y uso de vainilla natural.
A título indicativo, 1 kg de vainas de vainilla enteras vale alrededor de 500 euros cuando 1 kg de vainas de vainilla en polvo vale alrededor de 40 euros y un kilogramo de vainilla líquida artificial cuesta alrededor de 10 euros.
Síntesis de guayacol
En 1876, Karl Reimer preparó vainillina a partir de guayacol . Después de disolver el guayacol en una solución de hidróxido de potasio , el conjunto se hace reaccionar con cloroformo . Esta reacción da lugar a la formación de vainillina y de un isómero, metoxialdehído salicílico. Los dos compuestos así formados se separan mediante destilación al vapor a presión de 2 atmósferas .
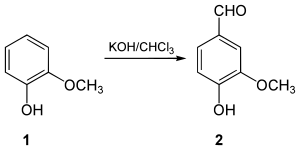
Síntesis de 4-hidroxibenzaldehído
La vainillina se puede sintetizar a partir de 4-hidroxibenzaldehído . Esta preparación se lleva a cabo en dos etapas que implican una sustitución aromática electrófila para incorporar un átomo de bromo en el anillo aromático seguido de una metoxilación organometálica utilizando un catalizador de cobre.
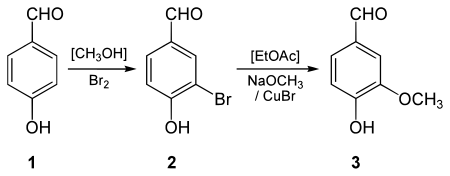
Síntesis de eugenol
El eugenol se extrae del clavo .
El eugenol (1) se convierte en isoeugenol (2), luego en acetato de isoeugenol, luego en acetato de vainillina, luego en vainillina .

Síntesis a partir de lignina
Utilizamos la lignina recuperada de la pulpa de la industria de aguas residuales . Esta ruta sintética oxida los ácidos lignosulfónicos mediante oxidación húmeda .
Síntesis de curcumina
La curcumina se extrae de la cúrcuma .
Biogénesis a partir de residuos de azúcar de la remolacha o de la industria del maíz
Un proceso de descomposición de ácido ferúlico de residuos industriales de maíz o remolacha azucarera (por un hongo) da como resultado un aroma rico en vainillina. Como el proceso es bioquímico, el sabor puede considerarse como un sabor natural y etiquetarse como tal en la composición de las preparaciones alimenticias.
Investigación y desarrollo
Un nuevo método presentado en 2017 por académicos indios que lo presenta como más respetuoso con el medio ambiente, utiliza, a presión atmosférica, un catalizador compuesto de elementos no raros ( sílice y cobre ) para aislar eficazmente la vainillina separándola de otros compuestos en agua hirviendo. .
Este catalizador se puede reciclar cuatro veces sin perder su eficiencia, mientras que los calisers tradicionales tuvieron que ser reemplazados después de su uso.
Además, este método ya no produce agua residual a un pH extremadamente alto (que requirió neutralización con ácido clorhídrico antes de descargarse al medio ambiente.
Diferencias de vainilla
La vainillina extraída de la vaina de vainilla es exactamente la misma que la elaborada industrialmente.
La diferencia de calidad proviene de la complejidad y riqueza del aroma natural de la vainilla que contiene muchos otros componentes, mientras que la vainillina obtenida por síntesis es químicamente pura. Por otro lado, los procesos de biogénesis conducen a la formación de un aroma complejo, y no a un producto químicamente puro .
Producción mundial
La vainillina es el sabor más elaborado del mundo, muy por delante de los sabores de chocolate y café; la producción de sabores de vainilla se estima en 25.000 toneladas por año.
usar
- La vainillina se utiliza por sus propiedades aromatizantes, ya sea sola o como componente de un aroma . No se debe abusar del aroma ya que tiene un sabor amargo en dosis altas. La vainillina (número Fema GRAS 3107) se utiliza en la creación de sabores de vainilla, chocolate y plátano .
- Es un producto intermedio para la producción de varios derivados para uso farmacéutico.
- Sus propiedades químicas hacen que en ocasiones se utilice en determinadas reacciones de la química analítica , en particular en forma de sulfovanilina .
- También se le atribuyen virtudes afrodisíacas .
- La vainillina sulfúrica (mezcla en ácido sulfúrico concentrado) se usa para medir terpenos por colorimetría
- La vainillina también se utiliza como aditivo en los líquidos de los cigarrillos electrónicos.
Notas y referencias
- CRC Handbook of Tables for Organic Compound Identification , tercera edición, 1984, ( ISBN 0-8493-0303-6 ) .
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- (en) ChemIDplus , " La vainillina USAN - RN: 121-33-5 " , en chem.sis.nlm.nih.gov , Biblioteca Nacional de Medicina (visitada 6 de octubre de, 2008 )
- (en) Carl L. Yaws, Manual de diagramas termodinámicos: compuestos orgánicos C8 a C28 , vol. 3, Huston, Texas, Pub del Golfo. Co.,1996, 396 p. ( ISBN 0-88415-859-4 )
- (en) WG Ungerer, Mercados de medicamentos y productos químicos , vol. 9, Mercados de drogas y productos químicos,30 de noviembre de 1921( leer en línea ) , pág. 1127-1128
- Théodore N. Gobley , Revista de farmacia y química: que contiene el trabajo de la Sociedad de Farmacia de París: una revisión médica , vol. 34, Doin,1858( leer en línea ) , pág. 401-405
- (De) F. Tiemann y W. Haarmann , " Ueber das Coniferin und seine Umwandlung in das aromatische Princip der Vanille " , Berichte der deutschen chemischen Gesellschaft , vol. 7, n o 1,1874, p. 608-623 ( DOI 10.1002 / cber.187400701193 )
- (de) K. Reimer , " Ueber Eine neue Bildungsweise aromatischer aldehído " , Berichte der Deutschen Chemischen Gesellschaft , vol. 9, n o 1,1876, p. 423-424 ( DOI 10.1002 / cber.187600901134 )
- (en) GA bardana (2005). Manual de ingredientes aromatizantes de Fenaroli. Quinta edición. Prensa CRC. ( ISBN 0849330343 ) pág. 1880-1881
- (en) GA Burdock (2005). Manual de ingredientes aromatizantes de Fenaroli. Quinta edición. Prensa CRC. ( ISBN 0849330343 ) pág. 639-640
- Artículo en "Bilan"
-
Douglass F, Patel S, Travis M, Emma E, Winkel, Síntesis de vainillina a partir de 4-hidroxibenzaldehído, J. Chem.
Ed., 2007: 84 (7): página 1158, DOI: 10.1021 / ed084p1158 - Mammou Faiza, “ SÍNTESIS, ESTUDIOS CINÉTICOS Y EVALUACIÓN DE LA ACTIVIDAD DE DERIVADOS DE EUGENOL. COMPOSICIÓN DEL ACEITE ESENCIAL EXTRAÍDO DE LA CLOU DE CLOU DE CLOU DE CLOU DE CLOU DE CLOU DE CLOU DE CLOU DE CLOU DE CLOU DE CLOU DE CLOU DE CLROFLE ” , en el repositorio institucional de la Universidad Abou Bekr Belkaid Tlemcen UABT ,1 st de julio de 2016(consultado el 28 de febrero de 2021 )
- Gary M. Lampman , Jennifer Andrews , Wayne Bratz y Otto Hanssen , “ Preparación de vainillina a partir de eugenol y aserrín ”, Journal of Chemical Education , vol. 54, n o 12,Diciembre de 1977, p. 776 ( ISSN 0021-9584 y 1938-1328 , DOI 10.1021 / ed054p776 , leído en línea , consultado el 13 de mayo de 2020 )
- (in) C. Maugans y C. Ellis , " Wet Air Oxidation: A Review of Commercial Sub-Critical Hydrothermal Treatment " , Vigésimo Primera Conferencia Internacional Anual sobre Tecnologías de Incineración y Tratamiento Térmico ,13-17 de mayo de 2002( leer en línea )
- Asther, M., Lesage-Meessen, L., Stentelaire, C. y Thibault, JF (1998). Setas de vainilla . Biofutur, 1998 (178), 32-34.
- Oddou J (2000) Diseño y extrapolación de un proceso microbiano para la producción de vainillina natural a partir de subproductos de la industria alimentaria (Tesis doctoral).
- Stentelaire, C. (1999). Control de las vías metabólicas de los hongos implicadas en la biotransformación de la fracción feruloílo de coproductos agrícolas en vainillina natural (Tesis doctoral)
- Micard, V., Renard, CMGC, Thibault, JF y Lesage-Meesen, L. (1995). ¿Es posible obtener vainillina natural de la pulpa de remolacha? . Conferencia de Inra, 149-149.
- Shivaji L. Bhanawase y Ganapati D. Yadav (2017), Novel encapsulado en sílice Cu - Al hidrotalcita Catalyst: oxidativo descarboxilación del vainillil ácido mandélico a vainillina en agua a presión atmosférica ; Indiana Eng. Chem. Res., Artículo ASAP; DOI: 10.1021 / acs.iecr.6b04982 ( resumen )
- Una forma más verde de hacer vainilla , publicado por Katherine Kornei el 17 de marzo de 2017 (Noticias de la revista Science)
- " Vanilla and Vanillin " , en http://www.societechimiquedefrance.fr
Artículo relacionado
- Vainilloide
- Isovanillina
- Etilvainillina
enlaces externos
- (en) Centro de información de plantas electrónicas en Royal Botanic Gardens, Kew 2003-11-8
- (fr) La cristalización de la vainillina
- (es) Compound Display 1183 Base de datos NCBI
- (es) COMPUESTO: C00755 www.Genome.net


