Epiclorhidrina
| (±) -Epiclorhidrina | |||
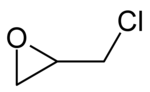
| |||
  R- enantiómero de epiclorhidrina (izquierda) y S -epiclorhidrina (derecha) |
|||
| Identificación | |||
|---|---|---|---|
| Nombre IUPAC | 2- (clorometil) oxirano | ||
| Sinónimos |
Cloruro de glicidilo de
|
||
| N o CAS | (R,S) | ||
| N o ECHA | 100,003,128 | ||
| N o EC | 203-439-8 | ||
| PubChem | |||
| Sonrisas |
ClCC1CO1 , |
||
| InChI |
InChI: InChI = 1 / C3H5ClO / c4-1-3-2-5-3 / h3H, 1-2H2 |
||
| Apariencia | líquido incoloro | ||
| Propiedades químicas | |||
| Fórmula |
C 3 H 5 Cl O [Isómeros] |
||
| Masa molar | 92.524 ± 0.005 g / mol C 38.94%, H 5.45%, Cl 38.32%, O 17.29%, 92.52 g / mol |
||
| Propiedades físicas | |||
| T ° fusión | -48 ° C | ||
| T ° hirviendo | 116,56 ° C | ||
| Solubilidad | 6,59 g / 100 ml (agua, 25 ° C ); Miscible con alcohol, éter, cloroformo , tricloroetileno , tetracloruro de carbono ; Inmiscible con hidrocarburos de petróleo |
||
| Parámetro de solubilidad δ | 22,5 MPa 1/2 ( 25 ° C ) | ||
| Densidad | 1.18066 g · cm -3 a 20.0 ° C | ||
| Temperatura de autoignición | 415,6 ° C | ||
| punto de inflamabilidad | 40,6 ° C | ||
| Presión de vapor saturante | 1.333 kPa a 16.6 ° C | ||
| Viscosidad dinámica | 1,03 MPa · s a 25 ° C | ||
| Precauciones | |||
| SGH | |||
     H226, H301, H311, H314, H331, H350,
H226 : inflamable líquido y vapor
H226, H301, H311, H314, H331, H350,
H226 : inflamable líquido y vapor H301 : Tóxico por ingestión H311 : Tóxico en contacto con la piel H314 : Provoca quemaduras graves en la piel y lesiones oculares H331 : tóxicos si se inhala H350 : causa del cáncer de mayo (indicar la vía de exposición de entrada si se ha demostrado concluyentemente que ninguna otra vía de exposición conduce al mismo peligro) |
|||
| WHMIS | |||
   B3, D1A, D2A, E, |
|||
| NFPA 704 | |||
| 3 3 2 | |||
| Transporte | |||
63 : material tóxico e inflamable (punto de inflamación 23 a 60 ° C , incluidos los valores límite) Número ONU : 2023 : EPICHLORHYDRIN Clase: 6.1 Etiquetas: 6.1 : Sustancias tóxicas 3 : Líquidos inflamables Embalaje: Grupo de embalaje II : materiales moderadamente peligrosos ;   |
|||
| Clasificación IARC | |||
| Grupo 2A, carcinógeno | |||
| Inhalación | TLV: 2 ppm | ||
| Piel | 7,6 mg / m3 | ||
| Ecotoxicologia | |||
| DL 50 |
90 mg · kg -1 (rata, oral ) 154 mg · kg -1 (rata, iv ) 150 mg · kg -1 (rata, sc ) 113 mg · kg -1 (rata, ip ) |
||
| LogP | 0,45 | ||
| Umbral de olor | bajo: 0.93 ppm | ||
| Unidades de SI y STP a menos que se indique lo contrario. | |||
La epiclorhidrina o epiclorhidrina y 1-cloro-2,3-epoxipropano , es un compuesto orgánico clorado de fórmula estructural CH 2 CHOCH 2 Cl, líquido volátil tóxico, incoloro a fuerte olor a ajo. Un átomo de carbono de la epiclorhidrina es quiral , por lo que hay dos formas enantioméricas de este compuesto.
A pesar de su nombre, la epiclorhidrina no pertenece a la familia de las clorhidrinas , ya que no es un alcohol halogenado, sino un epóxido . Por otro lado, ciertos intermedios directos en su síntesis, como el 2,3-dicloro-1-propnol y el 1,3-dicloro-2-propnol, son las clorohidrinas.
Producción
La epiclorhidrina está hecha de cloruro de alilo en dos etapas, primero, hidrocloración con ácido hipocloroso , lo que da como resultado una mezcla de clorohidrinas :
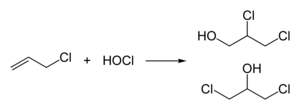
La segunda fase da como resultado la formación del epoxi mediante el tratamiento con una base :

Por esta vía, se producen anualmente más de 800.000 toneladas (1997) de epiclorhidrina.
Vía del glicerol
La epiclorhidrina fue descrita por primera vez en 1848 por Marcellin Berthelot . El compuesto se aisló durante los estudios de las reacciones entre el glicerol y el gas cloruro de hidrógeno .
Recordando la experiencia de Berthelot, se han comercializado fábricas de glicerol-epiclorhidrina (GTE, para glicerol-a-epiclorhidrina ). Esta tecnología aprovecha la disponibilidad de gliceroles económicos del procesamiento de biocombustibles . En el proceso desarrollado por Dow Chemical , el glicerol sufre dos reacciones de sustitución cuando se trata con cloruro de hidrógeno en presencia de un ácido carboxílico utilizado como catalizador . La reacción forma uno de los mismos dos intermedios que en el proceso de cloruro de alilo / ácido hipocloroso, 1,3-dicloro-2-propnol, y también se trata con una base para formar epiclorhidrina.

Otras rutas
Se continúan explorando otras rutas que involucran menos productos intermedios clorados. Se puede citar, por ejemplo, la epoxidación del cloruro de alilo .
usar
Síntesis de glicerol y resinas epoxi.
La epiclorhidrina se convierte principalmente en bisfenol-A-diglicidiléter (en) , un componente básico en la fabricación de resinas epoxi . También es un precursor de monómeros para otras resinas y polímeros, incluyendo resinas de intercambio iónico , poliéterpolioles para espumas de poliuretano retardantes de llama, alquilgliceril etersulfonatos para detergentes, elastómeros ( códigos de polímero CO, ECO) y resinas especiales para procesamiento de papel.
Otro uso es la conversión a glicerol sintético. Sin embargo, el rápido aumento en la producción de biodiesel , donde el glicerol es un desperdicio, ha dado como resultado una sobreabundancia de glicerol en el mercado, lo que hace que este proceso no sea rentable. El glicerol sintético ahora solo se usa en aplicaciones farmacéuticas y biotecnológicas sensibles donde los estándares de calidad son muy altos.
Aplicaciones menores y de nicho
La epiclorhidrina es un precursor versátil en la síntesis de muchos compuestos orgánicos. Por ejemplo, se puede convertir en nitrato de glicidilo , un aglutinante energético utilizado en composiciones explosivas y propulsoras. La epiclorhidrina se hace reaccionar con un nitrato alcalino, como el nitrato de sodio , produciendo nitrato de glicidilo y un cloruro alcalino. Se usa como solvente para celulosa , resinas y pinturas, y ha encontrado uso como fumigante contra insectos.
Los polímeros hechos de epiclorhidrina, por ejemplo resinas de poliamida-epiclorhidrina, se utilizan en el refuerzo de papel y en la industria alimentaria para fabricar bolsas de té , filtros de café y tripas sintéticas para salchichas / embutidos , así como para la purificación de agua .
Una aplicación bioquímica importante de la epiclorhidrina es su uso como agente reticulante para la producción de resinas de cromatografía de exclusión por tamaño en Sephadex (en) a partir de dextrano .
seguridad
La epiclorhidrina está clasificada por varias agencias y grupos internacionales de investigación en salud como un carcinógeno probable o probable en humanos. El consumo prolongado (oral) de niveles elevados de epiclorhidrina podría provocar problemas estomacales y un mayor riesgo de cáncer. La exposición ocupacional a la epiclorhidrina por inhalación podría causar irritación de los pulmones y un mayor riesgo de cáncer de pulmón.
La epiclorhidrina es inflamable y forma productos de descomposición peligrosos en condiciones de incendio. Es tóxico por inhalación, en contacto con la piel y por ingestión, y puede provocar quemaduras. Puede provocar sensibilización por contacto con la piel.
Notas y referencias
- ( fr ) Este artículo está tomado parcial o totalmente del artículo de Wikipedia en inglés titulado " Epichlorohydrin " ( ver la lista de autores ) .
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- (en) Guenter pared de agua, Robert Rieth, Kenneth T. Rowbottom, epóxidos , Wiley-VCH Verlag GmbH & Co, coll. "Enciclopedia de química industrial de Ullmann",15 de junio de 2000( DOI 10.1002 / 14356007.a09_531 , presentación en línea )
- "EPICHLOROHYDRIN" en Hazardous Substances Data Bank , consultado el 16 de julio de 2012
- (en) James E. Mark, Manual de propiedades físicas del polímero , Springer,2007, 2 nd ed. , 1076 p. ( ISBN 978-0-387-69002-5 y 0-387-69002-6 , leer en línea ) , pág. 294
- Entrada "Epichlorhydrin" en la base de datos química GESTIS de la IFA (organismo alemán responsable de la seguridad y salud) ( alemán , Inglés ), consultado el 3 de de diciembre de, 2010 (Javascript required)
- "Epiclorhidrina" en la base de datos de productos químicos Reptox de la CSST (organización de Quebec responsable de la seguridad y salud en el trabajo), consultado el 3 de diciembre de 2010
- Universidad UCB de Colorado
- (en) " epiclorhidrina " en ChemIDplus , visitada 03 de diciembre 2010
- "1-cloro-2,3-epoxipropano" , en ESIS , consultado el 3 de diciembre de 2010
- Enciclopedia de química industrial de Ullmann , Weinheim, Wiley-VCH,2005( DOI 10.1002 / 14356007.a01_425 )
- Marcellin Berthelot , “ Sobre las combinaciones de glicerina con ácidos y sobre la síntesis de los principios inmediatos de las grasas animales ”, Ann. Chim. Phys. , vol. 41,1854, p. 216–319 ( leer en línea [ archivo de2 de abril de 2015] , consultado el 2 de marzo de 2015 ).
- Doris de Guzman, " Growing glycerine-to-ECH plants " , ICIS Green Chemicals,20 de enero de 2011
- Bruce M. Bell , John R. Briggs , Robert M. Campbell , Susanne M. Chambers , Phil D. Gaarenstroom , Jeffrey G. Hippler , Bruce D. Hook , Kenneth Kearns , John M. Kenney , William J. Kruper , D James Schreck , Curt N. Theriault y Charles P. Wolfe , “La glicerina como materia prima renovable para la producción de epiclorhidrina. El proceso GTE ”, LIMPIO - Suelo, aire, agua , vol. 36, n o 8,2008, p. 657 ( DOI 10.1002 / clen.200800067 , lea en línea [ archivo de18 de julio de 2012] [reimpresión del texto completo], consultado el 5 de marzo de 2012 )
- Jun Li, Gongda Zhao, Shuang Gao, Ying Lv, Jian Li y Zuwei Xi, “ Epoxidación de cloruro de alilo a epiclorhidrina mediante un catalizador con soporte reversible con H2O2 en condiciones sin disolventes ”, Org. Proceso Res. Dev. , vol. 10, n o 5,2006, p. 876–880 ( DOI 10.1021 / op060108k )
- Ha Q. Pham y Maurice J. Marks , " Resinas epoxi ", Wiley-VCH , Weinheim,2012( ISBN 978-3527306732 , DOI 10.1002 / 14356007.a09_547.pub2 )
- " Umbrales de toxicidad aguda - Epiclorhidrina " , INERIS
- Phil Taylor , “¡ La glicerina sintética está de regreso (pero nunca se fue realmente)! » , Sobre tecnólogo en farmacia ,16 de octubre de 2008(consultado el 29 de noviembre de 2018 )
- Gould, RF Advanced Propellant Chemistry , ACS Chemistry Series 54, 1966
- " Laboratorios de pruebas de agua suburbana: hoja de datos de epiclorhidrina " [ archivo de5 de abril de 2012] , H2otest.com (consultado el 2 de diciembre de 2011 )
- " Sustancias químicas del gobierno de Canadá: oxirano, (clorometil) - (epiclorohidrina) número de registro CAS 106-89-8 " (consultado el 7 de mayo de 2013 )
- " GE Healthcare Life Sciences - Instrucciones para Sephadex Media " [ archivo de18 de febrero de 2012] , .gelifesciences.com (consultado el 2 de diciembre de 2011 )
- " Sistema integrado de información sobre riesgos de la EPA: epiclorhidrina (CASRN 106-89-8) " (consultado el 7 de mayo de 2013 )
- " Gobierno de Canadá: evaluación de detección de epiclorhidrina " (consultado el 7 de mayo de 2013 )
- " NIOSH Pocket Guide to Chemical Hazards - Epichlorohydrin " (consultado el 20 de septiembre de 2013 )
- " Información básica sobre la epiclorhidrina en el agua potable " (consultado el 7 de mayo de 2013 )
- " Gobierno de Canadá: evaluación de detección de epiclorhidrina " (consultado el 7 de mayo de 2013 )
