Tripsina
La tripsina ( EC ) es una peptidasa del jugo pancreático involucrada en la digestión de proteínas . Es una serina proteasa que hidroliza los enlaces peptídicos ubicados junto a C un residuo de lisina o arginina , que son aminoácidos básicos .
Tripsina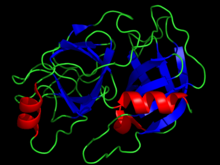 Estructura de la tripsina bovina cristalizada ( PDB 1UTN )
Estructura de la tripsina bovina cristalizada ( PDB 1UTN )
| Pfam | PF00089 |
|---|---|
| InterPro | IPR001254 |
| INTELIGENTE | SM00020 |
| PROSIDAD | PDOC00124 |
| MEROPS | S1 |
| SCOP | 1c2g |
| SUPERFAMILIA | 1c2g |
| CDD | cd00190 |
Síntesis
El páncreas lo sintetiza en forma de tripsinógeno ( proenzima inactiva) y luego se almacena en las vesículas enzimáticas de las células acinares desde donde se excreta durante la digestión . La activación del tripsinógeno en tripsina es el resultado de la hidrólisis del propéptido bajo la acción de la enteroquinasa o por el efecto autoactivante de la tripsina. La colecistoquinina-pancreozima activa la secreción de enzimas (por lo tanto, tripsina) en el jugo pancreático.
Actividad enzimática
Tripsina| EC No. | EC |
|---|---|
| número CAS |
| IUBMB | Entrada IUBMB |
|---|---|
| IntEnz | Vista IntEnz |
| BRENDA | Entrada BRENDA |
| KEGG | Entrada KEGG |
| MetaCyc | Camino metabólico |
| PRIAM | Perfil |
| PDB | Estructuras |
| IR | AmiGO / EGO |
La tripsina es una endoproteasa que hidroliza los enlaces peptídicos en los que un aminoácido básico ( Lys - | - Xaa o Arg - | - Xaa ) realiza su función ácida (excepto en el caso de que el siguiente aminoácido (aquí esquematizado por "Xaa") es una Prolina ). Corta estos aminoácidos en el C-terminal. En otras palabras, transforma las cadenas de polipéptidos en cadenas de proteínas más cortas para permitir la digestión . Efectivo a pH 7,5 - 8,5, se inactiva y se digiere en unas pocas horas a pH neutro (= 7) en el intestino.
La tripsina participa en la activación de otras enzimas como la alfa-quimotripsina mediante la escisión hidrolítica de la cadena polipeptídica del quimotripsinógeno.
Esta enzima en su S-tripsina o tripsina-como forma también se utiliza durante la 1 st semana del desarrollo embrionario humano, la segmentación. Es secretado por el trofoblasto para digerir la zona pelúcida que rodea al blastocisto. Este fenómeno se denomina brote que tiene lugar alrededor de D6, que permite la implantación en el endometrio.
Mecanismo
La tripsina pertenece a la familia de las serina proteasas de las que es arquetipo. Estas enzimas se caracterizan por la presencia de una tríada catalítica compuesta por cadenas laterales de tres aminoácidos : una serina (Ser-195), una histidina (His-57) y un aspartato (Asp-102). Estos residuos interactúan y forman un relé de carga que vuelve nucleófila la serina del sitio activo y permite el ataque del grupo carbonilo del enlace peptídico hidrolizado.
Además, la tripsina contiene un "agujero oxianiónico" bordeado por los grupos amida de la cadena principal del polipéptido al nivel de glicina 193 y serina 195. Esta cavidad recibe el átomo de oxígeno del grupo carbonilo del enlace péptico escindido y estabiliza el intermedio de reacción mediante promover la formación de una carga negativa en el oxígeno.
El reconocimiento de un residuo cargado positivamente justo aguas arriba del sitio de escisión se lleva a cabo mediante el grupo carboxilato (-COO - ) del aspartato 189 que se encuentra en la parte inferior del bolsillo de reconocimiento de la cadena lateral del aminoácido ubicado justo aguas arriba ( Lado N- terminal) del sitio de escisión. La interacción electrostática entre la carga positiva del aminoácido reconocido y la carga negativa del aspartato es el factor principal de esta selectividad.
Patologías asociadas
En pancreatitis y fibrosis quística , la tripsina al ser mal evacuada, es la principal causa de la reacción inflamatoria del páncreas.
usar
La tripsina se encuentra en la mayoría de los animales. Esta enzima se usa ampliamente para enfoques de investigación proteómica , especialmente para la caracterización y secuenciación de proteínas. Por tanto, se utiliza en particular en espectrometría de masas para digerir proteínas antes del análisis.
La tripsina se usa en cultivos celulares para separar las células adheridas a los frascos de cultivo o placas de Petri . De hecho, la tripsina escinde las proteínas de la membrana de adhesión y las células se encuentran en suspensión. Esta "tripsinización" se usa a diario para mantener cultivos celulares ( cambiando a un matraz de cultivo más grande o multiplicando los matraces), para contar las células mediante citometría de flujo o para realizar otros análisis. Sin embargo, este tratamiento afecta un poco a las células (viabilidad, marcadores de membrana), por lo que la acción de la tripsina debe ser limitada: se elimina lavando las células, también se inhibe mediante la adición de suero de ternero fetal (proteínas en gran exceso sobre las proteínas de membrana). ), o un inhibidor específico. Alternativamente, se utilizan otras enzimas.
La tripsina también se utiliza en inmunohematología para la detección de anticuerpos irregulares o incluso durante el establecimiento de un cariotipo : por ejemplo, hidrolizando histonas, y combinada con la tinción de Giemsa, permite la aparición de bandas G en el ADN y por tanto la identificación precisa de cromosomas. Por tanto, se puede detectar una anomalía cromosómica.
Secuencia de tripsina humana
La isoforma A contiene 304 aminoácidos.
10 20 30 40 50 60 70 80 90 100 MCGPDDRCPA RWPGPGRAVK CGKGLAAARP GRVERGGAQR GGAGLELHPL LGGRTWRAAR DADGCEALGT VAVPFDDDDK IVGGYTCEEN SLPYQVSLNS 110 120 130 140 150 160 170 180 190 200 GSHFCGGSLI SEQWVVSAAH CYKTRIQVRL GEHNIKVLEG NEQFINAAKI IRHPKYNRDT LDNDIMLIKL SSPAVINARV STISLPTTPP AAGTECLISG 210 220 230 240 250 260 270 280 290 300 WGNTLSFGAD YPDELKCLDA PVLTQAECKA SYPGKITNSM FCVGFLEGGK DSCQRDSGGP VVCNGQLQGV VSWGHGCAWK NRPGVYTKVY NYVDWIKDTI AANSIsoforma B contiene 260 aminoácidos.
10 20 30 40 50 60 70 80 90 100 MELHPLLGGR TWRAARDADG CEALGTVAVP FDDDDKIVGG YTCEENSLPY QVSLNSGSHF CGGSLISEQW VVSAAHCYKT RIQVRLGEHN IKVLEGNEQF 110 120 130 140 150 160 170 180 190 200 INAAKIIRHP KYNRDTLDND IMLIKLSSPA VINARVSTIS LPTTPPAAGT ECLISGWGNT LSFGADYPDE LKCLDAPVLT QAECKASYPG KITNSMFCVG 210 220 230 240 250 260 FLEGGKDSCQ RDSGGPVVCN GQLQGVVSWG HGCAWKNRPG VYTKVYNYVD WIKDTIAANSIsoforma C contiene 247 aminoácidos.
10 20 30 40 50 60 70 80 90 100 MNPFLILAFV GAAVAVPFDD DDKIVGGYTC EENSLPYQVS LNSGSHFCGG SLISEQWVVS AAHCYKTRIQ VRLGEHNIKV LEGNEQFINA AKIIRHPKYN 110 120 130 140 150 160 170 180 190 200 RDTLDNDIML IKLSSPAVIN ARVSTISLPT TPPAAGTECL ISGWGNTLSF GADYPDELKC LDAPVLTQAE CKASYPGKIT NSMFCVGFLE GGKDSCQRDS 210 220 230 240 GGPVVCNGQL QGVVSWGHGC AWKNRPGVYT KVYNYVDWIK DTIAANSNotas y referencias
- Los valores de la masa y el número de residuos se indica aquí son los de la proteína precursora resultante de la traducción del gen , antes de las modificaciones post-traduccionales , y puede diferir significativamente de los valores correspondientes Para la proteína funcional.
- http://www.interchim.fr/ft/1/158624.pdf Inhibidores de tripsina (SBTI, BPTI, SPTI)
- http://www.interchim.fr/ft/N/N68081.pdf Disociación suave de células por Accutase
Ver también
- La quimotripsina y carboxipeptidasa A, dos proteasas pancreáticas activadas por tripsina.
