Reacción de Bingel
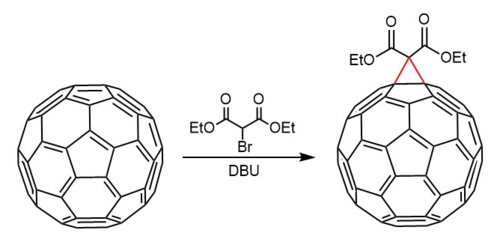
En la química del fullereno , la reacción de Bingel es una reacción de ciclopropanación de fullereno , formando un metanofulleno . Fue descrito por primera vez en 1993 por el químico alemán Carsten Bingel, con un reactivo derivado bromado de malonato de dietilo en presencia de una base fuerte como el hidruro de sodio o DBU . La reacción tiene lugar preferiblemente en los dobles enlaces más cortos en las uniones de dos hexágonos (6-6 enlaces), siendo la fuerza impulsora la liberación de la restricción estérica .
La reacción es importante porque permite introducir útiles extensiones en las esferas de fullereno. Estas extensiones modifican sus propiedades, por ejemplo, la solubilidad y el comportamiento electroquímico y, por lo tanto, amplían la gama de aplicaciones técnicas potenciales.
Mecanismo de reacción
El mecanismo de esta reacción es el siguiente: una base arranca el protón ácido del malonato generando un carbanión o un enolato que reacciona con el doble enlace del fullereno deficiente en electrones mediante una adición nucleofílica . Esto a su vez genera un carbanión que desplaza el bromo mediante una sustitución de nucleófilo alifático en un cierre de anillo de ciclopropano intramolecular .
Campo de aplicación
La reacción de Bingel es un método popular en la química del fullereno. El malonato (funcionalizado con un átomo de halógeno) a menudo se produce in situ utilizando una mezcla de base y tetrabromometano o yodo . También se ha observado que la reacción ocurre reemplazando grupos éster con grupos alquino en dialquinilmetanofullerenos .
Una alternativa a la reacción de Bingel es una reacción de fullereno con diazometano . Los ésteres de N- (difenilmetilen) glicina reaccionan en la reacción de Bingel de una manera similar pero diferente, produciendo fullereno dihidropirrol .
Comentarios-Bingel
Existen protocolos para la eliminación del grupo metano mediante reducción electrolítica o la acción del magnesio amalgamado.
Notas y referencias
- (fr) Este artículo está tomado parcial o totalmente del artículo de Wikipedia en inglés titulado " Reacción de Bingel " ( ver la lista de autores ) .
- Bingel, Carsten, " Cyclopropanierung von Fullerenen ", Chemische Berichte , vol. 126, n o 8,1993, p. 1957 ( DOI 10.1002 / cber.19931260829 )
- Yosuke Nakamura, Masato Suzuki, Yumi Imai y Jun Nishimura, “ 16 ”, Org. Letón. , vol. 6, n o 16,2004, p. 2797–2799 ( PMID 15281772 , DOI 10.1021 / ol048952n )
- Graham E. Ball, Glenn A. Burley, Leila Chaker, Bill C. Hawkins, James R. Williams, Paul A. Keller y Stephen G. Pyne, " Reasignación estructural de los productos de adición mono y bis de las reacciones de adición de ésteres de glicinato de N- (difenilmetileno) a [60] fullereno en condiciones Bingel ”, J. Org. Chem. , vol. 70, n o 21,2005, p. 8572–8574 ( PMID 16209611 , DOI 10.1021 / jo051282u )
- Roland Kessinger , Jeanne Crassous , Andreas Herrmann , Markus Rüttimann , Luis Echegoyen y François Diederich , " Preparación de C76 enantioméricamente puro con un método electroquímico general para la eliminación de puentes de di (alcoxicarbonil) metano de metanofullerenos: la reacción retro-Bingel " Angewandte Chemie International Edition , vol. 37, núms . 13-14,1998, p. 1919 ( DOI 10.1002 / (SICI) 1521-3773 (19980803) 37: 13/14 <1919 :: AID-ANIE1919> 3.0.CO; 2-X )
- M. ÁNgeles Herranz , Charles T. Cox y Luis Echegoyen , “ Reacciones de retrociclopropanación de fullerenos: análisis completos de productos ”, The Journal of Organic Chemistry , vol. 68, n o 12,2003, p. 5009–12 ( PMID 12790625 , DOI 10.1021 / jo034102u )
- Nicolle NP Moonen , Carlo Thilgen , François Diederich y Luis Echegoyen , " La reacción química retro-Bingel: eliminación selectiva de los sumandos de bis (alcoxicarbonil) metano de C60 y C70 con magnesio amalgamado ", Chemical Communications , n o 5,2000, p. 335 ( DOI 10.1039 / a909704j )