Yodometano
| Yodometano | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Estructura del yodometano |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificación | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre IUPAC | yoduro de metilo | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinónimos |
Yoduro de metilo monoyodometano |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.745 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 200-819-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sonrisas |
CI , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / CH3I / c1-2 / h1H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | líquido incoloro con un olor característico. se vuelve marrón al exponerse a la luz y la humedad. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades químicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fórmula bruta |
C H 3 I [isómeros] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa molar | 141,939 ± 0,001 g / mol C 8,46%, H 2,13%, I 89,41%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Momento dipolar | 1,59 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusión | −66,5 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° hirviendo | 42,5 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilidad | en agua a 20 ° C : 14 g · l -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parámetro de solubilidad δ | 9,9 cal 1/2 · cm -3/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad | 2,3 g · cm -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura de autoignición | 352 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Límites explosivos en el aire | 8,5 - 66% | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presión de vapor saturante | a 20 ° C : 50 kPa , 24,09 psi a 55 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto crítico | 65,9 bares , 254,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termoquímica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades electronicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re energía de ionización | 9.538 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades ópticas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Índice de refracción | 1,5304 ( 20 ° C , D) 1,5293 ( 21 ° C , D) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauciones | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Peligro H301, H312, H315, H331, H335, H351, H301 : Tóxico en caso de ingestión H312 : Nocivo en contacto con la piel H315 : Provoca irritación cutánea H331 : Tóxico en caso de inhalación H335 : Puede irritar el tracto respiratorio H351 : Se sospecha que provoca cáncer (indicar la vía de exposición si se ha demostrado formalmente que no existe otra vía de exposición conduce al mismo peligro) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Producto no clasificadoLa clasificación de este producto aún no ha sido validada por la divulgación del servicio de directorio toxicológico al 0,1% según la lista de divulgación de ingredientes. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transporte | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2644 : YODURO DE METILO |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Clasificación IARC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo 3 : No clasificable en cuanto a su carcinogenicidad para los seres humanos. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotoxicología | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 1,51-1,69 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unidades de SI y STP a menos que se indique lo contrario. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El yodometano , también conocido como yoduro de metilo , es un compuesto químico de fórmula CH 3 I, a veces señaló MeI. Es un haloalcano , derivado del metano , donde uno de los átomos de hidrógeno ha sido sustituido por un átomo de yodo . Se presenta en forma de líquido incoloro, denso, volátil y de olor etéreo, que adquiere una tez violácea cuando se expone a la luz debido a la presencia del diodo I 2 .. El yodometano se usa comúnmente en síntesis orgánica como donante de grupos metilo , en reacciones llamadas metilaciones . El arroz lo emite naturalmente en pequeñas cantidades .
El yodometano se hidroliza a 270 ° C , formando yoduro de hidrógeno , monóxido de carbono y dióxido de carbono .
Usos
Reacciones de metilación
El yodometano se utiliza principalmente para la metilación de otros compuestos, mediante reacciones de tipo S N 2 . Puede ser atacado estéricamente fácilmente por nucleófilos y el yoduro es un buen nucleófugo .
Se puede utilizar, por ejemplo, para la metilación de ácidos carboxílicos (transformación en metanoato de carboxilo ) o fenoles (formación de metoxibencenos):

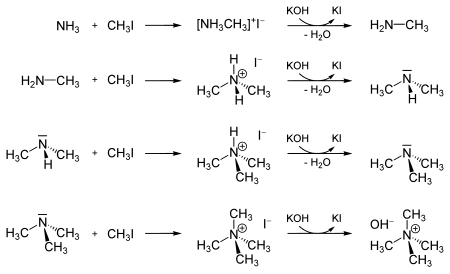
También se puede utilizar para la metilación de amoníaco y aminas derivadas a yodoamonio. Esta reacción puede continuar hasta la formación de un hidróxido de tetrametilamonio.
El yodometano también es un precursor del yoduro de metilmagnesio o "MeMgI", un reactivo de Grignard que se utiliza a menudo en la síntesis orgánica . MeMgI se forma con bastante facilidad, por lo que se utiliza con bastante frecuencia como ejemplo para enseñar la preparación de estos reactivos. Sin embargo, el uso de MeMgI ha sido reemplazado por el uso de metil-litio .
En el proceso de Monsanto , MeI se forma in situ mediante la reacción de metanol y yoduro de hidrógeno . Luego reacciona con monóxido de carbono en presencia de rodio para formar yoduro de etanoilo , un precursor del ácido acético (obtenido por hidrólisis ). Gran parte del ácido acético producido en el mundo se produce mediante este método.
Otro
Además de su uso como agente metilante, algunos proponen utilizar el yodometano como fungicida , herbicida , insecticida , nematicida o incluso en extintores . Puede utilizarse como desinfectante de suelos, sustituyendo al bromometano (cuyo uso ha sido prohibido por el Protocolo de Montreal ), y en microscopía por sus propiedades ligadas a su índice de refracción.
Producción y síntesis
El yodometano se puede sintetizar mediante una reacción exotérmica, mediante la reacción del yodo con metanol en presencia de fósforo . A continuación, el diidodo se transforma in situ en triyoduro de fósforo . Sigue una sustitución nucleofílica con metanol:
Otro método consiste en hacer reaccionar dimetilsulfato con yoduro de potasio en presencia de carbonato de calcio :
A continuación, se puede obtener yodometano por destilación después de lavar con tiosulfato de sodio para eliminar el exceso de yodo.
El yodometano también se puede producir en accidentes nucleares haciendo reaccionar compuestos orgánicos con "yodo de fusión".
Elección del yodometano como agente metilante
El yodometano es un excelente agente de metilación, pero tiene algunos inconvenientes. Además de su toxicidad ; comparado con otros halogenometanos ( especialmente clorometano ) su peso equivalente es mayor: un mol de MeI pesa casi tres veces más que un mol de MeCl. Sin embargo, el clorometano es un gas (como el bromometano ), lo que hace que su uso sea más delicado que el yodometano, que es un líquido. El clorometano es un agente metilante mucho más débil que el MeI, pero es suficiente en la mayoría de las reacciones.
Los yoduros son generalmente mucho más caros que sus equivalentes de cloruro o bromuro, pero el yodometano asequible no lo es. A escala comercial , se prefiere el dimetilsulfato , aunque tóxico, porque es barato y líquido.
Durante las reacciones de sustituciones nucleofílicas, la salida del grupo saliente, I - puede causar reacciones secundarias , porque es un nucleófilo poderoso . Finalmente, debido a su alta reactividad, el MeI es más peligroso para el personal que lo manipula que sus equivalentes bromados y clorados.
Toxicidad y efectos biológicos
El yodometano a DL 50 por administración oral de 76 mg · kg -1 para ratas, y en el hígado, se convierte rápidamente en S-metil glutatión . En los Estados Unidos, el yodometano se considera potencialmente cancerígeno según la clasificación de ACGIH (en) , NTP y EPA . La IARC lo clasifica en el grupo 3 ("inclasificable en cuanto a su carcinogenicidad para los seres humanos").
La inhalación de vapores de yodometano puede dañar los pulmones, el hígado, los riñones y el sistema nervioso. Provoca náuseas, mareos, tos y vómitos. El contacto prolongado con la piel provoca quemaduras. La inhalación masiva puede causar edema pulmonar .
Notas y referencias
- (fr) Este artículo está tomado parcial o totalmente del artículo de Wikipedia en inglés titulado " Yoduro de metilo " ( consulte la lista de autores ) .
- METIL IODIDE , hoja de seguridad (s) del Programa Internacional de Seguridad Química , consultado el 9 de mayo de 2009.
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- (en) Nicholas P. Chopey, Manual de cálculos de ingeniería química , McGraw-Hill,2004, 3 e ed. , 800 p. ( ISBN 978-0-07-136262-7 ) , pág. 1,43.
- (en) " Propiedades de varios gases " en flexwareinc.com (consultado el 12 de abril de 2010 ) .
- (en) Carl L. Yaws, Manual de diagramas termodinámicos: compuestos y elementos inorgánicos , vol. 1, 2 y 3, Huston, Texas, Gulf Pub. Co.,1996, 384 p. ( ISBN 0-88415-857-8 , 0-88415-858-6 y 0-88415-859-4 ).
- (en) David R. Lide, Manual de química y física , Boca Raton, CRC,2008, 89 ª ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , pág. 10-205.
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans , " Evaluations Globales de la Carcinogenicité pour l'Homme, Groupe 3 : Inclassables as to their carcinogenicity to Humans " , en http://monographs.iarc.fr , IARC,16 de enero de 2009(consultado el 22 de agosto de 2009 ) .
- Número de índice en la Tabla 3.1 del Anexo VI del Reglamento CE n o 1272/2008 (16 de diciembre de 2008).
- " Yodometano " en la base de datos de sustancias químicas Reptox de la CSST (organización de Quebec responsable de la seguridad y salud en el trabajo), consultado el 25 de abril de 2009.
- (en) KR Redeker, NY Wang, JC Low, A. McMillan, SC Tyler y RJ Cicerone, " Emisiones de haluros de metilo y metano de los arrozales " , Science , vol. 290,2000, p. 966–969 ( PMID 11062125 , DOI 10.1126 / science.290.5493.966 ).
- (en) CS Rey, WW Hartman: yoduro de metilo . En: Organic Synthesis , 1943, 2, S. 399 ( artículo ).
- (en) Johnson, K., " Metabolismo del yodometano en la rata " , Biochem J. , vol. 98,1966, p. 38–43.
Bibliografía
- Adams, RE, Browning Jr, WE, Cottrell, WB y Parker, GW (1965) La liberación y adsorción de yoduro de metilo en el accidente máximo creíble HFIR (No. ORNL-TM-1291) . Laboratorio Nacional Oak Ridge Laboratorio Nacional Oak Ridge. , Tenn.





