Ciclohexano
| ciclohexano | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
    Diferentes representaciones de una molécula de ciclohexano. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificación | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre IUPAC | ciclohexano | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100,003,461 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 203-806-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB03561 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 8078 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CHEBI | 29005 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sonrisas |
C1CCCCC1 , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C6H12 / c1-2-4-6-5-3-1 / h1-6H2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | líquido incoloro | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades químicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fórmula bruta |
C 6 H 12 [Isómeros] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa molar | 84.1595 ± 0.0056 g / mol C 85.63%, H 14.37%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Susceptibilidad magnética | 68,1 × 10 -6 cm 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusión | 6,47 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° hirviendo | 80,75 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilidad | en agua: ninguno; suelo. en alcohol , éter , acetona ; |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parámetro de solubilidad δ | 16,8 MPa 1/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad |
0,7786 g · cm -3 ( 25 ° C )
ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura de autoignición | 260 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto de inflamabilidad | −18 ° C (vaso cerrado) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Límites explosivos en el aire | 1,3 - 8,4 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
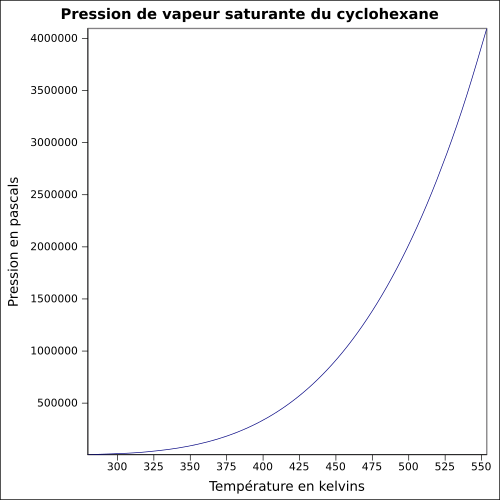
| Presión de vapor saturante | a 20 ° C : 12,7 kPa
ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Viscosidad dinámica | 0,98 mPa · s a 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto crítico | 280,3 ° C , 40,7 bares | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido | 1280 m · s -1 a 19 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termoquímica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vapor H ° | 3,6 x 10 5 J · kg-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
ecuación:
ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 3919,6 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades ópticas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Índice de refracción | 1.42662 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauciones | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
    Peligro H225, H304, H315, H336, H410, H225 : Liquide et vapeurs très inflammables H304 : Peut être mortel en cas d'ingestion et de pénétration dans les voies respiratoires H315 : Provoque une irritation cutanée H336 : Peut provoquer somnolence ou vertiges H410 : Très toxique pour les organismes aquatiques, entraîne des effets à A largo plazo |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  B2, D2B, B2 : Inflamable flash de líquido punto = -18 ° C taza Setaflash cerrado método D2B : Material tóxico que causa otros efectos tóxicos irritación de la piel en los animales 1,0% divulgación de acuerdo a la lista de divulgación ingrediente |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 1 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transporte | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
33 : sustancia líquida altamente inflamable (punto de inflamación por debajo de 21 ° C ) Número ONU : 1145 : CICLOHEXANO Clase: 3 Etiqueta: 3 : Líquidos inflamables Embalaje: Grupo de embalaje II : sustancias moderadamente peligrosas;  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotoxicología | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | 930 - 1.36 mil mg · kg -1 (ratas, oral) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 3,44 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Umbral de olor | bajo: 0,52 ppm alto: 784 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unidades de SI y STP a menos que se indique lo contrario. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El ciclohexano es un hidrocarburo alicíclico no etileno de la familia de los (mono) cicloalcanos de fórmula C 6 H 12 en bruto . El ciclohexano se utiliza como disolvente apolar en la industria química, pero también como reactivo para la producción industrial de ácido adípico y caprolactama , intermedios utilizados en la producción de nailon . La fórmula esquelética del ciclohexano se muestra al lado.
Producción
Resúmenes históricos
A diferencia de otros hidrocarburos, el ciclohexano no se encuentra en la naturaleza. Por tanto, varios químicos han intentado sintetizarlo:
- En 1867, Marcelin Berthelot procede a la reducción de benceno mediante ácido yodhídrico a temperatura elevada. Nombra su producto hexahidrobenceno, pensando que lo ha sintetizado. En 1870, Adolf von Baeyer repitió esta reacción y obtuvo el mismo producto.
- En 1890, Vladimir Markovnikov pensó que podría obtener el mismo producto destilando petróleo del Cáucaso. Él nombra su producto final hexanafteno.
Sin embargo, ambos productos tienen un punto de ebullición de aproximadamente 10 ° C más alto que el hexahidrobenceno y el hexanafteno tabulados. La inconsistencia fue resuelta en 1895 por V. Markovnikov , N. Kischner (en) y N. Zelinsky quienes demuestran que los productos obtenidos tienen una estructura tipo metilciclopropano, obtenida por una reacción de transposición inesperada .
No fue hasta 1894 que Baeyer sintetizó por primera vez mediante ciclohexano Dieckmann la condensación del ácido pimélico , seguida de múltiples etapas de reducción .

El mismo año, E. Haworth y WH Perkin Jr. (en) sintetizaron ciclohexano llevando a cabo una reacción de Wurtz con 1,6-dibromohexano .

Síntesis actual
En la actualidad, el ciclohexano se produce a escala industrial mediante la hidrogenación de benceno catalizada por níquel Raney . La producción de ciclohexano corresponde aproximadamente al 10% de las necesidades mundiales anuales de benceno . La reacción llevada a cabo a alta temperatura, entonces es altamente exotérmica con ΔH (500 K) = -216,37 kJ / mol. La reacción de deshidrogenación solo es significativa a partir de 300 ° C , lo que refleja una entropía de reacción negativa para la reacción de hidrogenación.

Usos
Como hidrocarburo, el ciclohexano es una molécula poco reactiva. Sin embargo, la gran mayoría del ciclohexano se usa para oxidar catalíticamente a ciclohexanol y ciclohexanona . Estos dos compuestos se utilizan respectivamente en la producción de ácido adípico , utilizado como materia prima para la fabricación de nailon-6,6 , y en la producción de caprolactama , un precursor del nailon-6 . Cada año se producen varios miles de toneladas de ciclohexanol y ciclohexanona .
El ciclohexano también se utiliza como disolvente orgánico apolar, aunque hoy en día se tiende a preferir el n-hexano . A menudo se utiliza como disolvente de recristalización porque muchos compuestos orgánicos son solubles en caliente en ciclohexano pero no en frío.
El ciclohexano también se usa para calibrar instrumentos de calorimetría diferencial de barrido debido a su cambio de fase cristalina neto a 186 K. Los vapores de ciclohexano también se usan en equipos de plantas de tratamiento térmico.
Geometría
Enfoque histórico
En 1890, Hermann Sachse (de) , un asistente de Berlín de 28 años, publicó instrucciones para doblar una hoja de papel para representar dos formas de ciclohexano, que llamó "simétrico" y "antisimétrico" (hoy llamado silla y bote). . Entiende que para cada forma, hay dos posiciones distintas para los átomos de hidrógeno (ahora llamados axiales y ecuatoriales), que dos formas "simétricas" pueden interconvertirse e incluso cómo ciertos sustituyentes pueden favorecer una forma u otra. ( Sachse-Mohr teoría (de) ). Desafortunadamente, expresa todos sus hallazgos en lenguaje matemático y pocos químicos lo entienden. Murió en 1893 sin que sus ideas pudieran desarrollarse.
En 1918, Ernst Mohr (de) se hizo cargo del trabajo de Sachse. Estudia todos los cicloalcanos para ampliar su teoría. En particular, predice que existen dos formas estables de la misma energía para la decalina , lo que será confirmado por Walter Hückel (de) en 1925. Mohr también tendrá la idea de que la difracción de rayos X podría permitir validar su teoría, pero la técnica es demasiado nueva para ser utilizada de manera confiable.
No fue hasta 1943 que Odd Hassel pudo demostrar la existencia de estas dos conformaciones y de las dos posiciones no equivalentes para los átomos de hidrógeno mediante el estudio de los vapores del ciclohexano por difracción de electrones .
Principales conformaciones del ciclohexano.
Dado que muchos compuestos tienen una estructura de anillo de 6 miembros, la estructura y la dinámica del ciclohexano son prototipos importantes. Los ángulos de un hexágono plano regular miden 120 °. Sin embargo, el ángulo formado por dos enlaces sucesivos en una cadena de carbono es de aproximadamente 109 ° según la teoría VSEPR . Por lo tanto, la molécula de ciclohexano no es plana para minimizar el estrés del ciclo.
La conformación predominante del ciclohexano a temperatura ambiente se denomina conformación de silla. Más del 99% de las moléculas de ciclohexano en solución adoptan esta conformación a 25 ° C. Todos los átomos de carbono son equivalentes allí y hay dos posiciones distintas para los átomos de hidrógeno: un átomo de hidrógeno que pertenece al plano medio del ciclo se dice que está en la posición ecuatorial, mientras que un átomo de hidrógeno que no pertenece a este plano es se dice que está en la posición axial. Por tanto, cada átomo de carbono está unido a un átomo de hidrógeno en la posición axial y a otro en la posición ecuatorial. Los sucesivos enlaces carbono-hidrógeno se desplazan, lo que minimiza la tensión de torsión del anillo.
La segunda conformación estable de la molécula de ciclohexano es la conformación de bote giratorio . Si la proporción de moléculas de ciclohexano en esta conformación es solo de aproximadamente 0,1% a 25 ° C, alcanza el 30% a 800 ° C. El enfriamiento repentino de la muestra permite entonces "congelar" la conformación de las diferentes moléculas. La conformación de bote retorcido es menos estable que la conformación de silla y, por lo tanto, es poco común en la naturaleza. Podemos señalar el caso del twistane , un isómero sintético del adamantano , todos los ciclohexanos de los cuales están en conformación de bote retorcido.
Inversión de la conformación de la silla
En realidad, hay dos conformaciones de silla diferentes, y la molécula de ciclohexano puede cambiar su conformación de equilibrio entre estas dos formas. Los átomos de hidrógeno en la posición axial en una conformación de silla se encuentran en la posición ecuatorial en la otra y viceversa. Estas dos conformaciones de silla están en rápido equilibrio a temperatura ambiente y, por lo tanto, son indistinguibles por RMN de protones a 25 ° C. El mecanismo detallado de la inversión de la conformación de la silla ha sido objeto de mucho estudio y debate, pero se conoce hoy en día.
También se conoce el perfil de energía de la inversión de la conformación de la silla. La conformación de media silla es el estado de transición que permite alcanzar la primera conformación de bote retorcido, y la conformación de bote es el estado de transición entre las dos conformaciones de bote retorcido. La energía de activación de la inversión de la conformación de la silla es 43 kJ / mol, que es menor que la energía de agitación térmica a 25 ° C: es por eso que las dos conformaciones de la silla están en equilibrio a temperatura ambiente.
Conformación mayoritaria de derivados de ciclohexano sustituidos
Derivados monosustituidosLas dos conformaciones de silla del ciclohexano tienen la misma energía. Por otro lado, si un átomo de hidrógeno es reemplazado por un sustituyente, estas dos conformaciones ya no tienen la misma energía. En una conformación de silla, el sustituyente está en la posición axial, mientras que en la otra está en la posición ecuatorial. En la posición axial, el sustituyente causa malestar estérico con los otros dos átomos de hidrógeno en la posición axial: estas interacciones se denominan interacciones 1,3-diaxiales. En la posición ecuatorial, estas interacciones no existen: por lo tanto, es la conformación de silla para la que el sustituyente está en la posición ecuatorial la que es de menor energía. La diferencia de entalpía libre entre estas dos conformaciones de silla se llama factor A y depende en gran medida del sustituyente. El valor de A varía desde casi cero para sustituyentes pequeños como el deuterio hasta aproximadamente 21 kJ / mol para sustituyentes grandes como el grupo terc-butilo.
Derivados disustituidosConsidere que los dos sustituyentes están en la posición relativa 1, 2 o 1, 4. Si están en configuración cis , las dos conformaciones de silla tienen un grupo en posición axial y otro en posición ecuatorial: las dos conformaciones de silla son entonces de la misma energía. Por otro lado, si los dos sustituyentes están en la configuración trans , solo la conformación de silla que tiene los dos grupos en la posición ecuatorial puede existir de manera significativa, porque las fuertes interacciones 1,3-diaxiales impiden que los dos grupos estén en la posición axial. simultaneamente.
Considere que los dos sustituyentes están ahora en la posición relativa 1,3. Si están en la configuración cis , el caso es similar a la configuración trans para los sustituyentes en la posición relativa 1, 2 o 1, 4. Por el contrario, si están en la configuración trans , el caso es similar a la configuración cis para los sustituyentes en la posición relativa 1, 2 o 1, 4.
Si los sustituyentes son muy voluminosos, la conformación de la silla puede no ser la más estable: en el caso del cis -1,4-di-terc-butilciclohexano, la conformación de bote retorcido permite colocar los dos grupos en una posición más favorable. que para la conformación de silla, para la cual un grupo terc-butilo está en una posición axial. Por tanto, se midió por RMN que la conformación de bote retorcido era más estable en 0,47 kJ / mol a 125 K que la conformación de silla.
Análogos heterocíclicos
Los análogos heterocíclicos del ciclohexano son ubicuos en el campo de los azúcares , piperidinas o dioxanos, entre otros. La conformación de silla es generalmente la más estable, pero los valores del factor A varían mucho cuando se reemplaza un grupo metileno con un átomo de oxígeno o nitrógeno, como lo demuestra el efecto anomérico . También podemos observar ciertos análogos heterocíclicos como el 1,2,4,5-tetratiano (SCH 2 S) 2 para los cuales no existen interacciones 1,3-diaxiales: muchas más moléculas están entonces en conformación de bote retorcido. Para su análogo tetrametil, 3,3,6,6-tetrametil-1,2,4,5-tetrathian, la conformación de bote retorcido es la conformación predominante.
Toxicidad y riesgos
Toxicidad
Debido a la toxicidad del ciclohexano, existen valores límite de exposición para proteger a las personas que trabajan con este compuesto:
- entre 300 y 375 ppm en Francia, dependiendo de la duración de la exposición,
- 200 ppm en Alemania,
- 100 ppm en los Estados Unidos.
Inflamabilidad
El ciclohexano es muy inflamable. Una fuga de ciclohexano en una fábrica del Reino Unido en Flixborough provocó una explosión en 1974, matando a 28 personas que trabajaban en el sitio.
Notas y referencias
- ciclohexano , hoja de seguridad de datos (s) del Programa Internacional para la Seguridad de Sustancias Químicas , consultado el 9 de mayo, 2009
- (En) Hyp Daubensee J., Jr. , James D. Wilson y John L. Laity, " Exaltación de susceptibilidad diamagnética en hidrocarburos " , Revista de la Sociedad Química Estadounidense , vol. 91, n o 8,9 de abril de 1968, p. 1991-1998
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- "Ciclohexano" en las sustancias peligrosas Banco de Datos , visitada 05 de mayo 2010
- (en) Iwona Owczarek y Krystyna Blazej, " temperaturas críticas recomendados. Parte II. Hidrocarburos aromáticos y cíclicos ” , J. Phys. Chem. Árbitro. Datos , vol. 33, n o 230 de abril de 2004, p. 541 ( DOI 10.1063 / 1.1647147 )
- (en) James E. Mark, Manual de propiedades físicas del polímero , Springer,2007, 2 nd ed. , 1076 p. ( ISBN 978-0-387-69002-5 y 0-387-69002-6 , leer en línea ) , pág. 294
- (en) JG Speight, Norbert Adolph Lange, Manual de química de Lange , Nueva York, McGraw-Hill ,2005, 16 ª ed. , 1623 p. ( ISBN 978-0-07-143220-7 , LCCN 84643191 ) , pág. 2,289
- (en) Robert H. Perry y Donald W. verde , de Perry Ingenieros Químicos Handbook , EE.UU., McGraw-Hill ,1997, 7 ª ed. , 2400 p. ( ISBN 978-0-07-049841-9 , LCCN 96051648 ) , pág. 2-50
- " Propiedades de varios gases " en flexwareinc.com (consultado el 12 de abril de 2010 )
- (en) William M. Haynes , Manual CRC de Química y Física , Boca Raton, CRC Press / Taylor y Francis,1 er de julio de 2010, 91 ª ed. , 2610 p. ( ISBN 9781439820773 , presentación en línea ) , p. 14-40
- (en) Carl L. Yaws, Manual de diagramas termodinámicos: compuestos orgánicos C5 a C7 , vol. 2, Huston, Texas, Pub del Golfo. Co.,1996, 400 p. ( ISBN 978-0-88415-858-5 , LCCN 96036328 )
- Número de índice en la tabla 3.1 del apéndice VI del reglamento CE No. 1272/2008 (16 de diciembre de 2008)
- " Ciclohexano " en la base de datos de productos químicos Reptox de la CSST (organización de Quebec responsable de la seguridad y salud ocupacional), consultado el 24 de abril de 2009
- ciclohexano en ChemIDplus
- " El ciclohexano, " en hazmap.nlm.nih.gov (visitada 14 de noviembre de, 2009 )
- M. Piraux, Química orgánica estática , Office international de librairie, Bruselas, p. 35 ( ISBN 978-2-87343-001-6 )
- (en) EW Warnhoff , " Las historias curiosamente entrelazadas del benceno y el ciclohexano " , Journal of Chemical Education , vol. 73, n o 6,Junio de 1996, p. 494 ( ISSN 0021-9584 y 1938-1328 , DOI 10.1021 / ed073p494 , leído en línea , consultado el 19 de abril de 2020 )
- Bertholet (1867) "Nuevas aplicaciones de métodos de reducción en química orgánica" , Boletín de la Sociedad Química de París , serie 2, 7 : 53-65.
- Bertholet (1868) "Método universal para reducir y saturar compuestos orgánicos con hidrógeno", Bulletin de la Société Chimique de Paris , serie 2, 9 : 8-31
- Adolf Baeyer (1870) "Ueber die Reduction aromatischer Kohlenwasserstoffe durch Jodphosphonium" (Sobre la reducción de compuestos aromáticos por yoduro de fosfonio [H 4 IP]), Annalen der Chemie und Pharmacie , 155 : 266-281
- Fred Fan Zhang, Thomas van Rijnman, Ji Soo Kim, Allen Cheng "Sobre los métodos actuales de hidrogenación de compuestos aromáticos, 1945 hasta la actualidad" Lunds Tekniska Högskola 2008
- Ceresana, " Benzene - Study: Market, Analysis, Trends 2021 - Ceresana " [ archivo de 21 de diciembre de 2017] , en www.ceresana.com (consultado el 4 de mayo de 2018 )
- (en) Michael Tuttle Musser , "El ciclohexanol y ciclohexanona" en Enciclopedia de Química Industrial de Ullmann , Wiley-VCH Verlag GmbH & Co. KGaA,15 de junio de 2000( ISBN 978-3-527-30673-2 , DOI 10.1002 / 14356007.a08_217 , leer en línea ) , a08_217
- (en) DM Price, " Calibración de temperatura de calorímetros de barrido diferencial " , Journal of Thermal Analysis , vol. 45, n o 6,1995, p. 1285–1296 ( DOI 10.1007 / BF02547423 )
- Esta historia se resume aquí: https://web.archive.org/web/20120228222221/https://webspace.yale.edu/chem125/125/history99/6Stereochemistry/Baeyer/Sachse.html Archivado el 28/02/2012 en Wayback Machine
- (en) " Odd Hassel - Biographical " en nobelprize.org (consultado el 20 de abril de 2020 )
- (en) Gurvinder Gill , Sr. Diwakar Pawar y Eric A. Noe , " Estudio conformacional de cis-1,4-Di-terc-butilciclohexano por espectroscopia de RMN dinámica y métodos computacionales. Observación de las conformaciones de sillas y botes giratorios ” , The Journal of Organic Chemistry , vol. 70, n o 26,diciembre de 2005, p. 10726–10731 ( ISSN 0022-3263 y 1520-6904 , DOI 10.1021 / jo051654z , leer en línea , consultado el 20 de abril de 2020 )
- INRS, hoja toxicológico n ° 17, cuadernos Documental - salud ocupacional y seguridad - N o 190, 1 st trimestre 2003
- Ministerio encargado del medio ambiente - DPPR / SEI / BARPI N o 5611










