Óxido de propileno
| Óxido de propileno | |||
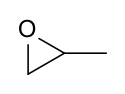 Estructura del óxido de propileno |
|||
| Identificación | |||
|---|---|---|---|
| Nombre IUPAC | metiloxirano | ||
| Sinónimos |
1,2-epoxipropano |
||
| N o CAS |
(RS) (R) - (+) (S) - (-) |
||
| N o ECHA | 100.000.800 | ||
| N o EC | 200-879-2 | ||
| PubChem | 6378 | ||
| CHEBI | 38685 | ||
| Sonrisas |
CC1CO1 , |
||
| InChI |
Std. InChI: InChI = 1S / C3H6O / c1-3-2-4-3 / h3H, 2H2,1H3 Std. InChIKey: GOOHAUXETOMSMM-UHFFFAOYSA-N |
||
| Apariencia | líquido incoloro con olor a éter | ||
| Propiedades químicas | |||
| Fórmula bruta |
C 3 H 6 O [isómeros] |
||
| Masa molar | 58.0791 ± 0.0031 g / mol C 62.04%, H 10.41%, O 27.55%, |
||
| Propiedades físicas | |||
| T ° fusión | −112 ° C | ||
| T ° hirviendo | 34,4 ° C | ||
| Solubilidad | 680 g · l -1 hasta 20 ° C | ||
| Densidad | 0,83 g · cm -3 | ||
| Temperatura de autoignición | 430 ° C | ||
| punto de inflamabilidad | −37 ° C | ||
| Punto crítico |
209,1 C , 4,91 MPa |
||
| Precauciones | |||
| SGH | |||
   Peligro H224, H302, H312, H315, H319, H332, H335, H340, H350, P201, P210, P261, P305 + P351 + P338, P308 + P313, H224 : Líquido y vapores extremadamente inflamables H302 : Nocivo en caso de ingestión H312 : Nocivo en contacto con la piel H315 : Provoca irritación cutánea H319 : Provoca irritación ocular grave H332 : Nocivo en caso de inhalación H335 : Puede irritar el sistema respiratorio H340 : Puede inducir anomalías genéticas (indicar vía de exposición si se demuestra de manera concluyente que ninguna otra vía de exposición conduce al mismo peligro) H350 : Puede causar cáncer (indicar la vía de exposición si se ha demostrado de manera concluyente que ninguna otra vía de exposición conduce al mismo peligro) P201 : Obtener instrucciones especiales antes de su uso. P210 : Mantener alejado de fuentes de calor, chispas, llama abierta o superficies calientes. - No fumar. P261 : Evite respirar el polvo / humo / gas / niebla / vapores / aerosoles. P305 + P351 + P338 : En caso de contacto con los ojos: Enjuagar cuidadosamente con agua durante varios minutos. Quítese los lentes de contacto si la víctima los está usando y se pueden quitar fácilmente. Continúe enjuagando. P308 + P313 : En caso de exposición probada o sospechada: consulte con un médico. |
|||
| Transporte | |||
33 : líquido muy inflamable (punto de inflamación inferior a 21 ° C ) Número ONU : 1280 : ÓXIDO DE PROPILENO Clase: 3 Etiqueta: 3 : Líquidos inflamables Embalaje: Grupo de embalaje I : sustancias muy peligrosas;  |
|||
| Clasificación IARC | |||
| grupo 2B : posiblemente cancerígeno para los seres humanos | |||
| Unidades de SI y STP a menos que se indique lo contrario. | |||
El óxido de propileno o 1,2-epoxipropano , es un compuesto químico de fórmula CH 3 CHCH 2 O. Se presenta en forma de líquido combustible incoloro, muy volátil con olor a éter y capaz de formar mezclas explosivas con el aire. Es un epóxido quiral generalmente utilizado en forma racémica . Se utiliza principalmente para producir polioles para la fabricación de poliuretanos . Tiene un isómero , oxetano , cuyo anillo contiene cuatro átomos , no tres.
Estereoquímica
El átomo de carbono que lleva el sustituyente metilo es quiral . Por tanto, el 1,2-epoxipropano existe en forma de dos enantiómeros:
- ( R ) - (+) - 1,2-epoxipropano de número CAS
- ( S ) - (-) - 1,2-epoxipropano de número CAS
Producción
La producción industrial de óxido de propileno comienza a partir de propileno CH 3 –CH = CH 2. Se utilizan dos enfoques principales, el primero por hidrocloración y el segundo por oxidación.
La ruta tradicional de hidrocloración implica la conversión de propileno en 1-cloro-2-propanol CH 3 –CHOH - CH 2 Cly 2-cloro-1-propanol CH 3 –CHCl - CH 2 OH :
2 CH 3 –CH = CH 2+ Cl 2+ H 2 O→ CH 3 –CHOH - CH 2 Cl+ CH 3 –CHCl - CH 2 OH.Esta mezcla de cloropropanoles luego se deshidroclora, por ejemplo:
CH 3 –CHOH - CH 2 Cl+ OH - → CH 3 C 2 H 3 O+ Cl - + H 2 O.La cal se utiliza a menudo para absorber Cl - cloruro de iones .
La otra ruta principal de síntesis de óxido de propileno es a través de la co-oxidación de etilbenceno C 6 H 5 CH 2 CH 3e isobutano HC (CH 3 ) 3. En presencia de catalizadores , la oxidación por aire se desarrolla de la siguiente manera:
CH 3 –CH = CH 2+ C 6 H 5 –CH 2 –CH 3+ O 2→ CH 3 C 2 H 3 O+ C 6 H 5 –CH = CH 2+ H 2 O.Los coproductos de estas reacciones, ya sea estireno C 6 H 5 –CH = CH 2o terc- butanol HOC (CH 3 ) 3, son materias primas importantes para otras reacciones. Por ejemplo, el terc- butanol puede reaccionar con metanol CH 3 OHpara dar metil terc-butil éter CH 3 OC (CH 3 ) 3(MTBE), un aditivo para combustibles de automoción : antes de la restricción actualmente impuesta al uso de MTBE en combustibles por los riesgos ecológicos que plantea, la ruta sintética por propileno e isobutano era una de las más importantes.
Un proceso alternativo que comienza con cumeno C 6 H 5 CH (CH 3 ) 2fue puesto en producción por Sumitomo Chemical enabril de 2003. Esta es una adaptación del proceso por co-oxidación usando hidroperóxido de cumeno en lugar de hidroperóxido de etilbenceno y reciclando el α-hidroxicumeno coproducido en cumeno, por deshidratación e hidrogenación .
Más recientemente, BASF y Dow Chemical pusieron en producción su primera línea implementando el proceso HPPO en el que el propileno es oxidado por peróxido de hidrógeno H 2 O 2 :
CH 3 –CH = CH 2+ H 2 O 2→ CH 3 C 2 H 3 O+ H 2 O.Se sabe que este proceso genera solo agua como subproducto.
Detección de espacio
La 14 de junio de 2016, Brett A. McGuire y sus colegas informan de la detección de óxido de propileno en la fase gaseosa de una capa molecular extendida fría alrededor de cúmulos protoestelares masivos anidados en la región de formación estelar Sagitario B2 . Previamente se habían detectado moléculas quirales en meteoritos y cometas de nuestro sistema solar , pero esta es la primera que se detecta en el espacio. También es una de las moléculas más complejas detectadas hasta la fecha en el espacio interestelar .
Notas y referencias
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- Entrada "Óxido de propileno" en la base de datos química GESTIS de la IFA (organismo alemán responsable de la seguridad y salud ocupacional) ( alemán , inglés ), consultado el 24 de febrero de 2013 (se requiere JavaScript ) .
- Ficha Sigma-Aldrich del compuesto Óxido de propileno , consultada el 24 de febrero de 2013.
- [McGuire et al. 2016] Brett A. McGuire y col. , " Descubrimiento de la molécula quiral interestelar óxido de propileno (CH 3 CHCH 2 O) "[" Descubrimiento de la molécula quiral interestelar de óxido de propileno (CH 3 CHCH 2 O) ”], Ciencia , Asociación Estadounidense para el Avance de la Ciencia, vol. 352, n o 6292, 17 de junio de 2016 (primera versión en línea el 14 de junio de 2016), p. 1449-1452 ( ISSN 0036-8075 y 1095-9203 , DOI 10.1126 / science.aae0328 )Los coautores del artículo son, además de Brett A. McGuire, P. Brandon Carroll, Ryan A. Loomis, Ian A. Finneran, Philip R. Jewell, Anthony J. Remijan y Geoffrey A. Blake. El artículo fue recibido por la editorial el 31 de diciembre de 2015 y aceptado para su publicación el 11 de mayo de 2016.
- “ una molécula orgánica detectaron en el espacio ”, http://fr.canoe.ca ,16 de junio de 2016( leer en línea ).