Leucopterina
| Leucopterina | |
| Identificación | |
|---|---|
| Sinónimos |
2-amino-5,8-dihidro-4,6,7 (1H) -pteridintriona |
| N o CAS | |
| N o ECHA | 100,007,044 |
| PubChem | 135403796 |
| Sonrisas |
C12 = C (NC (= O) C (= O) N1) N = C (NC2 = O) N , |
| InChI |
InChI: InChI = 1S / C6H5N5O3 / c7-6-10-2-1 (3 (12) 11-6) 8-4 (13) 5 (14) 9-2 / h (H, 8,13) (H4,7,9,10,11,12,14) InChIKey: SFLOGVVDXPCWGR-UHFFFAOYSA-N |
| Apariencia | cristales incoloros |
| Propiedades químicas | |
| Fórmula bruta |
C 6 H 5 N 5 O 3 [Isómeros] |
| Masa molar | 195.1356 ± 0.0071 g / mol C 36.93%, H 2.58%, N 35.89%, O 24.6%, |
| Propiedades físicas | |
| Solubilidad | muy poco soluble en agua (aproximadamente 1,25 g · l -1 a 20 ° C ) |
| Unidades de SI y STP a menos que se indique lo contrario. | |
La leucoptérina es un compuesto de los pigmentos de la familia ptériniques . Se presenta en forma de cristales incoloros, ligeramente solubles en agua.
Ocurrencia
La leucopterina se encuentra en la naturaleza en algunas especies de mariposas blancas.
También ha sido aislado por primera vez en 1926 por Clemens Schöpf (de) y Heinrich Otto Wieland alas Pierides , el Cabbage White y Green-veined White , que está en el origen de su nombre (el griego leukos , white y pteron , ala). Sin embargo, la leucopterina no es responsable de la coloración de las alas de estas mariposas. Este color blanco en realidad proviene del "reflejo de la luz en las escamas, en las que queda atrapado el aire" .
Propiedades
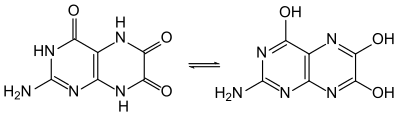
La leucopterina forma cristales casi incoloros que contienen medio equivalente de agua de cristalización (hemihidrato). Al igual que pterina , leukopterin puede sufrir equilibrio ceto-enólica , más precisamente en este caso lactama - lactima tautomería , transformando así en 2-amino-4,6,7-pteridintriol, otros tautómeros parciales son también posibles.. Sin embargo, la comparación de los espectros UV con los de otras pteridinas sustituidas indica que la forma de lactama es predominante.
La leucopterina es un ácido débil y, por lo tanto, se disuelve con sustancias alcalinas, por ejemplo, carbonato de sodio o sosa . La adición de ácido clorhídrico permite que el sólido incoloro se vuelva a precipitar, método utilizado por Schöpf y Purrmann para purificar la sustancia. La acidez es más alta para el grupo N (8) -H, seguido por el grupo N (3) -H y finalmente el grupo N (5) -H. Es posible preparar sales de sodio, bario y amonio a partir de este compuesto.
Biosíntesis
Un estudio radioquímico sobre orugas y pupas de Cabbage Pieris ( Pieris brassicae L. ), utilizando compuestos marcados con 14 carbonos, concluyó que la leucopterina de mariposa se producía a partir de guanina o guanosina , derivados de la purina , siendo probablemente el precursor inmediato la xantopterina . A partir de este compuesto, el grupo oxo en el carbono 8 puede introducirse mediante la acción de la xantina oxidasa .
Síntesis
Para probar su fórmula estructural, Robert Purrmann (de) sintetizó leucopterina en 1940 a partir de 2,4,5-triamino-1,6-dihidropirimidin-6-ona (2,4,5-triamino-6-hidroxipirimidina), calentado con exceso de ácido oxálico :

Notas y referencias
- (de) Este artículo está tomado parcial o totalmente del artículo de Wikipedia en alemán titulado “ Leukopterin ” ( ver lista de autores ) .
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- (de) Beilsteins Handbuch der Organischen Chemie, 4. Ergänzungswerk, Bd. 26 , p. 4017.
- (De) Clemens Schöpf, Heinrich Wieland, “ Über das Leukopterin, das weiße Flügelpigment der Kohlweißlinge (Pieris brassicae und P.napi). » , Berichte der deutschen chemischen Gesellschaft , vol. 59,1926, p. 2067–2072 ( DOI 10.1002 / cber.19260590865 )
- (De) Clemens Schöpf, Rolf Reichert, " Zur Kenntnis des Leukopterins " , Justus Liebigs Annalen der Chemie , vol. 548,1941, p. 82-94 ( DOI 10.1002 / jlac.19415480108 )
- (De) Albert Gossauer, Struktur und Reaktivität der Biomoleküle: eine Einführung in die organische Chemie , Zurich, Helvetica Chimica Acta,2006, 650 p. ( ISBN 978-3-906390-29-1 , leer en línea ) , pág. 504
- (de) Wolfgang Pfleiderer, Manfred Ruckwied, " Zur Struktur des Leukopterins " , Chem. Ber. , vol. 94,1961, p. 118-124
- (De) Friedrich Weygand, H. Simon, G. Dahms, M. Waldschmidt, HJ Schliep, H. Wacker, “ Über die Biogenese des Leucopterins ” , Angewandte Chemie , vol. 73,1961, p. 402–407 ( DOI 10.1002 / angel.19610731111 )
- (de) Robert Purrmann, “ Über die Flügelpigmente der Schmetterlinge. VII. Synthese des Leukopterins und Natur des Guanopterins ” , Justus Liebigs Annalen der Chemie , vol. 544,1940, p. 182-190 ( DOI 10.1002 / jlac.19405440111 )
- (de) Robert Purrmann, “ Konstitution und Synthese des sogenannten Anhydroleukopterins. Über die Flügelpigmente der Schmetterlinge XII ” , Justus Liebigs Annalen der Chemie , vol. 548,1941, p. 284–292 ( DOI 10.1002 / jlac.19415480121 )