Cianuro de dietilaluminio
| Cianuro de dietilaluminio | |||
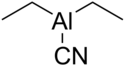
| |||
| Estructura del cianuro de dietilaluminio | |||
| Identificación | |||
|---|---|---|---|
| N o CAS | |||
| N o ECHA | 100.024.873 | ||
| N o EC | 227-359-8 | ||
| PubChem | 16683962 | ||
| Sonrisas |
CC [Al] (CC) C # N , |
||
| InChI |
Std. InChI: InChI = 1S / 2C2H5.CN.Al / c3 * 1-2; / h2 * 1H2,2H3 ;; Std. InChIKey: KWMUAEYVIFJZEB-UHFFFAOYSA-N |
||
| Propiedades químicas | |||
| Fórmula bruta |
C 5 H 10 Al N |
||
| Masa molar | 111,1211 ± 0,0049 g / mol C 54,04%, H 9,07%, Al 24,28%, N 12,6%, |
||
| Propiedades físicas | |||
| Densidad | 0,864 g · cm -3 a 25 ° C | ||
| Precauciones | |||
| SGH | |||
    Peligro H225, H304, H311, H315, H336, H361d, H373, H410, EUH032, P201, P210, P273, P280, P302, P304 + P340 + P310, H225 : Líquido y vapores muy inflamables H304 : Puede ser fatal si se ingiere y entra en las vías respiratorias H311 : Tóxico en contacto con la piel H315 : Provoca irritación cutánea H336 : Puede causar somnolencia o mareos H361d : Se sospecha que daña al feto. H373 : Se sospecha que existe peligro de daños graves a los órganos (enumere todos los órganos afectados, si se conocen) tras exposiciones repetidas o prolongadas (indique la vía de exposición si se ha demostrado de manera concluyente que ninguna otra vía de exposición conduce al mismo peligro) H410 : Muy tóxico para los organismos acuáticos con efectos duraderos EUH032 : En contacto con ácidos libera gas muy tóxico P201 : Obtenga instrucciones especiales antes de usar. P210 : Mantener alejado de fuentes de calor, chispas, llama abierta o superficies calientes. - No fumar. P273 : Evítese su liberación al medio ambiente. P280 : Use guantes de protección / ropa protectora / protección para los ojos / protección facial. P302 : Tras contacto con la piel: P304 + P340 + P310 : Tras inhalación : Transportar a la víctima al exterior y mantenerla en reposo en una posición confortable para respirar. Llamar inmediatamente a un CENTRO DE INFORMACIÓN TOXICOLÓGICA / médico. |
|||
| Transporte | |||
3123 : LÍQUIDO TÓXICO, REACTIVO AL AGUA, NOS Clase: 4.3 Etiquetas: 4.3 : Sustancias que, en contacto con el agua, emiten gases inflamables 6.1 : Sustancias tóxicas Envasado: Grupo de embalaje I : Sustancias muy peligrosas;   |
|||
| Unidades de SI y STP a menos que se indique lo contrario. | |||
El cianuro de dietilaluminio o reactivo Nagata , es un compuesto organometálico de fórmula química ((CH 3 CH 2 ) 2 NMA) n. Es una sustancia incolora que generalmente se maneja en solución en tolueno . Se utiliza para la hidrocianación de a, ß-insaturados cetonas .
Preparación
El cianuro de dietilaluminio se produjo inicialmente procesando trietilaluminio (CH 3 CH 2 ) 6 Al 2con un ligero exceso de cianuro de hidrógeno HCN:
n (CH 3 CH 2 ) 6 Al 2+ 2 n HCN ⟶ 2 ((CH 3 CH 2 ) 2 AlCN) n+ 2 n CH 3 CH 3.El producto generalmente se almacena en ampollas cerradas porque es altamente tóxico. Se disuelve en tolueno , benceno , hexano y éter diisopropílico . Se hidroliza rápidamente en agua y no es compatible con disolventes próticos .
Estructura
El cianuro de dietilaluminio no ha sido cristalografiado por rayos X, aunque sí otros cianuros de diorganoaluminio. Estos últimos tienen una fórmula general (R 2 AlCN) ny existen como trímeros o tetrámeros cíclicos ( n = 3 o 4 , respectivamente). Estos oligómeros tienen enlaces AlCN-Al.
Cianuro de bis [di (trimetilsilil) metil] aluminio (((CH 3 ) 3 Si) 2 CH) 2 AlCNes similar al cianuro de dietilaluminio. Su análisis cristalográfico muestra que es trimérico con la siguiente estructura:

.
Cianuro de bis ( terc- butil) aluminio ((CH 3 ) 3 C) 2 AlCN existe en forma tetramérica en fase cristalina:
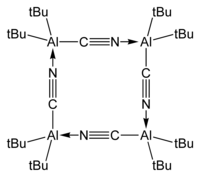
Aplicaciones
Cianuro de dietilaluminio se usa para la reacción Nagata , en particular la estequiométrica hidrocianación de α, beta-insaturados cetonas . La reacción depende de la basicidad del disolvente debido al carácter ácido del reactivo . El objetivo de esta reacción es producir nitrilos de alquilo, que son precursores de aminas , amidas , ésteres de ácidos carboxílicos y aldehídos .
- Ejemplo de hidrocianación .
Notas y referencias
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- Sigma-Aldrich hoja del compuesto solución de cianuro de dietilaluminio 1,0 M en tolueno , consultado el 7 de marzo, 2 021.
- (en) Wataru Mitsuru Nagata y Yoshioka , "los cianuros de alquilaluminio tienen potentes reactivos para la hidrocianación " , Tetrahedron Letters , vol. 7, n o 18, 1966, p. 1913-1918 ( DOI 10.1016 / S0040-4039 (00) 76271-X , leer en línea )
- (de) Werner Uhl, Uwe Schütz, Wolfgang Hiller y Maximiliano Heckel , “ Synthese und Kristallstruktur des trimeren [(Me 3 Si) 2 CH] 2 Al - CN » , Zeitschrift für anorganische und allgemeine Chemie , vol. 621, n o 5,Mayo de 1995, p. 823-828 ( DOI 10.1002 / zaac.19956210521 , leer en línea )
- (en) K. Wade y BK Wyatt , " Reacciones de compuestos de organoaluminio con cianuros. Parte III. Reacciones de trimetilaluminio, trietilaluminio, hidruro de dimetilaluminio e hidruro de dietilaluminio con dimetilcianamida ” , Journal of the Chemical Society A: inorgánico, físico, teórico , vol. 1969, 1969, p. 1121-1124 ( DOI 10.1039 / J19690001121 , leer en línea )
- (en) GE Coates y RN Mukherjee , " 35. cianuro de dimetilaluminio y su galio, indio, talio y similares; berilio y cianuro de metilberilio ” , Revista de la Sociedad Química (reanudado) , vol. 1963, 1963, p. 229-233 ( DOI 10.1039 / JR9630000229 , leer en línea )
- (en) Werner Uhl y Madhat Matar , " hidroaluminación de nitrilos e isonitrilos " , Zeitschrift für Naturforschung , vol. 59, 2004, p. 1214-1222 ( leer en línea )
- (in) Klaus Knabel y Heinrich Nöth , " Síntesis y estructura de algunos pseudohaluros de aluminio " , Zeitschrift für Naturforschung , vol. 60, 2005, p. 155-163 ( leer en línea )
- (en) W. Nagata y Sr. Yoshioka , " cianuro de dietilaluminio " , Organic Syntheses , vol. 52, 1972, p. 90 ( DOI 10.15227 / orgsyn.052.0090 , leer en línea )