Propano
| Propano | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 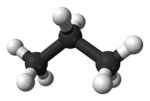  Molécula de propano |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificación | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre IUPAC | propano | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinónimos |
n -propano |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.753 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 200-827-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6334 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sonrisas |
CCC , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / C3H8 / c1-3-2 / h3H2,1-2H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | gas licuado comprimido, inodoro, incoloro | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades químicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fórmula bruta |
C 3 H 8 [Isómeros] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa molar | 44,0956 ± 0,003 g / mol C 81,71%, H 18,29%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Momento dipolar | 0,084 ± 0,001 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusión | −187,63 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° hirviendo | −42,1 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilidad | 75 mg · l -1 ( agua , 20 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parámetro de solubilidad δ | 13,1 MPa 1/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad |
2.0098 kg · m -3 ( 0 ° C , 1 015 mbar , gas) 0.5812 kg · l -1 ( -42,1 ° C , 1 015 mbar , líquido) ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura de autoignición | 470 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto de inflamabilidad | −104 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Límites explosivos en el aire |
1,7 - 10,8 % por volumen 31 - 202 g · m -3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presión de vapor saturante |
8,327 bar a 20 ° C 10,8 bar a 30 ° C 17,081 bar a 50 ° C ecuación:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto crítico | 96,75 ° C , 42,5 bar , 0,2 s -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Triple punto | 1,685 × 10 -9 bar a -188,15 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido | 1158 m · s -1 (líquido, -42,1 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termoquímica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 líquido, 1 bar | 171,0 J · mol -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gas | -104,7 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 líquido | -119,8 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vapor H ° |
16,25 kJ · mol -1 a 25 ° C 18,774 kJ · mol -1 a -42,11 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
73,6 J · mol -1 · K -1 ( 25 ° C , gas) 98,36 J · mol -1 · K -1 ( -43,15 ° C , líquido) ecuación:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 2 195,9 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | 2028,37 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades electronicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re energía de ionización | 10,95 ± 0,05 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauciones | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Peligro H220, H220 : gas extremadamente inflamable |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  A, B1, A : Presión absoluta del gas comprimido a 21,1 ° C = 853 kPa B1 : Límite inferior de inflamabilidad del gas inflamable = 2,1% Divulgación al 1,0% según los criterios de clasificación |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 2 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transporte | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
23 : gas inflamable Número ONU : 1978 : PROPANO Clase: 2.1 Etiqueta: 2.1 : Gases inflamables (corresponde a los grupos designados con una F mayúscula);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotoxicología | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 2,36 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Umbral de olor | bajo: 12,225 ppm alto: 20,005 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unidades de SI y STP a menos que se indique lo contrario. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El propano es un alcano lineal fórmula C 3 H 8. Hablamos de biopropano si es de origen no fósil.
Hoy en día se deriva principalmente de otros productos del petróleo mediante procesos termoquímicos del gas o del petróleo, pero también está comenzando a derivarse del biogás . Se utiliza comúnmente como fuente de energía química por combustión en motores de combustión interna, calderas, asadores.
Suele venderse en forma líquida, especialmente en forma de GLP (este es uno de sus principales componentes). Se utiliza un aditivo, etanotiol , como odorante para señalar posibles fugas.
usar
El propano se utiliza principalmente como combustible y combustible (es el componente principal del gas licuado de petróleo ).
En la industria, también se utiliza como reactivo para:
- la producción de etileno y propeno por craqueo al vapor ;
- en la síntesis de tetracloroetileno y tetraclorometano por clorolisis ;
- (recientemente) para sintetizar (por conversión catalizada por zeolita ) benceno , tolueno y xileno ;
- (recientemente) como alternativa o complemento a la fracturación hidráulica para la fracturación y estimulación de rocas yacimiento con el fin de extraer gas natural ( gas de esquisto ) según un método desarrollado por GasFrac, una pequeña empresa de gas con sede en Calgary ( Alberta ), especializada en fracturación hidráulica, que buscaba una solución igual de eficiente, pero que consumiera menos agua. El propano (a veces también se usa nitrógeno o una mezcla de gases) se insinúa mejor y más en las microfisuras de la roca y sale más fácilmente que el agua. Sin embargo, es un fluido mucho más peligroso de manipular que el agua.
Es posible una oxidación catalítica utilizando platino o paladio como catalizadores . Dado que el propano es una materia prima barata y abundante, se está estudiando intensamente su oxidación selectiva a monómeros ( propileno , ácido acrílico ).
Propiedades fisicoquímicas
El propano es un gas más denso que el aire (1,5 veces) en condiciones normales de temperatura y presión , por lo que forma bolsas en el suelo en una habitación llena de aire. Se descompone a partir de una temperatura superior a 780 - 800 ° C .
La combustión del propano es más limpia que la de la gasolina (gracias a su ventajosa relación H / C), pero significativamente más contaminante que la del metano o el hidrógeno . La presencia de enlaces CC crea residuos orgánicos además de vapor de agua y dióxido de carbono. Estos productos hacen visible la llama.
Producción y síntesis
El propano proviene principalmente de la purificación de gas natural o de la separación de gases licuados de petróleo (propano y butano ) de la destilación del petróleo crudo.
Efectos climáticos
La Tierra libera una megatonelada por año a la atmósfera.
Biopropano
El biopropano es un gas producido a partir de biomasa , que tiene la misma composición química que el propano comercial. En el caso de la primera refinería europea en Neste en Rotterdam , es un subproducto producto de la producción de biodiesel a partir de residuos industriales 68% (aceites de cocina, residuos de grasa animal (principalmente de Asia, pero también de Europa y Francia) y verduras aceites (de colza y de palma que constituyen el 32% restante de la mezcla)).
Según los análisis de ciclo de vida ordenados por Primagaz (evaluados durante un año con ADEME) “El biopropano emite 60 gramos de CO 2equivalente / kWh, es decir, aproximadamente un 78% menos que los combustibles fósiles de referencia […] 36 gramos de CO 2eq / kWh se deben al suministro de biomasa, 22 gramos a la fabricación, 0,5 gramos al transporte marítimo y 1,5 gramos a la distribución […] el fuel oil emite cinco veces más CO 2equivalente ”que el biopropano, lo que convierte a este último“ en el combustible con menor emisión del mercado […] El biopropano de Primagaz es producido en Rotterdam, Holanda, por Neste, con quien SHV Energy ha firmado una asociación de producción exclusiva de 40.000 toneladas de biopropano por año a partir de 2018 ” . De acuerdo con Primagaz, la mitad de los proyectos de construcción de viviendas unifamiliares servidos por Primagaz va a utilizar biopropane partir de 2019, al igual que, probablemente, algunas previstas viviendas sociales eco-barrios . Potencialmente, todo el territorio tendrá acceso a él, incluidos los 27.000 municipios no atendidos por la red de gas. Y está prevista una botella de gas biopropano antes de finales de 2018. En 2018, Primagaz prevé integrar un 8% de biopropano en el GLP de 1.750 estaciones francesas, pero en 2020 solo importará el 3% de sus ventas.
Economía
El propano se usa en tanques, sobre el suelo o subterráneos, y los proveedores lo llenan una o más veces al año, llamados tanques de propano. Por lo general, el tanque está disponible de forma gratuita a cambio de un compromiso de varios años.
En Francia, el mercado del gas propano es un oligopolio entre Antargaz (antes Antargaz-Finagaz), Butagaz , Primagaz y, en menor medida, Vitogaz .
Los proveedores facilitan el acceso al gas instalando depósitos en viviendas que no están conectadas al gas ciudad ( gas natural ). También hay tanques de combustible , pero el propano es una energía más limpia para consumir durante la combustión.
Notas y referencias
- PROPANO , hoja de seguridad (s) del Programa Internacional para la Seguridad de Sustancias Químicas , consultado el 9 de mayo, 2009
- (en) David R. Lide, Manual de química y física , Boca Raton, CRC,16 de junio de 2008, 89 ª ed. , 2736 p. ( ISBN 978-1-4200-6679-1 y 1-4200-6679-X ) , pág. 9-50
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- Manual de química, D. Lide, 2004-2005.
- Entrada "Propano" en la base de datos de productos químicos GESTIS de la IFA (organismo alemán responsable de la seguridad y salud en el trabajo) ( alemán , inglés ), consultado el 20 de abril de 2009 (se requiere JavaScript)
- (en) James E. Mark, Manual de propiedades físicas del polímero , Springer,2007, 2 nd ed. , 1076 p. ( ISBN 978-0-387-69002-5 y 0-387-69002-6 , leer en línea ) , pág. 294
- (en) Robert H. Perry y Donald W. verde , los ingenieros químicos Handbook de Perry , Estados Unidos, McGraw-Hill,1997, 7 ª ed. , 2400 p. ( ISBN 0-07-049841-5 ) , pág. 2-50
- " Propano " , en http://www.nist.gov/ (visitada 20 de abril 2009 )
- (en) W. M Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 ª ed. , 2610 p. ( ISBN 978-1-4398-2077-3 ) , pág. 14-40
- (en) Carl L. Yaws, Manual de diagramas termodinámicos: compuestos orgánicos C8 a C28 , vol. 1, Huston, Texas, Pub del Golfo. Co.,1996, 396 p. ( ISBN 0-88415-857-8 )
- los gases butano propano
- (en) David R. Lide, Manual de química y física , Boca Raton, CRC,2008, 89 ª ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , pág. 10-205
- Número de índice en la tabla 3.1 del apéndice VI del reglamento CE No. 1272/2008 (16 de diciembre de 2008)
- " Propano " en la base de datos de productos químicos Reptox de la CSST (organización de Quebec responsable de la seguridad y salud ocupacional), consultado el 24 de abril de 2009
- " Propano, " en hazmap.nlm.nih.gov (visitada 14 de noviembre de, 2009 )
- Karl Griesbaum, Arno Behr, Dieter Biedenkapp, Heinz-Werner Voges, Dorothea Garbe, Christian Paetz, Gerd Collin, Dieter Mayer, Hartmut Höke, Enciclopedia de Química Industrial de Ullmann , Hidrocarburos , Wiley-VCH Verlag,2000
- portal de la empresa Gasfrac
- Brino, A. y Albany, N. (2011), Nuevo método de fracturación hidráulica sin agua evita problemas de contaminación, pero los perforadores tardan en adoptarlo [PDF] , Insideclimatenews.org., 5 p.
- Tang, W., Xiao, W., Wang, S., Ren, Z., Ding, J. y Gao, PX (2018), Impulsar la oxidación catalítica del propano sobre agregados de nanocristales de Co 3 O 4 libres de PGM mediante lixiviación química : Estudio comparativo con catalizadores basados en Pt y Pd , Catálisis Aplicada B: Ambiental .
- (es) Juan Pablo Hernández , Adriana Echavarría y Luz Amparo Palacio , “ Síntesis de dos nuevos vanadatos de níquel y cobre-níquel utilizados para la deshidrogenación oxidativa del propano ” , Revista Facultad de Ingeniería Universidad de Antioquia ,Junio del 2013( ISSN 0120-6230 , leer en línea )
- (en) " Deshidrogenación oxidativa de propano con N2O sobre zeolita Cr / FeZSM-5 " , Ing. compet. , vol. 15,2013( leer en línea )
- (in) " EFECTO DEL VANADIO EN CATALIZADORES DERIVADOS DE MATERIALES HIDROTALCITA EN LA DESHIDROGENACIÓN OXIDATIVA DE PROPANO " , Revista Colombiana de Química ,2011( leer en línea )
- (en) " EFECTO PROMOTOR DEL MO SOBRE CATALIZADORES SOPORTADOS DE Pd / g-Al2O3 EN LA DESHIDROGENACIÓN OXIDATIVA DE PROPANO " , Dyna rev.fac.nac.minas ,2011( leer en línea )
- (in) Los estudios cinéticos de la oxidación del propano son Catalizadores basados en óxidos mixtos de Mo y V ,2011( leer en línea )
- (in) " La red de reacción en la etapa de oxidación del propano sobre catalizadores de óxido MoVTeNb M1 puros " , Journal of Catalysis , vol. 311,2014, p. 369-385 ( leer en línea )
- (in) " multifuncionalidad de catalizadores de óxido cristalino MoV (NBPT) M1 en la oxidación selectiva de propano y alcohol bencílico " , catálisis ACS ,2013, p. 1103-1113 ( leer en línea )
- (in) " Química de la superficie de la fase de óxido puro M1 MoVTeNb durante la operación de oxidación selectiva de propano a ácido acrílico " , Journal of Catalysis , vol. 285,2012, p. 48-60 ( leer en línea )
- La fabricación de fueloil , en FioulMarket.fr (consultado el 23 de agosto de 2012)
- Science et Vie , Sabemos lo que la Tierra desgasifica con hidrocarburos , n o 1098, marzo de 2009, p. 34 .
- Eva Gómez, " Primagaz lanzamientos biopropane en Francia " , en environnement-magazine.fr ,28 de marzo de 2018.
- Aurélie Barbaux, " Primagaz lanzamientos biopropane en Francia " ,28 de marzo de 2018(consultado el 23 de abril de 2019 ) .
- "14ª legislatura" , sobre questions.assemblee-nationale.fr
- " Total venderá su subsidiaria Totalgaz a Antargaz " , en Les Echos ,3 de julio de 2014(consultado el 5 de diciembre de 2019 )






