Ácido sulfúrico
| Ácido sulfúrico | |||
|
|||
| Identificación | |||
|---|---|---|---|
| Nombre IUPAC |
ácido sulfúrico sulfito de hidrógeno |
||
| N o CAS | |||
| N o ECHA | 100,029,066 | ||
| N o CE | 231-973-1 | ||
| PubChem | 1100 | ||
| Sonrisas |
OS (= O) O , |
||
| InChI |
InChI: InChI = 1S / H2O3S / c1-4 (2) 3 / h (H2,1,2,3) InChIKey: LSNNMFCWUKXFEE-UHFFFAOYSA-N |
||
| Propiedades químicas | |||
| Fórmula bruta | H 2 SO 3 | ||
| Masa molar | 82.079 ± 0.006 g / mol H 2.46%, O 58.48%, S 39.07%, |
||
| pKa | 1,81 y 6,99 | ||
| Propiedades físicas | |||
| Solubilidad | Miscible en agua | ||
| Densidad | 1,03 g · cm -3 ( 20 ° C ) | ||
| Precauciones | |||
| SGH | |||
 H314, H332, P280, P305, P310, P338, P351,
H314 : Provoca quemaduras graves en la piel y lesiones oculares graves
H314, H332, P280, P305, P310, P338, P351,
H314 : Provoca quemaduras graves en la piel y lesiones oculares graves H332 : Nocivo en caso de inhalación P280 : Llevar guantes / ropa protectora / protección ocular / protección facial P305 : Si entra en contacto con los ojos: P310 : Llamar inmediatamente a un CENTRO DE INFORMACIÓN TOXICOLÓGICA oa un médico. P338 : Quitar los lentes de contacto si la víctima los usa y se pueden quitar fácilmente. Continúe enjuagando. P351 : Enjuagar cuidadosamente con agua durante varios minutos. |
|||
| WHMIS | |||
 MI, E : Material corrosivo Transporte de mercancías peligrosas: clase 8 Divulgación al 1,0% según la lista de divulgación de ingredientes |
|||
| Transporte | |||
80 : corrosivo o con un grado menor de corrosividad Número ONU : 1833 : ACIDO SULFURO Clase: 8 Etiqueta: 8 : Sustancias corrosivas Embalaje: Grupo de embalaje II : Sustancias moderadamente peligrosas;  |
|||
| Unidades de SI y STP a menos que se indique lo contrario. | |||
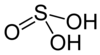
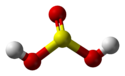
El ácido sulfúrico x es un compuesto químico de fórmula H 2 SO 3. Sin embargo, si se detectó en la fase gaseosa , no es seguro que exista realmente en solución .
Las bases conjugadas de este ácido son comunes: el anión hidrogenosulfito de fórmula HSO 3 -y el anión sulfito de fórmula SO 3 2-.
Descripción
El ácido sulfuroso es un ácido mineral resultante formalmente de la disolución del dióxido de azufre SO 2en agua H 2 Odependiendo de la reacción :
SO 2 (g) + H 2 O (l) → H 2 SO 3 (aq) : K << 10 -9 .Sin embargo, la molécula de H 2 SO 3solvatado por el agua no es estable y conduce inmediatamente a iones de sulfito de hidrógeno HSO 3 -y sulfito SO 3 2- :
SO 2 (g) + 2 H 2 O (l) H 3 O + (aq) + HSO 3 - (aq) : pK a1 = 1,81. HSO 3 - (ac) + H 2 O (l) H 3 O + (ac) + SO 3 2- (ac) : pK a2 = 6,99.Este tipo de solución ácida se utiliza como conservante de alimentos , especialmente para la conservación de frutos secos , vino y carnes , así como como desinfectante , agente reductor y blanqueador suave, utilizado especialmente en materiales que serían dañados por el lavado a los productos clorados. .
Notas y referencias
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- "ácido sulfuroso" Entrada en la base de datos químicos GESTIS del IFA (organismo alemán responsable de la seguridad y salud) ( alemán , Inglés ), Accessed November 27, 2,009 mil (JavaScript necesario)
- SIGMA ALDRICH
- " Ácido sulfuroso " en la base de datos de productos químicos Reptox de la CSST (organización de Quebec responsable de la seguridad y salud en el trabajo), consultado el 25 de abril de 2009
- D. Sülzle, M. Verhoeven, JK Terlouw, H. Schwarz, "Preparación y caracterización del ácido sulfuroso y su catión radical como moléculas estables en la fase gaseosa" Angew. Chem. En t. Edn. Engl. 27 , 1533 - 4 (1988). DOI: 10.1002 / ángel. 1988100112
