Ipilimumab
| Ipilimumab | |
| |
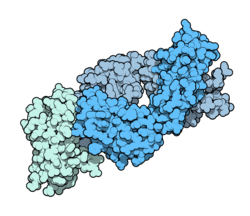
| Fragmento Fab (en) de ipilimumab (en azul) y de CTLA-4 (en verde). Entrada de 5TRU del banco de datos de proteínas . | |
| Identificación | |
|---|---|
| N o CAS | |
| Código ATC | |
| DrugBank | DB06186 |
| Propiedades químicas | |
| Fórmula bruta |
C 6742 H 9972 N 1732 O 2004 S 40 |
| Masa molar | 148 632,319 ± 7,239 g / mol C 54,48%, H 6,76%, N 16,32%, O 21,57%, S 0,86%, |
| Consideraciones terapéuticas | |
| Clase terapéutica | anticuerpo monoclonal para inmunoterapia |
| Unidades de SI y STP a menos que se indique lo contrario. | |
El ipilimumab (comercializado con el nombre de Yervoy ) es un anticuerpo monoclonal utilizado en el tratamiento del melanoma. Es un anticuerpo que inhibe el punto de control CTLA-4 de los linfocitos T , un punto de control activado por ciertos cánceres para reducir la eficiencia del linfocito.
El ipilimumab es un anticuerpo monoclonal humano de tipo IgG1 dirigido contra la proteína CTLA-4 (antígeno 4 del linfocito T citotóxico). La inhibición de este receptor presente en los linfocitos T da como resultado la activación del linfocito T.
Historia del descubrimiento
En 1987, los investigadores franceses descubrieron la proteína CTLA-4 presente en la superficie de linfocitos T . Luego, el investigador James Allison de Sloan Kettering en Nueva York impulsó el desarrollo de anticuerpos anti-CTLA-4. Medarex, que posteriormente fue adquirido por el laboratorio estadounidense Bristol Myers Squibb , continuó desarrollando ipilimumab.
Indicaciones, dosis y métodos de administración.
El tratamiento de inducción se administra a una dosis de 3 mg / kg mediante perfusión intravenosa durante un período de 90 minutos, cada 3 semanas hasta un total de 4 dosis.
Efectos secundarios
Pueden ser de mecanismo inmunológico, pudiendo la activación de linfocitos dirigirse contra autoantígenos. son esencialmente de tipo erupción cutánea y colitis . Otros ataques son más raros: hipofisitis , pancreatitis , hepatitis . Se han descrito casos de miocarditis fulminante.
Por tanto, se observa una colitis en uno de cada cinco, que suele responder bien a los esteroides o al infliximab, pero puede complicarse con una perforación intestinal. La apariencia en la colonoscopia es variable pero ciertos signos permiten distinguirla de la colitis ulcerosa : menor concentración de linfocitos tipo CD20 , menor plasmocitosis, menor distorsión de las criptas.
Eficiencia
Mejora la supervivencia en pacientes con melanoma metastásico utilizado solo o en combinación con dacarbazina . Su eficacia parece estar correlacionada con un mayor nivel de linfocitos después del tratamiento.
En el melanoma , la eficacia es aún más importante si el tratamiento se combina con nivolumab . Combinado con este último, es más eficaz que sunitinib en el cáncer de riñón avanzado .
Información administrativa
Autorización temporal de uso (ATU)
Se otorgó un ATU nominativo de 9 de octubre de 2007.
Se otorgó un ATU de cohorte de 18 de julio de 2011.
Autorización de comercialización (AMM)
Se concedió una autorización de comercialización centralizada el 13 de julio de 2011.
Notas y referencias
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- Jerome Groopman , " El ejército de células T ", The New Yorker ,23 de abril de 2012( ISSN 0028-792X , leído en línea , consultado el 7 de marzo de 2016 )
- http://www.bmsfrance.fr/nos-medicaments/Documents/YERVOY/AT_Yervoy_06-11-2013.pdf
- Michot JM, Bigenwald C, Champiat S et al. Eventos adversos relacionados con la inmunidad con bloqueo de los puntos de control inmunitarios: una revisión completa , Eur J Cancer, 2016; 54: 139–48
- Weber JS, Kähler KC, Hauschild A, Manejo de eventos adversos relacionados con el sistema inmunológico y cinética de respuesta con ipilimumab , J Clin Oncol, 2012; 30: 2691–7
- Johnson DB, Balko JM, Compton ML et al. Miocarditis fulminante con bloqueo de puntos de control inmunitario combinado , N Engl J Med, 2016; 375: 1749–55
- Beck KE, Blansfield JA, Tran KQ et al. Enterocolitis en pacientes con cáncer después del bloqueo de anticuerpos del antígeno 4 asociado a linfocitos T citotóxicos , J Clin Oncol, 2006; 24: 2283–9
- Minor DR, Chin K, Kashani-Sabet M, Infliximab en el tratamiento de la colitis inmunitaria inducida por anticuerpos anti-CTLA4 (ipilimumab) , Cancer Biother Radiopharm, 2009; 24: 321–5
- Mitchell KA, Kluger H, Sznol M, Hartman DJ, Colitis perforante inducida por ipilimumab , J Clin Gastroenterol, 2013; 47: 781–5
- Verschuren EC, van den Eertwegh AJ, Wonders J et al. Características clínicas, endoscópicas e histológicas de la colitis asociada a ipilimumab , Clin Gastroenterol Hepatol, 2016; 14: 836–42
- Adler BL, Pezhouh MK, Kim A et al. Características histopatológicas e inmunofenotípicas de la colitis asociada a ipilimumab en comparación con la colitis ulcerosa , J Int Med, 2018; 283: 568-577
- Hodi FS, O'Day SJ, McDermott DF et al. Mejor supervivencia con ipilimumab en pacientes con melanoma metastásico , N Engl J Med, 2010; 363: 711-723
- Robert C, Thomas L, Bondarenko I et al. Ipilimumab más dacarbazina para el melanoma metastásico no tratado previamente , N Engl J Med, 2011; 364: 2517-2526
- Ku GY, Yuan J, Page DB et al. Experiencia de una sola institución con ipilimumab en pacientes con melanoma avanzado en el entorno de uso compasivo: el recuento de linfocitos después de 2 dosis se correlaciona con la supervivencia , Cancer, 2010; 116: 1767-1775
- Wolchok JD, Kluger H, Callahan MK et al. Nivolumab más ipilimumab en melanoma avanzado , N Engl J Med, 2013; 369: 122-133
- Motzer RJ, Tannir NM, McDermott DF et al. Nivolumab más ipilimumab versus sunitinib en el carcinoma avanzado de células renales , N Engl J Med, 2018; 378: 1277-1290
- http://www.has-sante.fr/portail/upload/docs/application/pdf/2012-01/yervoy_14_12_2011_avis_ct_11462.pdf