Diborano
| Diborano | |||
| |||
 | |||
| Estructura del diborano | |||
| Identificación | |||
|---|---|---|---|
| Nombre IUPAC | diborano (6) | ||
| Sinónimos |
boranilidineborano |
||
| N o CAS | |||
| N o ECHA | 100,039,021 | ||
| N o CE | 242-940-6 | ||
| N o RTECS | HQ9275000 | ||
| PubChem | 6328200 | ||
| CHEBI | 33590 | ||
| Sonrisas |
[BH2] 1 [H] [BH2] [H] 1 , |
||
| InChI |
InChI: InChI = 1 / B2H6 / c1-2 / h1-2H3 Std. InChI: InChI = 1S / B2 / c1-2 Std. InChIKey: ZOCHARZZJNPSEU-UHFFFAOYSA-N |
||
| Apariencia | Gas comprimido, incoloro, de olor característico. | ||
| Propiedades químicas | |||
| Fórmula bruta | B 2 H 6 | ||
| Masa molar | 27,67 ± 0,014 g / mol H 21,86%, B 78,14%, |
||
| Propiedades físicas | |||
| T ° fusión | −165 ° C | ||
| T ° hirviendo | −92 ° C | ||
| Solubilidad | en agua: hidrolizado a hidrógeno y ácido bórico | ||
| Densidad | 1,18 kg · m -3 a 15 ° C | ||
| Temperatura de autoignición | 40 hasta 50 ° C | ||
| punto de inflamabilidad | 38 ° C | ||
| Límites explosivos en el aire | 0,8 - 88 % vol | ||
| Punto crítico | 40,5 bares , 289,8 K | ||
| Termoquímica | |||
| Δ vapor H ° | 14,28 kJ · mol -1 ( 1 atm , -92,49 ° C ) | ||
| Precauciones | |||
| SGH | |||
   Peligro H220, H280, H330, P210, P260, P304, P315, P340 , P377, P381, P403, P405, H220 : Gas extremadamente inflamable H280 : Contiene gas a presión; puede explotar si se calienta H330 : Mortal en caso de inhalación P210 : Mantener alejado de fuentes de calor, chispas, llama abierta o superficies calientes. - No fumar. P260 : No respire el polvo / humo / gas / niebla / vapores / aerosoles. P304 : En caso de inhalación: P315 : Obtenga atención médica inmediata. P340 : Transportar a la víctima al exterior y mantenerla en reposo en una posición confortable para respirar. P377 : Fuga de gas inflamado: No apagar si la fuga no se puede detener de forma segura. P381 : Eliminar todas las fuentes de ignición si se puede hacer sin riesgo. P403 : Almacenar en un lugar bien ventilado. P405 : Tienda cerrada. |
|||
| NFPA 704 | |||
| 4 4 3 W | |||
| Transporte | |||
263 : gas tóxico, inflamable Número ONU : 1911 : DIBORANE, COMPRIMIDO Clase: 2.3 Etiquetas: 2.3 : Gases tóxicos (corresponde a los grupos designados con una T mayúscula, es decir, T, TF, TC, TO, TFC y TOC) . 2.1 : Gases inflamables (corresponde a los grupos designados con una F mayúscula);   |
|||
| Ecotoxicología | |||
| Umbral de olor | bajo: 1.8 ppm alto: 3.5 ppm |
||
| Unidades de SI y STP a menos que se indique lo contrario. | |||
El diborano es un compuesto químico de fórmula B 2 H 6. Esta molécula , formada por boro e hidrógeno , resulta de la unión de dos grupos borano BH 3unidos por dos de sus átomos de hidrógeno. No debe confundirse con diborano (4) , de fórmula B 2 H 4, donde los dos átomos de boro están unidos por un enlace covalente ; El diborano a veces se denomina diborano (6) para distinguirlo de este compuesto.
A temperatura ambiente, es un gas incoloro con un olor dulzón que se enciende fácilmente en presencia de humedad. Forma mezclas altamente explosivas con el aire. Es un compuesto de boro clave con varias aplicaciones. Su formación es endotérmica y la entalpía libre de formación es positiva ( 36 kJ · mol -1 ) . Por lo tanto, el diborano tiende a descomponerse, liberando hidrógeno H 2, pero con una cinética bastante lenta.
Propiedades y estructura
El diborano es un gas incoloro más ligero que el aire; se condensa a -92,5 ° C por debajo de 101,3 kPa ; su densidad es 421 g · m -3 y su calor latente de vaporización es 515.39 kJ · mol -1 . Se solidifica a -165 ° C . A 15 ° C , su presión de vapor saturado es de 3,94 MPa y la relación entre los volúmenes de gas y líquido es de 362. Gaseoso, es muy inflamable y puede provocar espontáneamente violentas explosiones en el aire. Su punto crítico está a 16.6 ° C y 4.053 MPa .
El diborano se descompone lentamente, incluso a temperatura ambiente, en hidrógeno e hidruros de boro superiores. Esta descomposición se acelera al aumentar la temperatura. El diborano es sensible a la humedad y se hidroliza instantáneamente a hidrógeno y ácido bórico H 3 BO 3 después de la reacción exotérmica:
B 2 H 6+ 6 H 2 O→ 2 H 3 BO 3+ 6 H 2.En contacto con el litio y el aluminio , el diborano forma hidruros que pueden encenderse espontáneamente. No tiene acción corrosiva sobre los metales comunes pero ataca a la mayoría de cauchos y plásticos , excepto por ejemplo al politetrafluoroetileno [CF 2 -CF 2 ] ny policlorotrifluoroetileno [CClF-CF 2 ] n.
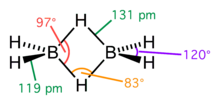
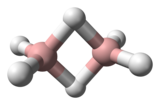
El diborano tiene una geometría D 2hcon dos átomos de hidrógeno de unión y cuatro átomos de hidrógeno terminales. Los enlaces entre los átomos de boro y los hidrógenos terminales son convencionales (un par de electrones implicados en cada enlace BH, formando un enlace covalente ), pero aquellos entre los átomos de boro y los enlaces de hidrógeno son de naturaleza diferente (un par de electrones implicados en cada puente BHB, formando un enlace de dos electrones de tres centros ). Por lo tanto, la longitud de estos enlaces es diferente: 119 μm para los BH terminales, pero 133 μm para los enlaces BH de los puentes BHB, lo que significa que la fuerza de estos enlaces también es diferente (más débil en el puente BHB que en el BH terminal vínculo).
El galio forma un compuesto de estructura similar: el digallano Ga 2 H 6.
Preparación de diborano
El diborano es un compuesto central en la química del boro y, por lo tanto, ha sido particularmente estudiado, por lo que existen muchas síntesis. La mayoría de las preparaciones utilizan hidruros con haluros o alcoholatos. La producción industrial utiliza trifluoruro de boro BF 3 :
2 BF 3+ 6 NaH→ B 2 H 6+ 6 NaFDos preparaciones de laboratorio utilizan tricloruro de boro BCl 3con tetrahidruroaluminato de litio LiAlH 4, o trifluoruro de boro BF 3con borohidruro de sodio NaBH 4 ; estos dos métodos tienen un rendimiento del 30% de diborano:
4 BCl 3+ 3 LiAlH 4→ 2 B 2 H 6+ 3 LiAlCl 4 4 BF 3+ 3 NaBH 4→ 2 B 2 H 6+ 3 NaBF 4La oxidación de las sales de borohidruro se puede utilizar para preparar pequeñas cantidades:
2 NaBH 4+ Yo 2→ 2 NaI+ B 2 H 6+ H 2Reacciones y uso
El diborano es un reactivo que encuentra un gran número de aplicaciones. Las reacciones en las que interviene a menudo involucran bases de Lewis para dar nuevas moléculas. Reacciona con el amoniaco para formar borazano BH 3 NH 3o borazina B 3 N 3 H 6 dependiendo de las condiciones de funcionamiento.
Se ha estudiado como propulsor en propulsión de cohetes (con oxidantes fluorados como el flúor F 2y OF 2 difluoruro de oxígeno), para la vulcanización de elastómeros , como catalizador en la polimerización de monómeros orgánicos, para aumentar la velocidad de la llama, como dopante en la industria de semiconductores y como reactivo para la producción de silicio ultrapuro destinado a circuitos electrónicos.
Notas y referencias
- DIBORANE , hoja (s) de seguridad del Programa Internacional sobre Seguridad de Sustancias Químicas , consultado el 9 de mayo de 2009
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- " Propiedades de varios gases " , en flexwareinc.com (consultado el 12 de abril de 2010 )
- (en) David R. Lide, Manual CRC de Química y Física , CRC Press,2009, 90 ª ed. , 2804 p. , Tapa dura ( ISBN 978-1-4200-9084-0 )
- Entrada "diborano" en la base de datos química GESTIS de la IFA (organismo alemán responsable de la seguridad y salud) ( alemán , Inglés ), Accessed September 14, 2011 (Javascript required)
- " Diborano " , en hazmap.nlm.nih.gov (consultado el 14 de noviembre de 2009 )
- Lo que da propulsores hipergólicos de alta potencia: 372 s de impulso específico para el propulsor OF 2/ B 2 H 6, ahora abandonado porque es caro y libera productos tóxicos.
