Óxido de oro (III)
| Óxido de oro ( III ) | |
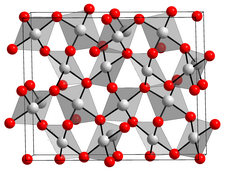
| |
| __ Au 3+ __ O 2− . | |
| Identificación | |
|---|---|
| Nombre IUPAC | óxido de oro ( III ) |
| Sinónimos |
sesquióxido de oro |
| N o CAS | |
| N o ECHA | 100,013,748 |
| N o EC | 215-122-1 |
| PubChem | 164805 |
| Sonrisas |
[O-2]. [O-2]. [O-2]. [Au + 3]. [Au + 3] , |
| InChI |
Std. InChI: InChI = 1S / 2Au.3O / q2 * + 3; 3 * -2 Std. InChIKey: DDYSHSNGZNCTKB-UHFFFAOYSA-N |
| Propiedades químicas | |
| Fórmula |
A las 2 O 3 |
| Masa molar | 441,9313 ± 0,0009 g / mol Au 89,14%, O 10,86%, |
| Precauciones | |
| SGH | |
 Atención H315, H319, P280, P305 + P351 + P338, P337 + P313, H315 : Provoca irritación cutánea H319 : Provoca irritación ocular grave P280 : Llevar guantes / ropa protectora / protección ocular / protección facial. P305 + P351 + P338 : En caso de contacto con los ojos: Enjuagar cuidadosamente con agua durante varios minutos. Quítese los lentes de contacto si la víctima los usa y se pueden quitar fácilmente. Continúe enjuagando. P337 + P313 : Si persiste la irritación ocular: Obtenga atención médica . |
|
| Unidades de SI y STP a menos que se indique lo contrario. | |
El óxido de oro ( III ) , o sesquióxido de oro , es un compuesto químico de fórmula In 2 O 3. Es el óxido de oro más estable. Es un sólido semiconductor cristalino marrón rojizo sensible a la luz que se descompone a 160 ° C devolviendo oro y oxígeno .
Debido a la naturaleza poco reactiva del oro, el óxido de oro ( III ) no se puede obtener por reacción directa del oxígeno O 2sobre oro en condiciones normales. Sin embargo, se puede producir haciendo reaccionar oro con oxígeno en un medio acuoso a una presión de varios miles de atmósferas , o con oxígeno en estado de plasma . También se puede obtener a partir de óxido de oro amorfo hidratado ( III ) por reacción con ácido perclórico HClO 4.y un perclorato de ClO 4- de metal alcalino en un tubo de cuarzo sellado a una temperatura de aproximadamente 250 ° C y una presión de aproximadamente 30 MPa .
Notas y referencias
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- hoja Sigma-Aldrich compuesto Gold (III) oxide hydrate , consultado el 9 de marzo de 2017.
- (en) Hongqing Shi, Ryoji Asahi y Catherine Stampfl , " Propiedades de los óxidos de oro en 2 O 3 y Au 2 O : Investigación de los primeros principios ” , Physical Review B , vol. 75, n o 20,Mayo de 2007, Artículo n o 205125 ( DOI 10.1103 / PhysRevB.75.205125 , código bib 2007PhRvB..75t5125S , leer en línea )
- (en) PG Jones, H. Rumpel, E. Schwarzmann, GM Sheldrick y H. Paulus , " Óxido de oro (III) " , Acta Crystallographica Scetion B , vol. B35, n o 6, 1979, p. 1435-1437 ( DOI 10.1107 / S0567740879006622 , leer en línea )