Hexaclorodisilano
| Hexaclorodisilano | |||
| |||
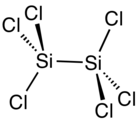
| Estructura del hexaclorodisilano | |||
| Identificación | |||
|---|---|---|---|
| N o CAS | |||
| N o ECHA | 100,033,353 | ||
| N o EC | 236-704-1 | ||
| PubChem | 83497 | ||
| Sonrisas |
[Si] ([Si] (Cl) (Cl) Cl) (Cl) (Cl) Cl , |
||
| InChI |
InChIKey: 1S / Cl6Si2 / c1-7 (2,3) 8 (4,5) 6 Est. InChI: InChI = LXEXBJXDGVGRAR-UHFFFAOYSA-N |
||
| Apariencia | líquido incoloro | ||
| Propiedades químicas | |||
| Fórmula bruta | Si 2 Cl 6 | ||
| Masa molar | 268,889 ± 0,013 g / mol Cl 79,11%, Si 20,89%, |
||
| Propiedades físicas | |||
| T ° hirviendo | 144 hasta 145,5 ° C | ||
| Densidad | 1.562 g · cm -3 a 25 ° C | ||
| Precauciones | |||
| SGH | |||
 Peligro H314, EUH014, P280, P310, P305 + P351 + P338, H314 : Provoca quemaduras graves en la piel y lesiones oculares. EUH014 : Reacciona violentamente con el agua. P280 : Llevar guantes / ropa protectora / protección ocular / protección facial. P310 : Llamar inmediatamente a un CENTRO DE INFORMACIÓN TOXICOLÓGICA oa un médico. P305 + P351 + P338 : En caso de contacto con los ojos: Enjuagar cuidadosamente con agua durante varios minutos. Quítese los lentes de contacto si la víctima los está usando y se pueden quitar fácilmente. Continúe enjuagando. |
|||
| Transporte | |||
2987 : CLOROSILANOS CORROSIVOS, NOS Clase: 8 Etiqueta: 8 : Sustanciascorrosivas Embalaje: Grupo de embalaje II : Sustancias medianamente peligrosas;  |
|||
| Unidades de SI y STP a menos que se indique lo contrario. | |||
El hexaclorodisilano es un compuesto químico de fórmula If 2 Cl 6. Aparece como un líquido incoloro y transparente que humea al contacto con el aire y es sensible a la hidrólisis . Como todos los perclorosilanos Si n Cl 2 n +2con n entre 2 y 6, se puede obtener haciendo reaccionar siliciuro de calcio CaSi 2con cloro Cl 2entre 230 y 250 ° C :
CaSi 2+ 4 Cl 2⟶ Si 2 Cl 6+ CaCl 2.También es posible producirlo haciendo reaccionar dicloruro de silicio SiCl 2o silicio con cloro Cl 2 :
2 SiCl 2+ Cl 2⟶ Si 2 Cl 6 ; 2 Si + 3 Cl 2⟶ Si 2 Cl 6.Es estable en aire y nitrógeno hasta temperaturas de al menos 400 ° C durante varias horas, pero incluso a temperatura ambiente se descompone en dodecacloroneopentasilano Si (SiCl 3 ) 4y tetracloruro de silicio SiCl 4cuando se coloca en presencia de bases de Lewis :
4 Si 2 Cl 6⟶ 3 SiCl 4+ Si (SiCl 3 ) 4.Esta conversión se utiliza para la producción de determinados componentes de silicio en la industria de los semiconductores , en particular células fotovoltaicas .
Notas y referencias
- Ficha Sigma-Aldrich para el compuesto Hexachlorodisilane 96% , consultada el 12 de febrero de 2021.
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- (de) Georg Brauer, en colaboración con Marianne Baudler, Handbuch der Chemie Präparativen Anorganischen , 3 e ed. revisado, vol. 1, Ferdinand Enke, Stuttgart 1975, pág. 657 . ( ISBN 3-432-02328-6 )
- (in) ESM Seo, Sr. Andreoli y R. Chiba , " Producción de tetracloruro de silicio por método de cloración utilizando cáscara de arroz como materia prima " , Journal of Materials Processing Technology , vol. 141, n o 3, noviembre de 2003, p. 351-356 ( DOI 10.1016 / S0924-0136 (03) 00287-5 , leer en línea )
- (in) HJ Emeléus y Muhammad Tufail , " Reacción del hexaclorodisilano con bases y haluros de alquilo " , Journal of Inorganic and Nuclear Chemistry , vol. 29, n o 8, Agosto 1967, p. 2081-2084 ( DOI 10.1016 / 0022-1902 (67) 80468-8 , leer en línea )
- (in) Walter Simmler , " Compuestos de silicio, inorgánicos " , Enciclopedia de química industrial de Ullmann , 15 de junio de 2000( DOI 10.1002 / 14356007.a24_001 , leer en línea )