Acetato de zinc
| Acetato de zinc | |||
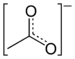 Estructura del acetato de zinc |
|||
| Identificación | |||
|---|---|---|---|
| Nombre IUPAC | diacetato de zinc | ||
| Sinónimos |
dicarbometoxicinc |
||
| N o CAS |
(anhidro) (dihidrato) |
||
| N o ECHA | 100,008,338 | ||
| N o EC | 209-170-2 | ||
| PubChem | 11192 | ||
| CHEBI | 62984 | ||
| N o E | E650 | ||
| Sonrisas |
CC (= O) [O -]. CC (= O) [O -]. [Zn + 2] , |
||
| InChI |
Std. InChI: InChI = 1S / 2C2H4O2.Zn / c2 * 1-2 (3) 4; / h2 * 1H3, (H, 3,4); / q ;; + 2 / p-2 Std. InChIKey: DJWUNCQRNNEAKC-UHFFFAOYSA-L |
||
| Apariencia | sólido cristalizado blanco con bajo olor acético | ||
| Propiedades químicas | |||
| Fórmula bruta |
C 4 H 6 O 4 Zn |
||
| Masa molar | 183,47 ± 0,02 g / mol C 26,19%, H 3,3%, O 34,88%, Zn 35,64%, |
||
| Propiedades físicas | |||
| T ° fusión | 237 ° C (descomposición; el dihidrato pierde su agua a 100 ° C ) | ||
| Solubilidad | 430 g · L -1 | ||
| Densidad |
1,84 g · cm -3 ( anhidro ) 1,735 g · cm -3 ( dihidrato ) |
||
| Precauciones | |||
| SGH | |||
  Atención H302, H410, P262, P273, H302 : Nocivo en caso de ingestión H410 : Muy tóxico para los organismos acuáticos con efectos duraderos P262 : Evítese el contacto con los ojos, la piel o la ropa. P273 : Evítese su liberación al medio ambiente. |
|||
| Transporte | |||
90 : material peligroso para el medio ambiente, materiales peligrosos diversos Número ONU : 3077 : SUSTANCIA SÓLIDA PELIGROSA PARA EL MEDIO AMBIENTE, NEP Clase: 9 Etiqueta: 9 : Materiales y artículos peligrosos diversos Embalaje: Grupo de embalaje III : sustancias de bajo peligro.  |
|||
| Unidades de SI y STP a menos que se indique lo contrario. | |||
El acetato de zinc es un compuesto químico de fórmula Zn [OOCCH 3 ] 2a menudo tiene la estructura de un Zn [OOCCH 3 ] 2 · 2H 2 O dihidrato. Anhidro o hidratado, el acetato aparece como un sólido blanco de olor débil y ambas formas se utilizan en síntesis química y como complementos alimenticios . Se produce por la acción del ácido acético CH 3 COOHsobre carbonato de zinc ZnCO 3( smithsonita ) o zinc elemental ( metálico ).
Los dos átomos de oxígeno del grupo acetato pueden unirse a iones de metal de varias formas y mediante varios tipos de enlaces. El acetato de zinc anhidro adopta una estructura polimérica en la que el átomo de zinc está coordinado con cuatro átomos de oxígeno en una geometría tetraédrica , cada uno de estos tetraedros está unido a sus vecinos por grupos acetato.
Los ligandos acetato no son bidentados . Por el contrario , la mayoría de los diacetatos metálicos tienen átomos metálicos en coordinación octaédrica con grupos acetato bidentados. En el acetato de zinc dihidratado, el átomo de zinc es octaédrico y ambos grupos acetato son bidentados.
El acetato de zinc se usa para reducir la absorción de cobre del intestino en la enfermedad de Wilson.
Notas y referencias
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- "Acetato de zinc" Entrada en la base de datos químicos GESTIS del IFA (organismo alemán responsable de la seguridad y salud) ( alemán , Inglés ), acceder las 24 de enero de 2.013 (requiere JavaScript)
- (en) JN van Niekerk, FRL Schoening y JH Talbot , " La estructura cristalina del acetato de zinc dihidrato, Zn (CH 3 COO) 2 .2H 2 O » , Acta Crystallographica , vol. 6, n hueso 8-9,Septiembre de 1953, p. 720-723 ( leer en línea ) DOI : 10.1107 / S0365110X53002015