Glucólisis
La glucólisis ( γλῠκὖς Glykys "dulce" y λύσις Lysis 'liberación') o Embden-Meyerhof-Parnas es una vía metabólica de captación de glucosa y producción de energía. Tiene lugar en el hialoplasma (o citosol) de la célula . Como sugiere su nombre, requiere glucosa y permite la producción de piruvato . Este último puede entrar en el ciclo de Krebs , que tiene lugar en las mitocondrias de eucariotas o en el citoplasma de bacterias en aerobiosis, o ser metabolizado por fermentación en anaerobiosis, por ejemplo para producir lactato o etanol .
Principio general
La glucólisis es un mecanismo de regeneración de ATP que no requiere oxígeno . Durante este proceso, somos testigos de:
- de las reacciones redox en las que se reduce un aceptor de electrones ( coenzima NAD + ):
- síntesis de ATP por fosforilación de ADP (formación de cuatro moléculas de ATP , pero consumo de dos moléculas de ATP , o formación neta total de dos moléculas de ATP ):
El símbolo P i representa aquí el fosfato inorgánico HPO 4 2-, o hidrogenofosfato.
Como la glucólisis da como resultado la reducción de coenzimas, va acompañada de la oxidación de moléculas orgánicas. Podemos decir que corresponde a la oxidación de la glucosa a piruvato :
glucosa + 2 NAD + → 2 CH 3 -CO-COO -+ 2 ( NADH + H + ),junto con:
2 ADP + 2 P i + 2 H + → 2 ATP + 2 H 2 O,un total de
glucosa + 2 ADP + 2 P i + 2 NAD + → 2 piruvato * + 2 ATP + 2 ( NADH + H + ) + 2 H 2 O.* El piruvato CH 3 -CO-COO -estrictamente hablando, la base conjugada del ácido pirúvico CH 3 -CO-COOH.
| D - glucosa | Piruvato | ||||
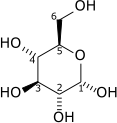
|
+ 2 ADP + 2 P i + 2 NAD + |
|
2 |
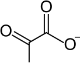
|
+ 2 ATP + 2 (NADH + H + ) + 2 H 2 O |
La glucólisis es de vital importancia para el cuerpo, ya que es la vía principal para el metabolismo de la glucosa. Es la única fuente metabólica de energía para el cerebro , contrayendo rápidamente los músculos esqueléticos o eritrocitos , excepto durante períodos de ayuno prolongado o actividad física prolongada. De hecho, tan pronto como se agoten las reservas de glucógeno hepático, el cuerpo degradará sus lípidos para liberar ácidos grasos libres y glicerol en la sangre , que se transformarán por beta-oxidación en cuerpos cetónicos . Entonces serán estos cuerpos cetónicos los que alimentarán al cerebro y al resto del cuerpo. Una vez producido, el piruvato puede seguir varias vías metabólicas según las condiciones ambientales.
- En la mayoría de los tejidos, cuando el oxígeno es abundante, el piruvato se oxida perdiendo el grupo carboxilo en forma de CO 2 , y la unidad de dos carbonos restante ingresa al ciclo del ácido cítrico y luego sufre fosforilaciones oxidativas, en un proceso llamado respiración celular .
- De lo contrario, en ausencia de oxígeno, el piruvato se puede reducir a lactato mediante la oxidación acoplada de NADH + H + a NAD + . Este proceso, llamado fermentación láctica , también se encuentra en ciertos microorganismos, como las bacterias del ácido láctico utilizadas en la fabricación de yogur.
- Finalmente, en microorganismos como las levaduras y en los tejidos de ciertas plantas , el piruvato se puede reducir a alcohol etílico ( etanol ), nuevamente con oxidación acoplada de NADH a NAD + . Es fermentación alcohólica .
Etapas de la glucólisis
La serie de 10 reacciones de la glucólisis se puede dividir en tres fases:
- Fase 1: La glucosa, una especie con 6 átomos de carbono C, se fosforila primero en las posiciones C 6 y C 1 (reacciones 1, 2 y 3);
- Fase 2: luego se escinde en dos moléculas de tres carbonos en forma de gliceraldehído-3-fosfato (reacciones 4 y 5)
- Fase 3: la energía invertida en las fosforilaciones se recupera finalmente en forma de ATP (reacciones 6 a 10).
Fase 1: Activación de hexosas por fosforilaciones sucesivas.
Fosforilación de glucosa a glucosa-6-fosfatoEsta reacción requiere un catión Mg 2+ como cofactor y consume una molécula de ATP para fosforilar cada molécula de glucosa . Ayuda a mantener la concentración de glucosa relativamente baja en el citoplasma para facilitar la entrada de moléculas de glucosa adicionales. Además, la glucosa-6-fosfato ya no puede salir de la célula, porque la membrana plasmática no tiene un transportador para esta molécula.

|
+ ATP → ADP + H + + |
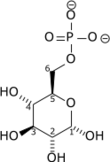
|
| Glucosa | Glucosa-6-fosfato | |
| Hexoquinasa - EC | ||
Esta reacción es irreversible. Es catalizada por una quinasa , ya sea una hexoquinasa , no específica para la glucosa que, en los mamíferos , se encuentra con mayor frecuencia en el músculo , o una glucocinasa , específica para la glucosa . Estas dos enzimas tienen diferentes constantes de Michaelis ( K M ) con valores respectivos de 0,1 mM y 10 mM sabiendo que la K M es inversamente proporcional a la afinidad de la enzima por sus sustratos. Estas dos enzimas dependen de Mg 2+ . En los seres humanos, la glucoquinasa se localiza en el hígado y en las células pancreáticas . De hecho, este último se adapta perfectamente a la función de almacenamiento del hígado (actúa principalmente durante una gran afluencia de glucosa, por ejemplo después de una comida, y por tanto contribuye a la regulación del azúcar en sangre ). Por tanto, una disfunción de esta enzima es responsable de ciertos tipos de diabetes ( diabetes MODY que, en el 50% de los casos, se debe a una mutación en la glucoquinasa ).
La fosforilación de glucosa no es específica de la glucólisis. Este paso también sirve como punto de partida en la ruta de las pentosas fosfato o para la glucogenogénesis.
Nota: todas las reacciones que tienen una alta variación de entalpía libre son irreversibles, y como esta fosforilación está muy favorecida energéticamente, la reacción es irreversible. Es por eso que estas enzimas están altamente reguladas para evitar que el sistema se acelere, como los otros dos pasos irreversibles de la glucólisis. ( Fosfofructoquinasa-1 , Piruvato cinasa ). La hexoquinasa es inhibida notablemente por su propio producto, la glucosa-6-fosfato ( retroalimentación negativa), y su expresión génica es inducida por la insulina . La glucosa-6-fosfato no inhibe la glucocinasa, pero la insulina induce su expresión génica.
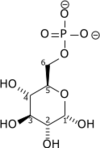
Isomerización de fructosa-6-fosfatoLa α- D -glucosa-6-fosfato producida durante la glucólisis se isomeriza a β- D -fructosa-6-fosfato mediante glucosa-6-fosfato isomerasa (GPI) o fosfohexosa isomerasa. Esta reacción es reversible y permanece orientada a la derecha debido a la concentración de Fru-6-P, que se mantiene bastante baja debido a su consumo inmediato por el siguiente paso de glucólisis.
|

|
|
| Glucosa-6-fosfato | Fructosa-6-fosfato | |
| Glucosa-6-fosfato isomerasa - EC | ||
El β- D -fructosa-6-fosfato (Fru-6-P) producido durante la reacción anterior se fosforila a β- D -fructosa-1,6-bisfosfato (Fru-1,6-BP) por la fosfofructoquinasa -1 ( PFK-1) de una molécula de ATP , convertida en ADP . Este consumo de energía hace que este paso sea irreversible y constituye un punto importante de regulación de la tasa de glucólisis. Un catión Mg 2+ actúa como cofactor .

|
+ ATP → ADP + H + + |

|
| Fructosa-6-fosfato | Fructosa-1,6-bisfosfato | |
| Fosfofructoquinasa-1 - EC | ||
Existen, principalmente en organismos distintos de los animales , diferentes enzimas capaces de fosforilar la fructosa-6-fosfato a partir de pirofosfato inorgánico en lugar de ATP. Este es el caso de la difosfato fructosa-6-fosfato 1-fosfotransferasa (PFP), que se encuentra en muchas plantas , ciertas bacterias , arqueas y protistas . Las arqueas raras tienen una variante de fosfofructoquinasa, esta vez usando ADP y no ATP.
Esta reacción, catalizada por una fosfofructoquinasa (PFK) es irreversible y dependiente de Mg 2+ . Esta enzima cataliza el primer paso específico de la glucólisis. Es de forma altamente controlada libre de ATP alostérico (ATP libre es la forma del ATP de magnesio no complejado), que es el producto final "útil" de la glucólisis. Cuanto mayor sea la concentración de ATP libre , más lenta será esta reacción y, a la inversa, cuanto menor sea la concentración de ATP libre , más activa será la enzima. Es un sistema de autocontrol para la glucólisis. Se han desarrollado varios modelos matemáticos de glucólisis y muestran que este paso es el más importante de los que controlan el flujo de glucólisis.
La inhibición por ATP es reversible por AMP , lo que permite mantener constante la relación ATP / AMP.
Pero sobre todo está regulado por fructosa-2,6-bisfosfato : de hecho, la producción de fructosa-2,6-bisfosfato a partir de fructosa-6-fosfato tiene la única función de demostrar la saturación de la vía en fructosa-6-fosfato ("demasiado lleno") porque la fructosa-2,6-bisfosfato no tiene que volverse metabólica. Por tanto , mediante alosterismo , la fructosa-2,6-bisfosfato activa la fosfofructoquinasa-1 para estimular el consumo de fructosa-6-fosfato y así prevenir su propia formación.
Fase 2: Escisión de fructosa-1,6-bisfosfato en dos moléculas de gliceraldehído-3-fosfato
Escisión en gliceraldehído-3-fosfato y dihidroxiacetona fosfatoLa β- D -fructosa-1,6-bisfosfato es escindida por una liasa , la fructosa-bisfosfato aldolasa , en D -gliceroraldehído-3-fosfato (G3P) y dihidroxiacetona fosfato (DHAP).

|

|
+ |

|
|
| Fructosa-1,6-bisfosfato | G3P | DHAP | ||
| Fructosa bisfosfato aldolasa - EC | ||||
Hay dos clases de aldolasas capaces de escindir la fructosa-1,6-bisfosfato: la clase I en animales y plantas , y la clase II en hongos y bacterias ; estas dos clases de enzimas utilizan diferentes mecanismos para escindir esta cetosis .
Isomerización de dihidroxiacetona fosfato a gliceraldehído-3-fosfatoEl fosfato dihidroxiacetona se isomeriza en D -gliceraldehído-3-fosfato mediante triosafosfato isomerasa . Esta reacción no se ve muy favorecida, tiene lugar a una tasa del 5% en la dirección “dihidroxiacetonafosfato → gliceraldehído-3-fosfato” y al 95% en la otra dirección.

|

|
|
| DHAP | G3P | |
| Triosa-fosfato isomerasa - EC | ||
Aunque en equilibrio la forma de cetosis (DHAP) es mucho más abundante que la forma de aldosa (G3P), la transformación de DHAP → G3P es rápida porque el compuesto G3P se elimina permanentemente mediante las siguientes reacciones de glucólisis.
Por tanto, cada molécula de β- D -fructosa-1,6-bisfosfato da como resultado en última instancia dos moléculas de D -gliceraldehído-3-fosfato (G3P).
Fase 3: Recuperación de la energía invertida en fosforilaciones
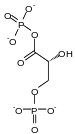
Fosforilación a ácido 1,3-bisfosfoglicéricoEl D -gliceraldehído-3-fosfato se fosforila en 1,3-bisfosfo- D- glicérato (1,3-BPG) por gliceraldehído 3-fosfato deshidrogenasa con reducción concomitante de una molécula de NAD + a NADH + H + ; es el único paso de la glucólisis donde se forma el poder reductor, en forma de NADH + H + . Esta reacción se equilibra desde el punto de vista de la carga eléctrica y el número de átomos de hidrógeno por el hecho de que el fosfato inorgánico (Pi) existe, en el medio citoplasmático , en forma del ion hidrogenofosfato HPO 4 2-.

|
+ NAD + + Pi NADH + H + + |
|
| G3P | 1,3-BPG | |
| Gliceraldehído-3-fosfato deshidrogenasa - EC | ||
Esta reacción redox, reversible y catalizada por una oxidorreductasa , conduce a la formación de un enlace aciltioéster con alto potencial de transferencia. Este paso constituye el inicio de la segunda parte de la glucólisis. La energía contenida en los enlaces con alto potencial de transferencia se utilizará para la síntesis de ATP. Se reducen las coenzimas (ganancia de electrones).
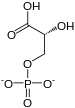
Conversión a 3-fosfoglicerato con recuperación de ATPEl grupo fosfato de alto potencial de transferencia del 1,3-bisfosfo- D- glicerato (1,3-BPG) permite que una molécula de ADP sea fosforilada en ATP para formar 3- fosfo - D -glicerato (3PG) bajo la acción de la fosfoglicerato quinasa ; es el primer paso de la glucólisis donde la energía se recupera en forma reutilizable, almacenada en ATP.

|
+ ADP ATP + |
|
| 1,3-BPG | 3PG | |
| Fosfoglicerato quinasa - EC | ||
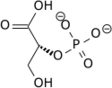
El 3- fosfo - D- glicerato se isomeriza en 2- fosfo - D- glicerato (2PG) mediante fosfoglicerato mutasa .

|
|
|
| 3PG | 2PG | |
| Fosfoglicerato mutasa - EC | ||
El 2- fosfo - D- glicerato (2PG) se deshidrata mediante una liasa , la enolasa (o fosfopiruvato hidratasa) para formar el fosfoenolpiruvato (PEP). Se requiere un catión Mg 2+ como catalizador para la reacción de deshidratación , mientras que un segundo Mg 2+ interviene con un papel "conformacional" en coordinación con el grupo carboxilo del 2- fosfo - D -glicerato.

|
H 2 O + |

|
| 2PG | ENERGÍA | |
| Enolasa (fosfopiruvato hidratasa) - EC | ||
El grupo fosfato con alto potencial de transferencia ( .DELTA.G ° ' = -61,9 kJ mol -1 ) del fosfoenolpiruvato permite la fosforilación de una molécula de ADP en ATP por la piruvato quinasa . Un catión Mg 2+ es necesario para esta reacción como cofactor .

|
+ ADP + H + → ATP + |

|
| ENERGÍA | Piruvato | |
| Piruvato quinasa - EC | ||
Durante esta reacción, el fosfoenolpiruvato se convierte de hecho irreversiblemente en enolpiruvato por la piruvato quinasa, y el enolpiruvato produce piruvato de manera reversible por tautomería .
Evaluación de glucólisis

Son usados:
- 1 mol de glucosa
- 2 moles de coenzimas oxidadas ( NAD + )
- 4 moles de ADP
- 2 moles de ATP
- 2 moles de fosfato inorgánico
Para producir :
- 2 moles de piruvato
- 2 moles de coenzimas reducidas ( NADH )
- 4 moles de ATP
- 2 moles de agua
- 2 moles de protones (H + )
De modo que se producen 2 mol de ATP procesando 1 mol de glucosa.
Regulación de la glucólisis
La glucólisis se regula principalmente a nivel de tres enzimas clave: PFK-1 , piruvato quinasa y hexoquinasa .
Regulación de PFK-1
El PFK-1 está controlado de manera alostérica :
- El ATP y el citrato actúan como inhibidores
- El AMP y la fructosa 2,6-bisfosfato actúan como activadores.
Por tanto, la concentración de fructosa-2,6-bisfosfato es esencial para la glucólisis. Está regulado por la fosfofructoquinasa-2, cuya actividad es diferente según el estado de fosforilación:
- bajo el efecto de la insulina ( hormona hipoglucémica ), se desfosforila y cataliza la reacción fructosa-6-fosfato + ATP → fructosa-2,6-bisfosfato + ADP ; aumenta la concentración de fructosa-2,6-bisfosfato y se acelera la glucólisis.
- bajo el efecto del glucagón (hormona hiperglucémica), se fosforila y cataliza la reacción: fructosa-2,6-bisfosfato + H 2 O→ fructosa-6-fosfato + Pi ; la concentración de fructosa-2,6-bisfosfato disminuye y la glucólisis se ralentiza.
Regulación de la piruvato quinasa
La piruvato quinasa está regulada alostéricamente y esto de manera ubicua:
- El AMP y la fructosa 1,6-bisfosfato son activadores
- El ATP , la acetil-CoA y la alanina son inhibidores.
En el hígado, también se regula de forma covalente (por la acción de las hormonas ).
- el glucagón actúa fosforilando esta enzima , que tiene el efecto de inhibir
- la insulina realiza la acción inversa, que tiene el efecto de activar la piruvato quinasa.
Regulación de la hexoquinasa
La actividad de esta enzima es inhibida por el producto de reacción, glucosa-6-fosfato . Si se acumula, su producción disminuye rápidamente para equilibrarse con su consumo. Este proceso evita la acumulación de metabolitos .
Reoxidación de coenzimas
La glucólisis cesa cuando las coenzimas reducidas no se reoxidan, especialmente cuando el NADH no se regenera en la forma NAD + . Por ejemplo, el paso catalizado por gliceraldehído-3-fosfato deshidrogenasa no puede ocurrir sin NAD + :

|
|
Oxidación junto con fosforilación de gliceraldehído-3-fosfato (G3P) a 1,3-bisfosfoglicerato (1,3-BPG) |
.
Hay dos vías metabólicas principales para esto, dependiendo del estado redox del medio:
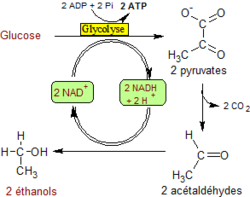
1) uno, en un ambiente anaeróbico , llamado fermentación , tiene lugar por fosforilación a nivel del sustrato y aceptación de electrones por una sustancia orgánica. Hay varios tipos: fermentación láctica (que se produce en el músculo sin oxígeno) fermentación ácido butírico , fermentación alcohólica . En la fermentación láctica, el NADH reduce directamente el piruvato a lactato . En la fermentación alcohólica provocada por levaduras , la glucólisis se prolonga mediante dos reacciones adicionales: la descarboxilación del piruvato a acetaldehído y luego la reducción de este último a etanol . Por tanto, en el primer caso, el piruvato sirve como aceptor de electrones final y el acetaldehído en el segundo caso.

|
|
|
|
Fermentación láctica : la regeneración de NAD + está asegurada por la reducción directa de piruvato a lactato piruvato + 2 H + + 2 e - → lactato |
Fermentación alcohólica : la regeneración de NAD + está asegurada por la reducción de acetaldehído a etanol acetaldehído + 2 H + + 2 e - → etanol |

|
| → glucólisis Ciclo de Krebs → cadena respiratoria El aceptor final de protones y electrones es el oxígeno del aire |
El balance energético de la glucólisis seguida de la respiración (32 ATP) es aproximadamente 20 veces mayor que el de la glucólisis seguida de la fermentación (2 ATP para la fermentación láctica).
Notas y referencias
- Biología molecular de la célula por Harvey Lodish, Arnold Berk, Paul Matsudaira, James Darnell , Chris A. Kaiser, Pierre L. Masson - página 301.
- Stephen D. Anton , Keelin Moehl , William T. Donahoo y Krisztina Marosi , " Activar el interruptor metabólico: comprender y aplicar los beneficios para la salud del ayuno ", Obesidad (Silver Spring, Maryland) , vol. 26, n o 2febrero 2018, p. 254–268 ( ISSN 1930-7381 , PMID 29086496 , PMCID 5783752 , DOI 10.1002 / oby.22065 , leído en línea , consultado el 19 de septiembre de 2019 )
- (en) Reginald H. Garrett y Charles M. Grisham , Bioquímica , Wadsworth Publishing Co Inc,2012, 5 ª ed. , 1280 p. ( ISBN 978-1-133-10629-6 y 1-133-10629-3 , leer en línea )
- Pascal Ribéreau-Gayon , Denis Dubourdieu , Bernard Donèche y Aline Lonvaud , Tratado de enología , t. 1: Microbiología del vino. Vinificación , Dunod,3 de octubre de 2012, 6 ª ed. ( ISBN 978-2-10-058234-1 y 2-10-058234-8 )
- (en) HS Seeholzer, A. Jaworowski, IA Rose , " enolpiruvato: determinación química como intermedio de piruvato quinasa " , Bioquímica , vol. 30, n o 3, 22 de enero de 1991, p. 727-732 ( leer en línea )
- George B. Johnson , Jonathan B. Losos , Peter H. Cuervo y Susan S. cantante ( trad. , De Inglés) Biología: versión de lujo , Bruselas / París, Superior De Boeck 15 de noviembre de 2009, 1406 p. ( ISBN 978-2-8041-6638-0 )
- Joseph-Pierre Guiraud , Microbiología alimentaria , Dunod, 18 de septiembre de 2012, 2 nd ed. ( ISBN 978-2-10-057008-9 y 2-10-057008-0 )
Ver también
Artículos relacionados
Otras rutas de degradación de la glucosa:
- Vía de las pentosas fosfatos
- Ruta Entner-Doudoroff
- Complejo de piruvato y piruvato deshidrogenasa
- Gluconeogénesis
