Cáncer de mama
Cáncer de mama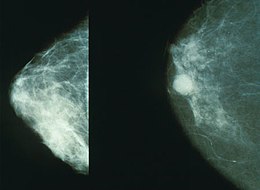 Mamografía que muestra el cáncer de mama a la derecha.
Mamografía que muestra el cáncer de mama a la derecha.
| Especialidad | Oncología |
|---|
| CISP - 2 | X76 |
|---|---|
| ICD - 10 | C50 |
| CIM - 9 | 174 - 175 , V10.3 |
| OMIM | 114480 |
| Enfermedades DB | 1598 |
| MedlinePlus | 000913 |
| eMedicina | 1947145, 345979 y 1276001 |
| eMedicina |
med / 2808 med / 3287 radio / 115 plástico / 521 |
| Malla | D001943 |
| Droga | El etinil estradiol , fluoximesterona ( en ) , vinblastina , capecitabina , dexrazoxano , idarubicina , metotrexato , carboplatino , paclitaxel , la mitoxantrona , la vinorelbina , trastuzumab , anastrozol , toremifeno ( en ) , letrozol , exemestano , epirubicina , docetaxel , tamoxifeno , dietilestilbestrol , irinotecán , cisplatino , estradiol , ciclofosfamida , clorambucilo , metiltestosterona ( en ) , melfalán , sargramostim ( en ) , leuprorelina , fulvestrant ( en ) , doxorrubicina , ifosfamida , testolactona ( en ) , fluorouracilo , aminoglutetimida ( en ) , megestrol ( en ) , goserelina acetato ( es ) , nandrolona , neratinib , tamoxifeno , vinorelbina y eribulina |
| Paciente del Reino Unido | Cáncer-de-mama-pro |
El cáncer de mama es un tumor maligno de la glándula mamaria . Es decir, es un cáncer que se origina en las unidades celulares cuya función es secretar leche, las unidades ducto-lobulillares de la mama , principalmente en las mujeres . 8 de cada 10 cánceres de mama ocurren después de los 50 años.
El primer cáncer del mundo, en 2016 afecta a 1,8 millones de mujeres al año en todo el mundo, incluidas 50.000 mujeres en Francia. Se espera que una de cada ocho mujeres sea diagnosticada con cáncer de mama durante su vida. El tratamiento del cáncer de mama ha mejorado drásticamente a lo largo de los años, lo que ha dado lugar a más casos de remisión.
5 a 10% de estos cánceres tienen un origen genético hereditario; Del 85 al 90% de los casos (la denominada forma esporádica o no hereditaria ) tienen un origen ambiental o desconocido. Una proporción significativa de cáncer de mama esporádico es inducida por la ingesta de hormonas, estrógenos y progesterona contenidos en anticonceptivos o tratamientos contra la menopausia. Los factores de riesgo también son el consumo de alcohol , azúcar, lácteos, grasas hidrogenadas , obesidad , falta de actividad física. Un primer embarazo tardío y la ausencia de lactancia materna también promoverían este cáncer.
El tratamiento llamará, según los protocolos, a cirugía, radioterapia, quimioterapia, la combinación de estos tratamientos puede complementarse con terapia hormonal.
Epidemiología
El riesgo aumenta significativamente con la edad entre 30 y 60 años; entonces es homogéneo entre 60 y 80 años; la edad promedio de diagnóstico es de 61 años.
Existen ciertos factores genéticos predisponentes, así como factores hormonales.
Cabe señalar que la incidencia ha disminuido significativamente (poco menos del 9%) en Estados Unidos desde 2003 y también en Francia, lo que correspondería a un menor uso de la terapia hormonal sustitutiva para la menopausia .
En 2002 , se evaluaron casi 1,1 millones de casos nuevos, con más de 400.000 muertes por cáncer de mama. La incidencia parece estar aumentando de manera constante con más de 1,6 millones de nuevos casos en 2010 y 425.000 muertes. Casi cuatro millones de mujeres desarrollan cáncer de mama . La frecuencia de los exámenes histológicos que concluyen en “cáncer” de mama depende sobre todo de la intensidad del cribado (ver sobrediagnóstico ). La mortalidad ha disminuido significativamente desde la década de 1990 en los países desarrollados. Sigue creciendo en otros países.
Cáncer de mama en Francia
La Francia es uno de los países donde la incidencia de cáncer de mama es muy alta en todo el mundo, y donde la tasa de incidencia de cáncer de mama ha aumentado más rápidamente (2,4 por cada 100 000 mujeres por año) durante el período 1980-2005, con una caída en esta tasa entre 2000 y 2005 (+ 2,1 por 100.000 mujeres por año).
- El cáncer de mama causó alrededor de 11.000 muertes cada año en la década de 2000, la mortalidad es estable (11.201 muertes en 2005).
- Una de cada ocho mujeres se ve afectada por el cáncer de mama en Francia.
- Representa más de uno de cada 3 nuevos casos de cáncer (36,7% en 2008) de todos los cánceres nuevos, en mujeres.
- En la década de 2000 , cada año se diagnosticaban alrededor de 50.000 nuevos cánceres de mama.
- En 2005 , este número fue de 49.814, lo que corresponde a una de las tasas de incidencia más altas de Europa. Esta tasa aumentó en Francia un 2,4% de media al año durante 25 años (de 1980 a 2005).
- Menos del 10% de los cánceres de mama ocurren antes de los 40 años, el 25% ocurren antes de los 50 años, casi la mitad antes de los 65 años.
- Casi el 10% de las mujeres desarrollan cáncer de mama. El 75% de los nuevos casos detectados se refieren a mujeres mayores de 50 años y este número aumenta constantemente: 35.000 en 1995 , 42.000 en 2001 .
Este cáncer es parte de uno de los tres cánceres para los que la supervivencia ha aumentado desde que la tasa de supervivencia aumentó del 80% al 87% a principios de la década de 2000, según un informe conjunto del Instituto de Vigilancia de Salud Pública, la red Francim. Registros de cáncer, el Instituto Nacional del Cáncer y los Hospitales de Lyon.
Cáncer de mama en Asia oriental
Cáncer de mama en ChinaEntre las mujeres de China , el cáncer de mama es la causa más común y principal de muerte por cáncer. La mortalidad por cáncer de mama ha aumentado en los últimos años. Les données des deuxième et troisième Enquêtes nationales par sondage rétrospective des causes de décès en Chine estiment que la mortalité liée au cancer du sein a augmenté entre 1990-1992 et 2004-2005 de 3,84 par 100 000 à 5,09 pour 100 000 habitantes. En 2008, se diagnosticaron alrededor de 169.000 nuevos casos de cáncer de mama, y fue el tipo de cáncer más comúnmente diagnosticado en mujeres chinas. En ese mismo año, la mortalidad por cáncer de mama fue de 5,7 por 100.000 habitantes, lo que resultó en aproximadamente 44.900 muertes.
Cáncer de mama en JapónSegún un estudio publicado en 2009, la incidencia de cáncer de mama es históricamente mucho más baja en Japón que en los países occidentales; entre 1998-2002 en Osaka hay una tasa de 32,0 por 100.000 mujeres, que se compara con una tasa de 105,6 por 100.000 mujeres caucásicas en Hawai y 107,5 por 100.000 mujeres japonesas en Hawai. El autor señala el mayor consumo de alimentos de soya en Japón que en los países occidentales y sus efectos en las tasas de cáncer de mama en el país.
Factores de riesgo
Cánceres esporádicos (no familiares)
Del 5 al 10% de los cánceres de mama diagnosticados son cánceres de mama predispuestos genéticamente. Los cánceres no familiares constituyen el 90 a 95% restante. Un tercio de estos, en los países occidentales, podrían prevenirse mediante un cambio en el estilo de vida.
Posibles mecanismosMuchas moléculas o combinaciones de moléculas parecen ser capaces de desencadenar o promover el cáncer de mama; sobre los mecanismos involucrados:
- Una inhibición del sistema de respuesta al daño del ADN podría estar involucrada en la mitad de los cánceres de mama, especialmente aquellos que son iniciados o facilitados por hormonas utilizadas para los tratamientos hormonales de la menopausia.
- Una proteína ( Akt1 ) se sobreexpresa en el 50% de los cánceres de mama esporádicos. Por lo tanto, podría predisponer al cáncer de mama y / o estar involucrado por otros procesos (ambientales y no genéticos). La activación de AKT1 da como resultado eficazmente la inhibición por secuestro de la proteína BRCA1 en el citoplasma ; sin embargo, si esta proteína ya no puede penetrar y circular en el núcleo, el ADN ya no se repara (como en ausencia del gen BRCA1 en el caso de muchos cánceres hereditarios). AKT1 también es activada por hormonas sospechosas de causar cáncer de mama (de forma crónica en mujeres que reciben una terapia hormonal prolongada basada en estrógenos). En este caso, el gen BRCA1 no mutado puede alterarse, lo que aumenta el riesgo de cáncer de mama.
- Asimismo, otra proteína; La “proteína quinasa CK2” (una enzima importante para la plasticidad de las células epiteliales ) parece estar involucrada en la progresión de estos cánceres; la alteración de la actividad de esta proteína se acompaña de una transformación de células epiteliales en células cancerosas (más móviles y fuente de metástasis). Esta proteína normalmente parece prevenir el mecanismo celular llamado “ Transición Epitelial-Mesenquimal ” (EMT; proceso de evolución de las células epiteliales a un estado mesenquimatoso y movilidad, acompañado de resistencia a ciertos medicamentos contra el cáncer ). Esta enzima combina dos elementos; una "subunidad catalítica" (CK2α) y una "subunidad reguladora" (CK2β). Una disfunción de la subunidad CK2β, que permite a la EMT, parece estar involucrada en la producción de metástasis para este tipo de cáncer.
El cáncer de mama es a menudo un cáncer dependiente de hormonas: por lo tanto, los factores que aumentan los niveles de estrógeno están en riesgo. Básicamente, el riesgo de cáncer de mama aumenta con la cantidad de ciclos menstruales, ya sean artificiales ( píldora de estrógeno-progestágeno ) o naturales.
La terapia de reemplazo hormonal para la menopausia aumenta significativamente el riesgo de desarrollar cáncer de mama.
La menopausia tardía y la pubertad precoz actúan aumentando el número de ciclos menstruales y, por tanto, los niveles de estrógeno. Los factores de la pubertad precoz son: obesidad infantil, mayor consumo de proteínas animales (carne, leche ), consumo de bebidas azucaradas, exposición a disruptores endocrinos .
No fertilidad o fertilidad tardíaLas mujeres que no han tenido hijos o que tuvieron su primer embarazo tarde (después de los 30 años) tienen un riesgo significativamente mayor de desarrollar cáncer de mama, en comparación con aquellas que tuvieron al menos un hijo antes de los 30 años. De hecho, son los ciclos que preceden al primer embarazo llevado a término los que parecen más peligrosos para la mama. El embarazo protege la mama cambiando las células de la mama en la dirección de una mayor diferenciación. Las células diferenciadas son menos sensibles a los carcinógenos, en particular los hormonales. Por tanto, el embarazo actúa como una vacuna contra los estrógenos. Cuanto antes se produzca este primer embarazo, mejor funcionará.
Contaminantes y otros disruptores endocrinosLa Endocrine Society , en un comunicado elaborado por expertos internacionales, subraya el paralelismo entre el aumento de la incidencia de cáncer de mama en los últimos 50 años y la proliferación de disruptores endocrinos , químicos sintéticos con acción estrogénica o estrogénica. Estos innumerables productos (los más conocidos son DES , DDT , Bisfenol A y dioxinas ), de diversas fuentes ( pesticidas , químicos industriales, plásticos y plastificantes , combustibles y otros químicos omnipresentes en el medio ambiente), son una fuente importante de preocupación para los endocrinólogos. . Por lo tanto, las niñas que estuvieron muy expuestas en el útero en la década de 1960 al DDT tienen un riesgo cuádruple de cáncer de mama según un estudio publicado a mediados de 2015. La comida juega un papel importante.
La Endocrine Society emite una serie de recomendaciones dirigidas a
- aumentar la comprensión de los efectos de los disruptores endocrinos (incluso mediante investigación básica y estudios clínicos);
- invocar el principio de precaución ;
- abogar por la participación individual y la de las sociedades científicas para dar a conocer el problema;
- realizar cambios legislativos.
Por razones poco conocidas, la obesidad aumenta el riesgo de cáncer de mama y, en particular, de la rápida proliferación de este cáncer. Esto se ha demostrado tanto in vivo como in vitro ; así, cuando se cocultivan células tumorales ( murinas o humanas) con adipocitos maduros, estos últimos aumentan las capacidades invasivas del cáncer. En general, la obesidad duplicaría el riesgo de cáncer de mama.
La obesidad, al aumentar la cantidad de tejido graso, aumenta el nivel de estrógeno en la sangre al activar una enzima llamada aromatasa . De hecho, esto convierte las hormonas de tipo andrógeno en estrógenos . Esto continúa después de la menopausia ; Un estudio mostró un mayor riesgo de cáncer de mama en mujeres posmenopáusicas en función de su aumento de peso.
Los adipocitos cultivados con células cancerosas exhiben un fenotipo modificado en términos de desgrasamiento y una disminución de los marcadores de adipocitos asociados con una activación anormal caracterizada por sobreexpresión de proteasas , en particular metaloproteinasa -11, y citocinas proinflamatorias ( interleucina-6 (IL-6 ) o IL-1β.
Por el contrario, las células tumorales del cáncer de mama modifican las células grasas ( adipocitos ) de la mama. Estas últimas secretan en particular factores proinflamatorios , incluida la interleucina 6 (que in vitro es suficiente para que por sí sola haga metástasis en las células cancerosas) . Esto podría explicar por qué la obesidad aumenta el riesgo de metástasis y la rápida propagación de este cáncer. Queda por comprender los determinantes de los diálogos entre las células cancerosas y los adipocitos, y los tumores más grandes y / o los ganglios linfáticos contribuyentes muestran niveles más altos de IL-6 en el tumor circundante t adipocitos.
Los adipocitos peritumorales exhiben un fenotipo modificado y características biológicas lo suficientemente específicas como para ser llamados adipocitos asociados al cáncer (o CAA para los adipocitos asociados al cáncer ).
Se ha demostrado que el consumo de grasas animales y de ácidos grasos trans (que forman parte de la composición de muchos preparados en la industria alimentaria) son factores de riesgo. Esta relación entre el nivel de grasa animal ingerida y el cáncer de mama se conoce desde hace mucho tiempo. La influencia de los lípidos poliinsaturados es menos obvia
Un estudio (Inserm-Gustave-Roussy, 1995-1998) ha demostrado que el riesgo de cáncer de mama aumenta en casi un 50% en mujeres con un nivel alto de ácidos grasos trans en sangre , productos que pueden estar presentes en alimentos procesados. panes y galletas, pasteles, tortas, patatas fritas, masa para pizza.
Productos lácteosVarios estudios científicos retienen la leche como factor de riesgo de cánceres hormonodependientes como los de próstata, ovarios y mama. El aumento del riesgo estaría relacionado con el aumento del nivel de IGF-1 en la sangre, en sí mismo fuertemente correlacionado con el consumo de leche. Por tanto, el vínculo parece establecerse en la fase premenopáusica y también parece coherente con la ausencia de cáncer observada en la población con síndrome de Laron , que no produce IGF-1 . La concentración de IGF-1 varía mucho según el tipo de leche (vaca, cabra, oveja, etc.), si es liviana, o el método de cría de rumiantes ( somatotropina bovina ). Sin embargo, otros estudios establecen más bien un papel protector vinculado al contenido de la leche en vitamina D y / o calcio.
Consumo de alcohol y tabacoEl aumento del riesgo y la frecuencia del cáncer de mama está relacionado, al menos en parte, con el aumento del consumo de alcohol en las mujeres;
- Numerosos estudios han demostrado que el consumo de alcohol (sea lo que sea; vino , cerveza o licor fuerte ) aumenta el riesgo de cáncer de mama. Este riesgo aumenta en promedio un 30% con tres vasos de alcohol al día. Los metaanálisis han confirmado el papel del alcohol en la génesis o facilitación del cáncer de mama. Un estudio encontró que este riesgo estaba sobreestimado, pero fue refutado por un metanálisis basado en 98 estudios de casos y controles y estudios prospectivos.
- El riesgo aumenta alrededor de un 10% por cada 10 g de alcohol adicional consumido en promedio por día con diferentes sensibilidades genéticas dependiendo del individuo, ciertas subpoblaciones expuestas a otros factores de riesgo cancerígenos también pueden ser más sensibles a él. Este riesgo se ve agravado por otros factores: tener más de 50 años, estar en la fase posmenopáusica, estar afectado por una enfermedad benigna de la mama, un tumor que involucre receptores de estrógenos y / o tumores avanzados / invasivos.
- Este riesgo se duplica con el consumo crónico de alcohol (en mujeres con un índice de masa corporal normal (IMC <25), mientras que la obesidad es otro factor que se cita con frecuencia).
- Las consecuencias del alcohol como factor cancerígeno o cofactor en la mama podrían ser bastante rápidas, porque las estadísticas muestran que el impacto del consumo reciente es más significativo que el del consumo anterior.
Existe una correlación entre el tabaquismo y la aparición de este cáncer.
Falta de vitamina DLa vitamina D y sus análogos farmacéuticos tienen efectos antiproliferativos y prodiferenciación. Por tanto, es de importancia para la prevención y el tratamiento de los cánceres en general. En particular, puede limitar una producción excesiva de estrógenos , actuando sobre la aromatasa .
El cáncer de mama se asocia a menudo con niveles bajos de vitamina D (deficiencia o insuficiencia en el 78% de los casos según un estudio de 145 pacientes). Un exceso de mortalidad por cáncer (incluido el cáncer de mama) en los afroamericanos se atribuye a la pigmentación de la piel, que bloquea más rayos ultravioleta de los necesarios en estas latitudes y dificulta significativamente la producción de vitamina D. Un estudio francés de la evolución durante 10 años de casi 68.000 mujeres confirmó la importancia del vínculo entre la deficiencia de vitamina D y la aparición del cáncer de mama. El análisis del índice de exposición a los rayos ultravioleta en estas mujeres mostró que solo las que estaban más expuestas a los rayos ultravioleta lograron una protección suficiente contra el cáncer de mama para que la ingesta de alimentos tuviera un impacto mensurable; para todos los demás, el equipo del INSERM concluye que, cuanto más al norte se vive, más difícil es alcanzar este umbral de vitamina D, que protege contra el cáncer de mama.
Es un término vago para cualquier enfermedad de la mama. Generalmente se reserva para anomalías benignas que pueden dar lugar a confusión con un tumor y para ello justificar una muestra ( biopsia ) para identificarlas con precisión. Algunos pueden promover el cáncer posterior y ameritan un control regular.
Una apariencia densa en la mamografía, especialmente si es extensa, aumentaría significativamente el riesgo de desarrollar cáncer de mama.
OtroHistóricamente, se había encontrado en mujeres que se habían sometido a muchas fluoroscopias cuando la tuberculosis pulmonar era muy común. Este riesgo también se había detectado en mujeres japonesas que habían sido irradiadas a dosis no letales durante explosiones nucleares en Hiroshima o Nagasaki . Esto es esencialmente el comienzo del XXI º casos de siglo radioterapia del tórax en el tratamiento de ciertos tipos de cáncer - enfermedad de Hodgkin , en particular - en las mujeres jóvenes en los que el riesgo de cáncer de mama aumenta considerablemente. Ciertas modalidades nuevas de exámenes radiológicos, como la tomografía computarizada coronaria , pueden conducir a una irradiación suficiente para aumentar el riesgo de cáncer de mama décadas después de que se realiza el examen.
El trabajo nocturno podría aumentar el riesgo de cáncer de mama. Este riesgo ha sido legalmente reconocido en Dinamarca y está sujeto a una compensación económica.
La lactancia materna actúa como protector contra el cáncer de mama, en particular al poner los ovarios a dormir y reducir el número de ciclos.
La interrupción del embarazo no aumenta el riesgo de cáncer de mama
En los países ricos (no se han realizado estudios sobre este punto en otros lugares), una altura al nacer superior a la media se correlaciona con un riesgo futuro de desarrollar cáncer de mama. La exposición fetal a ciertas hormonas involucradas en el crecimiento podría estar involucrada (por confirmar). El 5% de los cánceres de mama en mujeres nacidas en países desarrollados se ven afectados directamente.
En los hombresEl 1% del cáncer de mama lo desarrolla un hombre. En la misma etapa, el pronóstico es idéntico. Sin embargo, la glándula mamaria en los hombres es muy pequeña, el diagnóstico suele ser tardío, por lo que hay muchos más cánceres detectados en estadio avanzado, acompañados de afectación cutánea o planos profundos (T4). El riesgo de contraer cáncer de mama aumenta en hombres con antecedentes familiares de cáncer de mama, especialmente cuando hay una mutación en los genes BRCA1 y BRCA2.
Cánceres familiares
Del 5 al 10% de los cánceres de mama diagnosticados son cánceres de mama con predisposiciones genéticas, es decir, entre 2.000 y 4.000 personas afectadas cada año, de 550 a 1.000 muertes, en Francia. En 2008, diez genes se asociaron con un mayor riesgo de cáncer de mama. Nueve están vinculados al sistema de respuesta al daño del ADN. El décimo codifica una proteína que inhibe la acción de la enzima AKT1 (una enzima cuya inhibición también juega un papel en los cánceres no genéticos). Dos de estos diez genes (llamados BRCA1 y BRCA2) son los únicos responsables de la mitad de estos cánceres genéticamente predispuestos, o del 2,5 al 5% de todos los cánceres de mama.
CaracteristicasMuy a menudo, este tipo de cáncer de mama aparece en una mujer sin ningún problema de salud en particular. Muy raramente, la mujer es portadora de una enfermedad genética conocida.
Varios signos pueden sugerir cáncer de mama con predisposición genética :
- Edad joven (promedio de 43 años en lugar de 60 años en formas no transmisibles);
- Antecedentes familiares de cáncer de mama;
- Cánceres que ocurren en ambos senos sucesiva o simultáneamente;
- Aparición de un segundo cáncer en el ovario ;
- Tipo histológico medular de cáncer.
Es de tipo autosómico dominante . En una mujer, la presencia de una sola mutación del gen expone un riesgo del 80% de desarrollar cáncer de mama (en lugar del 10% sin una mutación).
El riesgo que corren las mujeres que provienen de una familia donde hay un gen anormal depende de si lo han heredado o no. Si el gen heredado no es anormal, el riesgo es el mismo que el de otras mujeres; si el gen está mutado, tendrán entre un 70% y un 80% de posibilidades de desarrollar cáncer de mama. El problema es similar para los riesgos de cáncer de ovario o de colon . En algunas familias, estos cánceres se pueden observar en la línea directa (abuela, madre, hija) o en parientes cercanos (tía, hermana, prima hermana). Estos cánceres generalmente ocurren en la primera parte de su vida.
Una prueba genética puede resaltar este riesgo, pero una prueba para un gen mutado solo es segura si es positiva (en este caso, se debe hacer un seguimiento de todos los familiares). Este acto tan especializado solo debe ser solicitado para familias cuyas esposas probablemente presenten una herencia en riesgo, demostrado por una consulta oncogenética que establecerá el árbol genealógico de esta familia.
Genes involucradosSe identifican varios genes pero los dos principales son:
- BRCA1 en el cromosoma 17 . Ya se han descrito más de 500 mutaciones o variaciones de secuencia.
- BRCA2 en el cromosoma 13 . Se han contado más de 100 mutaciones diferentes.
Solo una parte de todas estas mutaciones aumentan el factor de riesgo de cáncer. Las mutaciones del BRCA2 (1 en 1460) se encuentran con más frecuencia que las mutaciones del BRCA1 (1 en 1960). Estas mutaciones provocan, además del riesgo excesivo de cáncer de mama, un riesgo excesivo de cáncer de ovario.
La probabilidad de desarrollar cáncer de mama en una portadora de una mutación BRCA1 es aproximadamente del 65% antes de los 70 años (45% para las portadoras de una mutación BRCA2 ).
La evolución de los cánceres portadores de mutaciones BRCA1 es todavía poco conocida: empeoramiento según algunos, para otros, gravedad similar para portadores de mutaciones BRCA2 o no portadores de mutaciones.
La prevalencia de estas mutaciones sigue siendo baja en pacientes con cáncer de mama (menos del 4% para BRCA1 , aunque es el doble en judíos Ashkenazi).
Los otros genes afectados son PALB2, que participa en la estabilización de BRCA2 , ATM , CHEK2 , RAD51C , BARD1 o TP53 .
Asesoramiento geneticoEn algunos países, cualquier mujer que desee hacerlo puede beneficiarse del asesoramiento genético para determinar su riesgo de cáncer hereditario. Si la probabilidad de predisposición genética es superior al 25%, a estos pacientes se les ofrece un diagnóstico molecular. Esta investigación molecular es particularmente predictiva si conocemos la mutación en un padre que ya padece cáncer de mama con predisposición genética.
Vigilancia de mujeres de alto riesgoLas mujeres en riesgo de predisposición genética o portadoras de una mutación son monitoreadas por equipos de vigilancia clínica cada 6 meses a partir de los 20 años y mediante mamografías anuales a partir de los 30 . Entre los factores que aumentan el riesgo se encuentran la existencia de carcinoma ductal in situ , considerado una forma precancerosa, y el carcinoma lobulillar in situ , que es más leve pero puede convertirse en cáncer en 20 a 30% de los casos identificados.
Poner en pantalla
La detección y el tratamiento de tumores cuando son muy pequeños (menos de un centímetro de diámetro) es posible gracias a la mamografía y al seguimiento periódico. Esto reduce el riesgo de mortalidad y permite tratamientos menos pesados y menos traumáticos que la quimioterapia , la cirugía de “mutilación” (ablación). Es entre las edades de 50 y 74 cuando las mujeres están más expuestas a este tipo de cáncer. Una mamografía cada dos años permite un cribado eficaz, pero que expone un riesgo de sobrediagnóstico correspondiente a un falso positivo : se considera que la mujer tiene cáncer de mama cuando no lo es, exponiéndola así a un tratamiento injustificado con todos los efectos secundarios y los riesgos. que siguen. Por lo tanto, el beneficio de este examen debe documentarse cuidadosamente. Según un metanálisis de 2003, en algunos casos se puede demostrar una reducción significativa en la mortalidad por detección; sin embargo, el mismo metanálisis informa de otros dos estudios en competencia que no muestran una reducción significativa. Sin embargo, se critica esta existencia de reducción del riesgo.
En Francia, una estructura de gestión departamental o interdepartamental envía a todas las mujeres de 50 a 75 años una invitación para una mamografía gratuita (100% de apoyo financiero de la Seguridad Social) cada dos años. La invitación se puede enviar a petición del médico de cabecera , del ginecólogo o de la propia mujer. La visita debe realizarse a un radiólogo acreditado, miembro de la red especializada en cribado configurada a nivel de los departamentos. Esta estrategia se basa en particular en un informe de expertos elaborado en 2001-2 por el Departamento de Evaluación de Tecnología de la Agencia Nacional de Evaluación y Acreditación de la Atención Sanitaria. El objetivo declarado de este informe incluía un recordatorio de las recomendaciones francesas vigentes. El informe concluyó que, dado que no se ha demostrado la ineficacia de la mamografía de detección, deben mantenerse las recomendaciones en uso para la detección del cáncer de mama.
Una ecografía asociada a la mamografía puede detectar un mayor número de cánceres pero se asocia a un mayor número de falsos positivos (biopsia que invalida el diagnóstico de cáncer). Por tanto, queda por evaluar el lugar de este examen en la estrategia de detección.
La resonancia magnética (MRI) también sería una prueba prometedora con mayor sensibilidad que la mamografía.
Auto - examen era una técnica de detección muy popular en los años 1980 y 1990, todavía se recomienda, pero no se ha demostrado eficaz.
El uso de la termografía infrarroja, para la detección, es un examen con menos efectos secundarios (sin radiación), con mejor sensibilidad , menos falsos positivos y detección más temprana que la mamografía. El coste de la termografía también sería sensiblemente inferior al del cribado por mamografía, cuyo presupuesto anual es de 250 millones de euros. Sin embargo, en 2017, la termografía apenas se utilizó en Francia. La técnica mostró su sencillez a través de una noticia.
Más allá de los 75 años, no se ha demostrado el beneficio del cribado sistemático. Parece ser débil entre los 70 y los 75 años. Antes de los 50 años, el interés es discutible, sin disminución comprobada de la mortalidad.
Sobrediagnóstico
Antes de la menopausia , no se ha demostrado que la detección sistemática sea eficaz porque son comunes las anomalías sospechosas mínimas. En este caso, las desventajas parecen superar las ventajas, excepto para las mujeres en situación de riesgo.
El riesgo de un cribado sistemático es realizar un diagnóstico incorrecto y dar lugar a un tratamiento injustificado, con un coste y un riesgo como consecuencia. A esto se le llama sobrediagnóstico . En el cáncer de mama, la mamografía puede conducir a una tasa significativa de sobrediagnóstico. Esta proporción podría oscilar entre uno de cada diez y uno de cada cuatro, o incluso uno de cada dos. La relación entre el número de vidas salvadas y el número de mujeres con un sobrediagnóstico (que refleja parcialmente lo que se denomina relación beneficio / riesgo de un examen) puede variar de 1 en 2 a 1 en 10.
La explicación de estos sobrediagnósticos no es inequívoca: mala interpretación de documentos, cánceres de muy lenta evolución o incluso regresión espontánea de determinados tumores malignos.
Sin embargo, según el departamento de enfermedades crónicas del Instituto Francés de Vigilancia en Salud Pública , estos análisis deberían permitir en el futuro hacer el cribado aún más eficiente con el objetivo de identificar cánceres que evolucionarán de aquellos que permanecerán latentes, sin cuestionar el beneficio de la detección en sí.
Pechos densos
Para senos densos o extremadamente densos, una mamografía puede ser ineficaz para detectar el cáncer. Los estudios han medido que las mamografías no detectan el cáncer en casi un tercio a la mitad de los casos de mujeres con senos densos .
El tejido mamario denso interfiere con la capacidad de detectar cáncer con una mamografía. Actuando como una nube, el tejido mamario denso es blanco y puede enmascarar el cáncer que también parece blanco.
La densidad mamaria se puede medir mediante BI-RADS utilizando un sistema de puntuación de 1 a 4. Este sistema permite a los radiólogos medir y describir la densidad de las mamas.
BI-RADS 1: Tejido mamario denso <25% BI-RADS 2: Tejido mamario denso entre 26 y 50% BI-RADS 3: Tejido mamario denso entre 51 y 75% BI-RADS 4: Tejido mamario denso> 75%
Casi la mitad de las mujeres en los Estados Unidos tienen senos densos. En algunos estados, los radiólogos tienen la obligación legal de proporcionar a las mujeres la densidad de sus senos para que puedan tener una conversación informada con su equipo de atención médica sobre las pruebas adicionales que podrían necesitar.
Cinco hechos sobre el tejido denso en la mama:
. El 40% de las mujeres tienen senos densos. . La densidad mamaria es uno de los predictores más fiables de la ineficacia de la mamografía para detectar el cáncer existente. . la mamografía no detecta un cáncer existente en un tercio a la mitad de los casos según los estudios, para los senos densos. . La densidad mamaria es un predictor bien establecido del riesgo de cáncer de mama. . La alta densidad mamaria es un factor de riesgo más alto que tener dos parientes de primer grado con cáncer de mama.
Una ecografía combinada con una mamografía puede detectar una mayor cantidad de cánceres para mamas densas e hiperdensas. En una ecografía, algunos cánceres de mama aparecen de color negro y, por lo tanto, pueden detectarse. Una ecografía de mama no es suficiente por sí sola para la detección del cáncer de mama.
Otro tipo de exploración es la resonancia magnética.
Otro tipo de análisis se ha desarrollado en los Estados Unidos para superar la ineficacia de las mamografías para detectar el cáncer de senos densos. La imagen molecular de mama (MBI) es una herramienta de diagnóstico secundario muy eficaz .
Incluso con un resultado de mamografía negativo para mujeres con senos densos (o que se consideran en alto riesgo de cáncer de mama), se debe considerar la realización de pruebas de MBI adicionales.
Una imagen MBI representa un análisis funcional molecular activo de los tejidos debido a la toma de un radiomarcador inyectado en las venas. En estas imágenes, el tejido sano, denso o no, aparece en negro y el tejido enfermo aparece en blanco, debido a la absorción más rápida de los rayos gamma contenidos en la cavidad del radio-trazador.
Diagnóstico
Clínico
La palpación de la mama es el primer examen que se realiza. Debido a su ubicación anatómica, los senos son fáciles de palpar, especialmente cuando son de tamaño mediano o pequeño. Se recomienda que los pacientes realicen esta prueba ellos mismos de forma rutinaria al final de la menstruación.
Durante la palpación, la sospecha se basa en el descubrimiento de un nódulo , que puede detectarse mediante palpación desde aproximadamente 1 cm de diámetro. La irregularidad puede no ser dolorosa, pero cualquier anomalía reciente debe atraer especialmente la atención de la paciente y su médico.
Entre las irregularidades que el paciente puede observar por su cuenta:
- un hoyuelo o una arruga que ahueca la superficie del pecho con una apariencia de "piel de naranja";
- una deformación del pezón , retrayéndolo hacia adentro;
- una apariencia eccematosa del pezón que se enrojece, se vuelve costrosa o se erosiona;
- Secreción del pezón, especialmente si es sanguinolenta o negruzca.
La observación de uno de estos signos debería llevar a una consulta médica muy rápidamente. Sin embargo, solo el médico podrá juzgar qué exámenes adicionales son necesarios, porque todos estos signos no se encuentran solo en el caso de los cánceres. Un nódulo puede ser de naturaleza benigna:
- cuando es de consistencia sólida, puede ser un adenofibroma que se ha desarrollado en la glándula mamaria. Esto podría desarrollarse debido a un entorno bacteriano específico, que puede o no convertirse más tarde en adenocarcinoma .
- cuando es de naturaleza líquida, puede ser un quiste .
Mamografía
El médico puede decidir que su primer diagnóstico se confirme mediante una mamografía . La ecografía es un examen complementario que puede ayudar a localizar la falla para facilitar la extracción o reconocer si se trata de un quiste lleno de líquido, pero nunca puede reemplazar la mamografía. La mamografía, que se realiza con regularidad y como parte de los programas de cribado , permite diagnosticar la enfermedad en una fase lo suficientemente temprana como para que el tratamiento sea lo más conservador posible y al mismo tiempo eficaz. De hecho, siempre que el tamaño del tumor sea inferior a 1-2 cm, las posibilidades de recuperación son cercanas al 100%.
Confirmación del diagnóstico
Si todos los exámenes aún no permiten asegurar un buen diagnóstico y si persisten las dudas, entonces es necesario considerar una muestra tomada con mayor frecuencia con una aguja grande (trocar) bajo anestesia local sin hospitalización. La muestra, o biopsia , a menudo se realiza con una guía de ultrasonido o radiología; se habla entonces de guiada por ultrasonido biopsia y biopsia estereotáxica de mama. El diagnóstico de certeza se realizará mediante el estudio anatomopatológico de la muestra tomada.
Evaluación de la extensión
La búsqueda de metástasis es fundamental en la estrategia de tratamiento del cáncer de mama. Pero, a pesar de los numerosos estudios realizados o del conocimiento en profundidad de determinadas exploraciones, actualmente no existe una estrategia validada para la búsqueda sistemática de metástasis en el cáncer de mama.
La mayoría de las recomendaciones proponen actualmente un estudio de extensión que incluye radiografía de tórax, ecografía hepática y gammagrafía ósea. Para tumores muy pequeños, esta evaluación puede ser opcional. Por otro lado, para los tumores avanzados (inflamatorios, tumores multifocales, invasión significativa de los ganglios linfáticos), el riesgo metastásico inicial es alto y puede justificar una evaluación más profunda que incluya una tomografía computarizada (TC) de cuerpo entero y una resonancia magnética de mama. .
El tamaño del tumor, la existencia de adenopatías metastásicas, la existencia de afectación de la piel o de la pared torácica o de metástasis a distancia permiten establecer una clasificación clínica de los cánceres de mama.
| Clasificación TNM | Descripción |
|---|---|
| Tx | Tumor que no se puede evaluar por falta de información |
| T0 | Sin evidencia de tumor primario |
| Es | Carcinoma ductal in situ o carcinoma lobulillar in situ o enfermedad de Paget del pezón sin tumor subyacente |
|
T1 T1a T1b T1c |
Tumor menor de 2 cm en su dimensión más grande - T <0.5 cm - T entre 0.5 y 1 cm - T entre 1 y 2 cm |
| T2 | Tumor mayor de 2 cm y menor de 5 cm en su dimensión más grande |
| T3 | Tumor de más de 5 cm en su dimensión más grande |
|
T4 T4a T4b T4c T4d |
Tumor de cualquier tamaño con extensión: - a la pared torácica - edema o ulceración o nódulo de permeación de la piel - a la piel y la pared torácica Cáncer inflamatorio |
Diferentes tipos de cáncer de mama y carcinoma.
Clasificación de la OMS
El estudio anatomopatológico muestra la existencia de diferentes tipos de cáncer de mama. Según la Organización Mundial de la Salud , la siguiente tabla muestra la clasificación histológica de los cánceres de mama utilizados en todos los centros oncológicos.
Como con cualquier epitelial tumor, no son cánceres en situ . La variedad más común de cáncer de mama es el tipo ductal .
| Tumores epiteliales no infiltrantes |
| Carcinoma ductal in situ (intracanal) (DCIS) |
| Carcinoma lobulillar in situ (CLIS) |
| Infiltración de tumores epiteliales |
| Carcinoma ductal invasivo SAI (sin otra indicación) |
| Carcinoma ductal invasivo con componente intracanal predominante |
| Carcinoma lobulillar invasivo |
| Carcinoma mucinoso (coloide) |
| Carcinoma medular |
| Carcinoma papilar |
| Carcinoma tubular |
| Carcinoma adenoide quístico |
| Carcinoma secretor juvenil |
| Carcinoma apocrino |
| Carcinoma metaplásico de células escamosas |
| Carcinoma metaplásico de células fusiformes |
| Carcinoma condroide y metaplásico óseo |
| Carcinoma metaplásico de tipo mixto |
| Enfermedad de Paget del pezón |
Cáncer inflamatorio
El cáncer de mama inflamatorio es una forma muy rara de cáncer de mama (1-4%) que se desarrolla rápidamente en unos pocos días o semanas. Se propaga rápidamente por la vía linfática sin tener tiempo de formar un tumor. El bloqueo de los vasos linfáticos por las células cancerosas es la causa de una inflamación local de la mama en diversos grados. El diagnóstico de absceso mamario a menudo se menciona inicialmente, especialmente porque las imágenes (mamografía y ecografía) suelen ser negativas. Cualquier persistencia de un enrojecimiento de la mama más o menos doloroso requiere biopsias, que por sí solas confirmarán la enfermedad. El tratamiento se basa fundamentalmente en la quimioterapia, cuyos avances recientes han permitido curar en un gran número de casos.
Clasificación histológica y molecular
En el contexto de la investigación del cáncer de mama, cuatro tipos de cáncer de mama se distinguen principalmente según su morfología y la presencia de tres marcadores moleculares: el del receptor de estrógenos (RE) y la sobreexpresión del receptor. Progesterona (PR), y el Marcador HER2 , siendo este último un receptor de tipo EGFR. Las cuatro clases resultantes son:
- Basal o triple negativo: ER- / PR- / HER2-
- Sobreexpresión de HER2: ER- / PR- / HER2 +
- Luminal A: ER + / PR + / HER2-
- Luminal B: ER + / PR + / HER2 +
El nombre de los tipos basal y luminal proviene de la semejanza de los tumores con los correspondientes tejidos epiteliales mamarios normales. En general, los cánceres basales y que sobreexpresan HER2 tienen un pronóstico clínico precario.
Los estudios basados en el uso de chips de ADN sistemáticamente en cohortes de pacientes también pudieron aislar diferentes firmas de expresión génica y los cánceres de mama de tipo luminal tienden a expresar genes y proteínas GATA3 , KRT19 luego que los de tipo basal por otro lado lo hacen no expresan estos pero entre otros ETS1 y CD44 .
Tratos
Como ocurre con todos los cánceres, lo ideal es (desde un punto de vista médico) sobre la extirpación quirúrgica del tumor, que al mismo tiempo permite hacer el diagnóstico con certeza. El siguiente problema es hacer la valoración de la extensión : presencia o no de ganglios linfáticos afectados, presencia o ausencia de metástasis.
Sin embargo, la mutilación de los senos también corresponde generalmente para las mujeres a la mutilación psicológica y social, siendo los senos uno de los símbolos más fuertes de la feminidad. Algunas mujeres pueden experimentar esta mutilación como una negación de su feminidad y, por tanto, de su personalidad.
También existen otros tratamientos como la quimioterapia , la radioterapia y la terapia hormonal , que en algunos casos se pueden utilizar para reducir el tumor antes de la cirugía. La efectividad y los riesgos de cada tipo de tratamiento dependen del tipo de cáncer, su extensión y el sitio.
Estrategia terapéutica
Existen muchos tratamientos para el cáncer de mama, pero siempre deben individualizarse para un tratamiento óptimo. Por tanto, el análisis genómico del cáncer de mama revelaría alrededor de cincuenta tipos diferentes de cáncer de mama, cada tipo o grupo de los cuales sería susceptible a una terapia dirigida particular.
Para el cáncer de mama localizado, el tratamiento casi siempre tiene un objetivo curativo. Se basa en las cuatro armas terapéuticas que son la cirugía, la quimioterapia, la radioterapia y la terapia hormonal. La cirugía es un paso esencial en la cura del cáncer de mama, y otros tratamientos generalmente solo tienen como objetivo reducir el riesgo de recaída. Por tanto, estarán indicados si este riesgo es significativo y si el supuesto beneficio del tratamiento es suficiente, porque todos estos tratamientos tienen efectos secundarios. Por tanto, el beneficio esperado debe sopesarse con el riesgo de complicaciones.
Para el cáncer de mama metastásico: en esta etapa de desarrollo, es muy raro poder ofrecer un tratamiento curativo. Pero los tratamientos modernos a menudo permiten prolongar la supervivencia varios años. Es imposible detallar aquí las diferentes estrategias terapéuticas posibles porque dependen de una gran cantidad de factores. El tratamiento del cáncer de mama metastásico comienza con quimioterapia y terapia hormonal. El tratamiento quirúrgico o de radioterapia de los sitios metastásicos se puede considerar con un propósito curativo cuando todos los sitios son accesibles para el tratamiento (p. Ej., Metástasis hepática o vertebral única) o con fines paliativos ( p. Ej., Irradiación de una metástasis en un hueso doloroso).
Hay una serie de marcadores genéticos que se correlacionan con el pronóstico del cáncer de mama y, por lo tanto, pueden guiar potencialmente el tratamiento.
De los marcadores moleculares de gravedad y el pronóstico de cáncer de mama también existir. La metalotioneína (MT) es una. Se unen fácilmente a ciertos metales y están codificados por al menos 10 genes MT funcionales que están asociados con la proliferación de células de cáncer de mama, en particular cánceres de mama ductales invasivos. Esto hace que la MT sea un biomarcador de pronóstico para el cáncer de mama detectable por inmunohistoquímica . Cuantas más MT se expresen en el cáncer de mama, más severo será el cáncer.
Algunos tratamientos (agentes alquilantes o tamoxifeno ) pueden inhibirse por la sobreexpresión de metalotioneína (por ejemplo, en un paciente que ha sufrido intoxicación por metales pesados)
Cirugía
Extirpación de tumoresHay tres tipos de cirugía de mama: tumorectomía (extirpación del tumor), segmentectomía (extirpación de parte de la mama) y mastectomía (extirpación de toda la mama).
En los casos en que el tumor se trata lo suficientemente temprano, es posible una cirugía mínima (cirugía conservadora). A veces hay que extirpar todo el seno. La cirugía reconstructiva se puede realizar al mismo tiempo o de forma secundaria.
- Ilustración de cirugía reconstructiva de mama: recuperación de parte de los músculos del abdomen ( restus abdominus ) para reconstruir la mama, Instituto Nacional del Cáncer .
Esta técnica consiste en la extirpación de los ganglios linfáticos ubicados en el hueco axilar (a nivel de la axila). Esta operación tiene muchos efectos secundarios porque esta ablación desestabiliza la red linfática , lo que puede llevar a la aparición de linfedema (brazo grande). Es con el objetivo de reducir estos efectos secundarios que se implementó la técnica del ganglio centinela .
Técnica del ganglio centinelaEn un tumor, el ganglio centinela es el primero en recibir drenaje linfático.
El ganglio centinela se identifica mediante la inyección de un tinte, acompañado o no de un coloide radiactivo. Luego se retira para permitir un estudio anatomopatológico. Si el ganglio estudiado está sano, esta técnica evita tener que recurrir a la disección axilar (extirpación de casi todos los ganglios de la región), lo que daría lugar a secuelas importantes. Puede aplicarse a pacientes con un tumor de menos de 3 centímetros, y afectar hasta al 70% de ellos.
Esta técnica está validada, con una tasa de error inferior al 10%.
Prevención del dolor postoperatorio.Se puede obtener una reducción del riesgo de dolor posoperatorio crónico realizando anestesia locorregional en el momento de la cirugía. De tres a doce meses después de la cirugía de cáncer de mama, el dolor posoperatorio crónico se puede prevenir en una de cada siete personas ( número de personas a tratar ). Aunque alentadores, estos resultados se basan en pruebas de bajo nivel.
Monitoreo posoperatorioDespués del tratamiento inicial, es fundamental que el paciente se controle periódicamente.
No son necesarios más exámenes, pero la mamografía bilateral anual es esencial, especialmente en caso de cirugía conservadora. Dependiendo del caso, se puede combinar con otros exámenes adicionales definidos según cada caso.
Incluso el cáncer de mama tratado de manera óptima puede reaparecer localmente o a distancia ( metástasis ). La recurrencia puede ocurrir años después del tratamiento inicial, de ahí la importancia de mantener la vigilancia.
Radioterapia
Reduce la mortalidad de este cáncer, pero requiere de una técnica irreprochable para reducir la irradiación de tejidos sanos que puede conducir a un exceso de mortalidad por patología cardiovascular. Se hace una distinción entre la radioterapia de la mama y la de las áreas de los ganglios linfáticos. En caso de cirugía conservadora, siempre se debe realizar radioterapia porque reduce significativamente el riesgo de recurrencia local. La radioterapia será más importante cuanto más joven sea la mujer. En caso de extirpación total de la mama, la radioterapia está indicada, en determinados casos, para reducir el riesgo de recidiva local. La irradiación de las cadenas ganglionares depende de la ubicación del tumor y del resultado del examen anatomopatológico de los ganglios.
Efectos secundarios a largo plazoEl riesgo de muerte secundaria a la radioterapia en comparación con el de mortalidad cardiovascular no parece aumentar hasta la tercera década después del tratamiento, según un estudio que monitorea a más de 500.000 mujeres.
Un estudio europeo sobre los riesgos para el feto en el contexto de la radioterapia o quimioterapia para el tratamiento del cáncer ha demostrado que los fetos cuyas madres han sido tratadas durante el embarazo no tienen más defectos cardíacos que un niño no expuesto.
Para identificar los riesgos de fibrosis mamaria inducida por radioterapia, Inserm ha desarrollado una prueba para medir la "tasa de apoptosis linfocítica radioinducida (TALRI)". Cuanto mayor sea el nivel de TALRI, menor será el riesgo de fibrosis mamaria.
Quimioterapia
Consiste en administrar fármacos anticancerosos a intervalos fijos, generalmente cada 3 semanas. El número de ciclos de quimioterapia adyuvante (quimioterapia realizada después de la cirugía) para el cáncer de mama es de 4 a 6. Las ventajas de la quimioterapia adyuvante sobre el tratamiento quirúrgico sin quimioterapia son una reducción significativa de la mortalidad y una tasa de recurrencia más baja. En caso de afectación de los ganglios linfáticos axilares, el esquema que combina 3 ciclos de quimioterapia con antraciclina (Farmorubicin °) y ciclofosfamida (Endoxan °) y luego 3 ciclos con docetaxel (Taxotere °) es actualmente la referencia. Para los cánceres sin invasión ganglionar axilar, la búsqueda de factores con mal pronóstico que puedan explicar un desenlace desfavorable (alto grado histológico, ausencia de receptores hormonales, tamaño tumoral mayor de 15 o incluso 10 mm para algunos, etc.) también lo hace posible para indicar la indicación de 'quimioterapia adyuvante.
En el caso de un tumor avanzado o inflamatorio, a veces es necesario iniciar el tratamiento con quimioterapia ( quimioterapia neoadyuvante ) para reducir el tamaño del tumor y posiblemente permitir una cirugía conservadora.
La quimioterapia neoadyuvante también se utiliza para limitar el tamaño de la escisión: en ocasiones, una tumorectomía es suficiente cuando se planificó inicialmente una mastectomía con quimioterapia adyuvante.
En esta última indicación, mientras que la mortalidad global, el tiempo hasta el empeoramiento de la enfermedad y la tasa de recidiva a distancia no son diferentes de la quimioterapia adyuvante, las recidivas locorregionales son más frecuentes. Actualmente no existe un protocolo estándar de quimioterapia neoadyuvante.
Contras: fatiga general, náuseas y vómitos, caída temporal del cabello. Varían según los productos utilizados, y se controlan mejor y mejor.
Se ha demostrado que varios productos son eficaces en el tratamiento adyuvante del cáncer de mama y tienen un protocolo de referencia, pero otros productos están entrando en el mercado y / o se están estudiando.
Terapias dirigidas
El trastuzumab revolucionó el tratamiento de muchos pacientes. Se están evaluando otros fármacos. Estas moléculas a menudo se caracterizan por una buena tolerancia, sin embargo, son productos particularmente costosos.
TrastuzumabAlgunos cánceres de mama sobreexpresan significativamente el gen Her2 (esto afecta a alrededor del 25% de los cánceres de mama, a menudo con mal pronóstico, ya que Her2 , o CerbB2 , es el receptor de membrana que permite activar una de las vías para una mayor proliferación celular). Las células cancerosas luego exhiben una adicción oncogénica , y su supervivencia depende del funcionamiento de la vía de señalización inducida por Her2 . Esto es inhibido por trastuzumab (Herceptin °), un anticuerpo monoclonal que bloquea este receptor. Herceptin se utilizó por primera vez en una situación paliativa. En este contexto, Herceptin permitió, en promedio, duplicar el tiempo de supervivencia de estos pacientes. Agregado a la quimioterapia adyuvante, Herceptin ° administrado cada 21 días durante 12 meses reduce el riesgo de recaída en pacientes con HER2 + a la mitad y la mortalidad en aproximadamente un tercio.
Desde noviembre de 2017, Ontruzant, un fármaco biosimilar de trastuzumab , cuenta con la primera autorización de comercialización emitida por la Comisión Europea , permitiendo su distribución en la Unión Europea así como en Noruega , Islandia y Liechtenstein .
BevacizumabEn 2007 , se utilizó bevacizumab ( Avastin ) en el cáncer de mama metastásico (autorización de comercialización en Francia en 2007, metastásico de primera línea). Es un anticuerpo monoclonal anti- VEGF , administrado por infusión. Se une selectivamente a este factor de crecimiento y por lo tanto bloquea neo- angiogénesis . Combinado con paclitaxel , este tratamiento duplica el tiempo de respuesta (tiempo hasta la progresión de la enfermedad). Por otro lado, no aumenta el tiempo de supervivencia.
Sin embargo, en Francia, en mayo de 2011 , la Haute Autorité de Santé concluyó: “Dada la baja ganancia en la supervivencia sin recurrencia y la falta de mejora en la supervivencia general con la combinación de bevacizumab / taxano versus taxano, el beneficio de agregar bevacizumab al paclitaxel está menos establecido en la actualidad. Este interés se limita a pacientes que son negativos para los receptores HER2 , estrógeno y progesterona . " .
LapatinibEl lapatinib ( Tyverb ) administrado por vía oral es un inhibidor de la tirosina intracelular de la actividad quinasa del receptor HER2 y HER1 (EGFR). En pacientes que sobreexpresan HER2, en progresión tumoral con herceptin y que ya han recibido antraciclinas y taxanos, la combinación lapatinib- capecitabina duplica el tiempo de respuesta en comparación con capecitabina sola, sin beneficio sobre la supervivencia global. La autorización de comercialización se obtuvo en 2008.
Terapia hormonal
En aproximadamente dos tercios de los cánceres de mama, las células cancerosas tienen un exceso de receptores hormonales. Entonces se dice que el tumor es sensible a las hormonas porque el estrógeno estimula la proliferación cancerosa a través de estos receptores. En el cáncer de mama, los tratamientos hormonales actuarán reduciendo el nivel de estrógeno en sangre y, por tanto, estimulando los receptores hormonales (castración, anti-aromatasas), o bloqueando los receptores hormonales ( anti-estrógeno ).
Supresión ovárica- quirúrgico, por laparotomía o laparoscopia
- radiación, haciendo de 12 a 16 Gray en 4 a 8 fracciones sobre una pelvis pequeña, después de haber identificado la posición de los ovarios por ecografía;
- Médico, generalmente con agonistas LHRH
- Leuprorelina , Enantone LP 3,75 mg / 4 sem
- Goserelina , Zoladex 3.6 mg / 4 semanas
- Nota: Decapeptyl no tiene autorización de comercialización en cáncer de mama.
-
Tamoxifeno 20 mg d −1
- Mecanismo: antagonista parcial del receptor de estradiol
- Precaución: realizar un examen endometrial 1 / año, controlar la función hepática y los triglicéridos, dosificar estradiol en el plasma y añadir LHRH si aumenta, anticoncepción eficaz (teratogénica).
-
Fulvestrant 250 mg IM cada 28 días
- Mecanismo: antagonista del receptor de estrógenos sin acción agonista parcial.
El uso de tamoxifeno es beneficioso si hay receptores de estrógeno en el tumor independientemente de la edad del paciente. La duración óptima de la aplicación de la terapia hormonal adyuvante con tamoxifeno es de 5 años a una dosis de 20 mg d -1 . El uso de tamoxifeno reduce el riesgo de recurrencia en un 8% y el riesgo de muerte en un 5%.
Anti-aromatasasDesde 2004, se pueden ofrecer nuevas moléculas a mujeres posmenopáusicas. Estos son los inhibidores de la aromatasa . Las dos moléculas más evaluadas son anastrozol y letrozol . Su perfil de toxicidad es diferente al del tamoxifeno. La administración de estas dos moléculas permite reducir las recaídas después de la cirugía de cáncer de mama, sin beneficio en términos de supervivencia global ( frente al tamoxifeno).
-
Letrozol , Femara 2,5 mg d −1
- Mecanismo: inhibidor de la aromatasa no esteroideo
- Precaución: densidad ósea, dislipidemia
-
Anastrozol , Arimidex 1 mg
- Mecanismo: inhibidores de la aromatasa no esteroideos
- Precaución: densidad ósea, dislipidemia
-
Exemestano , Aromasin 25 mg
- Mecanismo: inhibidor de la aromatasa de esteroides
- Precaución: densidad ósea, dislipidemia
Prevención: cómo reducir el riesgo
Sabiendo que el cáncer de mama es una enfermedad hormonal, teóricamente se supone que es eficaz cualquier acción o terapia dirigida a reducir la duración e intensidad de la exposición al estrógeno oa los disruptores endocrinos que imitan estos estrógenos.
Acciones o eventos que reducen el riesgo
Se pueden tomar varios tipos de acciones para reducir el riesgo de desarrollar cáncer de mama.
Opciones ginecológicasLos factores de riesgo tienen un denominador común: el aumento de la impregnación hormonal de la mujer: directo, para los tratamientos hormonales de la menopausia, la píldora estrógeno-progestágeno, el aumento del número de ciclos menstruales (bajo número de embarazos o tiempos de lactancia cortos), o indirectamente a través del aumento de la actividad de la enzima aromatasa en grasas, por alcohol, sobrepeso, falta de actividad física. Así, se podría proponer una prevención primaria del cáncer de mama, que implique una modificación del estilo de vida.
La elección de la píldora anticonceptiva.Esto es para favorecer las píldoras que no contienen estrógenos que bloquean la actividad ovárica.
Un primer embarazo a temprana edadDisminuir la edad del primer embarazo reduce el riesgo de cáncer de mama porque los ciclos entre la pubertad y el primer embarazo a término parecen los más peligrosos desde este punto de vista. El primer embarazo llevado a término actuaría como una vacuna contra el cáncer al diferenciar los tejidos haciéndolos menos vulnerables a las hormonas. Por tanto, el embarazo actúa como una vacuna contra los estrógenos. Cuanto antes se produzca este primer embarazo, mejor funcionará.
Lactancia materna prolongadaLa lactancia materna prolongada (porque poner los ovarios "a dormir" ) reduce el riesgo. Según el informe de WCRF , la lactancia materna aporta beneficios independientemente de cuándo se desarrolle el cáncer (antes o después de la menopausia ).
Evitar la terapia hormonal de la menopausia (TRH)"El tratamiento hormonal para la menopausia ahora se considera un factor de riesgo para el cáncer de mama, especialmente cuando se toma durante más de 5 años", informó Le Figaro en 2008.
Elección de estilo de vida Pérdida de pesoLa obesidad y el sobrepeso aumentan el riesgo de cáncer de mama. El profesor Pierre Kerbrat (centro Eugène-Marquis, Rennes) estimó en 2008 que la lucha contra la obesidad femenina evitaría 13.000 nuevos casos de cáncer de mama al año en la Unión Europea.
Ejercicio físicoSegún el profesor Kerbrat, la práctica de 30 minutos de actividad física, 5 días a la semana, reduciría el número de nuevos casos entre un 30% y un 40%. El efecto protector proviene tanto de la lucha contra la obesidad como de la acción del ejercicio sobre las secreciones hormonales. Los estudios estadounidenses también han demostrado su efecto preventivo contra la recurrencia de la enfermedad.
Reducir el consumo de alcoholEl riesgo de cáncer de mama aumenta con la ingesta de alcohol. El consumo moderado de alcohol aumenta el riesgo entre un 20% y un 30%. Más precisamente, el riesgo aumenta en un 10% cuando el consumo diario de alcohol aumenta en 10 g de alcohol (es decir, un vaso).
Opciones de comidaReducirían el riesgo.
- Realizado mediante cuestionarios de 334.850 mujeres de 35 a 70 años e incluidas en la cohorte EPIC (Investigación prospectiva europea sobre el cáncer y la nutrición) (duración del seguimiento: 11,5 años), un estudio fechadoabril 2013muestra que no existe relación entre el consumo de flavonoides y lignanos ( fitoestrógenos ) y el riesgo de cáncer de mama, se tenga en cuenta o no el estado menopáusico y el estado de los receptores hormonales .
Los ácidos grasos trans en la sangre aumentan el riesgo de cáncer de mama de una mujer en casi un 50%. Los ácidos grasos trans se utilizan en alimentos procesados como panes y galletas industriales, bollería, tortas, patatas fritas, pizzas de pasta industrial.
- El té verde y / o la soja podrían (son) tener propiedades protectoras (lo que explicaría que en Europa 1 de cada 12 mujeres desarrollen este cáncer, frente a una de cada 80 en Japón donde se consumen estos alimentos) .
- Después de la aparición del cáncer de mama, duplicar el consumo de frutas y verduras no parece disminuir el riesgo de recurrencia.
- La suplementación con omega 3 se probó en 2008 para ver si mejoraba la quimioterapia.
- No tomar tratamientos hormonales reduciría el riesgo de cáncer de mama.
- Los tratamientos de tipo SERM ( tamoxifeno , raloxifeno ) reducirían el riesgo. Sin embargo, estos medicamentos tienen efectos secundarios significativos (aumento en el número de enfermedades tromboembólicas para las dos moléculas, cáncer de endometrio para el tamoxifeno) y su lugar aún no se ha determinado.
Tratamientos quirúrgicos "preventivos"
Se han propuesto tratamientos quirúrgicos preventivos en mujeres con antecedentes familiares de cáncer de mama con mutación en los genes BRCA1 o BRCA2. En estas mujeres, el riesgo de cáncer de mama varía entre el 40 y el 85% antes de los 80 años. Las propuestas quirúrgicas son la extirpación de ambas mamas con o sin ooforectomía bilateral, o la ooforectomía bilateral sola.
Los estudios observacionales actuales sobre mastectomía bilateral preventiva (MBP) muestran que podría reducir la incidencia de cáncer de mama y / o muerte, aunque estos estudios tienen limitaciones metodológicas. La satisfacción después de este procedimiento parece ser buena, con una disminución de la preocupación por el cáncer acompañada de una disminución de la imagen corporal y las sensaciones sexuales. En las mujeres que han tenido cáncer en una mama, la extirpación de la otra mama parece reducir la incidencia de cáncer, pero el efecto sobre la supervivencia a largo plazo es incierto debido al riesgo continuo de recurrencia o metástasis del cáncer original.
Aspectos psicológicos
Descubrir que tiene cáncer puede ser muy difícil de aceptar, ya que durante mucho tiempo se ha considerado que esta noticia es la de una muerte inminente. Además, la hospitalización, la cirugía y los tratamientos adyuvantes cambian profundamente la vida del paciente. Por tanto, es fundamental proporcionar a los pacientes un apoyo psicológico adecuado, que generalmente implica la participación en grupos de pacientes que están pasando por las mismas pruebas.
Sin embargo, los cánceres de mama diagnosticados tardíamente suelen ser muy mutilantes. Para las mujeres, esta mutilación mamaria generalmente corresponde a una mutilación psicológica y social. Siendo el pecho uno de los símbolos más fuertes de la feminidad , algunas mujeres pueden experimentar esta mutilación como una negación de su feminidad y por tanto de su personalidad.
La relación de pareja suele sufrir las consecuencias de la enfermedad. En el período posterior al tratamiento, la paciente o su pareja pueden expresar emociones negativas, como el reproche. Este tipo de situaciones deben ser tomadas en serio por los profesionales, ya que pueden estar asociadas a trastornos psicológicos como la depresión. Según Nicolás Favez, Sarah Ciro Notari, Tania Antonini y Linda Charvoz, es probable que este tipo de situaciones se presente en las primeras etapas de la enfermedad, e incluso cuando el pronóstico médico es optimista. En este contexto, se puede ofrecer cirugía reconstructiva , acompañada de atención psicológica.
Por tanto, el cáncer de mama no es solo un problema médico. Afecta la vida, el cuerpo y la confianza en uno mismo. Cuando una mujer recibe el veredicto de "cáncer de mama", sale del consultorio del médico con miedo en el estómago, con muchas preguntas sobre cómo será su vida en el futuro. ¿Cómo hablar de esto con sus familiares? ¿Cómo lidiar con la caída del cabello y la caída de las cejas? ¿Cómo salir de casa y enfrentarse a los ojos de los demás? ¿Cómo puede seguir cuidando a sus hijos? ¿Podrá todavía tener algunos? ¿Perderá su trabajo? ¿Qué pasará con su relación con el hombre de su vida? Tantas preguntas, pocas posibilidades de diálogo, muchos tabúes. A menudo, las mujeres recurren a la enfermedad y esto incluso es perjudicial para el éxito de la terapia.
Queda mucho por hacer para comunicarse adecuadamente con los pacientes y sus familias, pero también para mejorar de manera concreta la atención médica que se brinda a las mujeres y su calidad de vida en general.
En la cultura popular
La artista cómica Marie Reno apoya las acciones de concienciación sobre el cáncer de mama con su canción humorística ¡ Atención a tus tetas! .
Notas y referencias
- https://www.francetvinfo.fr/sante/cancer/cancer-du-sein-il-y-a-une-vraie-recrudescence_1815585.html
- André Cicolella, Cáncer de mama. Poniendo fin a la epidemia , ed. Les Petits Matins, 2016.
- (en) PM Ravdin, Cronin KA, Howlader N et al. " La disminución de la incidencia de cáncer de mama en 2003 en los Estados Unidos " , New Eng J Med , 2007; 356: 1670-1674
- "disminución de la incidencia de cáncer de mama en 2005 y 2006 en Francia: un fenómeno paradójico" Boletín del Cáncer , 2008; 95: 11-5
- (en) Forouzanfar MH, KJ Foreman, Delossantos AM et al. " Cáncer de mama y de cuello uterino en 187 países entre 1980 y 2010: un análisis sistemático " , Lancet , 2011
- Boyle y Ferley, 2004
- WCRF - Estadísticas de cáncer de mama
- IARC - Hoja informativa sobre el cáncer de mama
- Fuente Inserm 2008, consultado en 2008 10 04
- "Antoine Spire habla con David Khayat para Le Monde de l'Education" extractos de un artículo publicado en abril de 2006 en Le Monde de l'Education
- "avanzada de cáncer de mama: las promesas de un nuevo tratamiento" en futura-sciences.com
- Instituto de Vigilancia de la Salud Pública (InVS) INSERM
- " El cáncer de mama: hacia tratamientos menos intensivos " (consultado el 1 er de octubre de el año 2015 )
- Instituto Nacional del Cáncer, cáncer de mama, actualización de abril de 2008.
- " Cáncer: mejora la supervivencia en Francia " , en sante.lefigaro.fr (consultado el 2 de febrero de 2016 )
- Wang B, He M, Wang L, Engelgau MM, Zhao W, Wang L. Detección de cáncer de mama entre mujeres adultas en China, 2010. Prev Chronic Dis 2013; 10: 130136. DOI: https://dx.doi.org/10.5888/pcd10.130136
- (in) Nagata, Chisato, " Factores a considerar en la asociación entre la ingesta de isoflavonas de soja y el riesgo de cáncer de mama " , J Epidemiol , vol. 20, n o 22009, p. 83-89 ( ISSN 1349-9092 , DOI 10.2188 / jea.JE20090181 , leer en línea )
- Wooster R, Weber BL. Cáncer de mama y ovario . N Engl J Med 2003; 348: 2339-47
- general Cancer Curso P r JF GARZA
- Loibl S, Poortmans P, Morrow M, Denkert C, Curigliano G, cáncer de mama , Lancet, 2021; 397: 1750-69
- Isabelle Plo, Corentin Laulier, Fabienne Lebrun, Laurent Gauthier, Fabien Calvo y Bernard Lopez. AKT1 inhibe la recombinación homóloga al inducir la retención citoplásmica de BRCA1 y RAD51 . Investigación sobre el cáncer. 15 de noviembre de 2008.
- [ tratamientos hormonales promoverían el cáncer de mama? Comunicado de prensa de la CEA]
- Comunicado / Investigación de la Universidad Joseph Fourier (Grenoble) ; [CK2: un papel importante en la progresión de los tumores mamarios] ; 10 de mayo de 2012
- Clavel-Chapelon F, Número acumulado de ciclos menstruales y riesgo de cáncer de mama: resultados del estudio de cohorte E3N de mujeres francesas , Cancer Causes and Control, 2002; 13: 831-838
- Beral V, Cáncer de mama y terapia de reemplazo hormonal en el estudio de un millón de mujeres , Lancet, 2003; 362: 419-27
- niñas están llegando a la pubertad antes que nunca
- (en) Merrill RM Fugal S Novilla LB, Raphael ™, " Riesgo de cáncer asociado con la edad materna temprana y tardía en el primer nacimiento " , Gynecol Oncol , vol. 96, n o 3,2005, p. 583-93. ( PMID 15721398 , DOI j.ygyno.2004.11.038 )
- (en) Faupel-Badger JM, Arcaro KF, Balkam JJ, Eliassen AH, Sherman ME et al. , “ Remodelación posparto, lactancia y riesgo de cáncer de mama: resumen de un taller patrocinado por el Instituto Nacional del Cáncer ” , J Natl Cancer Inst , vol. 105, n o 3,2013, p. 166-74. ( PMID 23264680 , PMCID PMC3611853 , DOI 10.1093 / jnci / djs505 , lea en línea [html] )
- (en) Diamanti-Kandarakis E, Bourguignon JP, Giudice LC, et al. , “ Sustancias químicas disruptoras endocrinas: una declaración científica de la Endocrine Society ” , Endocr. Rvdo. , vol. 30, n o 4,Junio de 2009, p. 293–342 ( PMID 19502515 , PMCID 2726844 , DOI 10.1210 / er.2009-0002 )
- Romain Loury (2015) Detrás del cáncer de mama, DDT , 16 de junio de 2015
- "Dr. de Lorgeril - Las causas del cáncer de mama finalmente identificadas. ¿Cómo protegerse?"
- Células adiposas y cáncer de mama: una combinación peligrosa (según un comunicado de prensa del CNRS) 05/04/2011
- Cáncer de mama: las campañas de prevención son llamados para , en Le Figaro , 23 de octubre de 2008, página 11
- Mayor riesgo de cáncer de mama en mujeres posmenopáusicas en función de su aumento de peso
- Béatrice Dirat; Los adipocitos asociados al cáncer exhiben un fenotipo activado y contribuyen a la invasión del cáncer de mama ; Cancer Research, doi: 10.1158 / 0008-5472.CAN-10-3323 Cancer Res 1 de abril de 2011 71; 2455 Resumen )
- B. Dirat y col. La investigación del cáncer , 1 st de abril de 2011
- Estudio que muestra la correlación entre el cáncer de mama y el consumo de grasas animales que data de 1986
- Estudio sobre factores identificados de cáncer en España
- Ingesta de grasas en la dieta y riesgo de cáncer de mama: un estudio de casos y controles en China
- conclusiones de los trabajos por el Inserm y el Institut Gustave-Roussy dirigidos a evaluar el papel de los diferentes ácidos grasos en el desarrollo de cáncer de mama, a partir de ensayos de sangre recogidas 1995-1998 entre 25.000 de 100.000 mujeres siguieron como parte de lo que se -denominado E3N estudio .
- (in) El factor de crecimiento aumenta el riesgo de cáncer
- (in) Ingesta de leche, productos lácteos y lactosa y riesgo de cáncer de ovario: un metaanálisis de estudios epidemiológicos , International Journal of Cancer , vol. 118, número 2, pág. 431-441
- (in) Variación en el factor de crecimiento similar a la insulina-1 en plasma y la proteína de unión al factor de crecimiento similar a la insulina-3: factores personales y de estilo de vida (Estados Unidos)
- "Informe Andes, p76 / 210"
- (in) "Consumo de leche cruda o calentada de diferentes especies: una evaluación de los posibles beneficios nutricionales y para la salud, p4 / 14
- (in) "Asociación del contenido de IGF-1 con la leche entera, descremada y descremada en México"
- (in) Ingesta de productos lácteos, calcio y vitamina D y riesgo de cáncer de mama
- (in) Productos lácteos y riesgo de cáncer de mama
- [PDF] Informe de alcohol y el riesgo de cáncer de la red (60 páginas), Instituto Nacional del Cáncer, y Nácar, 2007)
- Xue F, Willett WC, Rosner BA, Hankinson SE, Michels KB, Fumar cigarrillos y la incidencia del cáncer de mama , Arch Intern Med, 2011; 171: 125-133
- (en) Lundqvist J, M Norlin, Wikvall K, " 1α, 25-dihidroxivitamina D (3) ejerce efectos específicos de tejido sobre el metabolismo de los andrógenos del estrógeno " , Biochim Biophys Acta ,enero 2011( PMID 21262387 , DOI 10.1016 / j.bbalip.2011.01.004 )
- (en) Napoli N, Vattikuti S, Ma C, et al. , “ Alta prevalencia de niveles bajos de vitamina D y molestias musculoesqueléticas en mujeres con cáncer de mama ” , Breast J , vol. 16, n o 6,2010, p. 609–16 ( PMID 21070438 , DOI 10.1111 / j.1524-4741.2010.01012.x )
- (in) Grant WB, Peiris AN, " Papel de la posible 25-hidroxivitamina D sérica en las disparidades de salud entre blanco y negro en los Estados Unidos " , J Am Med Dir Assoc , vol. 11, n o 9,noviembre 2010, p. 617–28 ( PMID 21029996 , DOI 10.1016 / j.jamda.2010.03.013 )
- (in) Engel P Fagherazzi G, S Mesrine, Boutron-Ruault MC, Clavel-Chapelon F, "Los efectos conjuntos de la vitamina D en la dieta y la exposición al sol son el riesgo de cáncer de mama: resultados de la cohorte francesa E3N " , Cancer Epidemiol. Biomarcadores Prev. , vol. 20, n o 1,enero 2011, p. 187–98 ( PMID 21127286 , DOI 10.1158 / 1055-9965.EPI-10-1039 )
- (in) Densidad mamográfica y el riesgo de detección de cáncer de mama y Norman F.Boyd, Helen Guo, Lisa J. Martin, Limei Sun, Jennifer Stone, Eve Fishell, Roberta A. Jong, Greg Hislop, Anna Chiarelli, Salomon Minkin, Martin J. Yaffe, New Eng J Med , 2007; 356: 227-236
- (en) Travis LB, Hill D, Dores GM, Gospodarowicz M, van Leeuwen EF, Holowaty E et al. “ Riesgo absoluto acumulativo de cáncer de mama para mujeres jóvenes tratadas por linfoma de Hodgkin ” J Natl Cancer Inst . 2005; 97: 1428-37
- (in) Einstein AJ, Henzlova MJ, Rajagopalan S, " Estimación del riesgo de cáncer asociado con la exposición a la radiación de la angiografía coronaria por tomografía computarizada de 64 cortes " JAMA 2007; 298: 317-323
- (en) Kolstad HA, " Trabajo nocturno y riesgo de cáncer de mama y otros cánceres: una revisión crítica de la evidencia epidemiológica " Scand J Work Around Health . 2008; 34: 5-22
- Los ciclos de luz que se alternan crónicamente aumentan el riesgo de cáncer de mama en ratones
- (en) Wise J, " Trabajadores del turno de noche daneses con cáncer de mama por compensación de fecha " BMJ . 2009; 338: b1152
- (en) Stuebe AM, Willett WC, Fei Xue, Michels KB, " Lactancia e incidencia de cáncer de mama premenopáusico ", Arch Intern Med . 2009; 169 (15): 1364-1371
- "La interrupción voluntaria del embarazo no aumenta el riesgo de cáncer de mama" (OMS, publicado en línea en junio de 2000)
- Silva IdS, Stavola BD, McCormack V, Grupo de colaboración sobre factores de riesgo prenatales y riesgo subsiguiente de cáncer de mama (2008), " Tamaño al nacer y riesgo de cáncer de mama: nuevo análisis de datos de participantes individuales de 32 estudios " ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? ) (Consultado el 2 de agosto de 2017 ) . PLoS Med 5 (9): e193
- Instituto Nacional contra el Cáncer, Cáncer de mama en hombres .
- Maalej M, Hentati D, Messai T, Kochbati L, El May A, Mrad K, Romdhane KB, Ben Abdallah M, Zouari B. Breast cancer in Tunisia in 2004: a comparative Clinical and epidemiological study. Toro Cáncer. Febrero de 2008; 95 (2): E5-9.
- Antoniou A, Pharoah PD, Narod S et als. Riesgos promedio de cáncer de mama y de ovario asociados con mutaciones BRCA1 o BRCA2 detectados en series de casos no seleccionadas para antecedentes familiares: un análisis combinado de 22 estudios , Am J Hum Genet, 2003; 72: 1117-1130
- Robson ME, Chappuis PO, Satagopan J, et al. Un análisis combinado de los resultados después del cáncer de mama: diferencias en la supervivencia según el estado de la mutación BRCA1 / BRCA2 y la administración de tratamiento adyuvante , Breast Cancer Res 2004; 6: R8-R17
- Rennert G, Bisland-Naggan S, Barnet-Griness O, et al. Resultados clínicos del cáncer de mama en portadoras de mutaciones BRCA1 y BRCA2 , N Engl J Med 2007; 357: 115-123
- John EM, Miron A, Gong G y Als. [2007; 298 (24): 2869-2876 Prevalencia de portadores patógenos de la mutación BRCA1 en 5 grupos G raciales / étnicos de EE . UU. ], JAMA, 2007; 298: 2869-2876
- Antoniou AC, Casadei S, Heikkinen T et al. Riesgo de cáncer de mama en familias con mutaciones en PALB2 , N Engl J Med, 2014; 371: 497-506
- Cáncer de mama in situ en el sitio web de la asociación para el cribado del cáncer en Meurthe et Moselle, consultado el 13 de enero de 2016
- "Cáncer de mama: las ilusiones de la detección", Coisne S y Lemarchand F., La Recherche , 395, marzo de 2006: 44-48
- Humphrey LL, Helfand M, Chan BKS, Woolf SH, Detección de cáncer de mama: resumen de la evidencia del grupo de trabajo de servicios preventivos de EE. UU. , Ann Intern Med , 2002: 137: 347-360
- resultados del ensayo Two-County de detección de mamografía no son compatibles con las estadísticas oficiales contemporáneas de cáncer de mama suecas Zahl PH, Peter C. Gøtzsche , Andersen JM, Maehlen J. Dan Med Bull. Noviembre de 2006; 53 (4): 438-40.
- Berg WA, Blume JD, Cormack JB, Detección combinada con ultrasonido y mamografía frente a mamografía sola en mujeres con riesgo elevado de cáncer de mama JAMA, 2008; 299: 2151-2163
- Leach MO, Boggis CR, Dixon AK et als. Detección con imágenes de resonancia magnética y mamografía de una población del Reino Unido con alto riesgo familiar de cáncer de mama: un estudio de cohorte multicéntrico prospectivo (MARIBS) , Lancet, 2005; 365: 1769-78
- Kösters JP, Peter C. Gøtzsche , Autoexamen regular o examen clínico para la detección temprana del cáncer de mama , Base de datos Cochrane de revisiones sistemáticas 2003, Número 2. Art. No .: CD003373. DOI: 10.1002 / 14651858.CD003373
- "Niramai utiliza imágenes térmicas e inteligencia artificial para revolucionar el diagnóstico del cáncer de mama"
- "You tube, termografía mamaria"
- "You tube: mamografía e imágenes térmicas"
- "Ncbi, 2014: un modelo novedoso para la detección inteligente del cáncer de mama en imágenes de termogramas".
- "Marzo de 2017: herramienta no invasiva de apoyo para el diagnóstico de cáncer de mama utilizando una cámara termográfica como sensor"
- "10 revisiones sistemáticas en farmacia, vol. 9, número 1, enero-diciembre de 2018, el efecto de la termografía en la detección del cáncer de mama"
- "2012, pizarra: cáncer de mama: un escándalo francés?"
- "Termografía para la detección del cáncer de mama"
- "Imágenes infrarrojas de la mama: una descripción general, p18 / 22"
- [artículo - [relacionado] "France-info, 2019: turista británica descubre su cáncer de mama ... mientras visita un museo"]
- Warner E, Detección de cáncer de mama , N Engl J Med, 2011; 365: 1025-1032
- Miller AB, To T, Baines CJ, Wall C, The Canadian National Breast Screening Study-1: mortalidad por cáncer de mama después de 11 a 16 años de seguimiento: un ensayo de detección aleatorio de mamografía en mujeres de 40 a 49 años , Ann Intern Med, 2002; 137: 305-312
- Moss SM, Cuckle H, Evans A, Johns L, Waller M, Bobrow L, Efecto del cribado mamográfico a partir de los 40 años sobre la mortalidad por cáncer de mama a los 10 años de seguimiento: un ensayo controlado aleatorio , Lancet, 2006; 368: 2053-2060
- Zackrisson S, Andersson I, Janzon L, Manjer J, Garne JP, Tasa de sobrediagnóstico de cáncer de mama 15 años después del final del ensayo de cribado mamográfico de Malmö: estudio de seguimiento , BMJ, 2006; 332: 689-92
- Welch HG, Schwartz LM, Woloshin S, Ramificaciones de la detección del cáncer de mama: 1 de cada 4 cánceres detectados por mamografía son pseudocánceres , BMJ, 2006; 332: 727
- Jørgensen KJ, Peter C. Gøtzsche , Sobrediagnóstico en programas de detección de mamografías organizados públicamente: revisión sistemática de las tendencias de incidencia , BMJ, 2009; 339: b2587
- Zahl PH, Maehlen J, Welch HG, La historia natural de los cánceres de mama invasivos detectados mediante mamografía de detección , Arch Intern Med, 2008; 168: 2311-6
- [1] .
- "Un defecto de la bacteria Methylobacterium en el tejido mamario canceroso"
- "EverZen: ¿Cuál es la tasa de supervivencia del cáncer de mama?"
- de Cabarrot E. Historia natural del cáncer de mama. Enciclopedia médico-quirúrgica . Ediciones científicas y médicas Elsevier SAS, París. Ginecología, 865-A-10, 2000.
- Cáncer de mama inflamatorio: preguntas y respuestas en el sitio web del Instituto Nacional del Cáncer .
- (in) X. Dai , " Clasificación de subtipos intrínsecos del cáncer de mama, uso clínico y tendencias futuras " , Am J Cancer Res , vol. 5, n o 10,15 de septiembre de 2015, p. 2929–2943 ( leer en línea ).
- (en) E. Charaffe-Jauffret , " El perfil de expresión génica de las líneas de células mamarias identificó nuevos marcadores basales potenciales " , Oncogene , vol. 25,6 de abril de 2006, p. 2273–2284 ( leer en línea ).
- "La revolución de la genómica" , 1 min 33 s / 3 min
- "Terapia dirigida 3m39 / 5m33"
- van 't Veer LJ, Dai H, van de Vijver MJ y Als. El perfil de expresión génica predice el resultado clínico del cáncer de mama , Nature, 2002; 415: 530-536
- Paik S, Shak S, Tang G y Als. Un ensayo multigénico para predecir la recurrencia del cáncer de mama con ganglios negativos tratados con tamoxifeno , N Engl J Med, 2004; 351: 2817-2826
- Wang Y, Klijn JG, Zhang Y y Als. Perfiles de expresión genética para predecir la metástasis remota del cáncer de mama primario con ganglios linfáticos negativos , Lancet, 2005; 365: 671-679
- Significa MA, Somji S, Lamm DL, Garrett SH, Slovinsky F, Todd JH, Significa DA. La sobreexpresión de la isoforma 3 de metalotioneína se asocia con cánceres de mama de mal pronóstico . Am J Pathol 159: 21-26, 2001.
- Nartey N, Cherian MG, Banerjee D. Localización inmunohistoquímica de metalotioneína en tumores de tiroides humanos . Am J Pathol 129: 177-182, 1987.
- Haerslev T, Jacobsen K, Nedergaard L, Zedeler K. Detección inmunohistoquímica de metalotioneína en carcinomas primarios de mama y sus metástasis en los ganglios linfáticos axilares. Pathol Res Pract 190: 675–681, 1994. 64.
- Haerslev T, Jacobsen K, Zedeler K. La importancia pronóstica de la metalotioneína inmunohistoquímicamente detectable en los carcinomas primarios de mama. APMIS 103: 279-285, 1995.
- Fresno M, Wu W, Rodríguez JM, Nadji M. Localización de metalotioneína en carcinomas de mama. Un estudio inmunohistoquímico. Virchows Arch A Pathol Anat Histopathol 423: 215-219, 1993.
- 5ª CONFERENCIA INTERNACIONAL SOBRE DOCUMENTOS DEL SIMPOSIO DE METALOTIONEÍNA La metalotioneína como biomarcador de pronóstico en el cáncer de mama Boon-Huat Bay, Rongxian Jin, Jingxiang Huang y Puay-Hoon Tan ( “ Resumen ” ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? ) (consultado el 2 de agosto de 2017 ) y “ artículo completo en PDF (6 páginas) ” ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? ) (consultado el 2 de agosto de 2017 ) )
- Ioachim E, Tsanou E, Briasoulis E, Batsis Ch, Karavasilis V, Charchanti A, Pavlidis N, Agnantis NJ. Estudio clínico-patológico de la expresión de hsp27, pS2, catepsina D y metalotioneína en el cáncer de mama invasivo primario . Breast 12: 111-119, 2003.
- Surowiak P, Matkowski R, Materna V, Gyorffy B, Wojna A, Pudelko M, Dziegiel P, Kornafel J, Zabel M. La expresión elevada de metalotioneína (MT) en el cáncer de mama ductal invasivo predice la resistencia al tamoxifeno . Histol Histopathol 20: 1037-1044, 2005.
- [PDF] Sitio web de la Organización Nacional de Sindicatos Liberales de Enfermeras
- Mansel RE, Fallowfield L, Kissin M et als. Ensayo multicéntrico aleatorizado de biopsia de ganglio centinela versus tratamiento axilar estándar en cáncer de mama operable: el ensayo ALMANAC , J. Natl Cancer Inst. , 2006; 98: 599-609.
- Erica J Weinstein , Jacob L Levene , Marc S Cohen y Doerthe A Andreae , " Anestésicos locales y anestesia regional versus analgesia convencional para prevenir el dolor posoperatorio persistente en adultos y niños ", Base de datos Cochrane de revisiones sistemáticas ,21 de junio de 2018( ISSN 1465-1858 , PMID 29926477 , PMCID PMC6377212 , DOI 10.1002 / 14651858.cd007105.pub4 , leído en línea , consultado el 21 de julio de 2020 )
- (en) Clarke M, Collins R, S Darby et al. "Efectos de la radioterapia y de las diferencias en la extensión de la cirugía para el cáncer de mama temprano sobre la recurrencia local y la supervivencia a 15 años: una descripción general de los ensayos aleatorizados" Lancet 2005; 366: 2087-106
- (en) Henson KE, McGale P, Taylor C, Darby SC. “Mortalidad relacionada con la radiación por enfermedades cardíacas y cáncer de pulmón más de 20 años después de la radioterapia para el cáncer de mama” British Journal of Cancer 20 de diciembre de 2012 DOI : 10.1038 / bjc.2012.575
- "El cáncer se puede tratar durante el embarazo " (consultado el 2 de octubre de 2015 )
- " Cáncer de mama: un análisis de sangre para predecir el impacto de la radioterapia " , en la revista Santé (consultado el 27 de enero de 2016 )
- (en) Romond EH, Perez EA, Bryant J et al. “Trastuzumab más quimioterapia adyuvante para el cáncer de mama operable HER2 positivo” N Engl J Med. 2005; 353: 1673-84
- " Medscape Francia - Información médica y recursos para médicos | Medscape France ” , en francais.medscape.com (consultado el 4 de septiembre de 2018 )
- (en-GB) John Wiley & Sons Ltd y The Atrium, Southern Gate , “ Ontruzant se lanza para convertirse en el primer biosimilar de Herceptin disponible en el Reino Unido | Pharmafile ” , en www.pharmafile.com (consultado el 4 de septiembre de 2018 )
- (en) Miller K, Wang M, Gralow J et al. “Paclitaxel más bevacizumab versus paclitaxel solo para el cáncer de mama metastásico” N Engl J Med. 2007; 357: 2666-76.
- Resumen del dictamen de la Haute Autorité de Santé (Francia), mayo de 2011
- (en) Geyer et al. “Lapatinib más capecitabina para el cáncer de mama avanzado positivo para HER2” ( Archivo • Wikiwix • Archive.is • Google • ¿Qué hacer? ) (Consultado el 2 de agosto de 2017 ) N Engl J Med. 2006; 355: 2733-43.
- Para anastrozol , menos cáncer de endometrio, menos isquemia cerebrovascular, menos trombosis venosa profunda, pero más fracturas y artralgia. Para letrozol , menos eventos tromboembólicos venosos, pero más artralgia, fracturas, problemas cardíacos y colesterol alto.
- Colditz, GA y Bohlke, K. (2014), Prioridades para la prevención primaria del cáncer de mama. CA: Revista sobre el cáncer para médicos, 64: 186-194. doi: 10.3322 / caac.21225
- programa de monografías de la IARC clasifica los anticonceptivos combinados combinados y la terapia hormonal monopáusica como carcinógenos , Agencia Internacional para la Investigación del Cáncer , comunicado de prensa del 29 de julio de 2005
- (en) Chavez-MacGregor M Elias SG, Onland-C Moret et al. Riesgo de cáncer de mama posmenopáusico y número acumulado de ciclos menstruales , Cancer Epidemiology Biomarkers & Prevention, 2005; 14: 799-804
- "Cáncer de mama: las campañas de prevención son llamados de" Le Figaro , 23 de Octubre, 2008
- (in) E. Riboli et al ". Poblaciones de estudio de investigación prospectiva europea sobre cáncer y nutrición (EPIC) y recopilación de datos ' Nutrición de salud pública , vol. 5, n o 6B,2002, p. 1113-1124 ( PMID 12639222 , leído en línea [html] , consultado el 16 de abril de 2013 )
- (en) R. Zamora-Ros et al., " La dieta de flavonoides y el consumo de lignanos y el cáncer de mama menopausia selon riesgo y el estado de los receptores hormonales en el estudio prospectivo europeo sobre cáncer y nutrición (EPIC) Estudio ' investigación y tratamiento del cáncer de mama ,2013( PMID 23572295 , leído en línea [html] , consultado el 16 de abril de 2013 )
- Conclusion of a Women's Healthy Eating and Living (WHEL), publicado en el verano de 2007 en JAMA
- Experimento realizado por INSERM en Tours (fuente: Science et Avenir de abril de 2008)
- Bevers, Therese B, Evidencia de raloxifeno como agente de reducción del riesgo de cáncer de mama para mujeres posmenopáusicas , JNCCN, 2007; 5: 817-822
- Nelson HD, Smith MB, Griffin JC, Fu R, Uso de medicamentos para reducir el riesgo de cáncer de mama primario , Ann Intern Med, 2013; 158: 604-614
- (in) Nora E Carbine , Liz Lostumbo Judi Wallace y Henry Ko , " Mastectomía reductora de riesgo para la prevención del cáncer de mama primario " , Base de datos Cochrane de revisiones sistemáticas ,5 de abril de 2018( PMID 29620792 , PMCID PMC6494635 , DOI 10.1002 / 14651858.CD002748.pub4 , leído en línea , consultado el 13 de mayo de 2019 )
- (en) Nicolas Favez , Sarah Cairo Notari , Tania Antonini et Linda Charvoz , « Attachment and couple satisfaction as predictors of expressed emotion in women facing breast cancer and their partners in the immediate post-surgery period » , British Journal of Health Psychology , Vuelo. 22, n o 1,1 st de febrero de 2017, p. 169–185 ( ISSN 2044-8287 , DOI 10.1111 / bjhp.12223 , leído en línea , consultado el 23 de agosto de 2017 )
- " Marie Reno - Pink October - The top of the news - 27 de septiembre de 2019 - Marie Réno - The top of the news on Rire & Chansons - Rire & Chansons " , en Rire & Chansons.fr (consultado el 7 de octubre de 2019 )
Ver también
Artículos relacionados
- Seno
- Cáncer de ovarios
- Cáncer de útero
- Mastectomía , prótesis
- Mitoxantrona
- Trastorno cognitivo posterior a la quimioterapia
- Atossa
- Oncotype DX
- Seintinelles
enlaces externos
- Registros de autoridad :
- Avisos en diccionarios generales o enciclopedias : Brockhaus Enzyklopädie • Encyclopædia Britannica
- Recursos relacionados con la salud :
- Versión de la CIE-10: 2016
- MalaCards
- Instituto Nacional del Cáncer
- Tesauro del NCI
- Orphanet
- (en) Clasificación Internacional de Atención Primaria
- (es) Enfermedades Ontología
- (es) DiseasesDB
- ( fr ) Herencia mendeliana en humanos
- ( fr ) Herencia mendeliana en humanos
- (sv) Internetmedicina
- (en + es) MedlinePlus
- (no + nn + nb) Tienda medisinske leksikon
- Cáncer de mama en el sitio web del seguro médico
- www.cancerdusein.org El sitio de “Breast Cancer Association, Parlons-en! », En el origen del mes de octubre Rose para concienciar sobre la lucha contra el cáncer de mama y la detección precoz, en Francia desde 1994
- Cáncer de mama en el sitio web de la Federación Nacional de Lucha contra el Cáncer
- Categoría de cáncer de mama del directorio dmoz
- GRCS, el grupo de investigación sobre cáncer de mama del centro de investigación CHUM en Montreal
- Radio Curie Una radio web informativa dedicada a las mujeres con cáncer de mama y sus seres queridos