Ácido carboxílico
El término ácido carboxílico se refiere a una molécula que comprende un grupo carboxilo (-C (O) OH). Son ácidos y sus bases conjugadas se denominan iones carboxilato .
En química orgánica , un grupo carboxilo es un grupo funcional compuesto por un átomo de carbono , unido por un doble enlace a un átomo de oxígeno y unido por un enlace sencillo a un grupo hidroxilo -OH.
General
En química , los ácidos carboxílicos R-COOH constituyen con los ácidos sulfónicos R-SO 3 H los dos tipos de ácidos de la química orgánica . Se encuentran abundantemente en la naturaleza como ácidos grasos ( lípidos ) y son muy importantes en la química industrial . Por ejemplo, el ácido acético no solo es un componente importante para las moléculas complejas que se encuentran en biología , sino que también es una molécula producida industrialmente que se encuentra en el vinagre . Uno de los más conocidos es el ácido acetilsalicílico o aspirina. El componente básico de las proteínas , los aminoácidos son los ácidos carboxílicos.
El grupo funcional característico es el grupo carboxilo, donde R es hidrógeno o un grupo orgánico:

Los ácidos carboxílicos tienen la fórmula bruta C n H 2 n O 2 cuando R es un grupo alquilo . Computar el número de insaturación da: . Esta insaturación refleja el doble enlace carbono-oxígeno .
Los grupos carboxilo a menudo se escriben en forma reducida: -COOH (forma no ionizada del grupo). La forma ionizada del grupo es: -COO - .
Este siempre se encuentra al final de la cadena de carbono . La adición de un grupo carboxilo a un compuesto orgánico es una carboxilación , la eliminación de este mismo grupo es una descarboxilación .
Iones carboxilato
Estas son las bases conjugadas R-COO - ácidos carboxílicos. Estas bases son generalmente bastante débiles . La carga negativa de la molécula se deslocaliza en los dos átomos de oxígeno del grupo carboxilo por mesomería, lo que explica la relativa estabilidad de este tipo de moléculas.

El ion carboxilato es un tensioactivo anfifílico , es la especie detergente de jabón . De hecho, el grupo carboxilato _COO- es hidrófilo porque es muy polar . Por otro lado, la cadena de carbono R es apolar y, por tanto, hidrófoba y lipófila .
Nomenclatura
- Sistemático: si el átomo de carbono del grupo carboxilo COOH está incluido en la cadena principal del hidrocarburo correspondiente (que tiene el mismo número de átomos de carbono, con CH 3 en lugar de COOH), se sigue el nombre de este. Hidrocarburo con el sufijo " -oico "(dioico para diácido), y precediéndolo con la palabra" ácido ". De lo contrario (en series cíclicas, por ejemplo), la palabra " ácido " va seguida del nombre del hidrocarburo al que se añade el sufijo "-carboxílico".
| Clase | Fórmula * del grupo característico |
Sufijo |
|---|---|---|
| Ácidos carboxílicos | - (C) OOH -COOH |
ácido-… ácido oico … -carboxílico |
- el ácido heptanoico CH 3 (CH 2 ) 5 -COOH puede denominarse alternativamente ácido hexano-1-carboxílico si el átomo de carbono de -COOH no está incluido en la numeración de la cadena;
- El ácido HOOC- (CH 2 ) 5 -COOH heptanodioico es un ácido dicarboxílico . El sufijo -oic va precedido del prefijo multiplicativo di- ;
- ácido ciclopentanocarboxílico: -COOH .
- Habitual: como muchos compuestos orgánicos, los ácidos carboxílicos tienen nombres comunes que se usan con frecuencia en la literatura y recuerdan la fuente de la cual fueron aislados por primera vez. Sin embargo, una lista definida por la IUPAC regula el uso de nombres triviales aceptados junto con los nombres sistemáticos.
| Tipo | Estructura | Nombre IUPAC | nombre común | Fuente |
|---|---|---|---|---|
| Monoácidos alifáticos | H-COOH | ácido metanoico | ácido fórmico | secretado por algunas hormigas (latín: formica , hormigas) |
| CH 3 -COOH | ácido etanoico | ácido acético | Latín: acetum , vinagre | |
| CH 3 CH 2 -COOH | ácido propanoico | ácido propiónico | Griego: peón , gordo | |
| CH 3 (CH 2 ) 2 -COOH | ácido butanoico | ácido butírico | Griego: bouturos , mantequilla | |
| CH 3 (CH 2 ) 3 -COOH | ácido pentanoico | ácido valérico | valeriana | |
| CH 3 (CH 2 ) 4 -COOH | ácido hexanoico | ácido caproico | ||
| CH 3 (CH 2 ) 5 -COOH | ácido heptanoico | acido enantico | ||
| CH 3 (CH 2 ) 6 -COOH | ácido octanoico | ácido caprílico | coco , leche materna | |
| CH 3 (CH 2 ) 7 -COOH | ácido nonanoico | ácido pelargónico | ||
| CH 3 (CH 2 ) 8 -COOH | ácido decanoico | ácido cáprico | ||
| CH 3 (CH 2 ) 9 -COOH | ácido undecanoico | ácido undecílico | ||
| CH 3 (CH 2 ) 10 -COOH | ácido dodecanoico | acido laurico | aceite de coco | |
| CH 3 (CH 2 ) 11 -COOH | ácido tridecanoico | ácido tridecílico | ||
| CH 3 (CH 2 ) 12 -COOH | ácido tetradecanoico | Ácido mirístico | nuez moscada | |
| CH 3 (CH 2 ) 13 -COOH | ácido pentadecanoico | ácido pentadecílico | ||
| CH 3 (CH 2 ) 14 -COOH | ácido hexadecanoico | ácido palmítico | aceite de palma | |
| CH 3 (CH 2 ) 15 -COOH | ácido heptadecanoico | ácido margárico | ||
| CH 3 (CH 2 ) 16 -COOH | ácido octodecanoico | ácido esteárico | grasas animales | |
| CH 3 (CH 2 ) 17 -COOH | ácido nonadecanoico | ácido nonadecílico | ||
| CH 3 (CH 2 ) 18 -COOH | ácido eicosanoico | ácido araquídico | aceite de maní , aceite de pescado y aceites vegetales | |
| CH 3 (CH 2 ) 20 -COOH | ácido docosanoico | ácido behénico | ||
| Monoácidos aromáticos | C 6 H 5 -COOH | ácido benzoico | benceno | |
| HO-C 6 H 4 -COOH | Ácido 2-hidroxibenzoico | ácido salicílico | fruta (como salicilato de metilo ) | |
| Ácidos de tiol | CH 3 CH (SH) -COOH | Ácido 2-mercaptopropanoico | ácido tiolactico |
NB: un dispositivo mnemónico para recordar los nombres de los ácidos lineales, en orden ascendente del número de átomos de carbono, es la siguiente oración: " O n M ángel S aucisse G rillée A P ungido" ( O xalique, M alonique, S uccinic , G lutarico, A dipico, P imélico). Los diácidos se utilizan para la síntesis de poliamidas y poliésteres .
Se pueden mencionar otros tipos de ácidos carboxílicos: los ácidos dicarboxílicos , los ácidos tricarboxílicos , los ácidos alfa- hidroxilés , los cetoácidos , los aminoácidos y los ácidos grasos .
Propiedades fisicas y estructurales
Expresar
Los ácidos carboxílicos son líquidos en condiciones normales siempre que su cadena de carbono tenga menos de ocho átomos de carbono. Son sólidos más allá de eso.
Los ácidos de bajo peso molecular tienen un olor fuerte; por ejemplo, el ácido butanoico es responsable del olor a mantequilla rancia.
Polaridad, solubilidad
La función del ácido carboxílico es fuertemente polar y es tanto donante como aceptor de enlaces de hidrógeno . Esto permite la creación de enlaces de hidrógeno, por ejemplo, con un disolvente polar como agua, alcohol y otros ácidos carboxílicos.

Debido a esta propiedad, los ácidos carboxílicos pequeños (hasta el ácido butanoico) son completamente solubles en agua. Las moléculas de ácido también son capaces de formar dímeros estables por enlaces de hidrógeno, lo que explica por qué su punto de ebullición es más alto que el de los alcoholes correspondientes.
Acidez
En solución en agua, el ácido se disocia parcialmente en el ion carboxilato, según la ecuación de balance :
Estos son ácidos débiles en agua ( p K A entre 4 y 5).
Como los alcoholes, los ácidos carboxílicos muestran un carácter ácido y básico: la desprotonación en iones carboxilato es fácil, pero la protonación es más difícil. Por tanto, tienen una pK A más baja que la de los alcoholes. De hecho, la acidez de los ácidos carboxílicos se explica por el efecto inductivo en el grupo carboxilo: el enlace C = O está muy polarizado ( electronegatividad del oxígeno mayor que la del carbono) lo que hace que el carbono sea electrófilo , y por tanto atrae electrones del otro oxígeno. Ahora bien, este otro oxígeno está unido a un hidrógeno, y este enlace también está polarizado , por lo que el electrón del hidrógeno que se ha acercado al oxígeno es a su vez atraído por el carbono electrófilo. Por lo tanto, este hidrógeno se vuelve muy fácilmente móvil, de ahí la acidez del grupo carboxilo.
La solubilidad del ácido carboxílico aumenta con el pH .
Espectroscopia
En infrarrojo (IR), el ácido carboxílico tiene dos bandas de valencia:
| Vibración | C = O | OH |
|---|---|---|
| Número de onda (cm −1 ) | 1,680-1,710 | 2.500-3.200 |
| Intensidad | (fuerte) | grande, mediano a fuerte |
Estructura

Según la teoría VSEPR :
- la geometría alrededor del átomo de carbono (enlaces) es de tipo trigonal;
- la geometría alrededor del átomo de oxígeno de la función carbonilo (doble enlace + dobletes libres) también es de tipo trigonal;
- la geometría alrededor del átomo de oxígeno de la función hidroxilo (enlaces + dobletes libres) es de tipo tetraédrico (AX 2 E 2 ).
El ácido carboxílico tiene varias formas mesoméricas .
Reactividad
Como se muestra, entre otros, las diferentes fórmulas mesoméricas del ácido carboxílico:
- los átomos de oxígeno son sitios nucleofílicos así como bases de Lewis;
- el carbono central es electrofílico;
- el átomo de hidrógeno electrófilo es ácido.
Derivados
Los ácidos carboxílicos tienen muchos derivados:
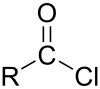
-
Anhídrido de ácido
- los ésteres
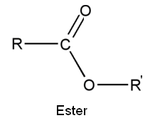
- las amidas

- el nitrilo
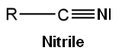
En términos de grupo saliente (nucleófugo), el orden de facilidad es:
Cl - (cloruro de acilo), RCOO - (anhídrido), RO - (éster), - NH 2 y - NR 1 R 2 (amidas).
Reducción
Oxidación
- Dióxido de carbono (CO 2)
Síntesis
Síntesis por oxidación
alcoholes o aldehídos Los ácidos carboxílicos pueden obtenerse por oxidación de aldehídos , y por tanto, de hecho, por doble oxidación de alcoholes primarios .de alquenos ejemplo: síntesis de ácido acético por oxidación de propeno
Síntesis de un derivado ácido
Es simplemente la hidrolisis de los diversos derivados ácidos.
ester- hidrólisis en medio ácido: retroesterificación
- hidrólisis en medio básico: saponificación del éster
Síntesis por reacción de un reactivo de Grignard sobre dióxido de carbono
ReacciónLa síntesis tiene lugar a baja temperatura ( -40 ° C ). El dióxido de carbono está entonces en forma sólida, llamada hielo seco . Se pone en exceso. Después de la reacción, se lleva a cabo la hidrólisis en medio ácido para obtener el ácido carboxílico.
MecanismoPrimer paso : adición del reactivo de Grignard al CO 2

Segundo paso : hidrólisis en medio ácido
Síntesis malónica
La síntesis malónica es un conjunto de reacciones que permiten la síntesis de muchos ácidos carboxílicos primarios o secundarios a partir del malonato de dietilo .
Ella está compuesta:
- una reacción ácido-base entre malonato de dietilo y etanoato ( sodio , potasio, etc. );
- una sustitución nucleofílica , donde el grupo deseado (primario o secundario) se inserta para el ácido carboxílico final;
- una doble saponificación de las dos funciones éster del malonato de dietilo sustituido, seguida de una acidificación del medio;
- descarboxilación (liberación de dióxido de carbono al calentar);
- transposición del producto final en ácido carboxílico por tautomería .
Esta síntesis es tanto más interesante ya que , a priori , que hace que sea posible sintetizar cualquier ácido carboxílico, ya que, aparte de un grupo terciario, parece que podemos poner lo que queremos en el lugar de R .
Notas y referencias
- R. Panico y J.-C. Richer, nomenclatura de compuestos orgánicos IUPAC , Masson, 1994, p. 70, 118- ( ISBN 978-2-225-84479-9 ) . Una matriz de sufijos (y prefijos) que se utiliza para describir algunos grupos de características importantes en nomenclatura sustitutiva está disponible en una IUPAC de referencia en línea (en inglés): sufijos y prefijos para características principales Algunos grupos en nomenclatura sustitutiva .
- Robert Panico, Jean-Claude Richer y Jean Rigaudy , Nomenclatura y terminología en química orgánica - Clases funcionales. Estereoquímica , Técnicas de ingeniería , 1996, p. 20 ( ISBN 2 85 059-001-0 ) .
- http://www.acdlabs.com/iupac/nomenclature/93/r93_705.htm











