Reacción de eliminación
En química orgánica , la eliminación (o β-eliminación ) es una reacción orgánica que transforma un alcano sustituido ( haloalcanos , alcoholes, etc.) en un derivado de etileno, o incluso en un alqueno , si es la molécula de partida, además del grupo saliente. , n 'es solo una cadena de carbono de tipo alcano.
Las condiciones son, además de duras, las de una sustitución nucleofílica , reacción similar en muchos aspectos y concurrente: la eliminación se produce en presencia de una base fuerte y calentando la mezcla de reacción.
Ecuación general
Uno de los principales ejemplos de eliminación es la conversión de un haloalcano en un alqueno ; luego hablamos de deshidrohalogenación :
Las bases más utilizadas son la sosa (Na + , HO - ), la potasa (K + , HO - ), o incluso los iones de alcoholato (RO - ) (obtenidos por reacción de sodio en un alcohol ROH, anhidro ).
Al igual que para la sustitución nucleofílica, hay una eliminación monomolecular y una eliminación bimolecular que se indica comúnmente como E1 y E2 respectivamente.
En el resto de este artículo, los ejemplos se dan con un derivado halogenado como reactivo.
Eliminación monomolecular
Cinética E1
La reacción de eliminación monomolecular se lleva a cabo en dos etapas: una etapa monomolecular que involucra solo la molécula del derivado halogenado en el lado del reactivo, que es la etapa cinéticamente limitante, seguida de una etapa bimolecular. En consecuencia, la cinética de la reacción, en la aproximación del paso cinéticamente determinante (o limitante ), depende solo de la concentración de la especie RX.
Por tanto, la reacción se caracteriza por una cinética de orden general 1, de órdenes parciales 1 con respecto al derivado halogenado y 0 con respecto a la base B | : v = k. [RX] , donde:
- [RX] representa la concentración de derivado halogenado en mol. L -1
- v representa la velocidad de la reacción de eliminación. Se expresa en mol.s −1 .
- k es la constante de velocidad: es de hecho la del paso cinéticamente limitante (k 1 ). Su unidad, Ls −1 , se deduce de las de los otros dos términos.
Mecanismo de E1
La reacción tiene lugar en dos etapas.
- Primer paso: salida del nucleófugo, formación de un carbocatión. este paso de formación de carbocatión es un paso lento, reversible e impone su velocidad a toda la reacción.
- Segundo paso: reacción ácido-base. La base arranca el protón. El doblete luego se "pliega" sobre el enlace carbono-carbono para formar un enlace doble . Dado que el enlace sencillo carbono-carbono puede rotar, se pueden formar dos estereoisómeros. Como esta reacción es mucho más rápida que la anterior, su velocidad no influye en la velocidad general.

Estereoselectividad y Regioselectividad
EstereoquímicaComo muestra el mecanismo, el paso a través de un carbocatión, que es una estructura plana, elimina cualquier elemento de estereoespecificidad a diferencia del mecanismo de eliminación bimolecular (ver a continuación).
Pero, si se pueden formar dos estereoiseómeros geométricos, no se forman en las mismas proporciones. El isómero más estable, es decir, el de menor energía, se forma predominantemente (esta es la regla de Zaitsev). Por tanto, es el isómero E el que se forma principalmente en ausencia de mesomeria. Por otro lado, si el doble enlace de sólo uno de los dos productos puede ser deslocalizado por mesomery, entonces es éste el que se formará principalmente. A esto se le llama estereoselectividad parcial.
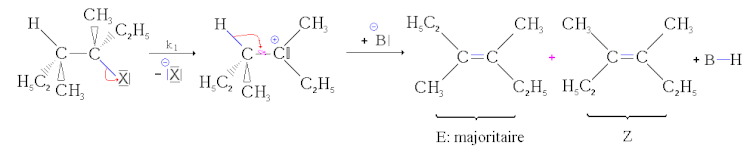 Regioquímica
Regioquímica
Cuando se pueden formar varios isómeros constitucionales, se forma preferentemente el alqueno termodinámicamente más estable. Si solo hay grupos alquilo, este es el alqueno más sustituido. Si la mesomeria puede intervenir, es el alqueno más conjugado que está en la mayoría. Esto se conoce como regioselectividad o regla de Zaïtsev .
Sin embargo, a veces se forma preferentemente el alqueno menos termodinámicamente estable, esto se conoce como eliminación de Hofmann . Este es particularmente el caso cuando la base utilizada está congestionada (por ejemplo, KtBuO) o cuando hay un ión amonio que se elimina, por ejemplo. (Molécula que lleva una amina en presencia de MeI en una cantidad de equivalentes suficientes para formar la sal de amonio, luego se coloca en presencia de óxido de plata húmedo y caliente. Formación del alqueno por eliminación de Hofmann y por lo tanto salida. De N (Me ) 3.)
Factores que influyen en la respuesta
Los parámetros que influyen en la eliminación de E1 son:
- el efecto de R-: el paso cinéticamente determinante es la formación del carbocatión (y no su reactividad), por lo que cuanto más estable es, más se favorece la reacción.
- el nucleófugo: siendo la escisión del enlace del grupo saliente C el paso clave en el mecanismo, la reacción depende en gran medida de la naturaleza de este nucleófugo. Cuanto mejor sea el grupo inicial, más rápida será la reacción. Por ejemplo, para la deshidratación de alcoholes, el primer paso es la protonación del alcohol para formar un oxonio y, por lo tanto, un mejor grupo saliente (H 2 O⇒HO - ). Una clasificación rápida de los grupos iniciales sería:
(el signo ">" significa: "mejor grupo inicial que")
Nótese que la base no influye en este tipo de reacción de orden 1 y esto en la medida en que no interviene durante el primer paso que determina la velocidad global de la reacción.
Grupo alquilo del derivado halogenadoEl mecanismo pasa por un intermedio de reacción del tipo carbocatión. Este último es tanto más estable cuanto más se sustituye. Así, la velocidad de reacción (por tanto de formación del carbocatión) progresa desde los derivados primarios, a los secundarios y luego a los terciarios. En la práctica, solo este último, y algunos derivados secundarios, reaccionan por este mecanismo.
NucleófugoCuanto más polarizable sea el enlace RX, más fácil será romperlo. Este enlace es, por lo tanto, de labilidad decreciente ("fragilidad") del flúor al yodo: F> Cl> Br> I.
(el símbolo ">" significa: "más rápido que")
Solvente- Polaridad: un disolvente polar estabiliza el carbocatión; así facilita la primera reacción. Por tanto, la velocidad aumenta con la polaridad del disolvente.
- Proticidad: un solvente prótico es más una desventaja: de hecho, corre el riesgo de competir con el carbocatión durante la reacción ácido-base (fuerte).
Competencia
Esta reacción no solo compite con la otra eliminación, sino también con las reacciones de sustituciones nucleofílicas, en particular con S N 1 . Esto último ocurre de hecho en condiciones similares (aparte del calentamiento).
Eliminación bimolecular
Cinético
La reacción de eliminación bimolecular tiene una cinética de orden global 2 y de orden parcial 1 con respecto al derivado halogenado RX y a la base B: - . La reacción tiene lugar en un solo paso que es bimolecular, por lo que la velocidad de la reacción sigue una ley tipo: v = k. [RX]. [B: - ] .
o :
- [RX] representa la concentración de derivado halogenado (expresada en mol. L -1)
- [B: - ] representa la concentración de base (expresada en mol. L −1 )
- v representa la velocidad de la reacción de eliminación. Se expresa en mol.s −1 .
- k es la constante de velocidad. Su unidad, Ls −1 .mol −1 , se deduce de las de los otros dos términos.
Mecanismo de E2
La eliminación bimolecular es una reacción bimolecular de un solo paso.
Durante el mismo paso elemental, se produce el desgarro del protón por la base, la formación del doble enlace y la salida del átomo de halógeno (nucleófugo) en forma de ión haluro. Hablamos de un mecanismo sincrónico o concertado.
Estereoquímica
E2 es una reacción estereoespecífica .
La reacción solo tiene lugar cuando el hidrógeno y el grupo saliente están en la posición anti-pleurplanar .
Factores que influyen en la respuesta
- La velocidad de reacción de un E2 varía solo ligeramente según la clase (primaria: I, secundaria: II, terciaria: III) del haluro considerado. Sin embargo, cuanto más alta es la clase, más rápida es la reacción (III> II> I) por razones estéricas (la eliminación permite eliminar sustituyentes voluminosos, y por lo tanto "voluminosos", en el producto final, presentes en el producto inicial, el reactivo , ya que se pasa de un ángulo de valencia de 109 ° 28 'en este, al nivel del carbono "sp 3 ", llevando el protón H, en un ángulo de valencia de 120 °, en el producto final donde este mismo carbono ahora "sp 2 hibridado "). En este caso generalmente se prefiere un haloalcano primario, pero cuando uno está en presencia de un haloalcano secundario, las reacciones del tipo E1 y E2 se distinguen por los efectos mesoméricos potenciales ( efecto "mesómero": término general que define un efecto electrónico correspondiente a una deslocalización de la carga, aquí positiva, en un grupo arilo, por ejemplo, un vecino inmediato, por lo tanto "en α", del enlace CH roto, se habla de "desprotonación", por la base fuerte). Cualquier sustituyente en la cadena de carbono capaz de estabilizar el ion carbenio (carbocatión C + ) a través de este tipo de efecto electrónico promoverá el mecanismo E1.
- La velocidad de reacción aumenta con la fuerza de la base, por lo que se necesita una base fuerte.
- El carácter nucleófugo del grupo saliente también influye en la reacción, pero esta influencia no es el parámetro principal a diferencia del mecanismo de eliminación unimolecular (E1).
- Para promover un mecanismo de reacción de eliminación bimolecular de E2, conviene utilizar un disolvente aprótico (DMSO, THF, tolueno, n-hexano, etc.)
Competencia
Esta reacción compite no solo con E1, sino también con reacciones de sustitución nucleofílica, en particular con S N 2 , que se produce en condiciones similares. Tenga en cuenta que una reacción de eliminación requerirá más energía que una reacción de sustitución correspondiente, generalmente mediante calentamiento.
Observaciones
La base utilizada también es un nucleófilo . Esto explica la competencia con las reacciones de sustituciones. Al final de la reacción, se pueden encontrar, mezclados, productos de eliminación y productos sustitutivos.